M.A. BOUDALIA,I. FERRAHTA, Service de Néphrologie, Dialyse et Transplantation Rénale, CHU Mustapha Bacha, Alger
Abstract : The evolution of dialysis techniques has revolutionized the prognosis of patients undergoing dialysis. The future of this technique currently involves quality of dialysis improvement by moving towards continuous purification through portable or implantations devices. We report here some promising technological trends currently under development
Key-words : Portable dialyzers, implantable dialyzer, renal regeneration, bioengineering.
Résumé : L’évolution des techniques de dialyse a permis de révolutionner le pronostic des patients bénéficiant d’épurations extrarénales. L’avenir de ces techniques implique actuellement l’amélioration de la qualité de dialyse par l’évolution vers l’épuration continue au travers de dispositifs portatifs ou implantations. Nous rapportons ici quelques voies technologiques prometteuses actuellement en développement.
Mots-clés : Dialyseurs portatifs, dialyseur implantable, régénération rénale, bio-ingénierie
La transmutation de l’hémodialyse
Au travers de tous les âges de la médecine, il est remarquable de noter l’implacable conjoncture entre l’innovation dans l’instrumentation scientifique et le progrès médical. Les exemples qui illustrent cette idée sont nombreux dans l’histoire de la médecine.
Ces exemples démontrent également que loin d’être une science isolée, la médecine, est une discipline pratique, qui applique l’ensemble des savoirs disponibles à chaque époque, dans le but de soulager la souffrance des hommes. L’épuration extrarénale ne fait pas exception à cette règle.
Bien des générations de docteurs en médecine ont collaboré étroitement avec leurs comparses d’autres disciplines (chimistes, physiciens, biologistes etc.), des ingénieurs, des hommes d’affaires et bien d’autres ; dans le seul et unique but de faire évoluer et progresser la suppléance artificielle des patients insuffisants rénaux.
Ces pionniers et explorateurs de la dialyse ont fait évoluer nos concepts et ont permis la survie d’innombrables malades. Cette épopée n’en est relativement qu’à ses débuts. Nous nous proposons dans cet article de faire un survol de certaines des voies possibles d’évolution de cette discipline.
L’épuration artificielle de demain :
Qu’attendons-nous des technologies de dialyse du futur ? D’innombrables propositions sont imaginables. Toute-fois, il est nécessaire d’établir des priorités en vue d’affecter les ressources nécessaires à la concrétisation de ces objectifs. Une commission d’experts réunis en Octobre 2018 au sein de la « Kidney Health Initiative (KHI) » a tenté de répondre de manière méthodique à cette question. Ce groupement créé par la « Food and Drug Administration » (FDA), et « The American Society for Nephrology » (ASN), a proposé une feuille de route visant à accélérer le développement des innovations dans le domaine de l’épuration extra rénale (EER). Dans leurs rapports, la KHI rappelle que plus de 2 millions de personnes sont actuellement en IRCT sous diverses modalités d’EER dans le monde. Mais surtout, que du fait du prix prohibitif de ces techniques, plus de 1 million de personnes meurent chaque année du fait de l’inaccessibilité de ces techniques dans les pays à faible revenu. [1]
Les principaux objectifs de cette feuille de route sont :
- L’amélioration de la qualité de vie des patients (amélioration de la mobilité des patients, réduction du temps consacré à la mise en place des thérapies…etc.),
- Optimiser l’aptitude aux activités sportives et au travail physique,
- Améliorer la nutrition et la liberté métabolique des patients,
- Lutter contre le caractère invasif des thérapies,
- Réduire le recours aux traitements pharmacologiques en agissant sur l’incidence des complications,
- Améliorer la durabilité des dispositifs et réduire l’impact financier de ces thérapies. Et enfin
- Développer des dispositifs ayant un coût commercial réduit. [1]
Les grands axes technologiques proposés sont de quatre types :
- L’amélioration des techniques actuelles d’EER,
- Le développement d’appareils portatifs,
- Le développement de dispositifs implantables bio- compatibles,
- La régénération rénale (remplacement cellulaire par des cellules souches par exemple).
Ces grands axes ne sont pas exhaustifs, mais restent les voies actuellement reconnues comme porteuses des plus grandes promesses de succès.
Les tentatives actuelles de développer un rein artificiel implantable ou portable font sensation dans les médias. Ces dispositifs dont le coût, ne peut être qu’inférieur à l’épuration en centre, pourraient permettre un accès bien plus étendu que celui actuellement proposé, principalement dans les pays en développement. Tout en éloignant le spectre de «la saignée» pluri-hebdomadaire de l’hémodialyse en centre.
Des dispositifs portables :
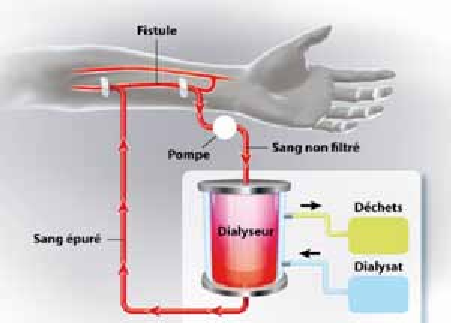
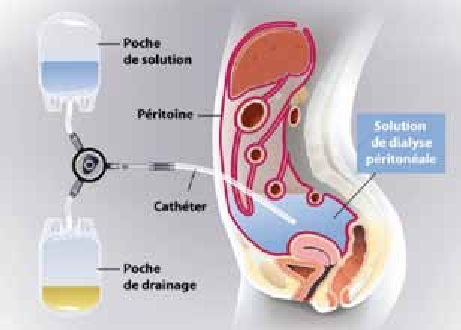
L’une des principales barrières à la conception d’un Rein Artificiel Portatif (RAP) est la quantité de dialysat transporté. En effet, une séance d’hémodialyse peut facilement consommer 140 l de dialysat par séance. La dialyse péritonéale utilise, quant à elle, près de 10 à 15 l/jour de dialysat. Les RAP actuellement en développement utilisent principalement des mécanismes de régénération du dialysat afin de réduire la quantité de dialysat transporté. Certains de ces mécanismes de régénération sont directement inspirés de travaux de la NASA (effectués dans les années 1950-1960) qui visaient à régénérer l’eau usagée des capsules spatiales afin de minimiser la taille des réservoirs d’eau.
Ce fut l’absorption des solutés (des déchets) par des cristaux de zirconium qui fut retenue pour équiper les modules spatiaux. Dans les années 1970, un système de régénération du dialysat utilisant ces mêmes cristaux fut adopté pour concevoir le premier dialyseur « relativement portatif », dénommé « REDY » (REgeneration of DialYsate) [2].
Ces dialyseurs rencontraient un relatif succès, principalement en Australie, où il permirent le développement de la dialyse à domicile. En effet, ces machines n’utilisent que 6l de dialysat par séance. De plus, le système est également suffisamment compact pour être transporté dans une malle de voiture.
Cependant, le prix prohibitif des cartouches et les complications « relativement rares » liées au processus chimique de régénération conduisirent cette technologie à être supplantée par les techniques de dialyse en centre dite « à passage unique ». Actuellement, plusieurs dispositifs de RAP sont en phase de test sur l’homme, ce qui devrait donc rapidement aboutir à leur commercialisation. Dans ce qui suit, nous verrons deux exemples ayant fait l’objet de nombreuses publications.
Le WAK PD :
Il s’agit de l’acronyme de « Wearable Artificial Kidney for Peritoneal Dialysis ». Développé par la AWAK Technologies d’origine singapourienne, il s’agit d’un appareil portatif permettant la réalisation de séance de DP de 8h en toute mobilité. La technique consiste à remplir le péritoine du patient avec 1 à 2 l de dialysat, puis de le connecter au dispositif portatif qui va effectuer la filtration de 500 ml de dialysat toutes les 7 minutes (soit 8 cycles de régénération par heure).
Après filtration, le dialysat est rechargé en glucose et en électrolytes puis réinjecté dans le péritoine. Un réservoir spécifique permet le recueil de l’UF produite. Au bout de 7h, la cartouche est considérée comme saturée et le processus s’arrête jusqu’au changement de cartouche. En tout le processus fournit 96 l de dialysat par jour [3].

Une étude portant sur 20 patients volontaires réalisée en Californie en 2008 utilisant un prototype de l’AWAK PD, permet d’évaluer que la clairance moyenne obtenue avoisine les 31 ml/min. Ces valeurs sont bien supérieures aux valeurs obtenues pour une DPCA standard [4].
Le WAK HD :
Le WAK HD, pour « Wearable Artificial Organs Inc » est un rein artificiel portatif. Il se porte comme une ceinture et pèse < 5 kg. Il ne nécessite que 400 ml de dialysat et fonctionne avec des piles AA de 1,5V (6 piles soit 9V).
Il est composé de 2 pompes (sang et dialysat), d’une seringue électrique pour l’héparine et d’un petit capillaire en polysulfone. Ce dispositif fut développé par Gura et al. dès le début des années 2000. Il fut testé sur l’homme dès 2005 [5], sans incident majeur et avec des résultats comparables à ceux de l’hémodialyse en centre sur le plan de la clairance. Il n’en reste pas moins que le poids du dispositif et les risques liés au déplacement de l’abord vasculaire lors des déplacements des patients imposent une amélioration du dispositif.
Il est toutefois notable que les grands noms de l’industrie de l’EER, comme Frésinus et Medtronic ont également entrepris la conception et la réalisation de leur propre WAK HD [12]. Il reste fort probable que le développement de ces dispositifs soit peu concluant en l’absence de nouvelles technologies d’abords vasculaires permettant de sécuriser les circuits sanguins extracorporels.

Images reproduites : site web du Dr Gura – https://drgura.com/
Les reins artificiels implantables :
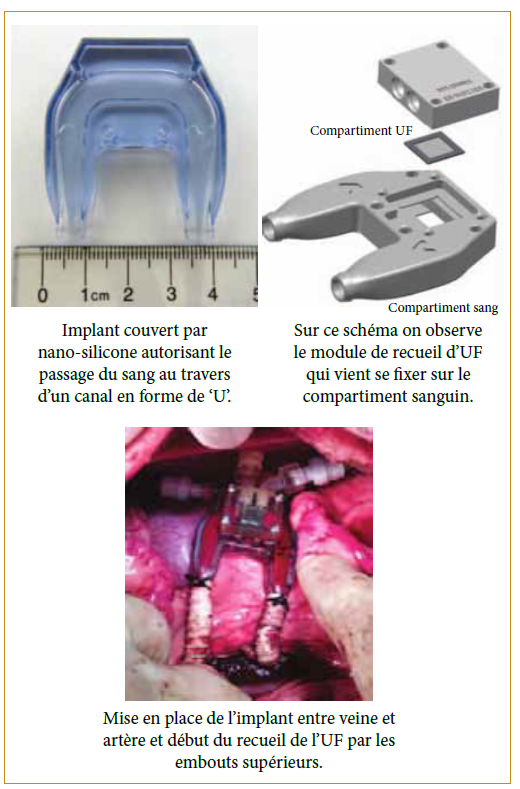
La mise en place d’un dispositif implantable doit répondre à plusieurs impératifs. Le premier d’entre eux reste la capacité du versant sanguin du dispositif à ne pas thromboser une fois implanté. Cela, même en l’absence d’une anticoagulation systémique pharmacologique. Les nanotechnologies viennent ici à la rescousse des patients en proposant l’utilisation de membrane en nano port de silicone. Les premiers essais de mise en place chirurgicale d’un dispositif d’ultrafiltration non-thrombotique chez l’animal ont eu lieu avec succès en
2016 [6]. Ces travaux réalisés par l’équipe de chirurgie et de bio-ingénierie de l’UCSF (Kensinger et Al), ont porté sur des tests in vivo de dispositif recouvert de ces membranes de nano-silicone. Cette tentative fut couronnée de succès avec des dispositifs implantés sur des chiens dans des périodes allant de 2 à 8 jours, sans thrombose constatée chez les 6 chiens opérés. L’UF recueillie allait de 1 à 10 L/24h.
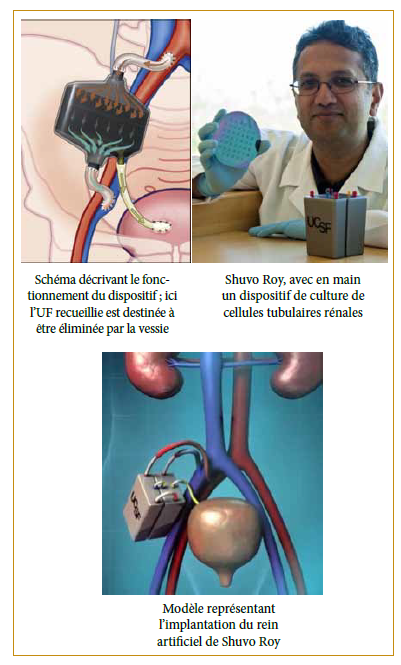
L’équipe de bio-ingénierie de UCSF, avec à sa tête Shuvo Roy, œuvrent actuellement au développement d’un dispositif implantable constitué de deux compartiments. Le premier compartiment (dit « HemoCartridge »), permet la formation d’UF à partir du sang (déjà développé pour l’équipe de Kensinger et Al). Le second (dit « Bio- Cartridge ») devrait permettre, à l’aide de cellules tubulaires en culture, de récupérer les éléments nutritifs de l’UF et de les restituer au sang. Mais également de concentrer l’UF recueillie qui est destinée à être éliminée dans la vessie afin de réduire les pertes liquidiennes [7].
La mise en culture de cellules tubulaires ne signifie cependant pas que celles-ci seront capables de modifier et de transporter les solutés. Ce point reste le plus complexe du problème. En effet, pour pouvoir réabsorber du glucose par exemple, la cellule tubulaire doit être polarisée. Elle doit avoir un pôle apical en contact avec
« l’urine ou l’UF » produite, et un pôle basal orienté vers le versant sanguin pour y excréter le glucose recueilli.
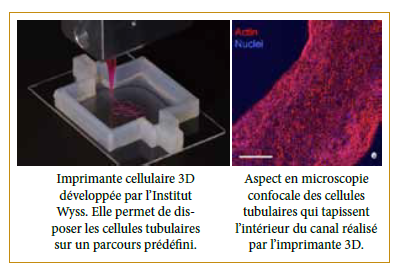
Un début de solution fut apporté par le département de Bio-engineering de Wyss (Harvard University). Humes et al ont publié en 2016, un procédé d’impression 3D de cellules tubulaires permettant d’obtenir in-vitro une structure similaire à un tubule néphronique, composé de cellules tubulaires polarisés présentant une activité proche de celle des cellules in-vivo [8]. Cet exploit permet d’imaginer la survie de structures tubulaires recouvertes de cellules tubulaires dans ce qui sera peut-être le premier rein artificiel implantable.
La régénération rénale :
La régénération d’organe implique un remplacement direct ou induit des cellules et structures histologiques altérées en vue de restaurer la fonction de l’organe.
Les moyens utilisés pouvant être l’utilisation de cellules, leurs dérivés (vésicules, cytokines, ARN/ADN) ou de biomatériaux (valves cardiaques, implant cristallin, stents vasculaires bioactifs, billes de polymères remplaçant les globules rouges, ou polymères résorbables de reconstruction osseuse) [9]. L’application des techniques de régénération au rein ont connu une croissance exponentielle des publications ces 10 dernières années. Il n’en reste pas moins que leurs applications cliniques restent au stade d’études fondamentales ou de recherche clinique.
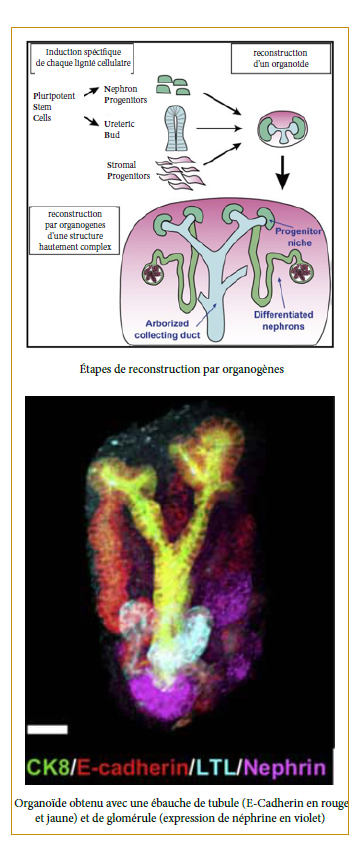
La reconstruction d’un tissu fait d’un seul type cellulaire est connue depuis de nombreuses années. Toutefois, pour la reconstruction d’un organe complexe, comme le rein, il n’est pas envisageable de simplement mettre en co-culture des précurseurs cellulaires et espérer les voir spontanément s’organiser pour former l’organe souhaité. Pour remédier à cet écueil, plusieurs méthodes sont à l’essai, allant du bioprinting 3D à la reconstruction d’un embryon complet ou non. L’équipe de Taguchi, de l’université de Kumamoto au Japon, a publié en 2017 des travaux accueillis comme une percée majeure dans le domaine de la reconstruction d’organe. Il réalise la mise en culture et le développement séquentiel d’un bourgeon néphronique in vitro. À partir de cellules issues de bourgeon urétéral et blastème métanéphrogène d’embryon de souris, ils réussirent à identifier les facteurs de croissance nécessaires au développement de ces cellules et à maintenir la survie et l’organogenèse de ces cellules vers la formation d’une structure complexe. Ils réussirent donc à développer in vitro un « Organoïde » rénal [10].
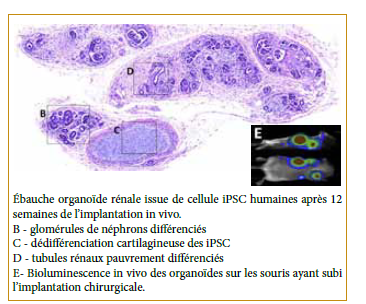
Bantounas et al. (U. Manchester, UK), ont également publié leurs travaux dans le domaine de l’organogenèse. Dans leurs publications de Mars 2018 [11], ils décrivent l’utilisation de cellules souches humaines induites (iPSC), cultivées par des procédés de différentiation cellulaire en lignées rénales. Ils utilisèrent la même procédure que celle proposée par Taguchi et al. pour développer un organoïde rénal. Puis ils procédèrent à l’implantation de ces organoïdes dans le tissu sous cutané de souris immunodéficientes. Après 12 semaines de suivi, ils constataient le développement des organoïdes vers des structures possédant des glomérules (certains étaient capables d’ultrafiltration), drainés par des pseudo-tubules. Ces résultats exceptionnels nous font entrevoir un futur où des organes humains pourraient être « cultivés » ou portés par des animaux d’élevage à but de remplacement d’organe. Toutefois, même si ces études démontrent la faisabilité conceptuelle d’une telle
« culture », il n’en reste pas moins que beaucoup d’autres travaux restent nécessaires à l’obtention de résultats opérationnels.
Conclusion :
De nombreuses innovations restent à venir. Toutefois, celles-ci font la part belle aux technologies de bio-ingénierie tissulaire. Ces procédés nécessiteront le développement, en vue de leur mise en place, de centres regroupant des qualifications médico-chirurgicales et d’explorations radio-biologiques spécialisées, mais également de bio-ingénieurs qui apporteront le support technique à l’entretien et la réparation de ces technologies (p. ex. par le réensemencement cellulaire des dispositifs implantés).
Il n’en reste pas moins que l’espoir de voir ces technologies être disponibles en thérapeutique humaine dans les décades à venir est important.
Bien qu’elles semblent issues de l’imaginaire d’un auteur de science-fiction, leurs prémices sont déjà bien là. Cela nous engage à poursuivre par nos efforts, l’enrichissement de nos savoirs qu’impose la révolution scientifique permanente. Cette progression des savoirs locaux est le seul gage permettant le transfert de ces technologies de santé.
Liens d’intérêts :
Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Technology Roadmap for Innovative Approaches to Renal Replacement Therapy. American Society of Nephrology. August 2018. https://khi.asn-online.org/
- Agar, John W. M. «Review: understanding sorbent dialysis systems.» Nephrology (Carlton)., vol. 15, no. 4, June 2010, pp. 406-11, doi:10.1111/j.1440-1797.2010.01321.x. https://www.ncbi.nlm.nih.gov/pubmed/20609091
- Salani, Megha, et al. «Innovations in Wearable and Implantable Artificial Kidneys.» Am. J. Kidney Dis., vol. 72, no. 5, Nov. 2018, pp. 745-51, doi:10.1053/j.ajkd.2018.06.005. https:// www.ncbi.nlm.nih.gov/pubmed/30146422
- Lee, David B. N. and Martin Roberts. «A peritoneal-based automated wearable artificial kidney.» Clin. Exp. Nephrol., vol. 12, no. 3, 1 June 2008, pp. 171-80, doi:10.1007/s10157-008-0050-9. https://www.ncbi.nlm.nih.gov/pubmed/18386116
- Davenport, Andrew, et al. «A wearable haemodialysis device for patients with end-stage renal failure: a pilot study.» Lancet, vol. 370, no. 9604, 15 Dec. 2007, pp. 2005-010, doi:10.1016/S0140-6736(07)61864-9. https://www.ncbi.nlm.nih.gov/pub- med/18083402
- Kensinger, Clark, et al. «First Implantation of Silicon Nanopore Membrane Hemofilters.» ASAIO J., vol. 62, no. 4, July 2016, pp. 491-5, doi:10.1097/MAT.0000000000000367.
- Homan, Kimberly A., et al. «Bioprinting of 3D Convoluted Renal Proximal Tubules on Perfusable Chips.» Sci. Rep., vol. 6, 11 Oct. 2016, p. 34845, doi:10.1038/srep34845. https://www.ncbi.nlm.nih.gov/pubmed/27725720
- Humes, H. David, et al. «Initial clinical results of the bioartificial kidney containing human cells in ICU patients with acute renal failure.» Kidney International, vol. 66, no. 4, 1 Oct. 2004, pp. 1578-88, doi:10.1111/j.1523-1755.2004.00923.x.
- Sumrita Bhat, Ashok Kumar-Biomaterials in Regenerative Medicine-Journal of Postgraduate Medicine Education and Re- search – :2012 – Volumn:46: 2- Pages No:81-89- DOI : 10.5005/ jp-journals-10028-1018.www.jaypeejournals.com/eJournals/ ShowText.aspx?ID=3179&Type=FREE&TYP=TOP&IID=24 4&Value=-1&isPDF=YES
- Taguchi, Atsuhiro and Ryuichi Nishinakamura. «Higher- Order Kidney Organogenesis from Pluripotent Stem Cells.» Cell Stem Cell, vol. 21, no. 6, 7 Dec. 2017, pp. 730-7466, doi:10.1016/j.stem.2017.10.011. https://www.ncbi.nlm.nih. gov/pubmed/29129523
- Bantounas, Ioannis, et al. «Generation of Functioning Nephrons by Implanting Human Pluripotent Stem Cell-Derived Kidney Progenitors.» Stem Cell Rep., vol. 10, no. 3, 13 Mar. 2018, pp. 766-79, doi:10.1016/j.stemcr.2018.01.008. www. ncbi.nlm.nih.gov/pubmed/29429961
- Van Gelder, Maaike K., et al. «From portable dialysis to a bioengineered kidney. «Expert Rev. Med. Devices, vol. 15, no. 5, May. 2018, pp. 323-36, doi:10.1080/17434440.2018.1462697 www.ncbi.nlm.nih.gov/pubmed/29633900