S. AISSANI, A. ZITOUNI, Service de Pneumologie,Hôpital Mohammed Seghir El Nekkache (HCA), Alger.
Abstract
The direct role of dietary factors in respiratory disease is increasingly suspected, but the direct relationship is unclear. It has long been known that cachexia dueto undernutrition in Chronic obstructive pulmonary disease in the chronic respiratory failure stage is a marker of high mortality. Respiratory functional rehabilitation with a consequent rich nutritional intake can improve the prognosis. Regular consumption of diet rich in fruits, vegetables, fish, and grains is associated with a reduced risk of new cases of Chronic obstructive pulmonary disease. A diet high in fiber is associated with better respiratory function and a reduced prevalence of Chronic obstructive pulmonary disease. In addition, a diet rich in antioxidants does not repair the damage caused by tobacco, but it does prevent it. Moreover, the deficient of diet can contribute to the dysfunction of the respiratory microbiota and increase the risk of respiratory diseases. Disruption of the microbiota is accompanied by high mortality in patients with Chronic obstructive pulmonary disease.
Keywords : Chronic obstructive pulmonary disease, diet, antioxidants, prevention, rehabilitation.
Résumé
Le rôle direct des facteurs alimentaires dans les maladies respiratoires est de plus en plus suspecté mais la relation directe n’est pas claire. Nous savons depuis longtemps que la cachexie due à la dénutrition au cours de la Broncho-pneumopathie chronique obstructive au stade d’insuffisance respiratoire chronique, est un marqueur de mortalité élevée. La réhabilitation fonctionnelle respiratoire comportant un apport nutritionnel riche, conséquent, peut améliorer le pronostic. La consommation régulière d’une alimentation riche en fruits, légumes, poissons et céréales est associée à un risque réduit de nouveaux cas de Broncho-pneumopathie chronique obstructive. Une alimentation riche en fibres est associée à une meilleure fonction respiratoire et une prévalence réduite de la Broncho-pneumopathie chronique obstructive. En outre, une alimentation riche en antioxydants ne permet pas de réparer les dégâts causés par le tabac mais elle permet de les prévenir. Par ailleurs, une alimentation déficiente peut contribuer au dysfonctionnement du microbiote respiratoire et augmenter le risque de maladies respiratoires. La perturbation du micro- biote s’accompagne d’une mortalité élevée chez les patients atteints de Broncho-pneumopathie chronique obstructive.
Mots-clés : Broncho-pneumopathie chronique obstructive, alimentation, antioxydants, prévention, réhabilitation.
Introduction
Le poumon est un organe dans lequel le stress oxydant a une importance particulière (1). Une alimentation pauvre en anti-oxydants peut augmenter la susceptibilité pulmonaire à l’agression oxydative dutabac ou de lapollution et à l’inflammation des voies aériennes. Les antioxydants synthétisés par l’organisme ou apportés par une alimentation riche en vitamines, comme les fruits et légumes, sont la première défense pulmonaire contre les radicaux
libres. Ils ont une action dans le liquide extracellulaire des voies aériennes depuis les fosses nasales jusqu’aux alvéoles et une action intracellulaire (2, 3).
Nous parlons souvent de l’effet protecteur de l’alimentation contre les maladies inflammatoires et cancers. Cet effet est attribué en particulier aux vitamines anti-oxydantes, aux acides gras oméga-3 et oméga-6 et à certains minéraux comme le sel et le magnésium.
L’augmentation des radicaux libres favorise l’inflammation au niveau du poumon et des bronches et par conséquence un risque élevé de maladies inflammatoires chroniques comme l’asthme, la Bronchopneumopathie chronique obstructive (BPCO), les pneumopathies infiltratives diffuses et le cancer (4).
Effets de la qualité de l’alimentation sur la BPCO
A- Dénutrition
La dénutrition est fréquente en cas d’insuffisance respiratoire chronique et souvent corrélée à un mauvais pronostic. Au cours des broncho-pneumopathies chroniques obstructives, il existe une augmentation des besoins énergétiques en raison de l’augmentation du travail respiratoire et des phénomènes inflammatoires sous la dépendance de cytokines pro-inflammatoires. Il se produit un déséquilibre entre les processus métaboliques cataboliques et anaboliques.
Sur le plan clinique, un cercle vicieux s’installe. L’organisme affaibli n’est plus réceptif aux signaux anaboliques; il en résulte alors une anorexie, une perte de poids et une malnutrition; Ce qui va détériorer plus la condition physique et la dyspnée avec altération de la qualité de vie (5). En plus de l’anorexie, l’organisme présente également un métabolisme énergétique pathologiquement augmenté mais inefficace du fait de l’inflammation systémique, il se produit alors une lipolyse et une myolyse généralisées médiées par les cytokines et une altération de la fonction mitochondriale hépatique (6, 7).
La dénutrition entraîne une fonte musculaire généralisée qui n’épargne pas les muscles respiratoires; ce qui va augmenter le travail des muscles respiratoires et les dépenses énergétiques de repos (8).
En plus, les défenses immunitaires sont classiquement diminuées chez le dénutri, favorisant ainsi les infections respiratoires (9) particulièrement chez les patients atteints de BPCO (8) .
B- Malnutrition
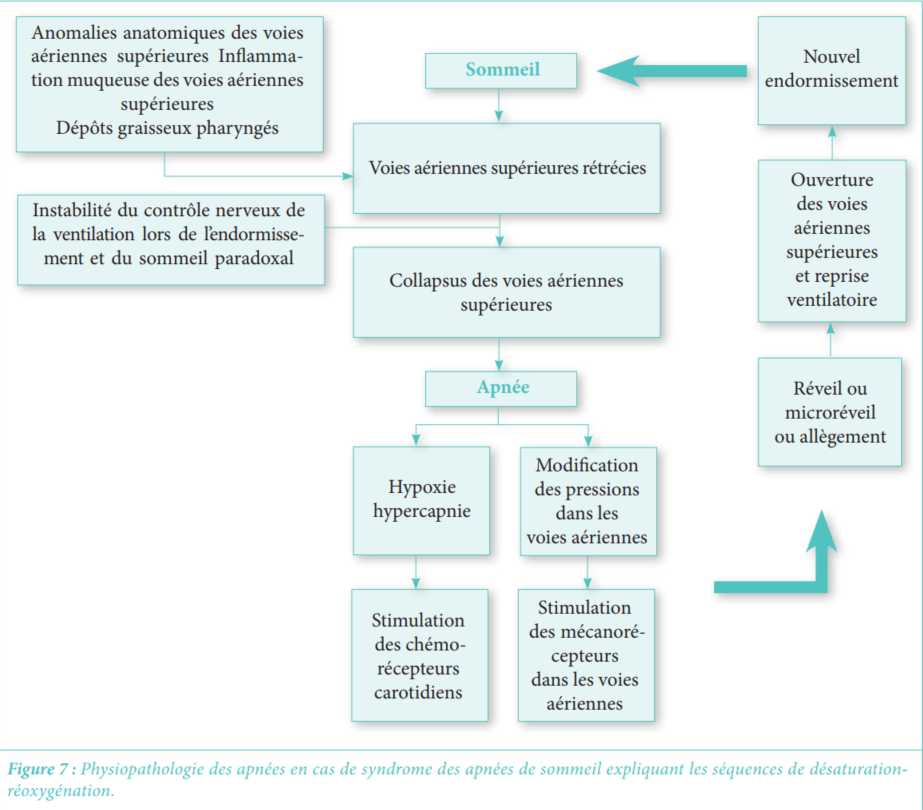
En plus de la limitation de l’activité physique chez les patients atteints de BPCO, une alimentation déséquilibrée riche en graisses et sucres peut entraîner une obésité. Si la cachexie aggrave la BPCO, l’obésité n’est pas dénuée de risque. Elle représente un facteur de risque du syndrome d’apnée obstructif du sommeil (SAOS) (10). L’association BPCO-SAOS sous le nom d’Overlap syndrome est un phénotype particulier de la BPCO. Les patients souffrant de ce syndrome sont les plus exposés aux complications respiratoires comme l’hypoxémie nocturne, l’hypercapnie diurne et l’hypertension artérielle pulmonaire (11). Dans ce cas, la perte de poids améliore le volume de réserve expiratoire, la capacité résiduelle fonctionnelle et les échanges gazeux; entraînant une augmentation de l’oxygénation du sang. La force musculaire respiratoire et la dyspnée s’améliorent également après la perte de poids (12).
Par ailleurs, certains aliments peuvent favoriser un reflux œso-gastro-œsophagien qui peut être à l’origine d’une toux spasmodique ou d’une exacerbation de la BPCO (13).
Effets des aliments sur la BPCO
Deux larges études de cohortes américaines sur 73228 femmes et 47026 hommes ont été réalisées sur l’effet de l’alimentation sur la BPCO. Il ressort qu’un régime riche en fruits, légumes, poissons et céréales était associé à un risque réduit de nouveaux cas de BPCO. En revanche, un régime riche en céréales transformées, viandes fumées et rouges, desserts et frites, était associé à un risque accru de BPCO. Il a été rapporté à l’inverse qu’une alimentation riche en fibres était associée de façon indépendante à une meilleure fonction respiratoire et une prévalence réduite de la BPCO (14).
Le rôle du magnésium sur la BPCO a été aussi trouvé sur la réduction du nombre et de la probabilité des exacerbations (15). La vitamine C est également associée à une meilleure fonction pulmonaire. La consommation de 40 à 144 mg/j de vitamine C étant corrélée à une différence en volume expiratoire maximum seconde (VEMS) de 22 à 53 ml et de la capacité vitale forcée de 23 à 79 ml (16).
Parailleurs, l’effet combiné de la vitamine C, la vitamine E et les caroténoïdes sur la fonction pulmonaire des sujets consommant une grande quantité de fruits frais (5 à 6 portions par jour, environ 70 g) est marqué par une incidence plus basse de la BPCO (17).
Un des paramètres reconnus comme étant des marqueurs de mortalité chez les patients atteints de BPCO est la cachexie due à la dénutrition. La réhabilitation fonctionnelle respiratoire comportant un apport nutritionnel riche en protéines peut améliorer le pronostic (18). Néanmoins, une alimentation riche en antioxydants ne permet pas de réparer les dégâts causés par le tabac mais elle permet de les prévenir. C’est ce qui a été rapporté dans une étude sur 10 ans, chez 680 patients ayant consommé des aliments riches en fruits (2 tomates et/ ou plus de 3 portions de fruits par jour); ceci est accompagné d’une diminution faible du VEMS et du risque de survenue de BPCO (19). Par ailleurs, une alimentation riche en fibres pourrait également améliorer le pronostic des BPCO (20).
Toutefois, s’il est connu que le tabac favorise la BPCO, l’effet protecteur de la vitamine C chez les fumeurs n’est pas clair. Le tabagisme est souvent associé à une alimentation de mauvaise qualité. En plus, la fumée de cigarettes est l’un des oxydants les plus puissants de la vitamine C et de la vitamine E dans le sang.
Vitamine D et BPCO
En raison du changement du mode de vie, l’homme passe plus de temps à l’intérieur, à l’abri du soleil; ceci a augmenté considérablement la carence en vitamine D dans le monde et en Algérie.
La vitamine D a des effets connus sur le développement des poumons et du système immunitaire. Elle peut protéger contre le développement, la gravité et l’évolution des maladies respiratoires. Au niveau de l’appareil respiratoire, les cellules épithéliales des voies aériennes possèdent la capacité de convertir la 25-dihydroxyvitamine D3 en 1,25-dihydroxyvitamine D3 active (21). De ce fait, la vitamine D jouera le rôle d’immunomodulateur puissant grâce à ces effets sur les lymphocytes T afin de réduire l’inflammation (22).
L’effet de la vitamine D ne se limite pas seulement à l’action anti-inflammatoire sur les voies aériennes. La vitamine D réduit l’hyperréactivité bronchique et freine le remodelage bronchique en agissant sur les muscles lisses des voies respiratoires (23).
Il a été démontré que le déficit en vitamine D est associé à une progression de la BPCO (24) avec risque élevé d’infections respiratoires (25) et d’exacerbation (26). La supplémentation en vitamine D pourrait réduire le risque d’exacerbations fatales chez les patients souffrant de BPCO (27).
Microbiote et BPCO
Le tractus respiratoire bas, considéré longtemps stérile, contient un microbiome respiratoire qui intervient pour renforcer le système immunitaire de l’homme. Son fonctionnement peut être altéré par plusieurs facteurs. Les chercheurs évoquent de plus en plus l’effet de l’alimentation dans le dysfonctionnement du microbiote respiratoire qui aura comme conséquence une augmentation du risque de maladies respiratoires comme l’asthme et la BPCO (28). La perturbation du microbiote s’accompagne d’une mortalité à un an plus élevée chez les patients atteints de BPCO (29).
Conclusion
L’alimentation peut jouer un rôle dans les maladies respiratoires. Elle pourrait ralentir une chaîne de réactions toxiques lorsqu’elle est équilibrée. Une alimentation déficiente en certains nutriments pourrait augmenter la susceptibilité des individus à des facteurs environnementaux tels que le tabac et favoriser la BPCO. Néanmoins, la complexité de l’alimentation, sa conservation et sa cuisson permettent d’expliquer la difficulté actuelle d’établir avec certitude le lien avec les maladies respiratoires.
Références
- Kelly FJ. Vitamins and respiratory disease: antioxidant micronutrients in pulmonary health and disease. Proc Nutr Soc. nov 2005; 64 (4): 510-26.
- Garait B. Le stress oxidant induit par voie métabolique (Régime alimen- taire) ou par voie gazeuse (Hyperoxie) et effet de la Glisodin. [Internet]. [gre- noble]: Université Joseph-Fourier – Grenoble I; 2006. Disponible sur : https:// tel.archives-ouvertes.fr/tel-00120861v1.
- Milbury PE, Richer AC. Understanding the Antioxidant Controversy: Scrutinizing the Fountain of Youth. InbundenEngelska; 2008. 192 p.
- Soomro S. Oxidative Stress and Inflammation. OJI. 2019; 09 (01): 1-20.
- Haehling S von, Arends J, Blum D, Hacker UT. Kachexie bei Tumo- rerkrankungen: erkennen und multimodal behandeln. Berlin: Springer Me- dizin; 2017. 140 p.
- Caterina Constantinou Cibely Cristine Fontes DE Oliveir, Dionyssios Mintzo- poulos, Silvia Busquet, Jianxin HE, and al. Nuclear magnetic resonance in conjunction with functional genomics suggests mitochondrial dysfunction in a murine model of cancer cachexia. Int J Mol Med. 27: 15-24, 2011.
- Maria Tsoli, Graham Robertson Cancer cachexia: malignant inflammation, tumorkines, and metabolic mayhem. Trends Endocrinol Metab. 2013; 4: 174-83.
- Boncompain-Gérard M, Gelas P, Liateni Z, Guérin C. Dénutrition de l’in- suffisant respiratoire chronique : physiopathologie et prise en charge. Réani- mation. Mars 2005; 14 (2): 79-86.
- Kumar Chandra R. Nutrition, immunity, and infection: Present knowledge and future directions. The Lancet. Mars 1983; 321 (8326): 688-91.
- B. Flávia, G, X.L. Nguyen-Plantin, Syndrome d’Apnées Obstructives du Sommeil et Obésité : quels traitements ? Obésité. 2015; (10): 193-7.
- Kopp, G., Lador, F., Adler, D. Le syndrome d’overlap chez le patient BPCO. Rev Med Suisse 2019. 2019; 5 (671): 2087-9.
- Mafort TT, Rufino R, Costa CH, Lopes AJ. Obesity: systemic and pul- monary complications, biochemical abnormalities, and impairment of lung function. Multidiscip Respir Med. déc 2016; 11 (1): 28.
- Morice A. Airway reflux asacauseofrespiratory disease. Breathe. 2013; 9: 256-66.
- Varraso R, Chiuve SE, Fung TT, Barr RG, Hu FB, Willett WC, et al. Alternate Healthy Eating Index 2010 and risk of chronic obstructive pulmonary disease among US women and men: prospective study. BMJ. 3 févr 2015; 350: h286.
- Aziz H, Blamoun A, Shubair M, Ismail M, DeBari V, Khan M. Serum magnesium levels and acute exacerbation of chronic obstructive pulmonary disease: A retrospective study. Annals of clinical and laboratory science. 2005; 35: 423-7.
- Romieu I, Trenga C. Diet and Obstructive Lung Diseases. Epidemiologic Reviews. 1 janv 2001; 23 (2): 268-87.
- Miedema I, Feskens EJM, Heederik D, Kromhout D. Dietary Determi- nants of Long-term Incidence of Chronic Nonspecific Lung Diseases: The Zutphen Study. American Journal of Epidemiology. 1993; 138 (1): 37-45.
- Celli BR, Cote CG, Lareau SC, Meek PM. Predictors of Survival in COPD: More than Just the FEV1. Respiratory Medicine. Juin 2008; 102: S27-35.
- Garcia-Larsen V, Potts JF, Omenaas E, Heinrich J, Svanes C, Garcia-Ayme- rich J, et al. Dietary antioxidants and 10-year lung function decline in adults from the ECRHS survey. Eur Respir J. déc 2017; 50 (6): 1602286.
- Young RP, Hopkins RJ. Is the“Western Diet” a New Smoking Gun for Chronic Obstructive Pulmonary Disease? Annals ATS. Juin 2018; 15 (6): 662-3.
- Hansdottir S, Monick MM, Hinde SL, Lovan N, Look DC, Hunninghake GW. Respiratory epithelial cells convert inactive vitamin D to its active form: potential effects on host defense. Journal of immunology. 2008; 181 (10): 7090-9.
- Dimeloe S, Nanzer A, Ryanna K, Hawrylowicz C. Regulatory T cells, inflam- mation andtheallergic response-The role ofglucocorticoids and Vitamin D. Jour- nal of Steroid Biochemistry and Molecular Biology. 2010; 120 (2-3): 86-95.
- Hall SC, Agrawal DK. Vitamin D and Bronchial Asthma: An Overview of Data From the Past 5 Years. Clinical Therapeutics. 2017; 39 (5): 917-29.
- Changhwan Kim 1 Yousang Ko 1 Ji Ye Jung Yeon-Mok Oh Sang-Do Lee Yong. Severe vitamin D deficiency is associated with emphysema progres- sion in male patients with COPD. respiratory medicine. 2020; 163, (105890, MARCH 01, 2020).
- Jolliffe DA, Greenberg L, Hooper RL, Mathyssen C, Rafiq R, de Jongh RT, et al. Vitamin D to prevent exacerbations of COPD: systematic review and meta-analysis of individual participant data from randomised controlled trials. Chronic obstructive pulmonary disease. Thorax 2019; 74: 337–345.
- Lokesh KS, Chaya SK, Jayaraj BS, Praveena AS, Krishna M, Madhivanan P, et al. Vitamin D deficiency is associated with chronic obstructive pulmo- nary disease and exacerbation of COPD. The Clinical Respiratory Journal. 2021; 15 (4): 389-99.
- Jolliffe DA, Greenberg L, Hooper RL, Griffiths CJ, Camargo CA, Kerley CP, et al. Vitamin D supplementation to prevent asthma exacerbations: a sys- tematic review and meta-analysis of individual participant data. The Lancet Respiratory Medicine. 2017; 5 (11): 881-90.
- Stokholm J, Martin J. Blaser, Jonathan Thorsen1, Morten A. Rasmussen, Johannes Waage, Rebecca K. Vinding, Ann-Marie M. Schoos, AsjaKunøe, Nadia R. Fink, Bo L. Chawes, Klaus Bønnelykke, Asker D. Brejnrod, Mar- tin S. Mortensen, Waleed Abu Al-Soud, Søren J. Sørensen& Hans Bisgaard. Maturation of the gut microbiome and risk of asthma in childhood. Nature communications. 2018; 9 (14):1-10.
- Mika M, Nita I, Morf L, Qi W, Beyeler S, Bernasconi E, et al. Microbial and host immune factors as drivers of COPD. ERJ Open Res. Juill 2018; 4 (3): 00015-2018.