K. DjILALI AIAD, CHU Abdelkader Hassani, Sidi Bel Abbès
Abstract : Cervicofacial cellulitis is a serious infection that concerns anatomical spaces delimited by aponeuroses, the latter covering the different organs of the neck. Mortality rate of this serious pathology varies from 6% to 76%. Prognosis of cervico-facial cellulitis depends on several parameters, the most important is early patient’s management. Materials and methods : We conducted a prospective descriptive and analytical study over a five-year period from April 1st 2008 to April 1st 2013, involving 69 patients, studying mortality-related factors. Five cases of mortality were recorded. The statistical analysis was performed by the Khi2 test or Fischer test; the result was significant for p <0.05. Results : Among the 69 cases of cervicofacial cellulitis, we recorded 5 cases of death, i.e. 7.25% of patients. The average age of deceased patients is 40.8 years, 80% of the deceased patients were male, of low socio-economic level, almost all alcohol-smoking and drug addicts, poor oral hygiene, hygiene oral defective, the majority are diabetics, all were treated with nonsteroidal anti-inflammatory drugs and antibiotics. In analytic study, those who are significantly related to mortality are: lack of occupation, low socio-economic level, alcoholism, as well as drug addiction: the risk of mortality is multiplied by 15 in drug-addicts; diabetes, the gaseous cellulitis type, bilateral location, were related to Bacteroides germs. Presence of dyspnea and septic shock are two clinical signs predictive of mortality. Conclusion : cervicofacial cellulitis is a serious condition. In our study; mortality is 7%, vital prognosis is related to multiple factors.
Résumé : Introduction : La cellulite cervico-faciale est une infection grave qui intéresse les espaces anatomiques délimités par les aponévroses, ces dernières recouvrent les différents organes du cou. Le taux de mortalité de cette pathologie grave varie de 6% à 76%. Le pronostic des cellulites cervico-faciales dépend de plusieurs paramètres, le plus important est la précocité de la prise en charge du patient. Matériels et méthodes : Nous avons mené une étude prospective descriptive et analytique sur une période de cinq ans du 1er Avril 2008 au 1er Avril 2013, qui concerne 69 patients, étudiant les facteurs liés à la mortalité. Cinq cas de mortalité ont été enregistrés. L’analyse statistique était réalisée par le test de Khi2 ou le test de Fischer, le résultat était significatif pour un p<0,05. Résultats : Parmi les 69 cas de cellulites cervico-faciales, nous avons enregistré 5 cas de décès, soit 7,25% des patients. L’âge moyen de nos patients décédés est de 40,8 ans, 80% des patients décédés sont de sexe masculin, de niveau socio-économique bas, presque tous alcoolo-tabagiques et toxicomanes, de mauvaise hygiène bucco- dentaire, d’hygiène bucco-dentaire défectueuse, la majorité sont diabétiques, tous ont été traités par antinflammatoires non stéroïdiens et antibiotiques. En étude analytique, ceux qui sont liés significativement à la mortalité sont : l’absence d’occupation, le niveau socio-économique bas, l’alcoolisme, ainsi que la toxicomanie : le risque de mortalité est multiplié par 15 chez les sujets toxicomanes. Le diabète, le type gazeux de la cellulite, le siège bilatéral, quand il s’agit du germe Bacteroides. La présence de la dyspnée et du choc septique sont deux signes cliniques prédictifs de la mortalité. Conclusion : la cellulite cervico-faciale est une pathologie grave. La mortalité dans notre étude est de 7%, le pronostic vital selon l’étude que nous avons réalisé est fonction de plusieurs facteurs.
Introduction :
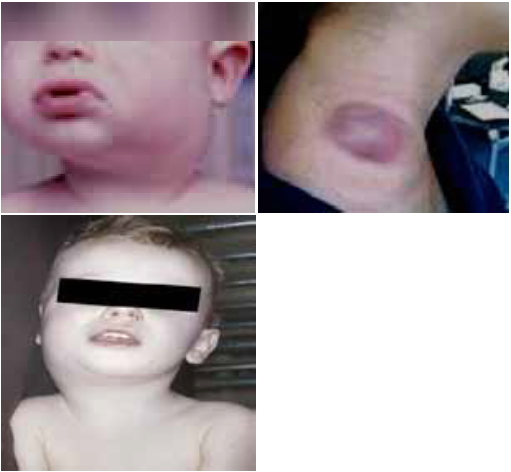
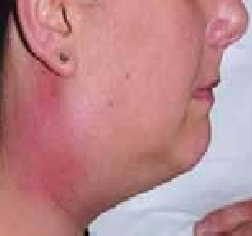
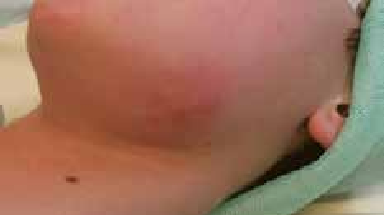
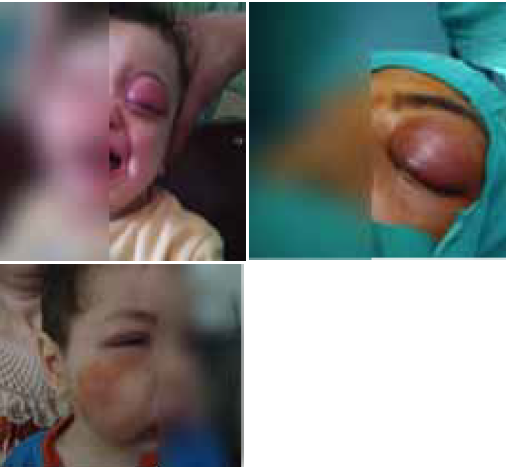
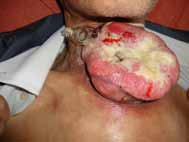
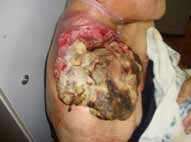
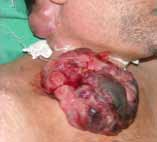
La cellulite cervico-faciale est une infection grave qui intéresse les espaces anatomiques délimités par les aponévroses, ces dernières recouvrent les différents organes du cou (muscles, glandes, viscères, axe vasculaire lui- même composé des gros vaisseaux du cou comme l’axe jugulo-carotidien).
Cet espace anatomique ou tissu celluleux est composé de tissu lymphatique, tissu graisseux, les vaisseaux et les nerfs. La gravité de ces infections réside dans leur évolution rapide vers des complications locales, locorégionales et générales mettant en jeu le pronostic vital, contrastant avec une bénignité apparente des foyers infectieux à l’origine de cette affection [1].
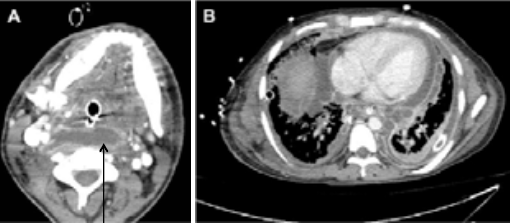
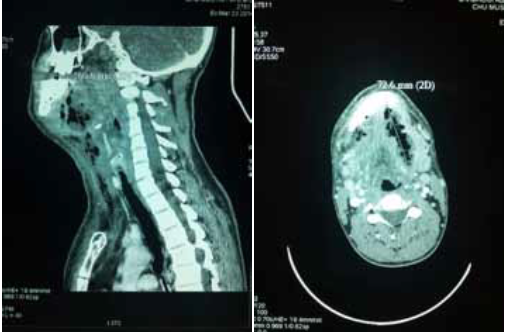
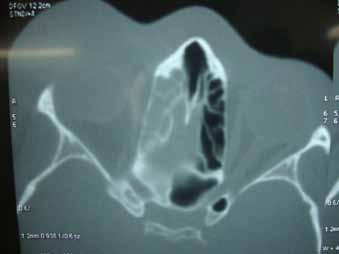
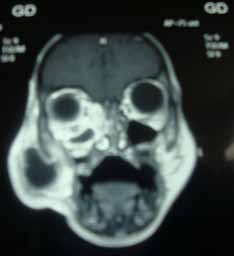
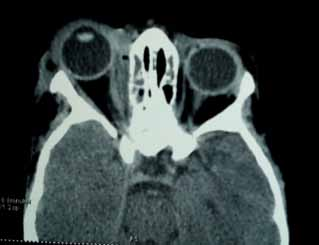
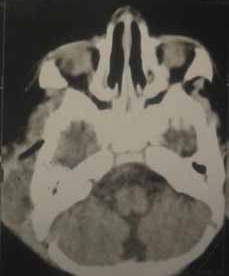
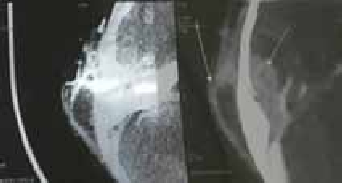
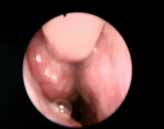
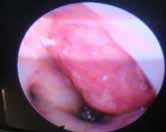
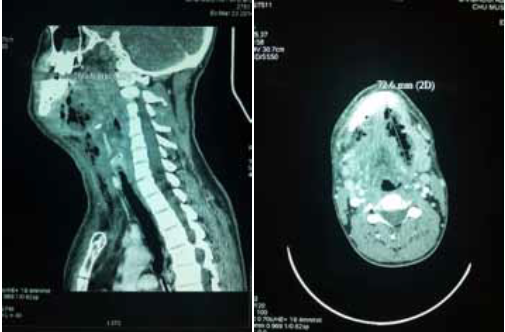
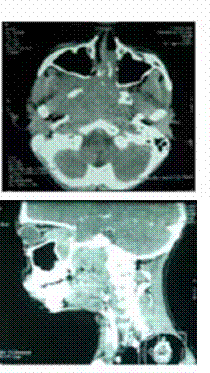
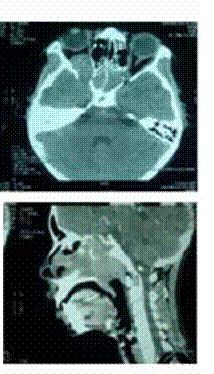
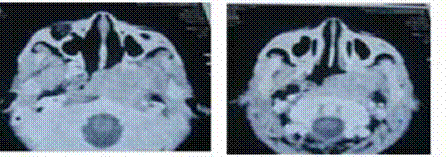
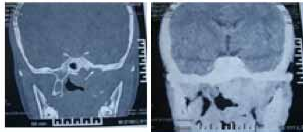
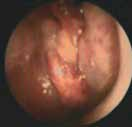
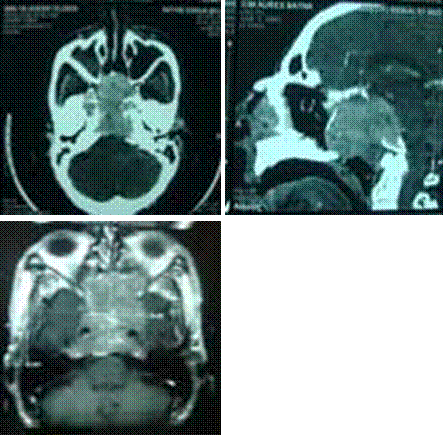
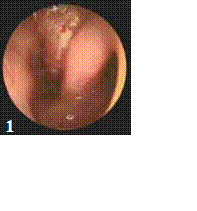
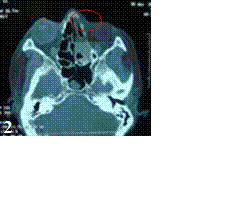
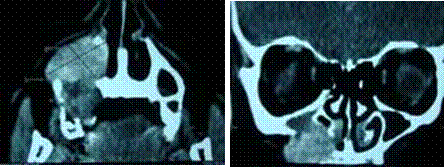
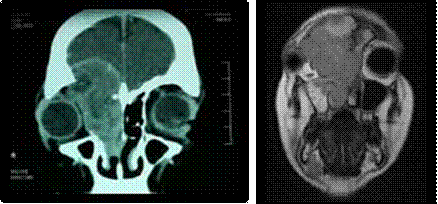
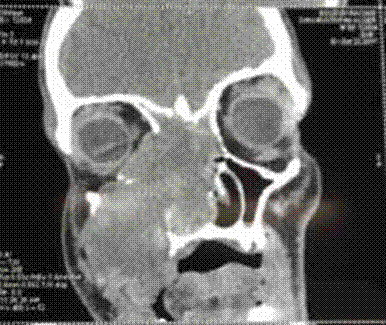
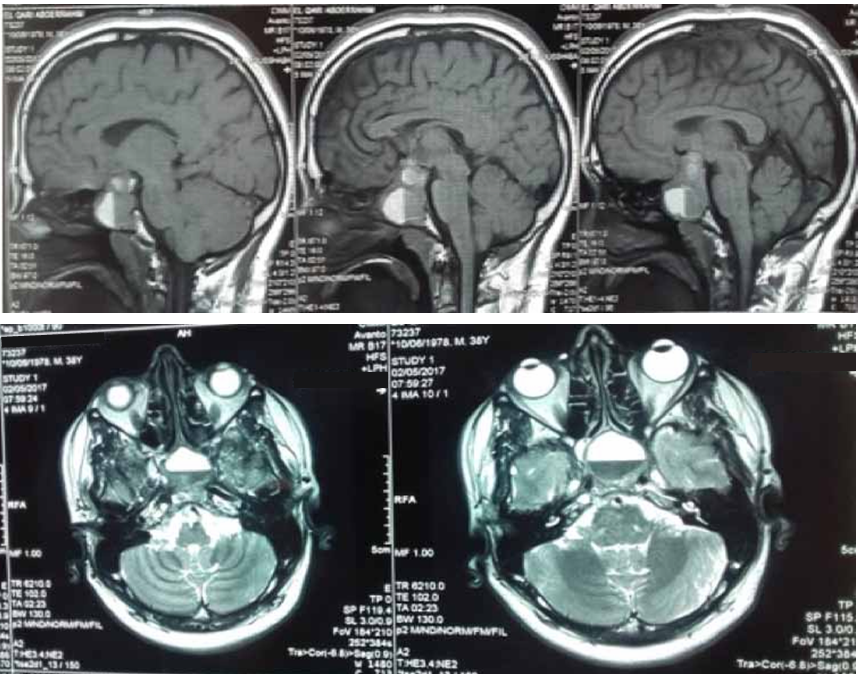
Le diagnostic positif est posé principalement par les données cliniques et les données de la tomodensitométrie.
Le taux de mortalité de cette pathologie grave varie de 6 % à 76 % [2,3].
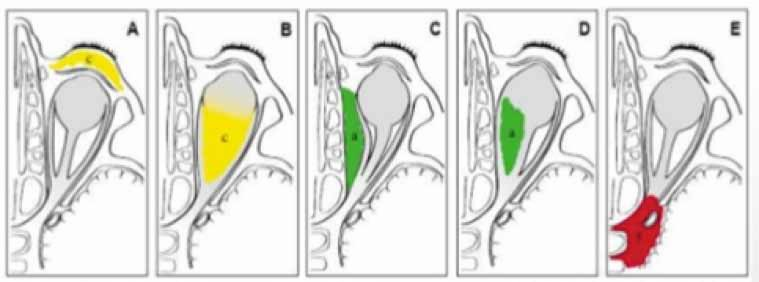
En absence du traitement à temps, l’extension se fait de haut en bas vers le médiastin entrainant une médiastinite elle-même de pronostic très grave, cette extension se fait via les fascias cervicaux selon trois voies de propagation : l’espace rétropharyngé, la gouttière vasculo- nerveuse de chaque côté et l’espace prétrachéal.
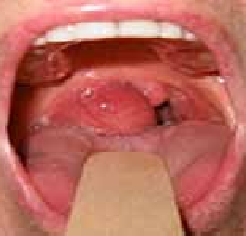
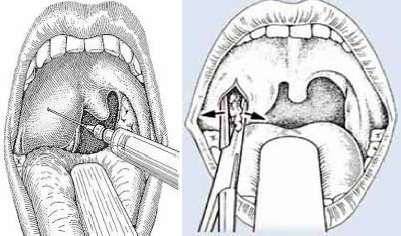
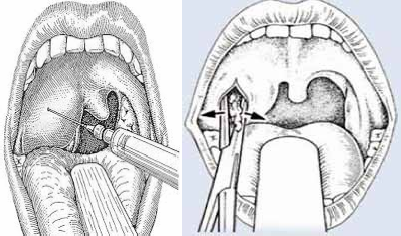
Dans de rare cas, l’extension se fait suite à une thrombophlébite septique, nous citons ici le cas de la veine faciale. L’origine dentaire a été évoquée dans les différentes séries et publications, suivie par les causes amygdaliennes et bucco-pharyngées.
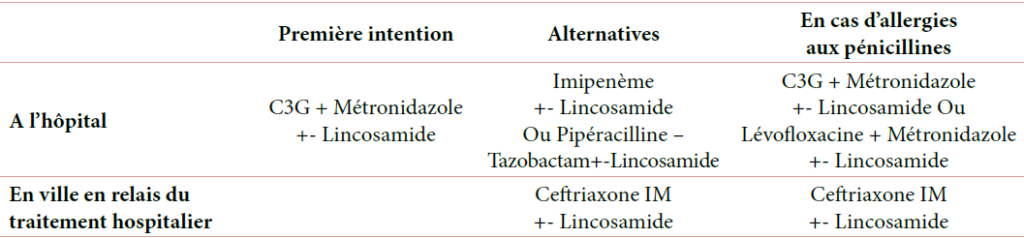
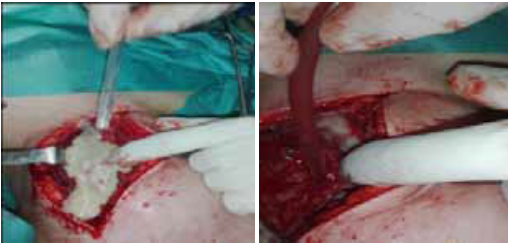
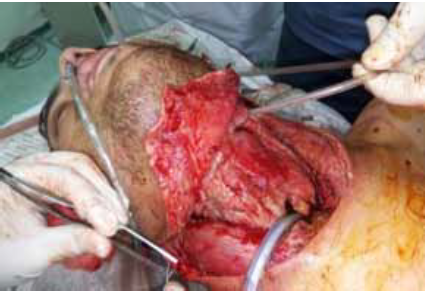
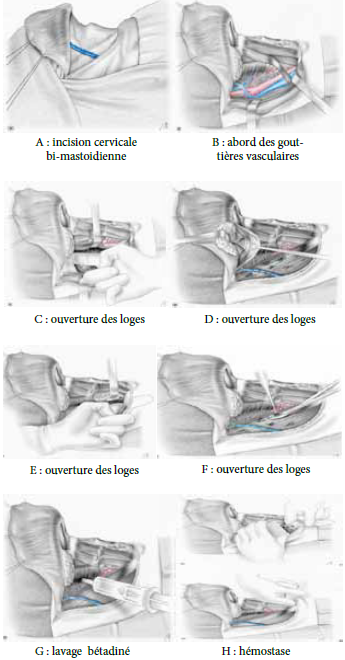
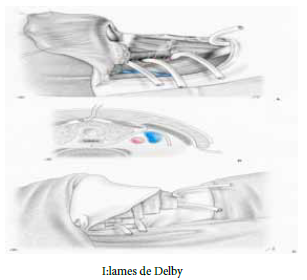
Le traitement est essentiellement chirurgical, consistant à réaliser une incision large en L d’André unilatérale ou bilatérale [6-7-8], une couverture antibiotique associant les bêtalactamines, les aminosides et les imidazolés, c’est le schéma recommandé par plusieurs auteurs [8,7,10,11,2,12].
Le pronostic des cellulites cervico-faciales dépend de plusieurs paramètres, le plus important est la précocité de la prise en charge du patient [3].
Matériels et méthodes :
Il s’agit d’une étude descriptive prospective dans le cadre de l’épidémiologie clinique, étudiant la mortalité des cellulites cervico-faciales suivie d’une étude analytique pronostique.
Notre étude concerne tous les cas de cellulites cervico-faciales vues en urgence, soit au service d’ORL du Centre Hospitalo-Universitaire de Sidi Bel Abbès, soit au service des Urgences Médico-Chirurgicales (UMC) au cours de la période allant du 1er Avril 2008 au 1er Avril 2013, et concerne 69 patients, cinq cas de mortalité ont été enregistrés.
Nous avons inclus dans l’étude tous les patients présentant une cellulite cervico-faciale, de tout âge, des deux sexes, au stade suppuré nécessitant une incision et drainage, nous avons exclu tous les cas de cellulites cervicales séreuses, les cellulites orbitaires, cellulites faciales isolées, abcès superficiels bien limités.
L’analyse statistique était réalisée par le test de Khi2 ou le test de Fischer, le résultat était significatif pour un p < 0,05.
Résultats :
Dans cette étude de 5 années, nous avons enregistré 69 cas de cellulites cervico-faciales, dont cinq patients sont décédés, soit un taux de mortalité de 7,25 % des patients recrutés.
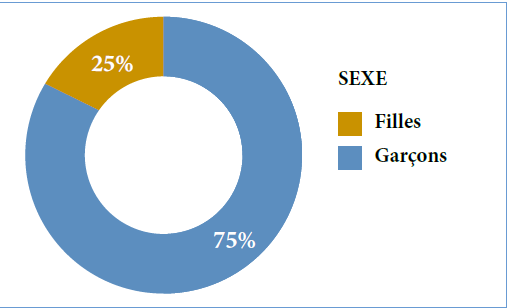
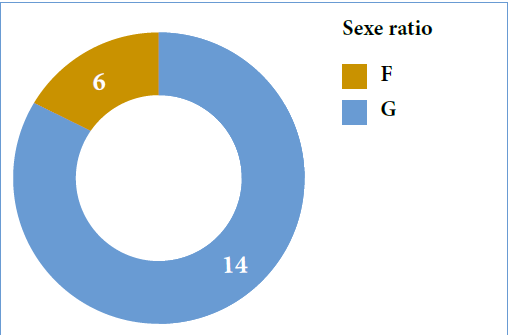
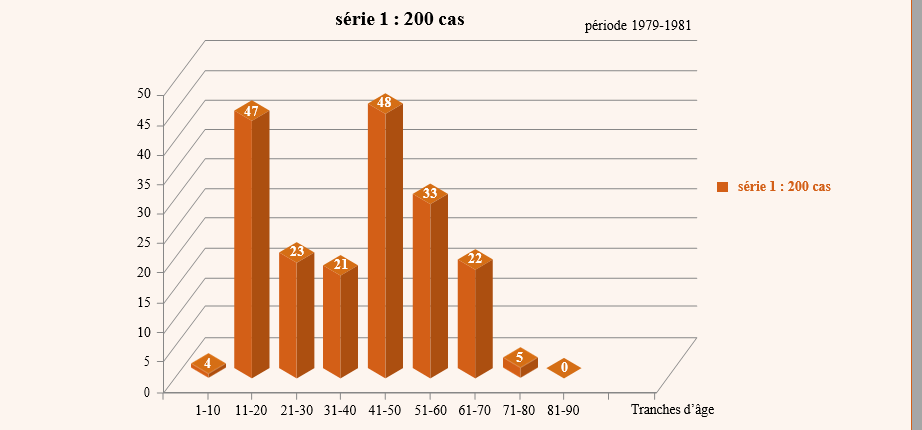
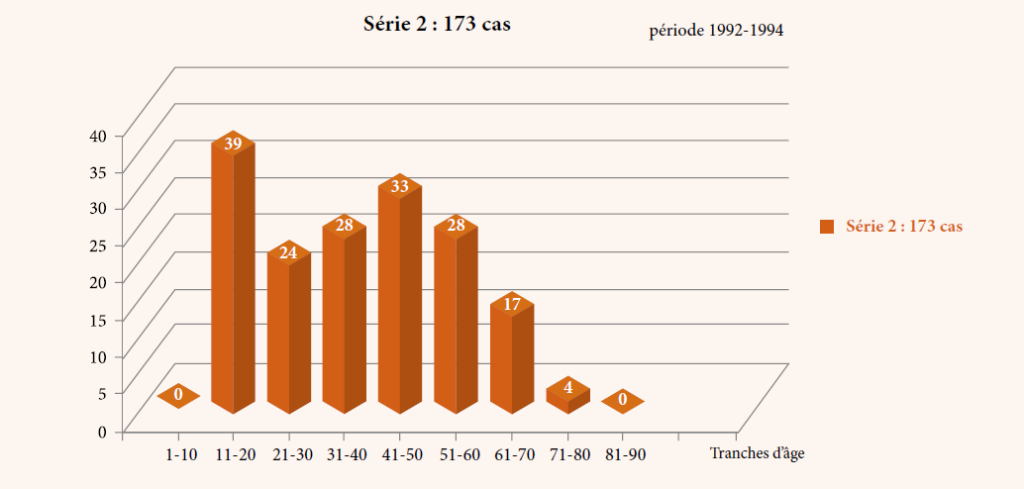
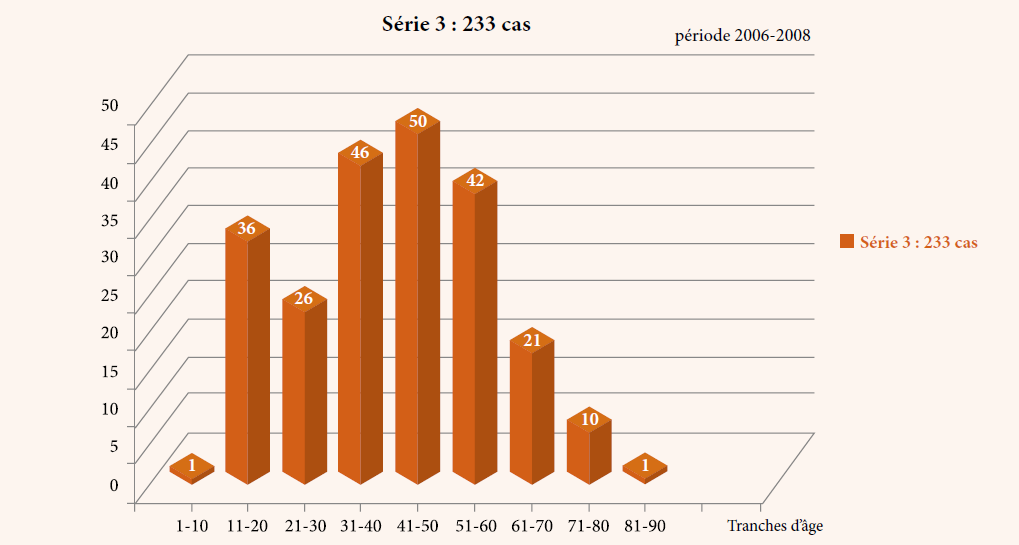
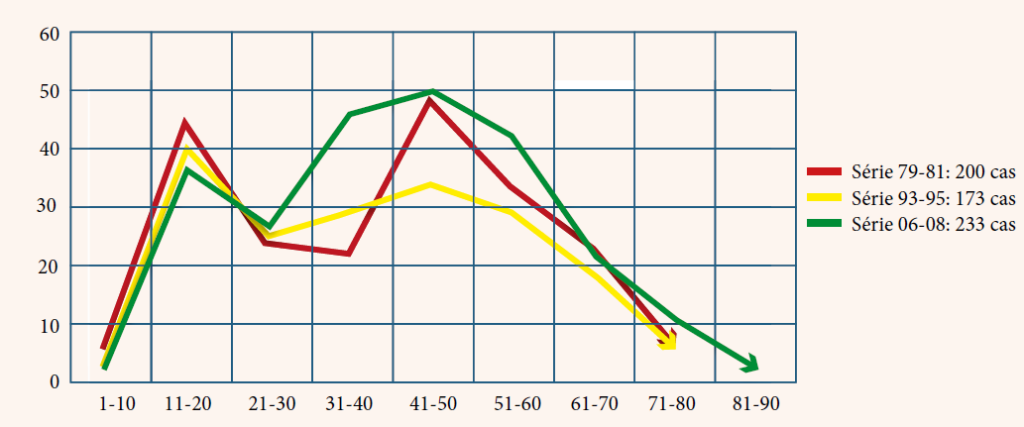
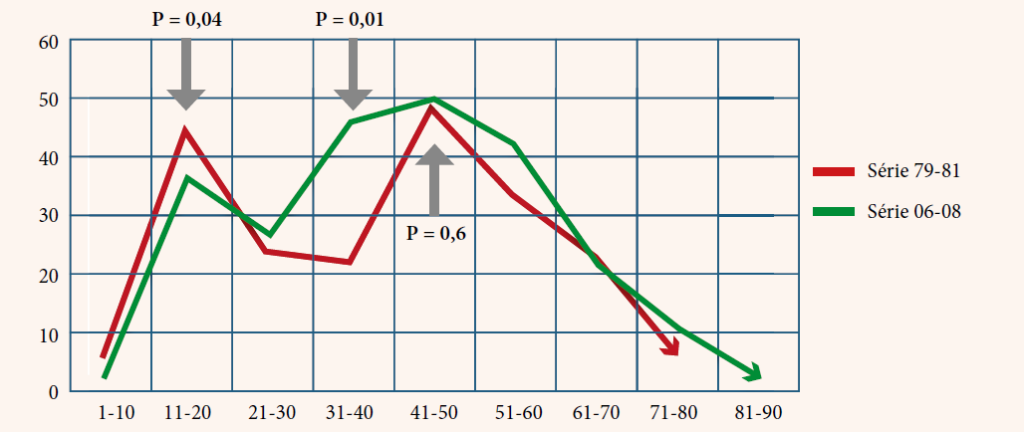
Parmi les 69 patients, nous avons recensé 45 hommes et 24 femmes, l’âge moyen de la série au moment du diagnostic est de 32,35 ans avec un écart-type de 15,12 ans. Parmi les cinq patients décédés, dont quatre hommes et une femme, les caractéristiques sociodémographiques, les habitudes de risque, le type de cellulite, le type de germe responsable, la prise médicamenteuse que ce soit des antibiotiques ou des anti-inflammatoires (stéroïdiens et non stéroïdiens), la cause de la cellulite et la cause de décès sont reportés dans le tableau no1 et no2.
| Patient NO | Âge (Ans) | Sexe | Diabète | HTA* | Tabac | Alcool | Toxicomanie |
| 1 | 36 | M | Oui | Oui | Oui | Oui | Oui |
| 2 | 22 | M | Oui | Oui | Oui | Oui | Oui |
| 3 | 77 | M | Oui | Oui | Oui | Oui | Oui |
| 4 | 34 | M | Oui | Oui | Oui | Oui | Oui |
| 5 | 35 | F | Non | Non | Non | Non | Non |
| Patient NO | AINS* | Antibiotique | Bactériologie | Causes | Type de cellulite | Causes de décès |
| 1 | Oui | Oui | Bacteroides | Dentaire | Phlegmoneuse | Choc |
| 2 | Oui | Oui | Bacteroides + Streptocoque | Dentaire | Gazeuse | Médiastinite |
| 3 | Oui | Oui | Non fait | Dentaire | Gazeuse | Médiastinite |
| 4 | Oui | Oui | Bacteroides | Dentaire | Gazeuse | Médiastinite |
| 5 | Oui | Oui | Non fait | Amygdalienne | Gazeuse | Médiastinite |
L’âge moyen de nos patients décédés est de 40,8 ans avec un écart type de 21,01 ans et des extrêmes de 22 ans et 77 ans. Une prédominance masculine a été remarquée chez les patients décédés soit 80 %, le sexe féminin représente 20% des patients, le diabète a été retrouvé chez 4 patients parmi 5 soit 80 %, deux patients parmi les cinq décédés sont hypertendus, les habitudes de risque représentées par le tabagisme, alcoolisme et toxicomanie sont présentes chez 80 % des cas.
Étude descriptive des cas décédés :
Dans une première étape, nous avons réalisé une étude descriptive des cas décédés, les résultats sont reportés dans le tableau N03.
| Facteurs | Effectifs | Fréquence |
| Féminin | 1 | 20,00 % |
| Masculin | 4 | 80,00 % |
| < 21 ans | 0 | 0,00 % |
| ≥21 | 5 | 100,00 % |
| NSE bon moyen* | 1 | 20,00 % |
| Bas niveau socio-économique | 4 | 80,00 % |
| Tabagisme | 4 | 80,00 % |
| Alcoolisme | 4 | 80,00 % |
| Toxicomanie | 4 | 80,00 % |
| Mauvaise hygiène bucco-dentaire | 5 | 100,00 % |
| Diabète | 4 | 80,00 % |
| HTA* | 2 | 40,00 % |
| AINS* | 5 | 100,00 % |
| AIS* | 1 | 20,00 % |
| ATB* | 5 | 100,00 % |
| Choc septique | 4 | 80,00 % |
| Médiastinite | 4 | 80,00 % |
NSE* : niveau socio-économique, AIS* : anti-inflammatoires stéroïdiens ; ATB* : antibiotique
80 % des patients décédés sont de sexe masculin, tous avaient plus de 20 ans, de niveau socio-économique bas, presque tous alcoolo-tabagiques et toxicomanes, et d’hygiène bucco-dentaire défectueuse, la majorité sont diabétiques, tous ont été traités par anti-inflammatoires non stéroïdiens et antibiotiques, 4 cas parmi les 5 patients décédés sont des médiastinites.
Par la suite, une étude analytique a été réalisée, nous avons étudié les paramètres suivants supposés favorisant de l’aggravation des cellulites cervico-faciales : âge, sexe, comorbidités : hypertension artérielle et diabète, prise médicamenteuse type anti-inflammatoires et anti-biotiques, le germe responsable de la cellulite, le type de cellulite : gazeuse ou phlegmoneuse, l’origine de la cellulite et la cause de décès, les résultats sont reportés dans le tableau No4.
| Facteurs étudiés | Incidence | P | OR |
| Non actif* | 14,29 % | 0,05 | – |
| NSE bas | 16,00 % | 0,05 | 8,19 |
| Alcoolisme | 16,00 % | 0,05 | 8,19 |
| Toxicomanie | 23,53 % | 0,01 | 15,69 |
| Bacteroides | 50,00 % | 0,003 | 30,5 |
| Dyspnée | 20,83 % | 0,004 | – |
| Choc septique | 57,14 % | 0,0002 | 81,33 |
| Diabète | 18,18 % | 0,03 | 10,22 |
| Type gazeux de la cellulite | 23,81 % | 0,002 | – |
Non actif* : concerne tous les patients retraités ou sans profession.
L’incidence de la mortalité identifiée dans deux groupes de patients, le premier présente le facteur, le deuxième n’ayant pas ce facteur, il s’agit de connaitre si le risque de la mortalité est modifié ou majoré, chez un groupe ayant des caractéristiques sociodémographiques particulières, les résultats retrouvés, à savoir que le risque de mortalité est majoré en présence de ces facteurs, et de façon significative : en absence d’occupation, l’incidence passe de 0% en présence d’occupation à 14,29 % en son absence, le p=0,05, le niveau socio-économique bas est également un facteur de mauvais pronostic, le risque de mortalité est multiplié par trois : il existe donc un lien évident et significatif entre ce facteur et la mortalité, le p = 0,05 et le OR est de 8.
Par la suite, nous avons étudié les habitudes de risque qui sont le tabagisme, alcoolisme, et toxicomanie, l’incidence de la mortalité est majorée par les habitudes et les comportements à risque, tous les chiffres d’incidence sont élevés en leur présence à des degrés différents : chez un patient atteint de cellulite cervico-faciale, la liaison est significative entre l’alcoolisme et la survenue de la mortalité avec un p=0,05 et un OR à 8,19 ; ainsi qu’avec la toxicomanie dont les paramètres d’association sont plus prononcés comme le montre le P qui a une valeur égale à 0,01, et un OR de 15,7 donc le risque de mortalité est multiplié par 15 chez les sujets toxicomanes.
Par contre et de façon plus ou moins inattendue le tabagisme n’est pas un facteur augmentant le risque de mortalité, bien que l’incidence soit plus élevée chez les tabagiques.
Dans l’ensemble, les patients hospitalisés pour une cellulite cervico-faciale et atteints d’une comorbidité: diabète et hypertension artérielle, s’exposent à un risque plus grand de mortalité, comme le montrent les incidences plus élevées chez les patients diabétiques (18,18 %) et/ ou hypertendus (15,38 %) par rapport aux non diabétiques et/ou non hypertendus, mais on constate une relation significativement prouvée entre la mortalité et le diabète avec un p=0,03, OR=10,22 donc le risque de mortalité est multiplié par 10 en présence du diabète.
Dans le même sens, les anti-inflammatoires et les antibiotiques ne sont pas des facteurs prédictifs de mortalité.
Pour le type de cellulite cervico-faciale, la mortalité est en fonction du type gazeux, la relation est significative (le p=0,002), les Bacteroides sont statistiquement liés à la mortalité, 50% des patients qui en sont atteints décèdent, contre seulement 3% dans le cas d’autres germes, la liaison est très significative p=0,003, et le OR=30,5.
Deux signes cliniques sont de très mauvais pronostic : la présence de la dyspnée et le choc septique avec un P égal respectivement à 0,0037 et 0,002.
La plupart des cas décédés avait une cellulite cervico-faciale d’origine dentaire, et 80% des causes de décès sont des
médiastinites, pour rappel le taux de médiastinite dans notre série de 69 patients est de 11,59% soit 8 cas de médiastinite et le taux de mortalité dans ces cas est de 50%.
Discussion :
La gravité des cellulites cervico-faciales réside dans ses complications qui sont souvent mortelles, le chirurgien est appelé à les diagnostiquer le plus tôt possible afin de prévenir l’issue fatale.
Le taux de mortalité de notre série de cellulites cervico-faciales est de 7,25 %.
La plupart des études retrouvent un chiffre qui varie entre 6 et 20%, notre chiffre se rapproche de celui de Patrice TRAN BA HUY [3] et Franck Petitpas [18] qui ont retrouvé un taux de 8%, au-dessous de celui retrouvé dans l’étude de Mohammedi [11] où le taux de mortalité est de 15%, Bontjan Laninnik [20] a trouvé un taux de mortalité de 3,5%.
Sung Youl Hyun [21] : dans une série de 30 patients a trouvé un taux de mortalité de 13,33%.
A. Jose [22] dans une étude en 2014 en Espagne a rapporté un taux de mortalité des cellulites cervico-faciales qui varie entre 7 à 20%, et dans les cellulites cervico-médiastinales la mortalité arrive à 41 %.
Selon Ramaraj et all [23] les cellulites dentaires seules présentent une mortalité de 19,2 %.
Notre étude analytique a permis de dégager et d’une manière objective les facteurs pronostiques :
1. Facteurs significatifs liés à la mortalité :
- Le niveau socio-économique bas (p=0,05),
- Sans profession et retraités (p=0,05),
- L’alcoolisme (p=0,05),
- Toxicomanie (p=0,011),
- Diabète (p=0,0329),
- Extraction dentaire (p=0,0026),
- Cellulites de type gazeux (p=0,002),
- Le germe responsable type Bacteroides (0,0035),
- Présence de dyspnée (p=0,0037),
- Présence du choc septique (p=,00019).
2. Facteurs tendant à la signification :
- Caries dentaires (p=0,161),
- Douleurs thoraciques (p=0,16).
3. Facteurs non significatifs : tous les autres facteurs ne sont pas significatifs.
Selon t. Backer [24], la mortalité est secondaire à l’insuffi- sance respiratoire, sepsis et défaillance multiviscérale [8]. Ces facteurs sont retrouvés dans notre étude avec une liaison très significative avec la mortalité
Ulubil et all [25] ont rapporté les facteurs de mauvais pronostic pour les cellulites cervico-faciales qui sont : âge avancé, retard thérapeutique, sexe féminin, diabète déséquilibré, atteinte pulmonaire associée et extension médiastinale. Parmi tous ces facteurs ; selon Nagendra Srinivas Chunduri et all [17], 4 facteurs conduisent à la morbi-mortalité :
- Le retard du traitement.
- Traitement inapproprié et incomplet notamment chirurgical.
- Association à une débilité.
- Infection polymicrobienne
Ces deux derniers facteurs, ont été confirmés par notre étude, comme des facteurs prédictifs de la mortalité.
| Les études | Taux de mortalité |
| Jose A. Tomas [19] | 7%-20 % |
| I. Mohammedi[11] | 15 % |
| Patrice tran ba huy [3] | 7,3 % |
| Sung YoulHyun [21] | 13,33 % |
| BontjanLaninnik [20] | 3,5 % |
| Bettina hohlweg-majert [2] | 19,2 % |
| N. Skitarelic [14] | 16-20 % |
| Jinn-Ming Wang [9] | 20,9 % |
| Gino Marioni [16] 2006 | 25,5 % |
| Nicholas P. [5] | 40 % |
| Notre serie | 07,24 % |
La plupart des études déclarent un taux élevé de mortalité en présence de médiastinite, ce taux s’élève à 50 % [13], et pour Lingaraj JB jusqu’à 40 % [15].
Gino Marioni [16] dans une étude analytique et descriptive a trouvé un taux de mortalité de 19 % ; les facteurs liés à la mortalité d’une manière significative sont l’association au diabète et de l’alcoolisme, [16] les mêmes résultats sont obtenus dans notre étude, pour d’autres auteurs le taux de mortalité varie entre 19 et 40 % [10], la lutte contre la mortalité commence par la prévention de ces facteurs.
Conclusion :
La cellulite cervico-faciale est une pathologie grave. La mortalité dans notre étude est de 7 %, le pronostic vital selon l’étude que nous avons réalisé est fonction : du choc septique, de la dyspnée, type gazeux de la cellulite,
Références :
- El Moussaoui, a. Bencheqroun. Une complication redoutable d’une cellulite cervicale après extraction dentaire. Journal européen des ur- gences, november 2007 volume 20, issue 3, pages 120-123.
- Bettina hohlweg-majert, nilsweyer, c. metzger, ralfschön. Cervico- facial necrotizing fasciitis. Diabetes research and clinical practice, may 2006 volume 72, issue 2, pages 206-208
- Patrice Tranbahuy, Jean-Philippe Blancal, Benjamin Verillaud, Alexandre Mebazaa, Philippe Herman. cervico-facial fascitiis. a major entemergency. bull. acad. natle méd. 2011, 195, no 3, 661-678
- R. J. Balcerak, J.M. Sisto, R.C. Bosack. Cervico-facial necrotizing fasciitis : .journal of oral and maxillofacial surgery, june 1988, volume 46, issue 6, pages 450-459
- Nicholas P. Mastros, Michael, Broniatowsk. Otolaryngology – head and neck surgery, January 1998,volume 118, issue 1, pages 140-141
- Pierre Gehanno, Joël Depondt. Chirurgie des cellulites cervico-me- diastinale. EMC techniques chirurgicales – tête et cou (1997) [46-535]
- Johnny C. Mao, Michael A. Carron, Kimberly R. Fountain, Robert J. Stachler, George H. Yoo, Robert H. Mathog, James M. Coticchia. craniofacial necrotizing fasciitis with and without thoracic extension: management strategies and outcome american journal of otolaryngo- logy, january-february 2009,volume 30, issue 1,pages 17-23
- Righini, E. Motto, G. Ferretti, K. Boubagra, E. Soriano, E. Reyt. Cellulites cervicales extensives et mediastinite descendante nécro- sante annales d’otolaryngologie et de chirurgie cervico-faciale, 2007, december, volume 124, issue 6, pages 292-300
- Jinn-Ming Wang, Hwee-Kheng Limb. Necrotizing fasciitis: eight- year experience and literature review. The Brazilian journal of infec- tious diseases.2013, 276; pages 7
- W.J. Zhang, X.Y. Cai, C. Yang, I.N. Zhou, I.Y. Zheng, B. Jiang. cer- vical necrotizing fasciitis due to methicillin-resistant staphylococcus aureus: a case report. international journal of oral and maxillofacial surgery, august 2010, volume 39, issue 8, pages 830-834
- Mohammedi, P. Ceruse, S. Duperret, J.M. Vedrinne. cervical ne- crotizing fasciitis: 10 years’ experience at a single institution. intensive care med (1999) 25: 829-834
- N.K. Sahoo, Kapiltomar. Necrotizing fasciitis of cervico-facial region due to odontogenic infection-journal of oral and maxillofacial surgery, medicine, and pathology, january 2014,volume 26, issue 1, pages 39-44;
- Franck Petitpas, Joaquim Mateo, Jean-Philippe Blancal, Olivier Mimoz. fasciites cervicales necrosantes. le praticien en anesthesie reanimation, february 2010 volume 14, issue 1, pages 4-8.
- N. Skitarelic, R. Mladina, M. Morovic, N. Skitarelic. Cervical Ne- crotizing Fasciitis: Sources and Outcomes-Infection 31 · 2003 · No. 1
- Langaraj JB, Sanjayrao, Kotrashettism, Chintannarad necrotizing cervical fasciitis: a case report and review of literature. J. maxillofac oral surg . 2009, 9(1):54-56
- Ginomarioni, Robertorinaldi, Giancarlo Ottaviano, Rosario Marchese-Ragona, Marina Savastano, Alberto Staffieri. cervical ne- crotizing fasciitis a nouvel clinical presentation of burkholderiacepa- cia infection-journal of infection, november 2006, volume 53, issue 5, pages 219-222
- Nagendra Srinivas Chunduri, Krishnaveni Madasu, Praveen Shri- mant Tammannavar, Pushpalatha-Necrotising fasciitis of odontoge- nic origin-BMJ Case Rep 2013.
- Franck, Petitpas, Philippe Blancal, Catherine Beigelman, Mourad
- Boudiaf, Didier Payen, Philippe Herman, Alexandre Mebazaa. factors associated with the mediastinal spread of cervical necrotizing fasciitis. Ann thorac surg 2011.2011.09.012
- Jose A. Tomás, Luis M. Floría, José Delhom, Mari C. Baquero- Cervical necrotizing fasciitis of non-odontogenic origin-American Journal of Emergency Medicine 32 (2014) 1441.e5–1441.e6
- Lanisnik, B. Cizmarevic, D. Debevc, P. Levart. Necrotizing fasciitis of the head and neck: 34 cases of a single institution experience. eur arch otorhinolaryngol (2010) 267:415–421
- Sungyoulhyun, Heekyun Oh, Jae Young Ryu Jinjookim, Ji- nyongcho, Hyeon Min Kim. closed suction drainage for deep neck infection original. journal of cranio-maxillofacial surgery, november 2013.
- Aldo Suárez. Tomás, Luis M. Floría, José Delhom, Mari C. Ba- quero-Cervical necrotizing fasciitis of non-odontogenic origin Case report and review of literature- Journal of Otolaryngology and Head and Neck Surgery Vol. 58, No. 2, April-June 2006.