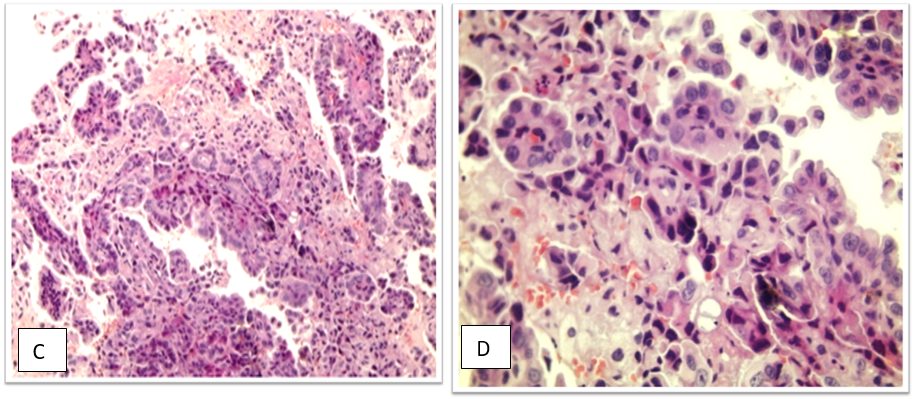
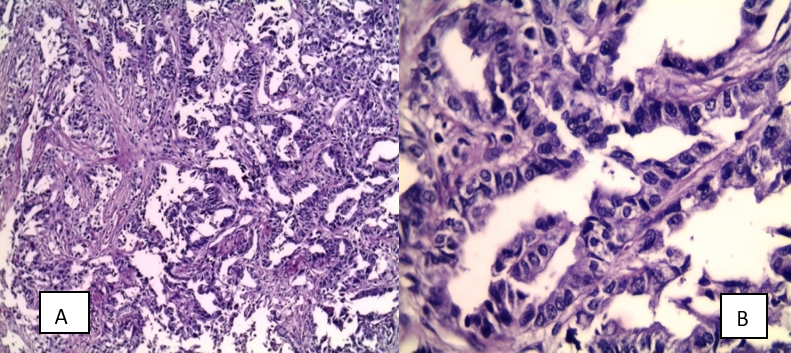
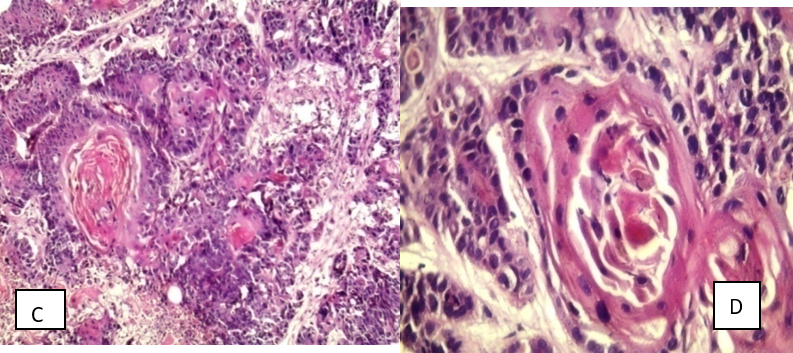
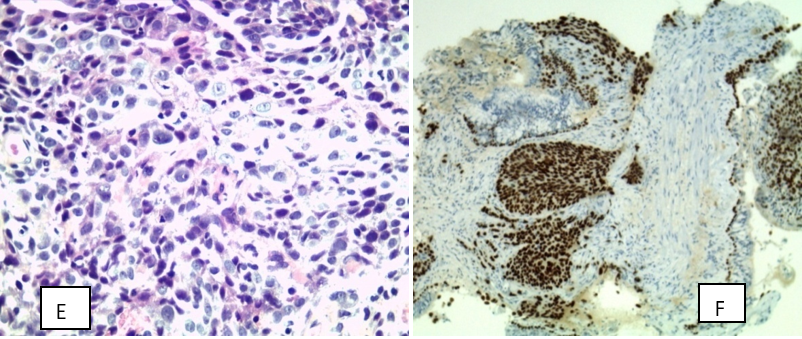
La radiothérapie est une arme thérapeutique incontournable dans la prise en charge des cancers bronchiques non à petites cellules non métastatiques qui s’inscrit avec la chirurgie et les traitements systémiques, la chimiothérapie, les thérapies ciblées et l’immunothérapie, dans une approche pluridisciplinaire.
A. Boukerche, Service de Radiothérapie – EHSO Emir Abdelkader, Oran. Faculté de Médecine, Université d’Oran 1.
Date de soumission : 27 Janvier 2021
Abstract: Radiotherapy is an essential therapeutic weapon in the management of non-small-cell non-metastatic lung cancer which is combined with surgery and systemic treatments, chemotherapy, targeted therapies and immunotherapy, in a multidisciplinary approach. Our objective is to describe the principles of conformational radiotherapy in 3 dimensions (RT-3D) thoracic used routinely, certain new techniques: conformational radiotherapy with intensity modulation (RCMI), radiotherapy in stereotactic conditions (SBRT), respiratory gated radiotherapy (Gating) and to address the indications for radiotherapy in non-small cell, non-metastatic lung cancer.
Keywords: Non-small-cell non-metastatic lung cancer, indication of radiotherapy, 3-D Conformal radiotherapy.
Résumé : La radiothérapie est une arme thérapeutique incontournable dans la prise en charge des cancers bronchiques non à petites cellules non métastatiques qui s’inscrit avec la chirurgie et les traitements systémiques, la chimiothérapie, les thérapies ciblées et l’immunothérapie, dans une approche pluridisciplinaire. Notre objectif est de décrire les principes de la radiothérapie conformationnelle en 3 dimensions (RT-3D) thoracique utilisée en routine, certaines nouvelles techniques : radiothérapie conformationnelle avec modulation d’intensité (RCMI), radiothérapie en conditions stéréotaxiques (SBRT), radiothérapie asservie à la respiration (Gating) et d’aborder les indications de radiothérapie dans les cancers bronchiques non à petites cellules non métastatiques.
Mots clés : Cancer bronchique non à petites cellules non métastatique, indication de la radiothérapie, radiothérapie conformationnelle 3 D.
Introduction
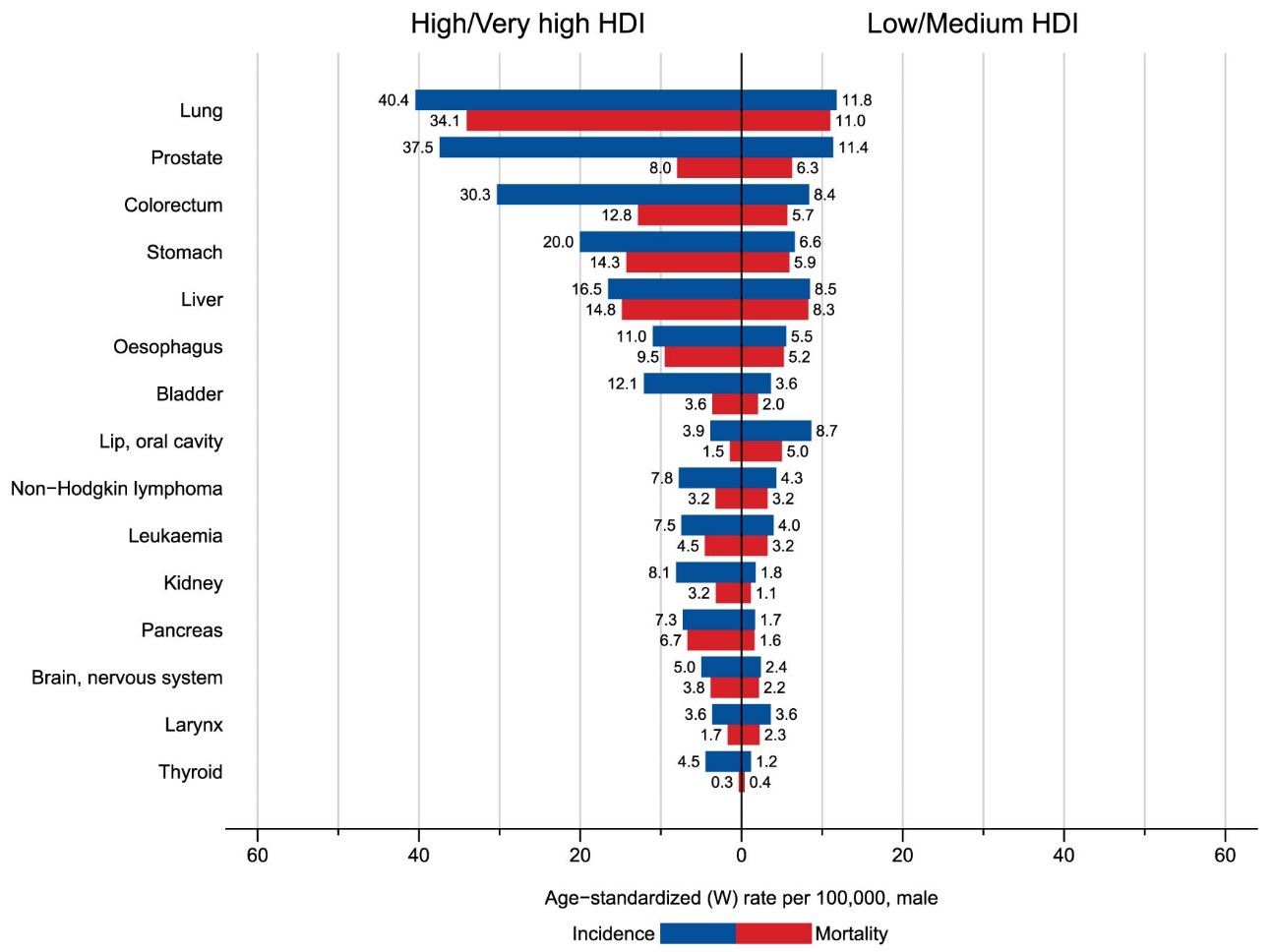
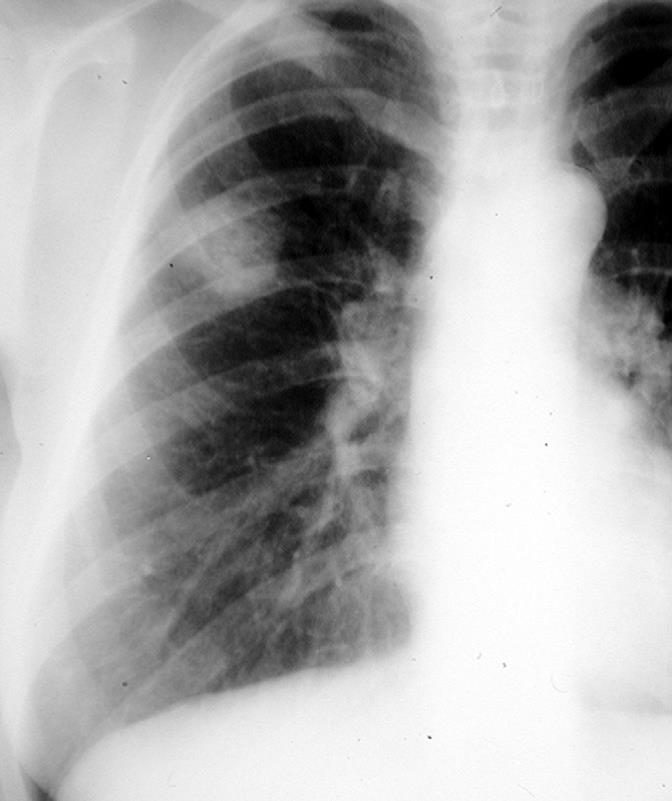
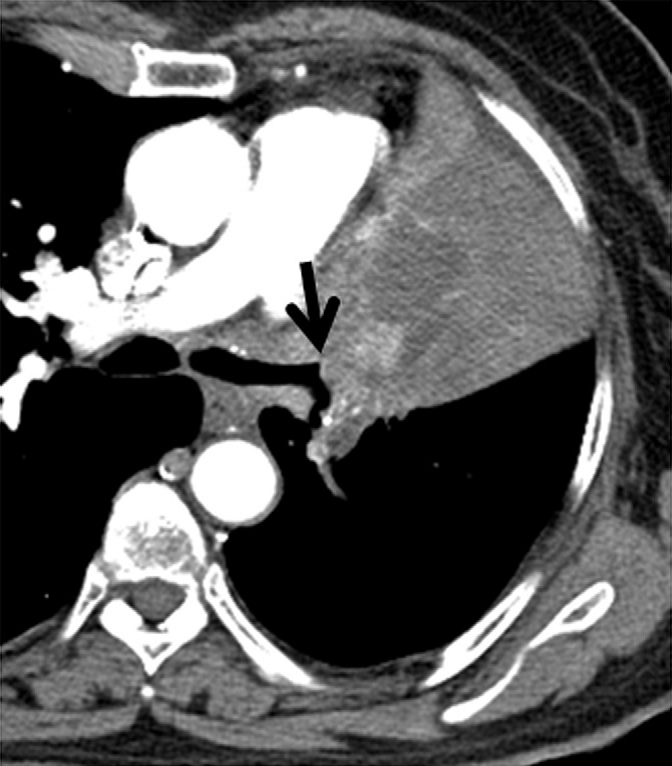
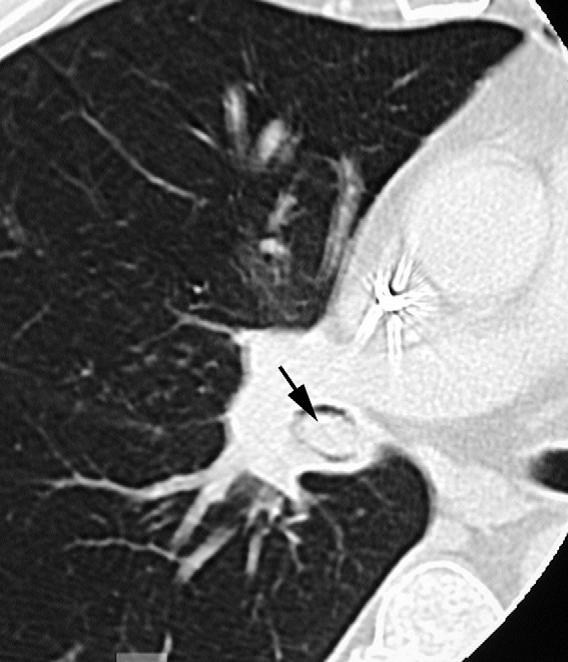
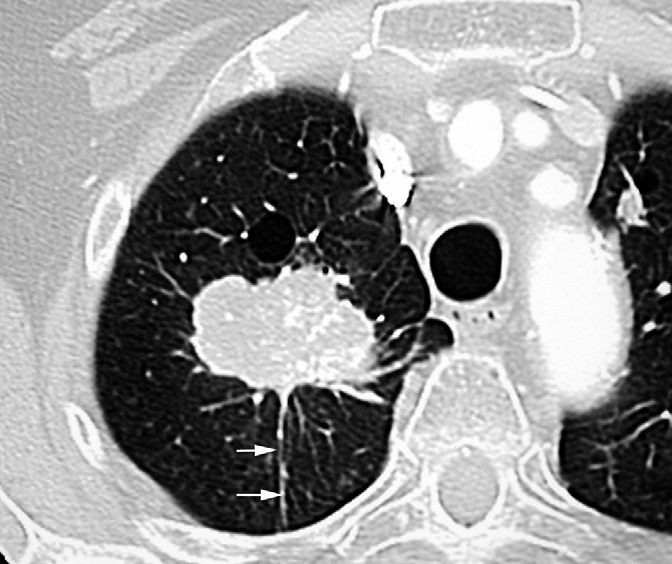
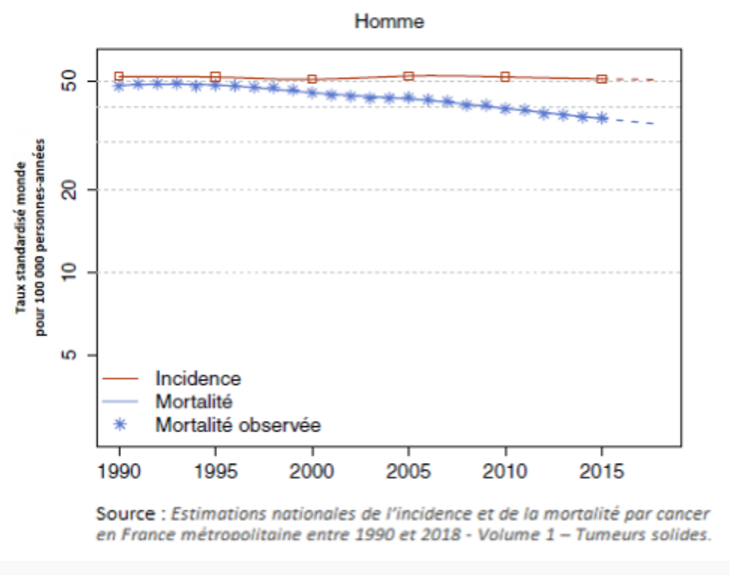
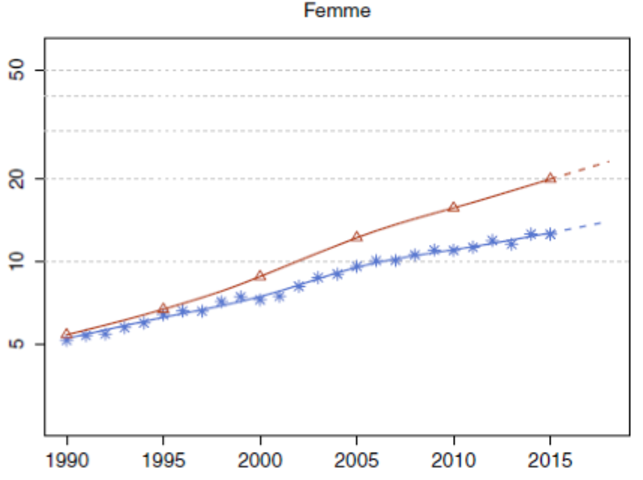
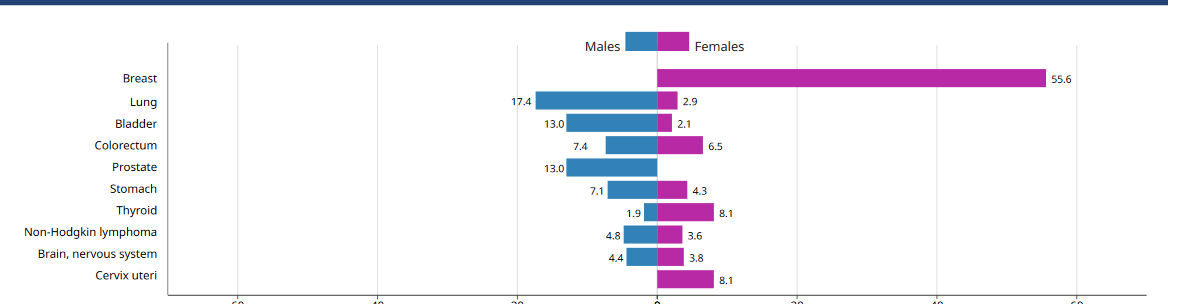
Les formes dites « non à petites cellules » représentent environ 85% des cancers du poumon et constituent l’histologie prédominante. Réputée de pronostic sombre, la survie de ces cancers est étroitement liée au stade de la maladie lors de son diagnostic et à sa prise en charge. Tous stades confondus, leurs taux de survie globale à 5 ans sont estimés autour de 14% à 20% [1-2].
Indications de la radiothérapie dans les stades non métastatiques
La stratégie thérapeutique initiale des cancers du poumon non à petites cellules est orientée grâce à la classification selon leur stade Tumor Node Metastasis (TNM) de l’Union Internationale Contre le Cancer (UICC) [8eme édition]. La détermination des volumes d’intérêt (volumes cibles et organes à risque), ainsi que la prescription des doses constituent des étapes clés pour la réussite du plan personnalisé du patient.
Stade I et II
La chirurgie représente la principale arme thérapeutique contre ces tumeurs. La radiothérapie normo fractionnée à visée curative est indiquée chez les patients non opérables ou refusant la chirurgie si l’état respiratoire du patient le permet. L’irradiation ne concernera que les volumes tumoraux. Pour les stades II, une radiothérapie post-opératoire peut être discutée en cas d’exérèse incomplète ou atteinte pariétale ; alors que pour les stades I, la radiothérapie en condition stéréotaxique devient une option thérapeutique [3,4].
Stade III et II
Pour les stades III résécables, il n’existe pas une attitude thérapeutique standardisée. La prise en charge repose sur un traitement multimodal, associant la chimiothérapie et la radiothérapie, voire la chirurgie. Pour les stades III non résécables, la chimioradiothérapie concomitante constitue le traitement de référence, mais elle doit être réservée aux patients en bon état général (indice de performance 0 ou 1), âgés de moins de 70 ans avec peu de maladies associées. Alors que pour les autres patients pour lesquels une chimioradiothérapie est difficile à réaliser, en raison de l’âge, de comorbidités associées, d’une altération de l’âge ou d’un important volume tumoral, le traitement séquentiel garde sa place. La radiothérapie exclusive peut être proposée. En situation postopératoire, les stades pN2 et les stades pT3R0 sont discutées en réunion de concertation pluridisciplinaire. Pour les stades pT3R1, la radiothérapie adjuvante constitue un standard [5-9].
Radiothérapie conformationnelle en 3 dimensions (RT 3D)
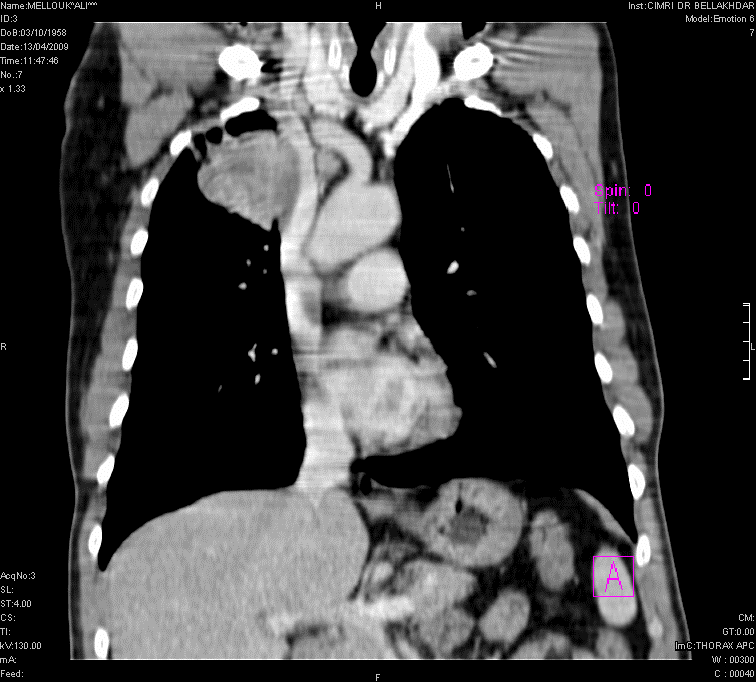
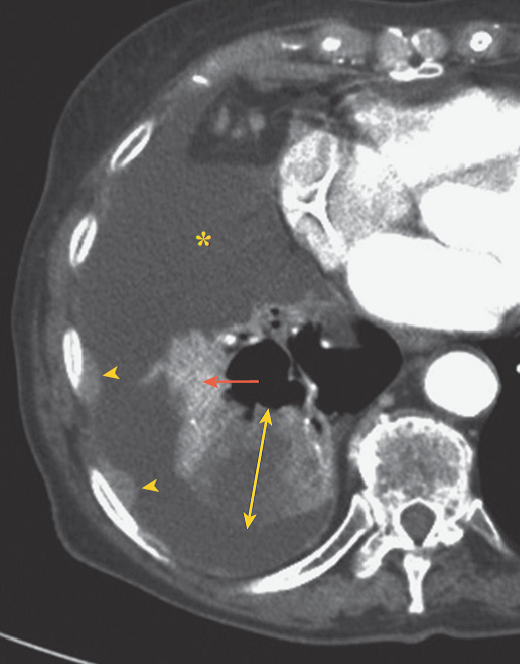
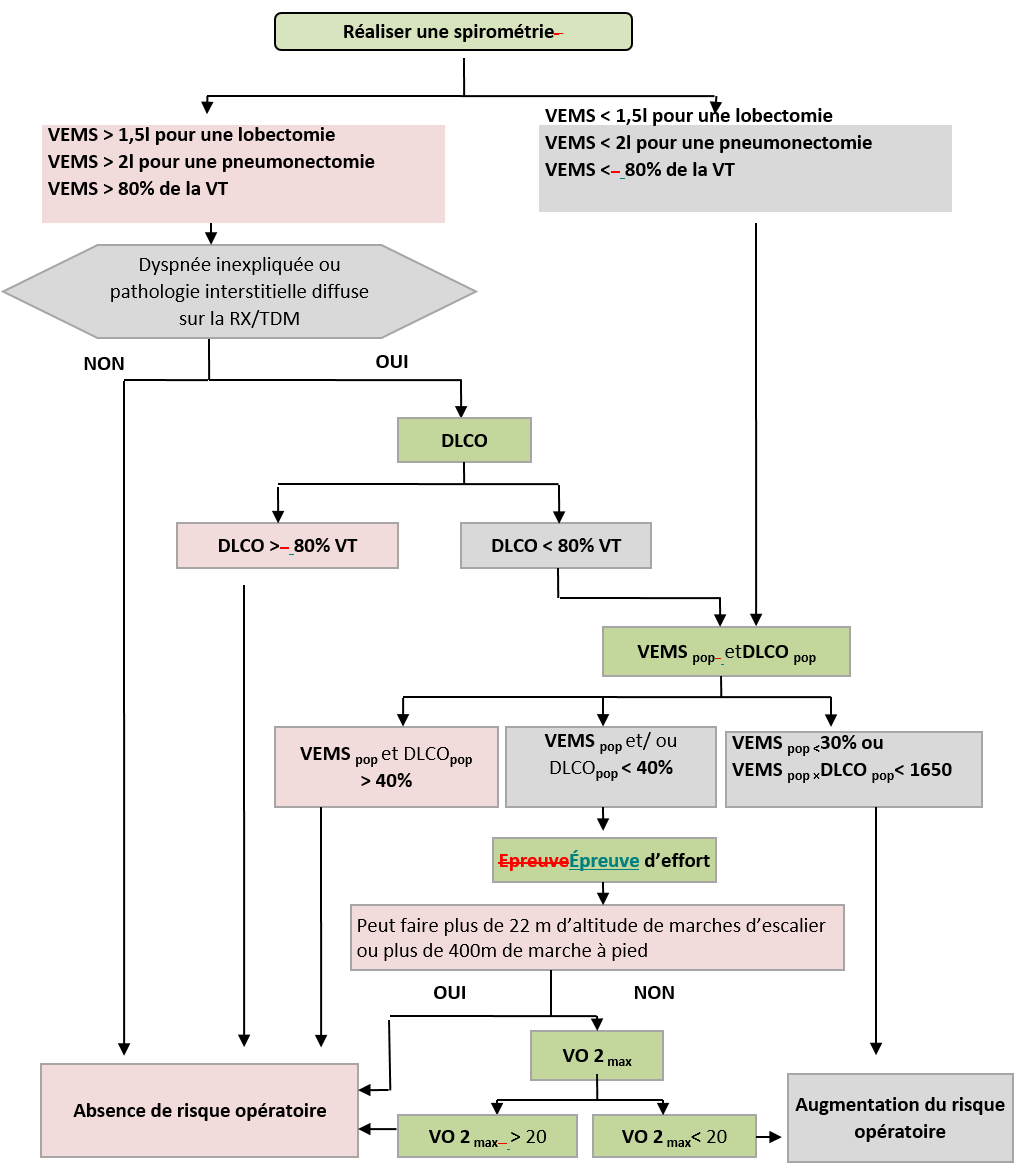
La RT 3D thoracique est la technique standard utilisée en routine pour les tumeurs en place ou en situation post-opératoire. Elle nécessite une évaluation préalable de la fonction respiratoire (VEMS et DLCO) et l’obtention du TEP scan du bilan diagnostique, qui permet de distinguer la tumeur de l’éventuelle atélectasie d’aval et de repérer les adénopathies. Une IRM d’évaluation peut être indiquée pour les tumeurs de l’apex ou situées dans la gouttière costo-vertébrale [10-11].
- Délinéation des volumes d’intérêt
Avant tout traitement, il est important de délinéer les volumes d’intérêt : volumes cible et organes à risque.
Pour cela, l’acquisition des données anatomiques doit être la plus précise possible. Elle est réalisée à l’aide d’une scanographie en position de traitement : en décubitus dorsal, avec le plus souvent un simple repose-bras ou un système d’immobilisation personnalisé pour améliorer la reproductibilité, les bras au-dessus de la tête ou le long du corps en cas de tumeur apicale, avec une injection de produit de contraste, après vérification de la clairance de la créatinine. Elle doit couvrir l’ensemble des structures anatomiques d’intérêt (poumons en totalité, cœur, œsophage, moelle épinière.). Habituellement, sa limite supérieure est la glotte et la limite inférieure est l’interligne L1–L2. L’épaisseur des coupes doit être inférieure à 5 mm ; une épaisseur de 2,5 mm est recommandée pour avoir une acquisition de qualité [12].
- Volume cible
Il comporte selon les situations cliniques : la tumeur, les adénopathies et les aires ganglionnaires atteintes selon la classification de Mountain. En cas de tumeur de l’apex ou d’atteinte massive des aires médiastinales hautes sous-jacentes (aire 1 et 2), l’aire sus claviculaire est irradiée. En cas de chimiothérapie néoadjuvante, le volume cible macroscopique correspond au volume tumoral initial d’avant la chimiothérapie à l’exception de la présence d’une importante atélectasie [13-15].
Le volume tumoral macroscopique (GTV T et GTV N)
Il correspond à la tumeur pulmonaire (GTVT) et aux adénopathies visibles à l’imagerie (GTVN). La définition de la fenêtre de contourage optimale pour la scanographie est importante. Pour la visualisation de la tumeur intra parenchymateuse, les valeurs optimales sont un niveau de –600 unités Hounsfield (UH) et une fenêtre de ±1600 UH ; et pour le médiastin, les valeurs optimales sont un niveau de +20 UH et une fenêtre de ±400 UH. Pour la tomographie par émission de positons (TEP), il n’y a pas de valeurs recommandées. Tout ganglion est considéré comme pathologique si son petit diamètre est supérieur à 1 cm, s’il fixe sur la TEP ou en cas de confirmation histologique de l’atteinte histologique (Prélèvement par médiastinoscopie, échoendoscopie bronchique…) [16-18].
Le volume cible anatomoclinique (CTV)
Il inclut le volume tumoral macroscopique de plus la maladie infraclinique :
Le CTVT : autour du GTVT, une marge est à ajouter. Elle doit tenir compte de l’envahissement tumoral microscopique non visible à l’imagerie. Cet envahissement varie de 5 à 8 mm selon le type histologique. Il inclut la bronche souche, le hile homolatéral et les éventuelles extensions de la plèvre médiastinale péri-tumorale en cas de situation postopératoire [19].
Le CTVN : pour les ganglions envahis, il est recommandé une marge de 5-8 mm autour du GTVN en fonction de la taille du ganglion et du type histologique de la tumeur primitive [19-21]. Lorsque la radiothérapie postopératoire est indiquée dans les stades localement avancés, le CTV comprend le moignon bronchique, les aires ganglionnaires médiastinales envahies selon le compte rendu histologique, le hile homolatéral et les aires ganglionnaires 4 et 7 [22].
Le volume cible prévisionnel (PTV)
La valeur de la marge autour du CTV est déterminé pour chaque centre en fonction de la technique utilisée ou la procédure de traitement. Le plus souvent, il s’agit d’une marge de 5 à 10 mm. Cette marge se décompose en marge pour tenir compte des mouvements internes (volume cible interne) et marge de positionnement (set-up margin). Ces deux marges sont indépendantes et doivent s’additionner de manière quadratique. Pour réduire le volume cible interne, en cas de tumeurs des lobes moyen et inférieur, il est recommandé d’utiliser une technique d’asservissement respiratoire (en blocage volontaire ou actif en inspiration profonde), ou une mid-ventilation à partir d’une scanographie quadridimensionnelle (4D-CT) [12,15,23-24].
- Les organes à risque (OAR)
Les principaux organes à risque pour l’irradiation pulmonaire comprennent les deux poumons, le cœur, l’œsophage, le plexus, les vertèbres et la moelle épinière. L’ensemble de ces organes doit apparaître sur les histogrammes dose-volume (Tableau 1) [25-26].
Pour les vertèbres, une attention particulière doit être portée aux doses reçues aux vertèbres qui peuvent présenter des fractures radio-induites secondaires. En cas de tumeurs de l’apex et des doses au-delà de 50 Gy, le plexus brachial doit être délinéé. La dose maximale à ne pas dépasser selon l’extension tumorale est de 55-60 Gy, une dose supérieure peut être délivrée, surtout lorsque la tumeur comprime le plexus brachial, après évaluation du rapport bénéfice-risque [27-28].
- Dose totale et fractionnement
La dose prescrite varie selon le type de radiothérapie délivrée : exclusive, en association ou non à la chimiothérapie ou en situation postopératoire.
En cas d’irradiation exclusive, la dose totale recommandée est de 66 à 70 Gy. Elle peut être abaisser en fonction des histogrammes dose-volume (HDV), de l’état respiratoire du patient (résultats des épreuves fonctionnelles respiratoires), de l’association concomitante à une chimiothérapie, mais jamais inférieure à 60 Gy, avec un étalement classique de 2 Gy qui est recommandé ; alors que l’irradiation prophylactique médiastinale à la dose de 46 Gy est proscrite en l’absence d’aires ganglionnaires envahies sur la tomodensitométrie ou la TEP [14,29-31].
En situation postopératoire, la place de la radiothérapie est discutée depuis la méta-analyse PORT. Une dose de 60 à 66 Gy est prescrite en zone d’exérèse, en cas de résection R1 ; et une dose de 50 à 56 Gy est à discuter en cas de tumeurs de stade pT3R0. Pour les stades pN2, la dose de 46 à 54 Gy au niveau médiastinal peut être proposée [8-9,32-34].
Radiothérapie conformationnelle avec modulation d’intensité (RCMI)
Technique de radiothérapie innovante en plein essor, la RCMI est de plus en plus utilisée dans le cancer du poumon, en particulier pour les tumeurs proches de la moelle épinière ou du cœur
Elle permet d’irradier des volumes concaves tout en générant de forts gradients de dose entre les volumes à traiter et à épargner, permettant ainsi une escalade de dose. Elle est proposée dans le traitement des formes localement avancés en raison du bénéfice dosimétrique théorique qu’elle apporte. Certaines études ont montré le bénéfice apporté par l’utilisation de cette technique sur le contrôle local et la survie, ainsi qu’une moindre toxicité pulmonaire post-radique ou œsophagienne, tout en permettant une escalade de dose [35-38].
Radiothérapie thoracique en conditions stéréotaxiques (SBRT)
Dans le cancer du poumon, la SBRT est réservée aux petites lésions : les T1N0 ou T2N0 inférieures à 5 cm, chez des patients le plus souvent inopérables en raison de comorbidités associées. La plupart des études ont rapporté un taux de control local supérieur à 85% et des taux de survie variables. Les fortes doses prescrites une précision millimétrique sont très hétérogènes. Elles varient de 3 à 22 Gy par fraction pouvant aller jusqu’ à des doses totales de 60 Gy en 3 fractions pour les tumeurs périphériques. Ces fortes doses délivrées par fraction correspondent à une dose équivalente biologique élevée supérieur à 100 Gy en fractionnement classique. En fonction de la localisation et la taille de la tumeur, le schéma de fractionnement est adopté [39-42].
Radiothérapie asservie à la respiration (Gating)
La technique de gating permet de mieux adapter les faisceaux d’irradiation à la tumeur pour protéger certains organes à risque, surtout le poumon et le cœur,
La technique la plus utilisée est celle du blocage spirométrique volontaire qui consiste à traiter le patient en inspiration profonde bloquée, sur un volume inspiratoire prédéfini, chaque faisceau étant délivré lors d’une courte apnée.
Alors que les techniques de synchronisation respiratoires consistent à suivre la respiration libre en temps réel et à déclencher l’acquisition du scanner puis de l’accélérateur linéaire toujours sur la même phase du cycle respiratoire, habituellement en fin d’expiration profonde car la moins mobile.
Cette technique est principalement utilisée pour l’irradiation des tumeurs proches du diaphragme, très mobiles et chez les patients atteints d’une insuffisance respiratoire importante [23,43-45].
Conclusion
La radiothérapie thoracique semble occuper une place de plus en plus importante dans la stratégie thérapeutique globale des cancers bronchiques non à petites cellules, surtout avec les avancées technologiques considérables que connait la radiothérapie, s’inscrivant ainsi dans une prise en charge pluridisciplinaire et multimodale.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Reck M, Heigener DF, Mok T, Soria JC, Rabe KF. Management of non-small-cell lung cancer: recent developments. Lancet 2013; 382:709–19.
- Cartier L, Fournel P. Principes et traitements par chimiothérapie et radiothérapie des cancers bronchiques non à petites cellules. EMC, Pneumologie, 6-002-L-12, 2009.
- Depierre A et al. Recommandations professionnelles cancer du poumon non à petites cellules formes localisées non opérables localement avancées et métastatiques. Boulogne-Billancourt : Institut national du cancer ; 2010, www.e-cancer.fr.
- Timmerman RD. The Quality of Toxicity Reporting and the Story of the Lung SBRT « No-Fly Zone ». In Regard to Oskan. Int J Radiat Oncol Biol Phys 2015; 93:726‑
- Non-small Cell Lung Cancer Collaborative Group. Chemotherapy in non-small cell lung cancer: a meta-analysis updated data on individual patients from 52 randomised clinical trials.Br Med J 1995; 311:899-908.
- Furuse K, Fukuoka KM, Kawahara M, Nishikawa H, Takada Y, Kudoh S, et al. Phase III study of concurrent versus sequential thoracic radiotherapy in combination with mitomycin, vindesine and cisplatin in unresectable stage III non-small cell lung cancer (NSCLC). J Clin Oncol1999 ;7: 692-9.
- Curran WJ, Paulus R, Langer CJ, Komaki R, Lee JS, Hauser S, etal. Sequential vs concurrent chemoradiation for stage III non-small cell lung cancer: Randomised phase III trial RTOG 94-10. J Natl Cancer Inst2011; 103:1-9.
- Port meta-analysis trialists group. Postoperative radiotherapy for non-small cell lung cancer: systematic review and meta-analysis of individual patient data from nine randomized controlled trials. Lancet 1998; 352:257–63.
- Machtay, Lee JH, Shrager JB, Kaiser LR, Glatstein. Risk of death from intercurrent disease is not excessively increased by modern postoperative radiotherapy for high risk resected non-small-cell lung carcinoma. J Clin Oncol 2001;19:3912–7.
- Konert T, Vogel W, MacManus MP, Nestle U, Belderbos J, GrégoireV, et al. PET/CT imaging for target volume delineation in curative intent radiotherapy of non-small cell lung cancer: IAEA consensus report 2014. Radiother Oncol 2015; 116:27‑
- Khalil A, Majlath M, Gounant V, Hess A, Laissy JP, Debray MP. Place de l’IRM dans le cancer bronchopulmonaire. J RadiolDiagetInterv2016; 97:411‑
- Senan S, De Ruysscher D, Giraud P, Mirimanoff R, Budach V. Literature based recommendations for treatment planning and execution in high-dose radiotherapy for lung cancer. RadiotherOncol2004;71:139–46.
- Chapet O, Kong FM, Quint LE, Chang AC, Ten Haken RK, Eisbruch A, et al. CT-based definition of thoracic lymph nodestations: an atlas from the University of Michigan. Int J Radiat Oncol Biol Phys 2005;63:170‑
- Van Sornsen de Koste JR, Lagerwaard FJ, Nijssen-Visser MRJ, Schuchhard-Schipper R, Joosten H, Senan S. What margins are necessary for incorporating mediastinal nodal mobility into involved-field radiotherapy for lung cancer? Int J Radiat Oncol Biol Phys 2002; 53:1211–5.
- Martel-Lafay I, Fourneret P, Ayadi M, Brun O, Buatois F, Carrie C, et al. Guide de bonne pratique pour la radiothérapie thoracique exclusive ou postopératoire des carcinomes non à petites cellules. Cancer Radiother2009;13:55–60.
- De Ruysscher D, Faivre-Finn C, Moeller D, Nestle U, Hurkmans CW, Le Pechoux C, et al. European Organization for Research and Treatment of Cancer (EORTC) recommendations for planning and delivery of high-dose, high precision radiotherapy for lung cancer. Radiother Oncol 2017; 124:1–10.
- Vaylet F, Bonnichon A, Salles Y, Gontier E, Bonardel G, Lefloch H, et al. La tomographie par émission de positons au (18F)-fluorodésoxyglucose([18F]FDG-TEP) dans la prise en charge du cancer bronchique non à petites cellules en 2006. Cancer Radiother2007;11:16–22.
- Konert T, Vogel W, MacManus MP, Nestle U, Belderbos J, Grégoire V, et al. PET/CT imaging for target volume delineation in curative intent radiotherapy of non-small cell lung cancer: IAEA consensus report 2014. Radiother Oncol2015; 116:27–34.
- Giraud P, Antoine M, Larrouy A, Milleron B, Callard P, De Rycke Y, et al. Evaluation of microscopic tumor extension in non-small-cell lung cancer for three-dimensional conformal radiotherapy planning. Int J Radiat Oncol BiolPhys 2000; 48:1015–24.
- Grills IS, Fitch DL, Goldstein NS, Yan D, Chmielewski GW, Welsh RJ, et al. Clinico-pathologic analysis of microscopic extension in lung adenocarcinoma: defining clinical target volume for radiotherapy. Int J Radiation Oncology Biol Phys 2007 ;69 :334–41.
- Yuan S, Meng X, Yu J, Mu D, Chao KS, Zhang J, et al. Determining optimal clinical target volume margins on the basis of microscopic extracapsular extension of metastatic nodes in patients with non-small-cell lung cancer. Int J Radiat Oncol Biol Phys 2007; 67:727–34.
- Le Péchoux C. Role of postoperative radiotherapy in resected non-small cell lung cancer: a reassessment based on new data. Oncologist 2011; 16:672–81.
- Giraud P, Yorke E, Jiang SB, Simon L, Rosenzweig K, Mageras G. Reduction of organ motion effects in IMRT and conformal 3D radiation delivery by using gating and tracking techniques. Cancer Radiother2006; 10:269–82.
- Wanet M, Sterpin E, Janssens G, Delor A, Lee JA, Geets X. Validation of the midposition strategy for lung tumors in helical Tomo-therapy. Radiother Oncol2014; 110:529–37.
- Kong FM, Ritter T, Quint DJ, Senan S, Gaspar LE, Komaki R, et al. Consideration of dose limits for organs at risk of thoracic radiotherapy: atlas for lung, proximal bronchial tree, esophagus, spinal cord, ribs, and brachial plexus. Int J Radiat Oncol Biol Phys 2011 ;81 :1442–57.
- Blais E, Pichon B, Mampuya A, Antoine M, Lagarde P, Kantor G, et al. Lung dose constraints for normo-fractionated radiotherapy and for stereotactic body radiation therapy Cancer Radiother2017; 21:584‑
- Rodríguez-Ruiz ME, San Miguel I, Gil-Bazo I, Perez-Gracia JL, Arbea L, Moreno-Jimenez M, et al. Pathological vertebral fracture after stereotactic body radiation therapy for lung metastases. Case report and literature review. RadiatOncol2012; 7:50.
- Hall WH, Guiou M, Lee NY, Dublin A, Narayan S, Vijayakumar S, et al. Development and validation of a standardized method for contouring the brachial plexus: preliminary dosimetric analysis among patients treated with IMRT for head-and-neck cancer. Int J Radiat Oncol Biol Phys 2008; 72:1362–7.
- Girard N, Mornex F. Chimioradiothérapie exclusive des cancers bronchiques non à petites cellules localement évolués. Cancer Radiother 2007 ;11 :67–76.
- Pfister DG, Johnson DH, Azzoli CG, Sause W, Smith TJ, Baker Jr S, et al. American Society of Clinical Oncology treatment of unresectable non- small-cell lung cancer guideline: update 2003. J Clin Oncol 2004; 22:330–53.
- Jeremic B. Incidental irradiation of nodal regions at risk during limited field radiotherapy in dose escalation studies in non-small cell lung cancer (NSCLC).Enough to convert no-elective to elective nodal irradiation (ENI)? Radiother Oncol 2003; 71:123–5.
- Mackillop WJ, Bates JHT, O’Sullivan B, Withers HR. The effect of delay in treatment on local control by radiotherapy. Int J Radiat Oncol Biol Phys1996 ;34 :243–50.
- Moretti L, Roelandts M, Berghmans T, Van Houtte P. Les traitements adjuvants dans les cancers bronchiques non à petites cellules. Cancer Radiother 2007 ;11 :53–8.
- Murray CJ, Lopez AD. Mortality by cause for eight regions of the world: global burden of disease study. Lancet 1997; 349:1269–76.
- Bezjak A, Rumble RB, Rodrigues G, Hope A, Warde P. Intensity-modulated radiotherapy in the treatment of lung cancer. Clin Oncol (R Coll Radiol)2012; 24:508–20.
- Chan C, Lang S, Rowbottom C, Guckenberger M, Faivre-Finn C, for the IASLC Advanced Radiation Technology Committee. Intensity-modulated radiotherapy for lung cancer: current status and future developments. J Thorac Oncol2014 ;9 :1598–608.
- Shirvani SM, Jiang J, Gomez DR, Chang JY, Buchholz TA, Smith BD. Intensity modulated radiotherapy for stage III non-small cell lung cancer in the United States: predictors of use and association with toxicities. Lung Cancer 2013; 82:252‑
- Koshy M, Malik R, Spiotto M, Mahmood U, Rusthoven CG, Sher DJ. Association between intensity modulated radiotherapy and survival in patients with stage III non-small cell lung cancer treated with chemoradiotherapy. Lung Cancer 2017; 108:222‑
- Shah JL, Loo BW Jr. Stereotactic Ablative Radiotherapy for Early-Stage Lung Cancer. Semin Radiat Oncol 2017; 27:218‑
- Caillet V, Booth JT, Keall P. IGRT and motion management during lung SBRT delivery. Phys Med 2017; 44:113‑
- Timmerman RD. The Quality of Toxicity Reporting and the Story of the Lung SBRT « No-Fly Zone ». In Regard to Oskan. Int J Radiat Oncol Biol Phys 2015; 93:726‑
- Vansteenkiste J, Crinò L, Dooms C, Douillard JY, Faivre-Finn C, Lim E, et al.2ndESMO consensus conference on lung cancer: early-stage non-small-cell lung cancer consensus on diagnosis, treatment and follow-up. Ann Oncol 2014; 25:1462–74.
- Boda-Heggemann J, Knopf AC, Simeonova-Chergou A, Wertz H, Stieler F, Jahnke A, et al. Deep Inspiration Breath Hold-Based Radiation Therapy: A Clinical Review. Int J Radiat Oncol Biol Phys 2016 ;94 :478‑
- Giraud P, Djadi-Prat J, Morvan E, Morelle M, Remmonay R, Pourel N, et al. Dosimetric and clinical benefits of respiratory gated radiotherapy for lung and breast cancers: results of the STIC 2003 Cancer Radiother 2012; 16:272‑
- Giraud P, Morvan E, Claude L, Mornex F, Le Pechoux C, Bachaud JM, et al. Respiratory gating techniques for optimization of lung cancer radiotherapy. J Thorac Oncol 2011 ;6 :2058–68.
Tableau 1 : Principales contraintes de dose aux organes à risque pour une irradiation thoracique normo fractionnée [25-26].
| Poumon | RT | ARCC | Post Lobectomie | Post Pneumonectomie |
| Dose moyenne pulmonaire (Gy) | <20Gy | <20Gy | <15Gy | <8-10Gy |
| V20 | <40% | ≤35% | <20% | <10% |
| V30 | ≤20% | ≤20% | ||
| Cœur | ||||
| V40 | ≤30% | |||
| D100 | ≤30Gy | |||
| Œsophage | ||||
| V50 | ≤35% | |||
| Moelle épinière | ||||
| Dose maximale | 45 Gy |
RT : radiothérapie ; ARCC : association radiochimiothérapie