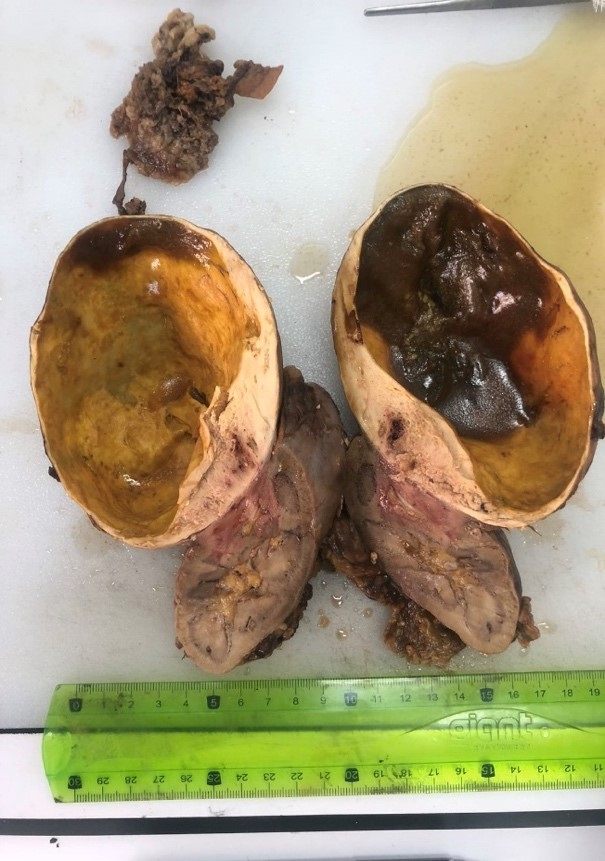
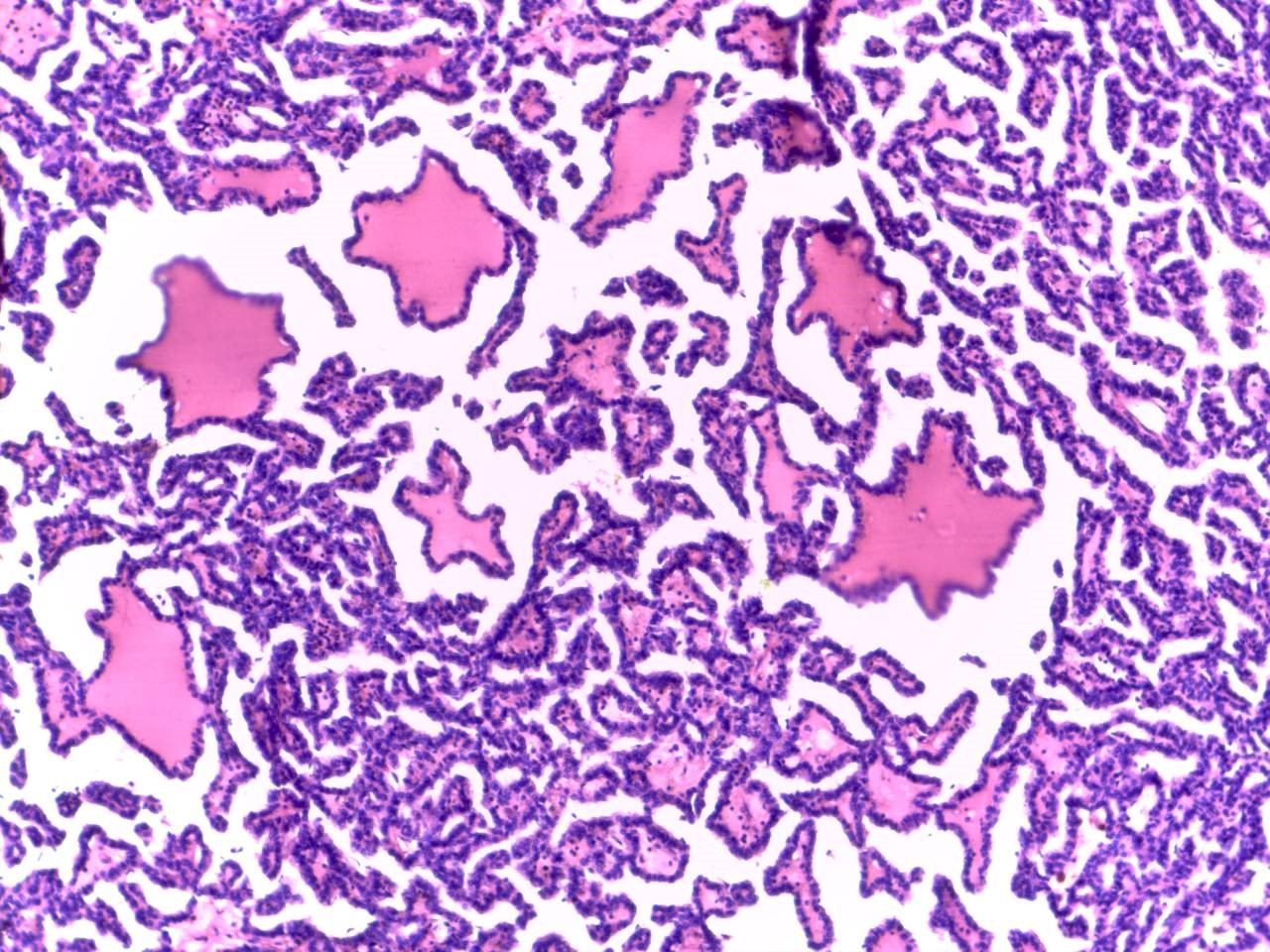
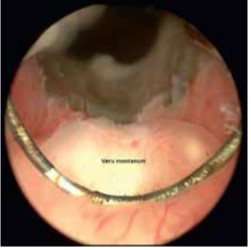
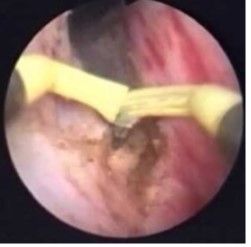
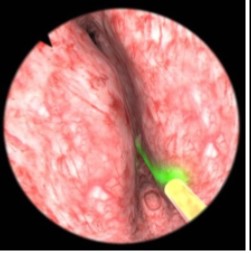
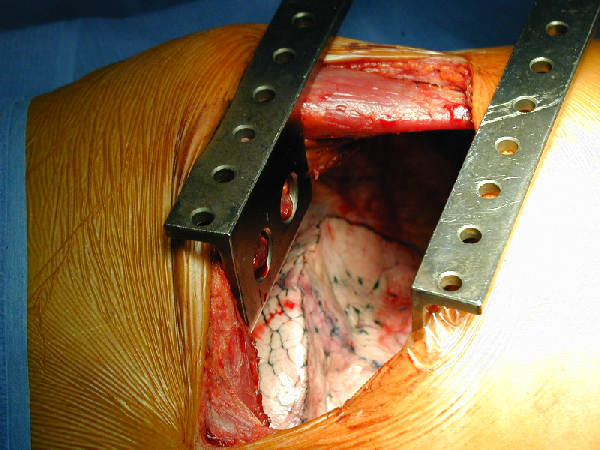
Étudier la sexualité et la qualité de vie des patients porteurs d’une dérivation urinaire cutanée non continente en fonction de l’âge, suite à une cystectomie pour tumeur de vessie localisée, opérés dans le service d’urologie de l’EHU Oran.
S. Kerroumi1,2, C. Ouanezar1,2, S. Gourine1, S. Taleb1,2, A.D. Lansari1,2, A. Bazzi1,2, M.J. Yousfi1,2
1 Service d’Urologie, EHU 1er Novembre 1954, Oran.
2 Laboratoire de Recherche Santé et Environnement, Faculté de Médecine d’Oran.
Date de soumission : 08 Décembre 2020.
Abstract: Objective: To study sexuality and quality of life of patients with non-continental cutaneous urinary diversion according to age, following cystectomy for a localized bladder tumour performed in the urology department of the Oran EHU. Methods: Two questionnaires we redistributed to patients who underwent cystectomy with a non-continental cutaneous shunt for a localized bladder tumour (PT1-2 N0 M0) and who did not undergo chemotherapy for a period of 03 years between 2013 and 2015. The first self-administered questionnaire included 25 closed questions established in its original French version. The IIEF score in its Arabic version is the second questionnaire to evaluate the erectile function of our patients. These two self-administered questionnaires we redistributed to patients during their follow-up consultations. The results were analysed with a 5% risk and the Yates correction of the Chi 2 test. Results: Among the 146 cystectomies made during this period, there are 85 patients included in the study including 09 women. The mean age was 67.3 years with a 12-month follow-up. Two populations differed in their satisfaction and embarrassment according to age (57 patients <65 years, 28 patients> 65 years). In the group less than 65 years of age, 52 lead types Bricker (91.2%) and 05 ureterostomy (8.7%) cutaneous were performed. 11 patients (19.2%) changed post-operative occupational activity, 44 patients (77.19%) reported no embarrassment in their relational lives, 15 patients (26.31%) reported an ostomy problem. Fifty-one patients (89.47%) were satisfied of their quality of life. Most patients were autonomous and they describe their sexual activity as very disturbed. In the group over 65 years, 23 lead types Bricker (82.14%) and 05 ureterostomy (17.85%) cutaneous were performed. Eighteen patients (64.28%) were autonomous in the ostomy appliance, 16 patients (57.14%) described no gene in their relational lives, 19 patients (67.85%) described a stoma problem. Twenty-two patients (78.57%) were satisfied with their quality of life. Most patients did not change their occupational activity. Conclusion: In our study, there was a significant difference in ostomy appliance problems and socio-occupational status (p <0.00. P <0.00 respectively) between the two groups in the study. Most of the patients regardless of age were satisfied with their derivations with a very disturbed sex life.
Key words: Non-continent urinary diversion, cystectomy, sexuality, quality of life.
Introduction
Actuellement, l’étude de la sexualité et la qualité de vie représentent deux paramètres essentiels en dehors de la survie, dans l’évaluation de la pertinence d’une dérivation urinaire après une cystectomie. La qualité de vie est une notion complexe incluant plusieurs dimensions ; psychologique, physique et émotionnelle ainsi que les notions d’autonomie et de relations sociales du patient [1,2].
L’étude de la sexualité peut s’effectuer à travers des questionnaires validés comme ; IIEF, DAN PSS et Urolife, regroupés selon le modèle de représentation de la sexualité de l’homme publié par le CTMH [3]. La cystectomie est une source d’atteinte de la fonction érectile qu’on va étudier à travers le questionnaire validé IIEF [4].
En effet, la cystectomie touche profondément l’image corporelle et la qualité de vie par un mécanisme déstabilisateur précoce souvent transitoire. Il y a également les effets secondaires de la chirurgie elle-même avec perte de poids, fatigue, troubles digestifs et urinaires ; avec souvent une période plus ou moins prolongée de soins post-opératoires, source d’inquiétude [5].
Ces dernières années, plusieurs techniques de dérivations urinaires ont été créés pour améliorer l’image corporelle et la qualité de vie. Il est admis que le patient s’adapte naturellement à sa dérivation avec une qualité de vie acceptable voire améliorée à long terme.
Dans la plupart des études de la qualité de vie après une dérivation urinaire, l’âge et le stade tumoral sont considérés comme des facteurs neutres. Actuellement, les patients dérivés sont de plus en plus jeunes avec des stades avancés.
L’objectif de notre travail est d’évaluer l’impact de l’âge sur la qualité de vie après une dérivation urinaire.
Résumé : Objectif : Étudier la sexualité et la qualité de vie des patients porteurs d’une dérivation urinaire cutanée non continente en fonction de l’âge, suite à une cystectomie pour tumeur de vessie localisée, opérés dans le service d’urologie de l’EHU Oran. Méthodes : Deux questionnaires ont été distribués aux patients opérés d’une cystectomie avec une dérivation cutanée non continente pour une tumeur de vessie localisée (PT1-2 N0 M0) ; qui n’ont pas subi une chimiothérapie pendant une durée de 03 ans, entre 2013 et 2015. Le premier auto-questionnaire comprenait 25 questions fermées établies dans sa version originale en français. Le score IIEF est le 2ème questionnaire afin d’évaluer la fonction érectile de nos patients. Ces deux auto-questionnaires ont été distribués aux patients pendant leurs consultations de suivi. Les résultats ont été analysés avec un risque α à 5% et la correction de Yates du test du Khi 2. Résultats : Parmi les 146 cystectomies faites pendant cette période, il y a 85 patients inclus dans l’étude dont 09 femmes. L’âge moyen était de 67,3 ans avec un recul de 12 mois. Les deux populations différaient dans leur satisfaction et leur gêne en fonction de l’âge (57 patients < 65 ans, 28 patients ≥ 65 ans). Dans le groupe des moins de 65 ans, 52 dérivations type Bricker (91,2%), et 05 urétérostomies cutanées (8,7%) ont été réalisées. Onze patients (19,2%) ont changé d’activité professionnelle post-opératoire, 44 patients (77,19%) n’ont décrit aucune gêne dans leur vie relationnelle, 15 patients (26,31%) ont décrit un problème de stomie. Cinquante et un patients (89,47%) étaient satisfaits de leur qualité de vie. La plupart des patients étaient autonomes et qualifient leur activité sexuelle comme très perturbée. Dans le groupe plus de 65 ans, 23 dérivations type Bricker (82,14%) et 05 urétérostomies cutanées (17.85 %) ont été réalisées. Dix-huit patients (64,28%) étaient autonomes dans l’appareillage de la stomie, 16 patients (57,14%) ont décrit aucune gêne dans leur vie relationnelle, 19 patients (67,85%) ont décrit un problème de stomie. Vingt-deux patients (78,57%) étaient satisfaits de leur qualité de vie. La plupart des patients n’ont pas changé d’activité professionnelle. Conclusion : Dans notre étude, il existe une différence significative dans les problèmes de l’appareillage des stomies et dans la situation socio-professionnelle (p<0,00 ; p<0,00 respectivement), entre les deux groupes de l’étude. La plupart des patients quel que soit l’âge, étaient satisfaits de leurs dérivations, avec une vie sexuelle très perturbée.
Mots clés : Dérivation urinaire non continente, cystectomie, sexualité, qualité de vie.
Matériels et méthodes
Entre janvier 2013 et décembre 2015, deux questionnaires en français ont été distribués aux patients opérés d’une tumeur de vessie localisée (PT1-2 N0 M0), avec une dérivation urinaire cutanée non continente au service d’urologie de l’EHU d’Oran. Les patients inclus dans l’étude n’ont pas subi de chimiothérapie adjuvante.
Notre étude a été basée, d’une part, sur des données recueillies à partir des dossiers des patients concernant l’indication opératoire, le geste chirurgical, les suites opératoires ; et d’autre part, sur l’analyse d’un ensemble de questionnaires validés.
Le premier auto-questionnaire comprenait 25 questions fermées, établi dans sa version originale en français. Ce questionnaire spécifique a été développé et validé, il y a quelques années (6) (Annexe1). Il est simple, court, englobant plusieurs thèmes :
- La situation socio-professionnelle du patient.
- Les fonctionnements moteurs (possibilité de se déplacer, d’effectuer telles ou telles tâches matérielles), l’activité sexuelle, le transit digestif.
- La vie relationnelle a été envisagée à différents niveaux, social, professionnel et familial.
- Une appréciation globale directe de la satisfaction du patient au sujet de sa dérivation.
Les réponses se présentaient, soit sous forme dichotomique, soit selon trois ou quatre modalités. Dans la formulation des questions, les patients avaient la possibilité de refuser de répondre en cochant la case « non concerné par la question ».
Le score IIEF est le 2ème auto-questionnaire pour évaluer la fonction érectile. Ces deux auto-questionnaires ont été distribués aux patients pendant leurs consultations de suivi.
L’analyse statistique a été réalisée avec le logiciel SPSS version 20, en prenant un risque α à 5%. Le test du Khi 2 avec la correction de Yates est utilisé pour les caractères qualitatifs.
Résultats
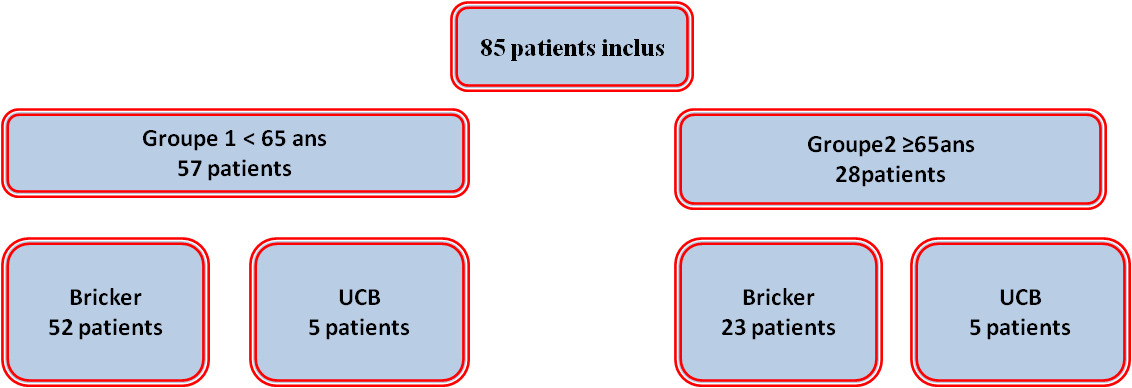
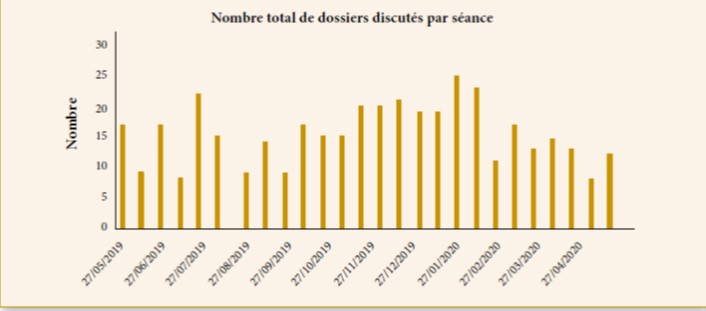
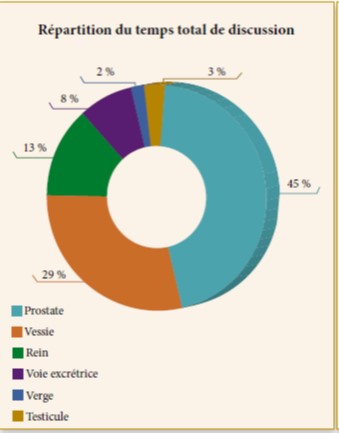
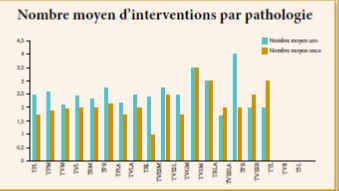
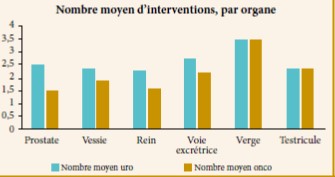
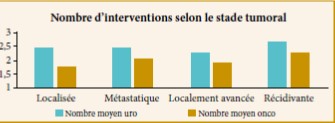
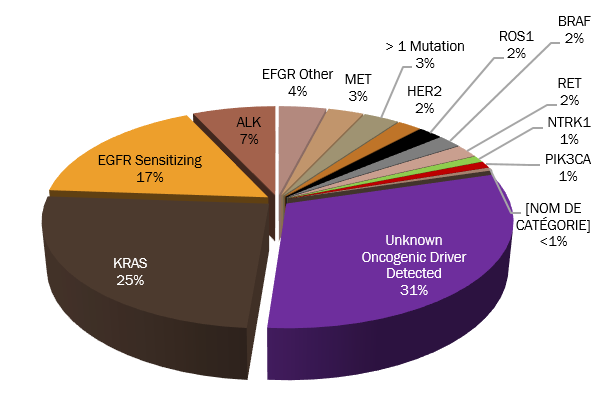
Parmi les 146 cystectomies faites pendant cette période, il y a 85 patients inclus dans l’étude dont 09 femmes. L’âge moyen était de 67,3 ans avec un recul de 12 mois. Les deux populations différaient dans leur satisfaction et leur gêne en fonction de l’âge (57 patients < 65 ans, 28 patients ≥ 65 ans). Aucun patient n’a subi de chimiothérapie adjuvante. Plusieurs items vont être analysés à savoir l’activité professionnelle, la gêne fonctionnelle, les problèmes de stomies, la satisfaction personnelle et l’autonomie, ainsi la fonction érectile (fig1).
Fig. 1 : Répartition selon la dérivation
L’activité professionnelle
Une activité professionnelle avant le geste opératoire est rapportée chez 45 patients (78,9%) dans le groupe 1 contre 19 patients (67,8%) dans le groupe 2.
Le changement d’activité à cause de l’intervention est estimé chez les patients de moins et de plus de 65 ans à 11 et 15 patients (24,4% contre 78,9 %, p<0.00). Plus de la moitié des patients de moins de 65 ans (34 patients ; 59,6%) déclarent qu’ils ont arrêté ou bien gardé leur activité après l’intervention.
La gêne fonctionnelle
Quarante-quatre patients et 16 patients (77,19% contre 57,14%, p=0.7) du groupe 1 et 2 respectivement ont décrit aucune gêne dans leur vie relationnelle familiale pour effectuer des tâches domestiques ou du bricolage (fig. 2).
Groupe 1 < 65 ans
Groupe 2 ≥ 65 ans
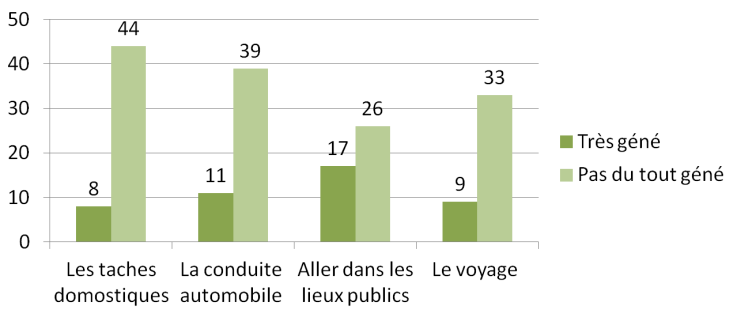
Fig. 2 : Répartition des patients en fonction des items de la gêne fonctionnelle.
Les problèmes de stomies
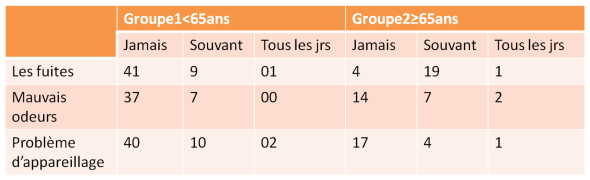
Les fuites d’urine représentent un facteur qui altère rapidement la qualité de vie. Neuf patients décrivent des fuites d’urine à travers la poche très souvent du groupe 1 contre 20 patients du groupe 2(p<0.00).
Les troubles digestifs occupent 64.9% et 57.1% (37 et17 patients) du groupe 1 et 2 respectif (Tableau1).
Tableau 1 : Répartition des patients en fonction des items des problèmes de stomies.
La satisfaction personnelle
La majorité des patients (51 patient/22 patients) du groupe 1 et 2 se déclarent satisfait de leur dérivation urinaire. Cinquante-cinq patients et 18 patients dans les deux groupes sont autonomes pour leur changement d’appareillage (fig. 3).
La consultation chez une infirmière stomathérapeute est estimée chez le groupe 1 et 2 à 15,7% et 10,7% respectivement.
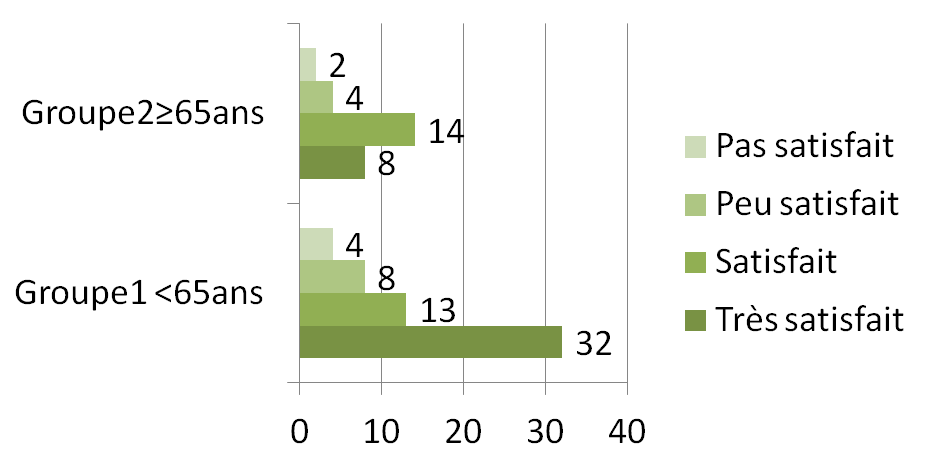
Fig. 3 : Satisfaction personnelle
L’activité sexuelle
Une activité sexuelle avant la cystectomie est estimée à 68,4 % chez les patients de moins de 65 ans et 32,1% dans le groupe 2. La cystectomie perturbe fortement la vie sexuelle dans les deux groupes (36,8% du groupe 1 contre 53,5% du groupe 2). Certains rapportent même qu’ils ne sont plus concernés par cette question (15,7 % du groupe 1 ; 21,4% du groupe 2).
Les raisons de leur perturbation dans le groupe 1 étaient : l’absence d’érection dans 13 cas, l’absence de désir dans 5 cas et les deux raisons associées dans 3 cas. Dans le groupe 2 les raisons de leurs perturbation sont liées à : l’absence d’érection dans 9 cas, l’absence de désir dans 3 cas et les deux raisons associées dans 3 cas.
Discussion
Le but de cette analyse est de montrer l’influence de l’âge sur la qualité de vie suite à une cystectomie avec dérivation urinaire non continente. Notre étude représente l’une des analyses rapportées dans la littérature étudiant l’impact de l’âge sur la qualité de vie. Malgré son caractère monocentrique, elle représente l’une de quelques séries dans la littérature qui aborde ce sujet. La plupart des études rapportées essaient de valider les questionnaires de la qualité de vie ou comparer une dérivation à une autre. Elles étaient rarement orientées sur l’analyse d’un facteur comme l’âge et son impact sur la qualité de vie.
Actuellement, la dérivation urinaire non continente type Bricker occupe toujours la 1ère place des dérivations au monde. Le rapport de l’OMS en 2007 sur le recensement des dérivations à partir de plusieurs séries publiées, donnait un taux de remplacement vésical de 47% sur un total de plus de 7.000 cystectomies (7). En France, en 2014, une étude a recensé le nombre de cystectomies réalisées de 2003 à 2013, ainsi que le type de dérivation urinaire. Tous sexes confondus, 9.053 remplacements de vessie ont été réalisés sur la période, soit 27,2% de l’ensemble des cystectomies (8).
Ce qui montre que la dérivation non continente type Bricker reste toujours une dérivation de choix qui rassemble deux paramètres essentiels à savoir : une rapidité de réalisation et un retentissement positif sur la qualité de vie.
Globalement, l’étude de la qualité de vie est très complexe en oncologie, à commencer par sa définition, il n’existe pas de consensus (9). Il existe plusieurs questionnaires validés mais insuffisants pour analyser le retentissement d’un geste opératoire sur la qualité de vie à savoir ; FLZM et le SF-36., QLQC 30, FACT-Bl, HADS (Hospital Anxiety and Depression Scale). On a utilisé deux auto-questionnaires validés, rédigés en français ; Le questionnaire de Dr Castgnola et l’IIEF. Ces questionnaires ont été distribués aux participants pendant la consultation après un an de suivi ce qui nous a permis d’avoir 100% de retour. Il est admis que les informations obtenues sur la qualité de vie sont d’autant plus pertinentes qu’elles le sont sans l’intervention directe du praticien impliqué, c’est pour cette raison qu’on a exclu tous les patients qui n’arrivent pas à lire les questionnaires (10).
Les individus inclus sont des patients de tout genre, opérés à notre niveau pour une tumeur de vessie localisée sur spécimen de cystectomie suivi d’une dérivation urinaire non continente type Bricker ou urétérostomie cutanée, qui n’ont pas subi de chimiothérapie ou un traitement complémentaire d’une complication post-opératoire pendant la 1ère année.
Les données épidémiologiques retrouvées sont : 146 cystectomies faites pendant cette période, 85 patients inclus dans la majorité étaient des hommes. L’âge moyen était de 67,3 ans avec un recul minimum de 12 mois. Aucun patient n’a subi de chimiothérapie adjuvante. On a divisé notre échantillon en deux populations identiques avec un seuil de 65 ans.
Le changement d’activité professionnelle à cause de l’image corporelle modifiée par la dérivation urinaire est constaté chez les patients moins et plus de 65 ans, à 11 et 15 patients avec une différence significative (24,4% contre 78,9%, p<0.00). Le changement d’activité a été étudié dans la série du Dr Babaiana de 110 patients ayant eu, au MD Anderson Cancer Center, une cystectomie totale avec opération de Bricker, chez qui l’activité professionnelle post-opératoire a été évaluée : 47,3% des patients ont poursuivi une activité professionnelle ; 34,5% ont conservé une activité modérée et 18,2% sont devenus sédentaires [1]. La chimiothérapie et l’âge sont les facteurs prépondérants d’une conservation d’activité professionnelle post-opératoire (11).
La plupart des patients du groupe 1 et 2 se déclarent satisfaits de leurs dérivations urinaires avec un score de gêne fonctionnelle dans leurs vie socio-professionnelle pratiquement identique sans différence significatif. Ceci est expliqué par le fait qu’on ait choisi une dérivation non continente dans les deux groupes, qui modifie l’image corporelle et qui a un retentissement perceptible sur la vie relationnelle du patient.
Même si on change le type de dérivation, la satisfaction globale physique et sociale est la même dans les deux groupes, ce qui a été prouvé dans la série de Dr Boydaqui qui a comparé, dans une étude rétrospective non randomisée, la qualité de vie des patients après intervention de Bricker ou poche de Kock continente (12). Les patients des 2 groupes avaient le même niveau de satisfaction globale physique et sociale : activités de loisirs, activités physiques et sexuelles. Cependant les patients porteurs d’une poche de Kock (statistiquement plus jeunes), avaient une reprise d’activité sexuelle plus précoce (p<0.001). En réalité on ne peut pas comparer deux dérivations urinaires parce que les populations et les problèmes spécifiques de chaque dérivation sont différents. Dans notre série, bien que les deux populations aient eu la même dérivation, il n’avait pas de différence significative en matière de satisfaction entre les deux groupes.
L’activité sexuelle après la cystectomie est fortement perturbée dans les deux groupes avec un taux de 68,4 % chez les patients de moins de 65 ans et 32,1% dans le groupe 2. La tumeur de vessie exige un geste chirurgical radical sans respect ni de la prostate, ni des bandelettes neuro-vasculaires, ce qui perturbe fortement la fonction érectile.
Malgré la relative rareté des fuites, grâce en particulier aux progrès des systèmes d’appareillage, elles représentent le facteur principal qui altère la qualité de vie. Celles-ci sont toujours autant redoutées. Entre les deux groupes, on a noté une différence significative avec, dans le groupe des moins de 65 ans, une bonne gestion, avec moins de fuites par apport au groupe 2.
Leur prévention passe par un positionnement et une réalisation parfaites de la stomie, et une éducation précise et répétée des patients.
Enfin, ce travail soulève un point très discuté : quel que soit la dérivation urinaire choisie, la qualité de vie passe par le choix du patient, du type de dérivation avant le geste opératoire, et elle se concrétise par une éducation bien menée, et une acceptation du patient de sa nouvelle image corporelle (13). Il faut rappeler qu’il n’existe aucun travail montrant clairement la supériorité d’une dérivation par rapport à une autre (14). Notre travail prouve que les patients jeunes ont moins de changement de leur statut socio-professionnel en post-opératoire, et ils ont moins de problèmes d’appareillage. Mais la satisfaction globale est la même quel que soit l’âge du patient et quelle que soit la dérivation pratiquée.
Conclusion
Dans notre étude, il existe une différence significative dans les problèmes de l’appareillage des stomies et dans la situation socioprofessionnelle (p<0,00 ; p<0,00 respectivement) entre les deux groupes de l’étude. La plupart des patients quel que soit l’âge, étaient satisfait de leurs dérivations avec une vie sexuelle très perturbée. Finalement ce n’est pas l’âge ni le type de dérivation qui va impacter la qualité de vie, par contre, on doit insister que le fait qu’un patient informé ait choisi personnellement le type de dérivation est déterminant pour l’acceptation de sa situation post-opératoire.
Morris a montré (comme pour le cancer du sein) que pour avoir une meilleure qualité de vie post-opératoire, il faut que le patient ait participé à la décision du type de dérivation urinaire choisie (14,5).
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Référence
- Smith K.W., Avis N.E., Assmann S.F. Distinguishing between quality of life and health status in quality of life research: a meta-analysis. Qual Life Res 1999; 8:447-459.
- C. Cullough LB. Concept of the quality of life: a philosophical analysis. In: Assessment of the quality of life. Wenger NK, Mattson ME, Furberg CD, Elinson J ed. Le Jacq Publ. Inc., 1984.
- Lukacs B, CTMH. Proposition d’un modèle de représentation de la sexualité de l’homme. Comparaison des questionnaires de sexualité. Prog Urol 2005 ; 15 :185-91.
- Rosen RC, Cappelleri JC, Smith MD, et al. Development and evaluation of an abridged, 5-item version of the International index of Erectile Function (IIEF-5) as a diagnostic tool for erectile dysfunction. Int J Impot Res 1999;11(6):319-26.
- Zerbib M., Bouchot O. Qualité de vie et dérivation urinaire. Partie B. Chapitre III. Prog Urol, 2002, 947.
- Christian Castagnola, Jean-Marie Marechal, Marie-Thérèse Hanauer, Marwan Dawahra, Jean-Michel Dubernard. Qualité de vie et dérivations urinaires cutanées. Résultats d’un questionnaire adressé à 73 patients. Progrès en Urologie (1996), 6, 207-216.
- Leon P, Drouin S, Seisen T, Vincent M, Mozer P, Cussenot O, et al. Évolution du nombre de cystectomies totales en France pour tumeur infiltrante de la vessie au cours des 10 dernières années : analyse objective des données nationales du PMSI. Prog En Urol. 2014 Nov. ;24(13) :804.
- World Health Organization (WHO) Consensus Conference on Bladder Cancer, Hautmann RE, Abol-Enein H, Hafez K, Haro I, Mansson W, et al. Urinary diversion. Urology. 2007 Jan;69(1 Suppl):17–49.
- Bowling A. Measuring health: a review of quality of life measurement scales; 1997.
- Mansson A., Henningsohn L., Steineck G., Mansson W. Neutral third party versus treating institution for evaluating quality of life after radical cystectomy. Eur Urol 2004; 46:195-199.
- Babaian R. J., Smith D. B.: Effect of ileal conduit on patients’ activities following radical cystectomy. Urology, 1991, 37: 33-35.
- Mottet, C. Castagnola, P. Rischmann, M. Deixonne, M. Guyot, P. Coloby, P. Mangin. Qualité de vie après cystectomie : enquête nationale de l’Association française d’urologie (AFU), la Fédération des stomisés de France (FSF) et de l’Association française des entérostomathérapeutes (AFET) chez des patients ayant eu une dérivation urinaire cutanée non continente ou un remplacement vésical orthotopique. Prog Urol, 2008,18, 5, 292-298.
- Gerharz E.W., Mansson A., Hunt S., Skinner E.C., Mansson W. Quality of life after cystectomy and urinary diversion: an evidence-based analysis. J. Urol 2005; 174:1729-1736.
- Morris J, Ingham R.: Choice of surgery for early breast cancer: psychosocial considerations. Soc Sci Med, 1988, 27: 1257-1262.