F. Sadouki, C. Haouichat, Service de Rhumatologie. CHU Djilali Bounaâma, Douéra, Alger
Date de soumission : 01 Juillet 2020.
Abstract: Osteoarthritis is the most common osteoarticular disease and obesity is a major risk factor for osteoarthritis of the weight-bearing joints (knees, hips). Its pathophysiology has seen great advances in recent years. Mechanical stress transformed into enzymatic and cytokine stress creates a systemic and metabolic link between osteoarthritis and obesity illustrated by the association of digital osteoarthritis with obesity. This systemic link involves many molecular actors including adipokines, on the other hand the comorbidities associated with obesity would have an impact on the risk of developing osteoarthritis.
Key words: osteoarthritis, obesity, adipokines.
Résumé : L’arthrose est la maladie ostéo-articulaire la plus fréquente et l’obésité est un facteur de risque majeur d’arthrose des articulations portantes (genoux, hanches). Sa physiopathologie a connu de grandes avancées ces dernières années. Le stress mécanique transformé en stress enzymatique et cytokinique crée un lien systémique et métabolique entre arthrose et obésité illustré par l’association de l’arthrose digitale à l’obésité. Ce lien systémique fait intervenir de nombreux acteurs moléculaires parmi lesquels les adipokines. D’autre part les comorbidités associées à l’obésité auraient un impact sur le risque de développer une arthrose.
Mots clés : arthrose, obésité, adipokines
- Introduction
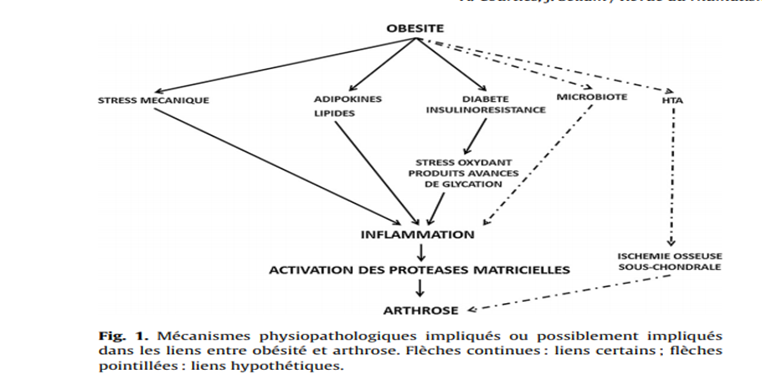
L’obésité est reconnue de longue date, comme un facteur de risque important d’arthrose des membres inférieurs par les contraintes mécaniques appliquées aux articulations portantes (genoux, hanches). Plus récemment d’autres facteurs ont été impliqués dans la survenue de l’arthrose. Le stress mécanique excessif (lié au surpoids), et responsable de l’usure du cartilage, active dans les chondrocytes, une réponse inflammatoire et enzymatique participant à la dégradation du cartilage. Il existe également un lien systémique et métabolique illustré par l’association entre l’arthrose des mains et l’obésité [1]. Ce lien fait intervenir de nombreux acteurs moléculaires parmi lesquels les adipokines, les cytokines pro-inflammatoires, les acides gras et les lipides. D’autre part, les comorbidités cardio-métaboliques associées à l’obésité, telles que le diabète de type 2 et l’hypertension artérielle auraient un impact direct sur les tissus articulaires et donc sur le risque de développer une arthrose [2]. Enfin, certains mécanismes décrits plus récemment dans la physiopathologie de l’obésité comme les anomalies du microbiote pourraient aussi participer à ce lien [3].
- Physiopathologie de l’arthrose
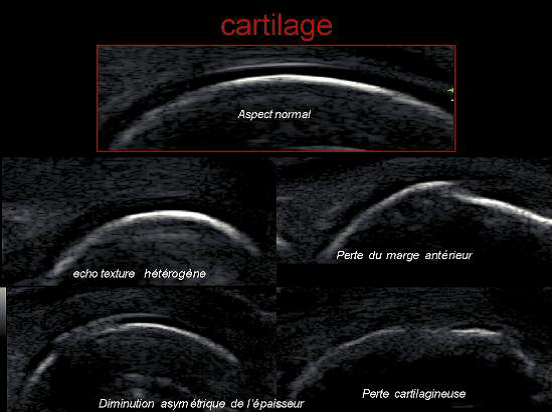
Le cartilage articulaire est composé d’un seul type cellulaire : le chondrocyte, responsable à la fois de la production et de la dégradation de la matrice extracellulaire. Cette matrice est constituée de collagène de type II, de protéines non collagéniques (protéoglycanes) et d’eau. L’ensemble forme un tissu conjonctif spécialisé qui joue un rôle essentiel dans le glissement des surfaces osseuses entre elles et dans la réponse de l’articulation aux contraintes qui lui sont appliquées, dites physiologiques et qui sont essentielles au maintien de l’homéostasie du cartilage et à son remodelage, physiologiquement faible [4]. L’homéostasie tissulaire est caractérisée par un équilibre entre synthèse et dégradation de la matrice cartilagineuse.
- Contraintes mécaniques sur les articulations portantes
L’effet délétère de l’obésité sur les articulations portantes passe par un stress mécanique excessif. L’excès de contraintes aboutit à des réponses chondrocytaires anormales entraînant une perte de l’homéostasie tissulaire.
Physiologiquement, le cartilage est avasculaire et non innervé, il se nourrit par ses interactions avec le liquide synovial et l’os sous-chondral. Son renouvellement est très lent car l’activité des chondrocytes est faible. Chaque chondrocyte porte un cil qui participe à sa biomécanique physiologique. La présence du cil conditionne la transduction du signal mécanique en signal biochimique conférant au chondrocyte la fonction de mécanorécepteur avec production de glycosaminoglycanes [5]. De même, les ostéoblastes sont mécano-sensibles et libèrent des cytokines pro-inflammatoires sous l’effet du stress mécanique [6].
- Rôle des facteurs systémiques
- Composante systémique de l’obésité
Le tissu adipeux blanc synthétise du tumor necrosis factor alpha (TNF?), dont l’expression est élevée dans les adipocytes et dans le sérum des souris obèses, et influence directement la captation du glucose par les tissus périphériques en réponse à l’insuline [7,8].
Le lien entre inflammation, obésité et insulinorésistance a fait émerger le concept de méta-inflammation (pour metabolic inflammation), qui serait impliquée dans les complications de l’obésité, notamment métaboliques et cardiovasculaires.
Outre les cytokines pro-inflammatoires ‘’classiques’’ telles que le TNF, l’IL-1, l’IL-6 ou les chimiokines, le tissu adipeux produit les adipokines, ou ‘’cytokines adipocytaires’’.
Les adipokines sont définies comme des molécules synthétisées exclusivement ou majoritairement par le tissu adipeux, circulant dans le sang et susceptibles d’avoir une action à distance du tissu adipeux [9].
Les principales adipokines étudiées sont la leptine, l’adiponectine connue pour être protectrice d’un point de vue cardiométabolique et la visfatine, mais on compte également la ghreline, la résistine, la vaspine, l’adipsine, l’omentine et l’adrénomédulline [9].
De nombreuses publications ont ainsi fait le lien entre adipokines et obésité, et entre adipokines et complications cardiovasculaires et métaboliques de l’obésité.
- Composante systémique de l’arthrose
Selon la même approche, il a été montré que l’obésité est un facteur de risque d’arthrose via des mécanismes systémiques. Une étude récente a montré que les facteurs métaboliques interviennent de manière prépondérante sur l’arthrose des mains tandis que le stress mécanique reste le mécanisme pathologique principal aux genoux [4].
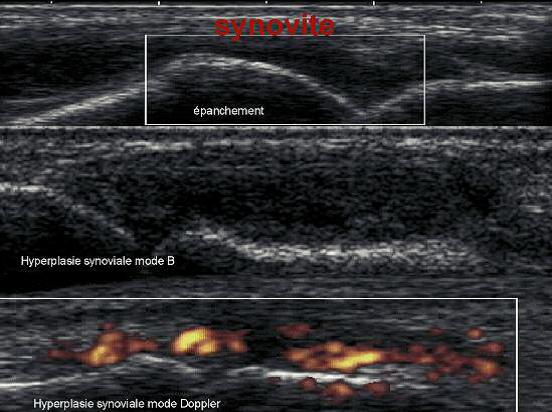
Le rôle des cytokines pro-inflammatoires ‘’classiques’’ (TNF?, IL-1, IL-6, IL-8) dans l’arthrose avait déjà fait l’objet de nombreux travaux du fait de la présence d’une inflammation synoviale observée chez de nombreux patients [4]. Les liens systémiques entre obésité et arthrose ont récemment mis en avant le rôle des adipokines dans la physiopathologie de l’arthrose ainsi que celui des lipides (Fig.1).
- Les adipokines
Par définition les adipokines sont principalement produites par le tissu adipeux, elles sont aussi produites par les tissus articulaires. L’étude des adipokines peut, soit être centrée sur leur rôle physiopathologique dans l’arthrose, soit portée sur des dosages sanguins et synoviaux comme biomarqueurs de la maladie, des symptômes ou de sa sévérité.
Parmi ces adipokines, les rôles de la leptine et de la visfatine ou nicotinamide phosphoribosyl-transférase (NAMPT) ont été étudiés. Leurs taux sériques et/ou synovial sont augmentés chez le sujet arthrosique par rapport aux témoins, et l’expression de la leptine par les chondrocytes articulaires est intimement corrélée avec la sévérité de l’arthrose [10]. In vitro, elles ont démontré toutes les deux, des effets pro-inflammatoires, pro-cataboliques, pro-oxydatif et antiprolifératifs sur les cellules du cartilage et de la membrane synoviale [11].
L’adiponectine, existe sous plusieurs isoformes ayant des poids moléculaires différents. Elle est exprimée par les chondrocytes et a globalement une action pro-inflammatoire sur le cartilage et induit également la production de protéases matricielles et de molécules d’adhésion favorisant la venue de leucocytes dans l’articulation [12,13]. En effet, certains travaux lui ont conféré un rôle protecteur sur le cartilage [14,15] ; tandis que ses propriétés anti-inflammatoires, liées à certaines de ses isoformes, sont bien démontrées sur l’endothélium. L’adiponectine favorise aussi la prolifération des ostéoblastes [16].
L’approche ‘’biomarqueur’’ a fait l’objet de nombreux travaux avec le dosage des adipokines dans le liquide synovial ou le sérum/plasma de patients arthrosiques. Il est soit comparé avec le taux plasmatique et synovial d’une même adipokine chez un même patient arthrosique, soit entre une population de patients arthrosiques et de sujets témoins.
Une étude récente montre une corrélation entre le taux d’adipokines (adiponectine, visfatine, leptine et résistine) dans le liquide synovial et la douleur arthrosique (au genou ou à la hanche) chez des patients au stade de prothèse [17]. Le taux plasmatique de leptine est corrélé à la sévérité de la gonarthrose, indépendamment du sexe et de l’indice de masse corporelle.
Le taux sérique d’adiponectine a aussi été retrouvé plus élevé dans les formes érosives d’arthrose digitale comparativement aux formes non érosives et dans les formes radiographiques plus sévères de gonarthrose au stade de prothèse [18].
En fait, les études de biomarqueurs sont nombreuses avec des résultats hétérogènes, bien que les perturbations des taux d’adipokines dans le sang et le liquide synovial chez les patients arthrosiques sont maintenant bien connues, il ne paraît pas envisageable d’utiliser dans le futur les mesures des taux sanguins d’adipokines comme un outil clinique prédictif de l’évolution ou de la sévérité clinique ou radiographique de la maladie. Aussi à ce jour, on ne peut envisager les adipokines comme une cible thérapeutique directe dans l’arthrose.
- Les lipides
La dyslipidémie associée à l’obésité se caractérise par un taux élevé de triglycérides, des taux diminués de HDL-cholestérol souvent associé à une augmentation du LDL-cholestérol et une augmentation des acides gras circulants (free fatty acids). Ces acides gras en excès favorisent l’insulinorésistance et certains, tels que le palmitate, l’acide linoléique ou encore oléique, s’accumulent dans les tissus articulaires et notamment dans les chondrocytes et dans le liquide synovial où certains démontrent un rôle pro-inflammatoire et pro-catabolique au cours de l’arthrose [19,20]. Le LDL-cholestérol a aussi démontré un rôle possible dans l’arthrose, notamment dans sa forme oxydée dont le taux sérique, synovial et l’expression dans le cartilage sont augmentés au cours de l’arthrose ; et est associé à des formes plus sévères et plus douloureuses chez l’homme [21].
L’ensemble de ces anomalies expliquent en partie l’association entre dyslipidémie, obésité, insulinorésistance et arthrose.
- Rôle des comorbidités cardiométaboliques
L’arthrose et l’obésité sont intégrées dans un phénotype clinique plus large du fait de l’association entre syndrome métabolique et arthrose, appelé arthrose métabolique[1] [2]. Au sein de ce phénotype, outre les liens directs entre obésité et arthrose, sont étudiés les liens entre l’arthrose et les autres pathologies cardio-métaboliques (diabète, insulinorésistance et hypertension artérielle). Chacune de ces pathologies est capable d’induire une inflammation chronique de bas grade, via différents stress métaboliques, pouvant intervenir dans le développement de l’arthrose [22].
- La graisse infra-patellaire : un rôle à part dans la gonarthrose
Situé dans l’articulation du genou en position intracapsulaire mais extra-synoviale, ce tissu pourrait jouer un rôle local dans la gonarthrose. Il comprend un infiltrat inflammatoire fait de macrophages [23], et se caractérise par la libération de leptine, d’IL-6, d’adiponectine et de visfatine [24]. La leptine retrouvée à plus forte concentration dans le liquide articulaire que dans le sérum pourrait provenir en partie de ce tissu. Son implication dans la douleur est aussi évoquée du fait qu’il contient des fibres nerveuses. Cependant, son volume n’est pas influencé par l’indice de masse corporelle et ne semble pas être corrélé au degré d’arthrose [25].
- Microbiote
Hypothèse explorée actuellement : le rôle de la dysbiose du microbiote intestinal de l’obésité et du syndrome métabolique dans l’arthrose. Il est possible que les anomalies du microbiome du sujet obèse entraînent des modifications du taux d’endotoxines qui pourraient induire à leur tour une réponse immunitaire innée au sein des tissus articulaires. Ainsi au cours de la gonarthrose, la concentration de LPS[2] et de sa protéine de liaison LPSBP[3] dans le sérum et le liquide synovial est corrélée à l’abondance des macrophages dans la synoviale et à la sévérité de l’arthrose du genou [26].
- Sarcopénie
Une des autres complications musculo-squelettiques associées à l’obésité est la sarcopénie. Or le muscle participe au métabolisme énergétique, puisque c’est le principal consommateur de glucose mais il a aussi un rôle essentiel dans l’homéostasie de l’articulation. Chez l’homme, la sarcopénie du sujet obèse est associée à 3 fois plus de risque de gonarthrose que le sujet avec une composition corporelle dite normale. Ce risque est supérieur à celui de l’obésité ou à celui de la sarcopénie prises isolément [27].
Ainsi les anomalies musculaires du sujet obèse pourraient favoriser la survenue et/ou la progression d’une arthrose. Cependant le lien de causalité direct reste difficile à faire puisque l’arthrose est une maladie pourvoyeuse de handicap entraînant une sédentarité et donc une sarcopénie.
- Conclusion
Les liens entre obésité et arthrose sont nombreux. Ils sont mieux connus ces dernières années depuis les grandes avancées dans la physiopathologie de l’arthrose. L’inflammation métabolique de bas grade, point commun à tous les mécanismes, permettra d’envisager de nouvelles voies thérapeutiques spécifiques.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Yusuf E, Nelissen RG, Ioan-Facsinay A, et al. Association between weight or body mass index and hand osteoarthritis: a systematic review. Ann Rheum Dis 2010; 69:761–5]
- Sellam J, Berenbaum F. Is osteoarthritis a metabolic disease? Joint Bone Spine 2013; 80:568–73.
- Metcalfe D, Harte AL, Aletrari MO, et al. Does endotoxemia contribute to osteoarthritis in obese patients? Clin Sci 2012; 123:627–34.
- Courties A, Sellam J. Obésité et arthrose: données physiopathologiques. Revue du rhumatisme monographies (2016), http:// dx.org/10.1016/j.monrhu.2015.11.003
- WannAKT, Zuo N, Haycraft CJ, et al. Primary cilia mediate mechano-transduction through control of ATP-induced Ca2+ signaling in compressed chondrocytes. FASEB J 2012; 26:1663–71.
- Sanchez C, Gabay O, Salvat C, et al. Mechanical loading highly increases IL-6 production and decreases OPG expression by osteoblasts. Osteoarthritis Cartilage 2009; 17:473–81
- Hotamisligil GS, Shargill NS, Spiegelman BM. Adipose expression of tumor necrosis factor-alpha: direct role in obesity-linked insulin resistance. Science 1993; 259:87–91.
- Hotamisligil GS. Inflammation and metabolic disorders. Nature 2006; 444:860–7.
- Trayhurn P, Wood IS. Adipokines: inflammation and the pleiotropic role of white adipose tissue. Br J Nutr 2004; 92:347–55undefined(15)00108-3/sbref0110]
- Simopoulou T, Malizos KN, Iliopoulos D, et al. Differential expression of leptin and leptin’s receptor isoform (Ob-Rb) mRNA between advanced and minimally affected osteoarthritic cartilage: effect on cartilage metabolism. Osteoarthritis Cartilage 2007; 15:872–83.
- Gómez R, Scotece M, Conde J, et al. Adiponectin and leptin increase IL-8 production in human chondrocytes. Ann Rheum Dis 2011; 70:2052–4.
- Koskinen A, Juslin S, Nieminen R, et al. Adiponectin associates with markers of cartilage degradation in osteoarthritis and induces production of proinflammatory and catabolic factors through mitogen-activated protein kinase pathways. Arthritis Res Ther 2011;13: R184
- Francin P-J, Abot A, Guillaume C, et al. Association between adiponectin and cartilage degradation in human osteoarthritis. Osteoarthritis Cartilage 2014; 22:519–26
- Chen T-H, Chen L, Hsieh M-S, et al. Evidence for a protective role for adiponectin in osteoarthritis. Biochim Biophys Acta 2006; 1762:711–8.
- Challa TD, Rais Y, Ornan EM. Effect of adiponectin on ATDC5 proliferation, differentiation and signaling pathways. Mol Cell Endocrinol 2010; 323:282–91.
- Luo X-H, Guo L-J, Xie H, et al. Adiponectin stimulates RANKL and inhibits OPG expression in human osteoblasts through the MAPK signaling pathway. J Bone Miner Res 2006; 21:1648–56
- Bas S, Finckh A, Puskas GJ, et al. Adipokines correlate with pain in lower limb osteoarthritis: different associations in hip and knee. Int Orthop 2014; 38:2577–83.
- Staikos C, Ververidis A, Drosos G, et al. The association of adipokine levels in plasma and synovial fluid with the severity of knee osteoarthritis. Rheumatology (Oxford) 2013; 52:1077–83.
- Loef M, Schoones JW, Kloppenburg M, et al. Fatty acids and osteoarthritis: different types, different effects. Joint Bone Spine 2018, undefined
- Kim S, Hwang J, Kim J, et al. Metabolite profiles of synovial fluid change with the radiographic severity of knee osteoarthritis. Joint Bone Spine 2017; 84:605–10.
- Tootsi K, Märtson A, Kals J, et al. Metabolic factors and oxidative stress in osteoarthritis: a case-control study. Scand J Clin Lab Invest 2017; 77:520–6
- Courties A, Gualillo O, Berenbaum F, et al. Metabolic stress-induced joint inflammation and osteoarthritis. Osteoarthritis Cartilage 2015; 23:1955–65.
- Bastiaansen-Jenniskens YM, Clockaerts S, Feijt C, et al. Infrapatellar fat pad of patients with end-stage osteoarthritis inhibits catabolic mediators in cartilage. Ann Rheum Dis 2012; 71:288–94
- Klein-Wieringa IR, Kloppenburg M, Bastiaansen-Jenniskens YM, et al. The infrapatellar fat pad of patients with osteoarthritis has an inflammatory phenotype. Ann Rheum Dis 2011; 70:851–7.
- Cai J, Xu J, Wang K, et al. Association between infrapatellar fat pad volume and knee structural changes in patients with knee osteoarthritis. J Rheumatol 2015; 42:1878–84.
- Huang ZY, Stabler T, Pei FX, et al. Both systemic and local lipopolysaccharide (LPS) burden are associated with knee OA severity and inflammation. Osteoarthritis Cartilage 2016; 24:1769–75
- Lee S, KimT-N, KimS-H. Sarcopenic obesity is more closely associated with knee osteoarthritis than is nonsarcopenic obesity: a cross-sectional study. Arthritis Rheum 2012; 64:3947–54
[1] Voir dans ce même numéro, l’article de S. Lehtihet sur ce sujet (NDLR).
[2] Lipopolysaccharides (NDLR).
[3] Lipopolysaccharide-binding protein (NDLR).