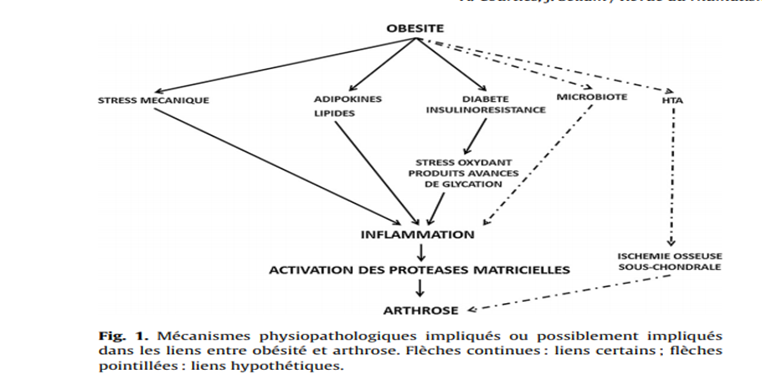
L’hormonothérapie constitue une étape incontournable dans la prise en charge du cancer du sein RE positif, l’œstrogène est l’hormone principale impliquée dans le développement et la récidive du cancer du sein hormonosensible]
Zemmour, B. Larbaoui, EHS Emir Abd El Kader, Oran.
Date de soumission : 27 Août 2019.
Abstract: In breast cancer, hormone therapy is the first targeted treatment aimed at reducing local or metastatic relapse risk of ER positive cancers [1]. 70 to 75% of these cancers express estrogen receptor (ER) and/or progesterone receptor (PR) [2,3], adjuvant treatment is well codified, adjuvant hormonal therapy extended beyond 5 years is a subject of controversy, the major therapeutic advances are seen in metastatic setting with the associations of aromatase inhibitors and targeted therapies.
Key words: ER, PR, Tamoxifen, Aromatase inhibitors, Targeted therapies.
Résumé : Dans le cancer du sein, l’hormonothérapie est le premier traitement ciblé qui vise à réduire le risque de rechute locale ou métastatique des cancers hormonodépendants [1]. 70 à 75% de ces cancers expriment les récepteurs hormonaux à l’œstrogène (ER) et/ou à la progestérone (PR) [2,3] ; le traitement adjuvant est bien codifié, l’hormonothérapie adjuvante étendue au-delà de 5 ans est un sujet de controverse, les grandes avancées thérapeutiques se voient en situation métastatique avec les associations des inhibiteurs de l’aromatase avec les thérapies ciblées.
Mots clés : ER, PR, Tamoxifène, inhibiteurs de l’aromatase, thérapies ciblées.
Introduction
L’hormonothérapie constitue une étape incontournable dans la prise en charge du cancer du sein RE positif, l’œstrogène est l’hormone principale impliquée dans le développement et la récidive du cancer du sein hormonosensible, Beatson avait déjà décrit en 1896 la régression d’un carcinome du sein après une ovariectomie [3]. Depuis, les avancées de l’hormonothérapie sont spectaculaires.
Le seuil de positivité des récepteurs hormonaux est un sujet de controverse en raison de la variabilité de l’expression seulement la plupart des experts s’accordent sur un seuil de 10% (1% aux US) [4] puisque la réponse à l’hormonothérapie dépend étroitement du degré de positivité des deux récepteurs (RE et RP).
Chez la femme pré-ménopausée
Le cancer du sein se voit de plus en plus chez la femme jeune non ménopausée, le tamoxifène est un modulateur sélectif des récepteurs aux œstrogènes, synthétisé en 1962 comme inducteur de l’ovulation. On découvre par la suite qu’il inhibe la croissance des cellules tumorales par action compétitive sur les récepteurs hormonaux. En 1975, c’est le premier anti estrogène commercialisé [5].
L’avantage du tamoxifène en adjuvant est démontré dans la méta-analyse Early Breast Cancer Trialists Collaborative Group (EBCTCG) qui regroupe 33.000 femmes. Il réduit la mortalité par cancer du sein à 15 ans de 30% quel que soit l’âge, le statut ganglionnaire et la chimiothérapie associée [5].
Dans l’état actuel des connaissances, en situation adjuvante, le tamoxifène utilisé pendant 5 ans réduit le risque de rechute de 39% chez la femme pré-ménopausée et la femme ménopausée.
Les analogues de la LH-RH
Ils agissent en incitant l’hypophyse à sécréter la FSH jusqu’à épuisement de la glande et chute du taux de FSH, LH et Œstradiol circulant.
Les essais TEXT and SOFT ont évalué l’apport de la suppression ovarienne associée à l’hormonothérapie adjuvante chez la femme pré-ménopausée.
L’étude TEXT a inclus 2.672 patientes randomisées à recevoir tamoxifène ou exemestane associées chacune à la suppression de la fonction ovarienne, l’étude SOFT a recruté 3.066 patientes pour le même design de l’étude TEXT avec en plus un bras tamoxifène seul.
L’ensemble des traitements ont été reçus pendant 05 ans et un suivi médian de 8-9 ans est observé.
Dans l’analyse combinée, les résultats sont en faveur de l’association de la suppression ovarienne avec l’hormonothérapie avec un HR=0,77 (IC 95% 0,67-0,90) p<0,001 [6].
Chez la femme ménopausée :
La ménopause est définie comme suit :
- Annexectomie bilatérale préalable
- Age ≥ 60 ans
- Age < 60 ans et aménorrhée d’au moins 12 mois en l’absence de chimiothérapie, de tamoxifène ou suppression ovarienne et FSH, œstradiol aux normes de ménopause.
Si patiente sous Torémifène et âge < 60 ans : FSH, œstradiol aux normes de ménopause [7].
NB : l’aménorrhée chimio-induite n’est pas une ménopause.
Les inhibiteurs de l’aromatase (IA) de la troisième génération ont été utilisés dans le traitement du cancer du sein depuis les années 1990.
Les IA inhibent la transformation des androgènes provenant de la surrénale en œstrogènes dans les tissus périphériques et les cellules tumorales. Ce qui entraîne chez la femme ménopausée une chute du taux d’œstrogène circulant [4].
Il existe deux types d’ IA : les non stéroïdiens réversibles (Anastrozole et Letrozole) et les IA stéroïdiens non-réversibles (Exemestane).
Les trois molécules sont considérées comme équivalentes pour l’efficacité et la toxicité.
Elles sont devenues un standard de traitement dans l’hormonothérapie adjuvante de la femme ménopausée.
| Étude | Type | Effectif | Schéma | Résultats DFS |
| BIG 1-98[8] | P III | 8.028 04 Bras | 5 ans T/ 5 ans L/ 2 ans Tam-3 ans L 2 ans L-3 ans T | Avec Letrozole HR = 0,91 IC 95% 0.81-1.01 |
| ATAC[9] | P III | 9.366 | 5ans T vs 5 ans A | HR= 0.85 IC 95% 0.76-0.94 p=0.003 |
| IES[10] | P III | 2-3 ans T suivies de 2-3 ans Evs 5 ans T | HR =0.93 IC95% 0.80-1.07 | |
| TEAM[11] | P III | 9.775 | 2-3 ans T suivies de 2-3 ans Evs 5 ans E | HR =0.97IC 95% 0.88-1.08 p=0.604 |
T = tamoxifène ; L = Letrozole ; A = Anastrozole ; E = Exemestane ; HR = hazard ratio ; IC = intervalle de confiance.
Toutes ces études ont comparé le Tamoxifène à une anti-aromatase et ont conclu que chez la femme ménopausée l’indication actuelle est d’inclure une anti aromatase en up-front ou en switch.
D’autres études ont comparé les inhibiteurs de l’aromatase entre elles dont :
Tableau : Études ayant comparé les inhibiteurs de l’aromatase entre elles
| Etude | Phase | Effectif | Schéma | Résultats |
| MA 27 [12] | III | 7.576 | Anastrozole (1 mg/j) vs Exemestane (25 mg/j) | HR 1.02, 95% CI (0.87, 1,18); p=0.85 |
| FACE [13] | III | 4.136 | Anastrozole (1 mg/j) vs Letrozole (2,5 mg/j) | DFS à 5 ans 82,9%(A) vs 84,9% (L) HR 0,93, 95% CI (0.80, 1,07); p=0.31 |
La prolongation de l’hormonothérapie adjuvante au-delà de 5 ans
Les résultats ont montré que chez des patientes non sélectionnées, 10 ans de tamoxifène ne sont pas plus bénéfiques que les 05 ans standard, ATLAS aTTom ont montré que 10 ans de tamoxifène sont supérieurs à 5 ans de tamoxifène chez des patients qui présentent une maladie de mauvais pronostic (âge jeune, infiltration ganglionnaire, haut grade) ; mais il faut savoir que 10 ans de tamoxifène est corrélé avec un taux plus important de cancers de l’endomètre et de maladie thrombo-embolique.
Aussi, la prolongation par inhibiteurs de l’aromatase n’est licite que chez les patientes qui ont reçu du tamoxifène en adjuvant.
Tableau : La poursuite du Tamoxifène après 5 ans de Tamoxifène :
| Etude | Phase | Effectif | Schéma | Résultats |
| ATLAS [14] | III | 12.894 | 5 ans vs 10 ans de Tam | Analyse poolée : réduction du risque de décès de 9% RR 0.91, 95% CI (0.84, 0.97); p=0.008 |
| ATTom [14] | III | 6.953 | 5 ans vs 10 ans de Tam | |
| NSABP B14 [15] | III | 1.172 | 10 ans de Tam vs 5 ans Placebo | DFS 78% vs 82% p= 0,03 en faveur de 5 ans Tam |
| Scottish [16] | III | 342 | Tam adj vs Tam après rechute | Pas de bénéfice du Tam au-delà de 05 ans. |
| ECOG 4181 [17] | III | 193 | 5 ans Tam vs Tam jusqu’à progression | HR = 0,68 p = 0,13 |
Tableau : La poursuite par IA après 5 ans de Tamoxifène :
| Étude | Phase | Effectif | Schéma | SSM |
| MA17 [18] | III | 5170 | 3 ans L vs Nihil | HR = 0,57 |
| NSABP B33 [19] | III | 1598 | 5 ans E | HR = 0,68 |
| ABCSG-6a [20] | III | 856 | 3 ans A | HR = 0,62 |
L : Letrozole ; E : Exemestane ; A : Anastrozole ; SSM : Survie sans Maladie ; HR : Hazard ratio ; Nihil : rien
MA-17, NSABP B33 et ABCsg 6a ont démontré que la poursuite de l’hormonothérapie par inhibiteur de l’aromatase après 5 ans de Tamoxifène améliore la survie sans maladie.
Tableau : La poursuite 5 ans IA après 5 ans d’Hormonothérapie adjuvante :
| Étude | Phase | Effectif | Schéma | SSM | |
| DATA [21] | III | 1.912 | 2-3 ans T : 6 ans Avs 3 ans A | HR 0,79(0,62-1,02) p=0,07 | |
| IDEAL [22] | III | 1.824 | 5 ans T/IA :5 ans L vs 2,5 ans L | HR 0 ,96(0,76-1,20) p=0,70 | |
| NSABP B42 [23] | III | 3.923 | 5 ans T/IA : | HR 0,85(0,73-0,99) p=0,048 | |
T : Tamoxifène ; A : Anastrozole ; IA : Inhibiteur de l’aromatase ; L : Letrozole ; vs : versus ; HR Hazard ratio
Les trois études : DATA, IDEAL, NSABP B42 n’ont pas atteint leur objectif principal.
Les analyses par sous-groupes suggèrent qu’une population à risque élevé de rechute bénéficie de cette stratégie prolongée, la décision doit donc tenir compte des toxicités des inhibiteurs de l’aromatase notamment la majoration de l’ostéoporose et des évènements vasculaires artériels.
Les effets secondaires
Les effets indésirables de ces traitements peuvent être handicapants et affecter sérieusement la qualité de vie de ces patientes.
Tableau : Toxicités des traitements
| Symptôme | Tamoxifène | Inhibiteurs de l’aromatase |
| Baisse de la libido | + | ++ |
| Bouffées de chaleur | + | + |
| Cancer de l’utérus | + | – |
| hypercholestérolémie | – | ± |
| Modifications pondérales | + | + |
| Ostéopénie/ostéoporose | En pré-ménopause | + |
| Pertes vaginales | + | – |
| Sécheresse vaginale | Surtout en pré-ménopause | + |
| Thrombo-embolie | + | (-) |
| Troubles cognitifs | + | + |
| Troubles du sommeil | + | + |
Le Fulvestrant
Le Fulvestrant est un anti-œstrogène qui se distingue du tamoxifène car il s’agit d’un anti-œstrogène « pur», il induit une dégradation des récepteurs aux œstrogènes [24].
L’étude « Confirm » a permis de définir les doses du fulvestrant à 500 mg J1-J14-J28 puis tous les 28 jours, l’essai de phase II « FIRST» a montré une supériorité du Fulvestrant par rapport à l’Anastrozole avec une PFS de 23,1 mois vs 13,1 mois (p=0,01) [25] ; et l’essai de phase III « FALCON » qui a recruté 462 patientes est venu confirmer cette supériorité du Fulvestrant avec une PFS de 16,6 mois vs 13,8 mois pour l’Anastrozole (HR : 0,797 IC 95 % 0,63-0,99 p= 0,0486) [26]. Depuis, le Fulvestrant a regagné la première ligne d’hormonothérapie dans le cancer du sein RH positif, Her 2 négatif.
Les associations de l’hormonothérapie
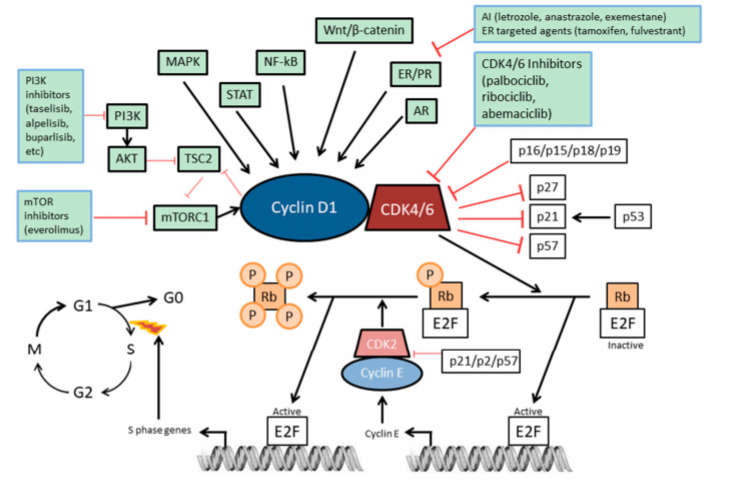
Figure : les principales voies de signalisation impliquées et les principaux produits impliqués dans la résistance à l’hormonothérapie du cancer du sein RH positif-Her 2 négatif en phase métastatique [24].
Les inhibiteurs de cycline CDK4/6
Le complexe CDK 4/6-cycline D conduit à la phosphorylation et l’inactivation de la protéine Rb puis la progression du cycle cellulaire de la phase G1 à la phase S [27].
Ces trois dernières années ont été marquées par la confirmation de trois inhibiteurs CDK4/6 Palbociclib, Ribociclib et Abémaciclib dans le traitement du cancer du sein métastatique RH positif et Her 2 négatif.
Tableau : Comparaison des différents inhibiteurs de cycline (les 03 CDK)
| PALBOCICLIB | RIBOCICLIB | ABEMACICLIB | |
| Dosage | 125 mg/j | 600 mg/j | 200 mg 2x/j |
| Schéma | 03 sem. (01 sem. de repos) | 03 sem. (01 sem. de repos) | Administration continue |
| Pharmacocinétique | Tmax 4,2-5,5 h T1/2 25,9- 26,7 h | Tmax 4 h T1/2 24-36 h | Tmax 4-6 h T1/2 17-38 h (Passe la barrière hémato-méningée) |
| Pénétration du SNC | Non | Non | Oui |
| Toxicités limitantes | Neutropénie, thrombopénie | Neutropénie, thrombopénie | Fatigue |
| Autres toxicités | Nausées, anorexie, diarrhée, fatigue, anémie | Nausées, mucite Créat, allongement QT | Diarrhée, neutropénie |
Tmax : Temps où la concentration maximale est atteinte, T1/2 : temps de demi-vie.
La neutropénie des inhibiteurs de CDK 4/6 se distingue par une réversibilité rapide, qui reflète un effet cytostatique sur les précurseurs neutrophiles au niveau médullaire. Ainsi, le palbociclib et le ribociclib sont administrés de façon intermittente afin de permettre une récupération hématologique. De façon intéressante, l’abémaciclib présente une toxicité digestive plus importante, à type de diarrhée, et qui nécessite une chimioprophylaxie par lopéramide tandis que la neutropénie est moins évidente, ce qui permet une administration continue.
Dans le cancer du sein localement avancé et /ou métastatique RH positif, Her 2 négatif
- L’association palbociclib/létrozole est approuvée aux USA depuis février 2016
- L’association palbociclib/Fulvestrant est indiquée depuis février 2017
- Le Palbociclib est actuellement enregistré en Algérie.
- Depuis mars 2017 la FDA approuve l’association Ribociclib/anti-aromatase
- Et depuis septembre 2017 abemaciclib est approuvé aux USA pour les patientes qui présentent un cancer du sein localement avancé ou métastatique RH positif, Her2 négatif ayant reçu une hormonothérapie antérieure [28,29,30].
Les inhibiteurs mTOR
Grace à la compréhension des mécanismes de l’hormono-résistance et l’identification des voies et des cibles impliquées, la voie mTOR est ciblée.
| Étude Phase Effectifs Schéma SSP BOLERO 2 [31] III 724 RH+Her2- Après IA Exemestane (25 mg/j) +/- Everolimus (10 mg/j) 6,9 mois vs 2,8 mois HR 0,43 (IC 95% 0.35-0,54) p<0,0001 TAM-RAD [32] II 111 Tamoxifène (20 mg/j) +/- Everolimus (10 mg/j) 8,6 mois vs 4,5 mois P=0,0026 BRE-43 [32] II 31 Fulvestrant + Everolimus 7,4 mois (IC 95%1,9-12,1) |
Les résultats intéressants de l’étude Boléro-2 ont permis l’AMM de l’association Exemextane/Everolimus après progression aux inhibiteurs de l’aromatase, en prenant en considération les toxicités de l’everolimus (mucite, pneumopathie et désordres métaboliques).
Les inhibiteurs PI3K
Les aberrations de la voie PI3K/AKT/mTOR sont courantes dans le cancer du sein, car environ 40% des patientes atteintes un cancer du sein RH positifs et Her 2 négatif présentent une mutation PI3KCA, ceci active la voie PI3K et mène à une résistance à l’hormonothérapie, Alpelisib est un inhibiteur α sélectif de la PI3K oral, l’isoforme α est la forme mutée dans le cancer du sein.
| Étude Phase Effectif Schéma SSP SOLAR-1 [33] III 572 Dont 341 PI3KCA mutées Fulvestrant + Alpelisib (300 mg/j) vs Fulvestrant + Placebo Chez la population PI3KCA mutée 11,1 mois vs 3,7 mois HR 0,48 IC 95% (0,32-0,71)p=0,00065 SANDPIPER [34] III 516 PI3KCA Mutées R2:1 Fulvestrant + Taselisib vs Fulvestrant + Placebo 7,4 mois vs 5,4 mois HR 0 ,70 (IC 95% 0.56-0.89) p=0,0037 Belle -3 [35] III 432 R 2 :1 Fulvestrant + Buparlisib vs Fulvestrant + Placebo 3.9 mois vs 1.8 mois HR 0.67 (IC 95% (0.53-0.84) p = 0.0003 |
La relation entre les voies CDK 4/6 et PI3K-mTOR
Il existe un « crosstalk » entre ces différentes voies certaines études ont trouvé que leur inhibition combinée permet débloquer la croissance tumorale.
En effet, Vora et al., ont découvert que les inhibiteurs CDK4/6 étaient capables de sensibiliser les lignées cellulaires mutées PI3KCA aux inhibiteurs PI3K, par la suite Herrera-Abreu et ses collègues ont montré que la combinaison des inhibiteurs CDK4/6 et de PI3k induisent l’apoptose des cellules tumorales, d’autres auteurs ont aussi trouvé que la combinaison d’inhibiteurs CDK4/6 et PI3K avec l’hormonothérapie était d’autant plus efficace[35], Ces résultats ont été obtenus in vitro, et une confirmation par des études cliniques est indispensable.
Conclusion
Selon les recommandations de l’ASCO, ABC et NCCN 2019 l’hormonothérapie est le standard de traitement de première ligne pour le cancer du sein RE positif métastatique hormis la crise viscérale[36].
Associés ou non aux analogues LHRH, le tamoxifène et les inhibiteurs de l’aromatase sont les acteurs principaux de l’hormonothérapie, le fulvestrant est un anti-œstrogène « pur » qui induit une dégradation du récepteur à l’œstrogène, il est bien toléré et offre une alternative thérapeutique aussi intéressante.
Une bonne connaissance des mécanismes d’action et des effets secondaires de tous ces produits permet d’assurer une prévention efficace des toxicités et une meilleure adhérence et observance du traitement tout en offrant à la patiente une bonne qualité de vie et une survie prolongée.
Les nouvelles voies de recherche vont vers les associations multiples pour tenter de bloquer plusieurs voies de signalisation pour optimiser les résultats et prolonger encore la survie.
Prendre en considération le choix de la patiente, et son éducation pour la prévention des effets secondaires, sont les garanties d’une bonne observance du traitement.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Medioni, Hormonothérapie des cancers du sein en situation adjuvante, et métastatique et néoadjuvante. EMC Gynécologie ; 2012 7(2) 1-16 (article 877-A-10).
- Inhibiteurs CDK 4/6 et cancers du sein métastatiques hormono-dépendants Cyclin-dependent kinases 4/6 inhibitors in hormone receptor positive metastatic breast cancers, Diéras, M.P. Sablin, J.Y. Pierga.
- Hormonothérapie dans le Cancer du Sein : Efficacité et effets adverses ; Rahel Odermatt ; Anita Wolfer ; Khalil Zaman ; Revue Médicale Suisse 2013 vol9 1090-1094.
- Nouvelles stratégies thérapeutiques dans le cancer du sein hormono-dépendant métastatique Paul Vilquin : Pascale Cohen, Thierry Maudelonde, Olivier Tredan, Isabelle Treilleux, Thomas Bachelot, Pierre-Etienne Heudel, Bull Cancer 2015; 102: 367–380
- Le tamoxifène en situation adjuvante dans le cancer du sein : trente ans d’expérience, 26es journées de la SFSPM, Nancy, novembre 2004
- Tailoring Adjuvant Endocrine Therapy for Premenopausal Breast Cancer, Prudence A et al, for the SOFT and TEXT Investigators and the International Breast Cancer Study Group, N Engl J Med 2018; 379:122-137, DOI: 10.1056/NEJMoa1803164
- NCCN Guidelines Version 4.2018
- Adjuvant Letrozole and Tamoxifen Alone or Sequentially for Postmenopausal Women With Hormone Receptor–Positive Breast Cancer: Long-Term Follow-Up of the BIG 1-98 Trial. Thomas Ruhstaller, MD & al, BIG 1-98 Collaborative Group and the International Breast Cancer Study Group, Journal of Clinical Oncology2019 37:2, 105-114
- Effect of anastrozole and tamoxifen as adjuvant treatment for early-stage breast cancer: 10-year analysis of the ATAC trial.,Cuzick J1, Sestak I, Baum M, Buzdar A, Howell A, Dowsett M, Forbes JF; ATAC/LATTE investigators., Lancet Oncol 2010 Dec;11(12):1135-41. doi: 10.1016/S1470-2045(10)70257-6. Epub 2010 Nov 17.
- Exemestane as adjuvant treatment of early breast cancer: intergroup exemestane study/tamoxifenexemestane adjuvant multicenter trials, Jones SE, Clin Breast Cancer 2006 Feb;6Suppl 2:S41-4.
- Adjuvant tamoxifen and exemestane in women with postmenopausal early breast cancer (TEAM): 10-year follow-up of a multicentre, open-label, randomised, phase 3 trial, Derks MGM, Blok EJ, Seynaeve C, Nortier JWR, Kranenbarg EM, Liefers GJ, Putter H, Kroep JR, Rea D, Hasenburg A, Markopoulos C, Paridaens R, Smeets JBE, Dirix LY, van de Velde CJH; Lancet Oncol2017 Sep;18(9):1211-1220. doi: 10.1016/S1470-2045(17)30419-9. Epub 2017 Jul 18.
- Exemestane versus anastrozole in postmenopausal women with early breast cancer: NCIC CTG MA.27–a randomized controlled phase III trial, Goss PE1, Ingle JN, Pritchard KI, Ellis MJ, Sledge GW, Budd GT, RabaglioM, Ansari RH, Johnson DB, Tozer R, D’Souza DP, Chalchal H, Spadafora S, Stearns V, Perez EA, Liedke PE, Lang I, Elliott C, Gelmon KA, Chapman JA, Shepherd LE; J ClinOncol2013 Apr 10;31(11):1398-404. doi: 10.1200/JCO.2012.44.7805. Epub 2013 Jan 28.
- The FACE trial: letrozole or anastrozole as initial adjuvant therapy? Jonat W, Mundhenke C, Cancer Invest2007 Feb;25(1):14-8.
- Azim HA, Saadeldeen A. Commentary on “aTTom”: long-term effects of continuing adjuvant Tamoxifen to 10 years. Chin ClinOncol 2014;3(1):7. doi: 10.3978/ j.issn.2304-3865.2013.12.02
- NSABP Breast Cancer Clinical Trials: Recent Results and Future Directions, Eleftherios P. Mamounas, MD Clin Med Res 2003 Oct; 1(4): 309–326.
- Scottish adjuvant tamoxifen trial: a randomized study updated to 15 years; H.J Stewart, Prescott, Robin J; Forrest, A P,Journal of the National Cancer Institute, Vol. 93, No. 6, 2001, p. 456-62.
- Duration of Adjuvant Tamoxifen Therapy John Bryant, Bernard Fisher, James Dignam ,journal of the National Cancer Institute Monographs No. 30, 2001.
- Extending Aromatase-Inhibitor Adjuvant Therapy to 10 YearsPaul E. Goss, M.D., Ph.D., James N. Ingle, M.D., Kathleen I. Pritchard, M.D., Nicholas J. Robert, M.D., Hyman Muss, M.D., Julie Gralow, M.D., Karen Gelmon, M.D., Tim Whelan, B.M., B.Ch., Kathrin Strasser-Weippl, M.D.,Sheldon Rubin, M.D. KerenSturtz, M.D., Antonio C. Wolff, M.D.,etal.NEngl J Med 2016; 375:209-219DOI: 10.1056/NEJMoa1604700
- Benefit from exemestane as extended adjuvant therapy after 5 years of adjuvant tamoxifen: intention-to-treat analysis of the National Surgical Adjuvant Breast And Bowel Project B-33 trial.,Mamounas EP1, Jeong JH, Wickerham DL, Smith RE, Ganz PA, Land SR, Eisen A, Fehrenbacher L, Farrar WB, Atkins JN, Pajon ER, Vogel VG, Kroener JF, Hutchins LF, Robidoux A, Hoehn JL, Ingle JN, Geyer CE Jr, Costantino JP , Wolmark N.Clin.Oncol 2008 Apr 20;26(12):1965-71. doi: 10.1200/JCO.2007.14.0228. Epub 2008 Mar 10.
20. Extended adjuvant therapy with anastrozole among postmenopausal breast cancer patients: results from the randomized Austrian Breast and Colorectal Cancer Study Group Trial 6a.?Jakesz R1, Greil R, Gnant M, Schmid M, Kwasny W, Kubista E, Mlineritsch B, Tausch C, Stierer M, Hofbauer F, Renner K, Dadak C, Rücklinger E, Samonigg H; AustrianBreast and Colorectal Cancer Study Group.J.Nat.CancerInst 2007 Dec 19;99(24):1845-53. Epub 2007 Dec 11
21. Extended adjuvant aromatase inhibition after sequential endocrine therapy (DATA): a randomised, phase 3 trial.,Tjan-Heijnen VCG, van Hellemond IEG, Peer PGM, Swinkels ACP, Smorenburg CH, van der Sangen MJC, Kroep JR, De Graaf H, Honkoop AH, Erdkamp FLG, van den Berkmortel FWPJ, de Boer M, de Roos WK, Linn SC, Imholz ALT, Seynaeve CM; Dutch Breast Cancer Research Group (BOOG) for the DATA Investigators lancet Oncol2017 Nov;18(11):1502-1511. doi: 10.1016/S1470-2045(17)30600-9. Epub 2017 Oct 12.
22. Optimal Duration of Extended Adjuvant Endocrine Therapy for Early Breast Cancer; Results of the IDEAL Trial.,Blok EJ, Kroep JR, Meershoek-Klein Kranenbarg E, Duijm-de Carpentier M, Putter H, van den Bosch J, Maartense E, van Leeuwen-Stok AE, Liefers GJ, Nortier JWR, Rutgers EJT, van de Velde CJH1; IDEAL Study Group, J Nat Cancer Inst. 2018 Jan 1;110(1). doi: 10.1093/jnci/djx134;
23. Use of Letrozole after aromatase inhibitor based therapy in postmenopausal breast cancer (NRG Oncology/NSABP B-42): a randomized, double blind, placebo controlled, phase 3 trial, Prof Eleftherios, P mamounas MD, Hanna Bandos PhD, prof Barry C Lembersky MD, Prof Jong HyeonJeong PhD, prof Charles E Geyer Jr MD, PrivaRastogi MD et al The Lancet Oncology Volume 20 Issue 1, p 88-99, January 01 2019.
24. Hormonothérapie des cancers du sein; Patricia de Cremoux ; Bull Cancer 2011 : 98 ; 1311-1319.
25. Activity of fulvestrant 500 mg versus anastrozole 1 mg as first-line treatment for advanced breast cancer: results from the FIRST study, Robertson JF, Llombart-Cussac A, Rolski J, Feltl D, Dewar J, Macpherson E, Lindemann J, Ellis MJ, J ClinOncol2009 Sep 20;27(27):4530-5.
26. Fulvestrant 500 mg versus anastrozole 1 mg for hormone receptor-positive advanced breast cancer (FALCON): an international, randomised, double-blind, phase 3 trial, Prof John F R Robertson, MD ,Prof Igor M Bondarenko, PhD, Ekaterina Trishkina, PhD, Mikhail Dvorkin, MD, Prof Lawrence Panasci, MD, Alexey Manikhas, MD,et al, The Lancet Vol 388, Issue 10063, p 2997-3005, Dec 17,2016.
- Updates on the CDK4/6 Inhibitory Strategy and Combinations in Breast Cancer NavidSobhani et al Cells, april 2019, 8, 321; doi:10.3390/cells8040321
- Ma CX, Ellis MJ, Petroni GR, Guo Z, Cai SR, Ryan CE, et al. A phase II study ofUCN-01 in combination with irinotecan in patients with metastatic triple negative breast cancer. Breast Cancer ResTreat. 2013;137:483–92.
- TargetingtheCyclin- dependantKinases CDK 4/6 in oestrogenreceptor positive breastcancersRichard.S.Finn, Alexey Aleshinand Denis. J.Slamon, Finn et al. Breast Cancer Research (2016) 18:17 DOI 10.1186/s13058-015-0661-5
- 27- Resultsfrom Monarch1 trialofAbemaciclibmonotherapy Phase II data Elli lilly&companyjune 03 2016
- Everolimus in Postmenopausal Hormone-Receptor–Positive Advanced Breast Cancer José Baselga, M.D., Ph.D., Mario Campone, M.D., Ph.D., Martine Piccart, M.D., Ph.D., Howard A. Burris, III, M.D., Hope S. Rugo, M.D., TarekSahmoud, M.D., Ph.D., Shinzaburo Noguchi, M.D., Michael Gnant, M.D., Kathleen I. Pritchard, M.D., Fabienne Lebrun, M.D., J. Thaddeus Beck, M.D., Yoshinori Ito, M.D,et al, February9,2012,NEnglJMed2012;366:520-529DOI: 10.1056/NEJMoa1109653.
- Everolimus in The treatment of Metastatic Breast Cancer ; Melanie E Royce and Diaa Osman Breast Cancer 2015;9:p73-79 doi 10.4137/BCBCR.S29268.
- SOLAR-1: Alpelisib in Patients With PIK3CA-Mutated HR-Positive, HER2-Negative Advanced Breast Cancer Cut-off 12 juin 2018; www.clinicaltrials.gov (NCT02437318).
- SANDPIPER: Phase III study of the PI3-kinase (PI3K) inhibitor taselisib (GDC-0032) plus fulvestrant in patients (pts) with estrogen receptor (ER)-positive, HER2-negative locally advanced or metastatic breast cancer (BC) enriched for pts with PIK3CA-mutant tumors.JoseBaselga et al ;Journal of Clinical Oncology2018 36:18_suppl, LBA1006-LBA1006
- Buparlisib plus fulvestrant in post menopausal women with hormone-receptor positive, Her 2 negative advanced breast cancer progressing on or after mTOR inhibitor (BELLE-3): a randomized, double blind, placebo –controlled, phase 3trial; Angelo Di Leo, Prof Stephen MD,Johnston MD, KeunSeok lee MD et al, The Lancet Oncology, vol 19, issue 1 p 87-100 January , 01, 2018.
- fatimacardoso et al Ann Oncol 2014 ; 1-18


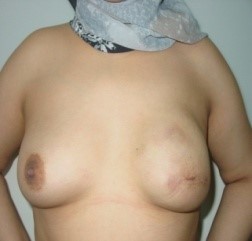


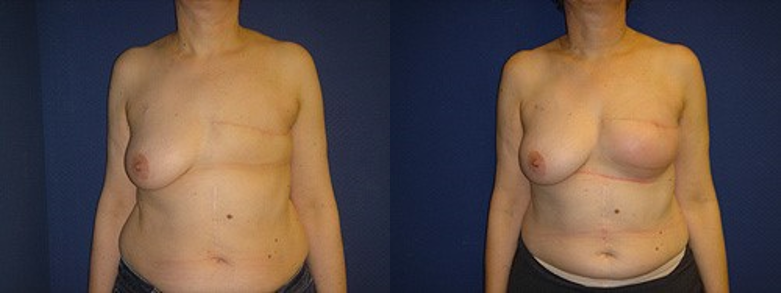
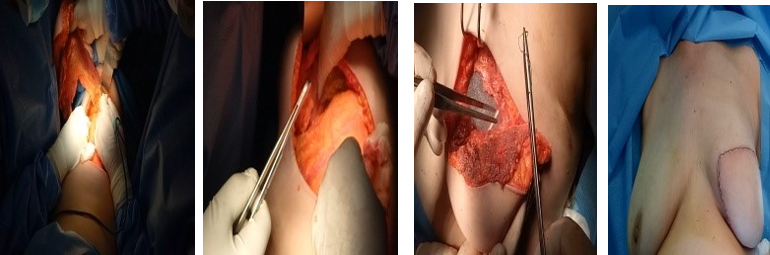
 (Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC
(Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC