Y. KACIMI, I. ABAYAHIA I. TOUILEB, M. SULAIMAN,N. AIT MOULOUD, M. TERAHI; Service d’Ophtalmologie, CHU Nafissa Hamoud, Husein dey, Alger
Abstract
Grave’s Orbitopathy (OD) is an inflammatory disease in which immune disorder leads to an increase in the volume of striated muscle and orbital fat with multiple clinical consequences. Exophthalmos or proptoss is the major sign, Grave’s orbitopathy representing the 1st cause of exophthalmos in adults. Palpebral retraction, diplopia, and inflammatory signs (conjunctival hyperaemia, chemosis, and eyelids swelling) are also observed depending on the activity and severity of the disease. The management of OD is multidisciplinary. The management of OD include quit smoking (a major risk factor), and treatment of dysthyroidism (synthetic anti-thyroid drugs or replacement therapy) aimed at obtaining euthyroidism. In the acute phase, treatment is based on intravenous corticosteroids as first line medication. Surgery is only required when OD is stabilized (non-active phase) after medical treatment, or in emergency when the visual prognosis is engaged. The management of inflammatory OD refractory to corticosteroids requires immunosuppressive treatments as second-line medication.
Keywords : Inflammatory disease, Grave’s disease, proptosis, EUGOGO, corticosteroid therapy, Immunosuppressive treatment, orbital decompression.
Résumé
L’orbitopathie dysthyroïdienne (OD) est une pathologie inflammatoire de l’orbite où le désordre auto-immun conduit à l’augmentation de volume des muscles striés et de la graisse orbitaire avec de multiples conséquences cliniques. Cliniquement, l’exophtalmie en est le signe majeur, l’OD représentant la 1ère cause d’exophtalmie chez l’adulte. La rétraction palpébrale, la diplopie et des signes inflammatoires (hyperhémie conjonctivale, chémosis, œdème palpébral) complètent plus ou moins le tableau et renseignent sur l’activité et la sévérité de la maladie. La prise en charge de l’OD est multidisciplinaire. Les différents volets du traitement comportent notamment l’arrêt du tabagisme, facteur majeur d’aggravation et le traitement de la dysthyroïdie (anti-thyroïdiens de synthèse ou traitement substitutif) visant l’obtention d’une euthyroïdie. A la phase aiguë, le traitement repose sur la corticothérapie par bolus intraveineux. Le traitement chirurgical n’intervient qu’à la phase séquellaire, ou en urgence lorsque le pronostic visuel est engagé. La prise en charge des OD inflammatoires réfractaires aux bolus de corticoïdes, fait appel aux traitements immunosuppresseurs.
Mots-clés : Pathologie inflammatoire, maladie de Basedow, exophtalmie, EUGOGO, corticothérapie, immunosuppresseur, décompression orbitaire.
Introduction
L’orbitopathie dysthyroïdienne (OD) est une pathologie relativement fréquente rencontrée en ophtalmologie, en endocrinologie ou en médecine interne.
Il s’agit d’une affection dysimmunitaire chronique touchant la glande thyroïde avec pour conséquence une perturbation hormonale ainsi qu’un processus inflammatoire touchant les tissus (muscles et graisses) orbitaires.
L’OD est le plus souvent rencontrée dans le contexte d’une hyperthyroïdie (Maladie de Basedow). Cependant, elle peut également être retrouvée dans une moindre mesure dans les hypothyroïdies (Thyroïdite d’Hashimoto) mais également, de façon plus rare, sans atteinte apparente de la thyroïde, en euthyroïdie, on parle de syndrome de Means. Cette maladie touche préférentiellement les femmes, parallèlement, les hommes présentent plutôt des formes graves.
Le tabagisme constitue un facteur déclenchant ou aggravant. Sa prise en charge se fait dans un cadre pluridisciplinaire.
Sa prévention est un axe fondamental dans la prise en charge des pathologies de la thyroïde, son traitement comporte plusieurs volets.
Physiopathologie
La pathogénie de la maladie de Basedow demeure incomplètement élucidée.
Il s’agit d’un désordre immunologique impliquant les lymphocytes B et T et les fibroblastes orbitaires, au cours duquel des auto-anticorps sont dirigés contre les récepteurs de la TSH. Ainsi, les lymphocytes T activés vont sécréter des cytokines, notamment l’IL-4 et amplifier la réponse des lymphocytes B qui sécrètentlesauto-anticorpscaractéristiquesdelamaladie: les TRAK. Ceci entraîne une synthèse excessive d’hormones thyroïdiennes par les thyréocytes au niveau thyroïdien.
L’orbite, représente donc la seconde cible des auto-anticorps [1]. Les fibroblastes orbitaires, expriment à leur surface des R-TSH et des R-IGF1 (insuline-like growth factor-1 receptor) qui sont pris pour cible par ces auto-anticorps [2].
Ceux-ci répondent en proliférant et en se différenciant en cellules effectrices, synthétisant divers médiateurs et cytokines: ils sont non seulement responsables de la synthèse de glycosaminoglycanes (GAG), mais se différencient en myofibroblastes ou lipofibroblastes (adipocytes).
Le potentiel de différenciation des fibroblastes dépend de l’expression d’un antigène de surface le Thy-1 : sous l’effet du TGF-β (transforming growth factor β) il y a différenciation des fibroblastes Thy-1 positifs en myofibroblastes, et les fibroblastes Thy-1 négatifs en adipocytes.
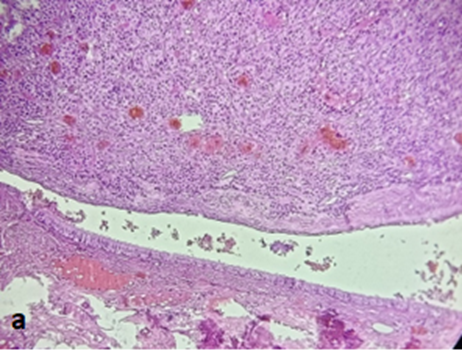
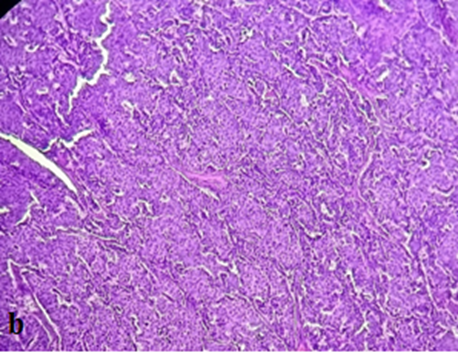
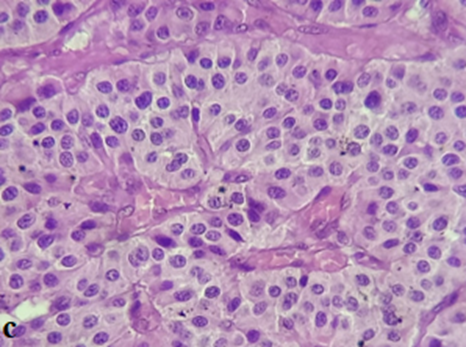
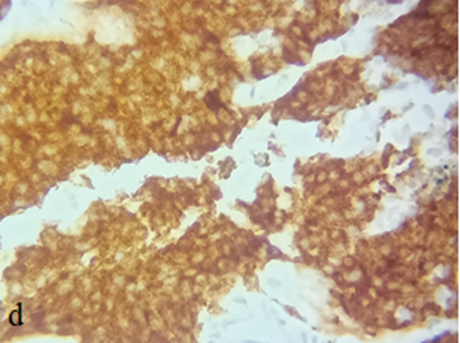
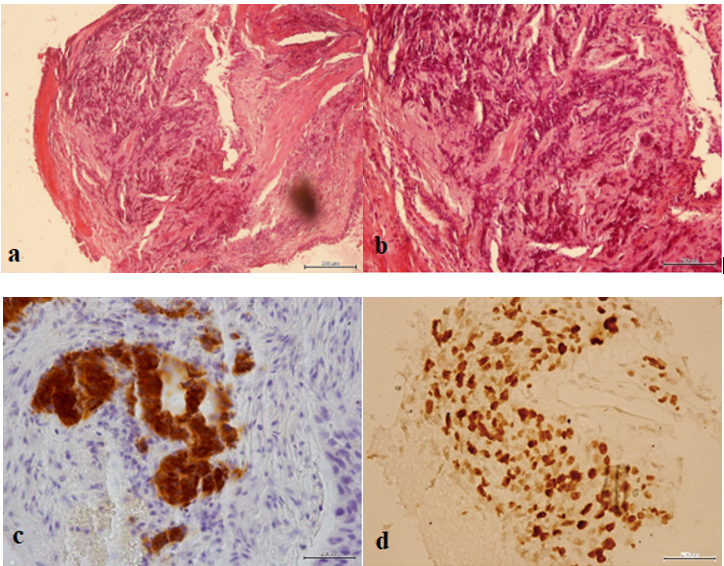
Histologiquement, il y a accumulation de glycosaminoglycanes dans les muscles et/ou la graisse orbitaire, avec infiltration puis fibrose des muscles oculomoteurs et de la graisse orbitaire, expliquant le tableau clinique.
Epidémiologie et facteurs de risque
L’OD touche préférentiellement les femmes. Les hommes sont davantage sujets à des formes plus sévères d’OD. L’hyperthyroïdie avec un titre élevé d’anticorps anti-RTSH est un facteur de risque prouvé de survenue d’OD chez les patients dysthyroïdiens [3].
Le tabagisme est un facteur de risque prouvé de survenue ou d’aggravation d’une OD.
- Concernant le tabac :
Il augmente le risque de survenue d’une orbitopathie en cas de maladie de Basedow, les sujets fumeurs développent des formes plus sévères d’OD.
L’apparition de novo ou la progression d’une OD après traitement thyroïdien par Iode radioactif est plus fréquente chez les patients tabagiques, les patients fumeurs ont une réponse plus retardée ainsi que moins de bons résultats lors d’un traitement immunosuppresseur.
Le sevrage tabagique améliore le pronostic de prise en charge de l’OD.
Plus récemment, des études se sont intéressées à l’effet néfaste de l’hypercholestérolémie.
En effet, il s’avère qu’un taux élevé de LDL cholestérol représente un facteur de décompensation de l’OD [4], reflet d’une action pro-inflammatoire du LDL-cholestérol.
Malgré l’absence d’essais contrôlés et randomisés pour étayer ces affirmations, l’usage des statines pour le contrôle du taux de LDL-cholestérol paraît raisonnable.
Enfin, l’Iode radioactif (IRA thérapie) est un facteur de risque confirmé de récidive ou de survenue d’une OD [5,6], son effet sur le déclenchement d’une poussée peut être prévenu par administration concomitante d’une corticothérapie orale [7].
Clinique
Le début est le plus souvent insidieux sans orientation spécifique, avec photophobie, larmoiement, sensation de corps étrangers, douleurs oculaires, œdème des paupières et diplopie. L’atteinte est le plus souvent bilatérale dans 80 à 90 % des cas. Lorsqu’elle est unilatérale, il existe toujours une atteinte controlatérale minime à rechercher sur les explorations neuroradiologiques.
L’atteinte inflammatoire et l’augmentation de la pression intra-orbitaire peuvent entraîner une symptomatologie riche, qui varie également selon le stade de la maladie.
A- Atteintes de la surface oculaire
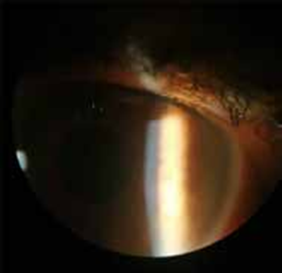
Il s’agit de signes inflammatoires essentiellement présents au stade précoce : hyperhémie conjonctivale en regard de l’insertion des muscles oculomoteurs, œdème palpébral, chémosis, œdème caronculaire, ainsi que des douleurs rétro-orbitaires.
D’autres signes, moins spécifiques, peuvent se voir : photophobie, larmoiement, syndrome sec, l’atteinte cornéenne, allant de la kératite sèche à l’ulcère voire l’abcès de cornée, surtout en cas de lagophtalmie.

B- Atteinte palpébrale
Quasi constante, c’est l’atteinte la plus fréquemment retrouvée dans l’OD.
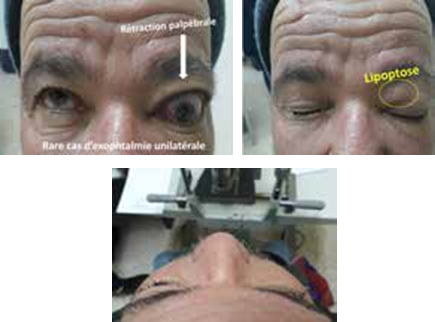
La rétraction palpébrale supérieure et/ou inférieure est évaluée cliniquement en mesurant la distance entre le bord libre des paupières et le limbe scléro-cornéen.
À l’état normal, le bord libre de la paupière supérieure recouvre le limbe de 2 mm environ et le bord libre palpébral inférieur affieure le limbe.
On parle de rétraction mineure lorsque la paupière supérieure est au limbe avec exposition sclérale («scleral show » est inférieure ou égale à 2 mm), de rétraction moyenne si la paupière supérieure est éloignée de 2 à 6 mm de la position normale et au-delà de 6 mm on juge la rétraction sévère.
L’asynergie oculopalpébrale (signe de von Graefe) est un élément caractéristique: la rétraction palpébrale supérieure entraîne un retard, voire une impossibilité de suivre le mouvement du globe oculaire dans le regard vers le bas, avec l’apparition d’un scleral show.
La lipoptose est caractérisée par l’apparition de « poches » inesthétiques liées à un affaiblissement du septum orbitaire.
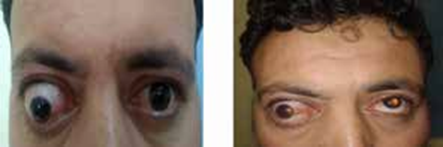
C- Exophtalmie
C’est la protrusion anormale du globe oculaire, en avant du cadre osseux orbitaire, en général axile, bilatérale le plus souvent, parfois asymétrique, très rarement unilatérale.
Elle résulte de l’augmentation de volume des muscles oculo-moteurs et /ou de la graisse orbitaire aux dépens d’un volume inextensible, l’orbite osseuse.
Cliniquement, elle peut être mesurée par l’exophtalmomètre de Hertel : Protrusion > 21 mm ou écart > 2mm entre les deux yeux.
D- Diplopie
Fréquente, la diplopie est présente dans 60 % des OD. Elle est parfois transitoire, en rapport avec les poussées évolutives de la maladie. Elle évolue en deux phases : la première, inflammatoire, avec
infiltration lymphoplasmocytaire et élargissement diffus du corps musculaire, au cours de laquelle le traitement médical vise à éviter la survenue de la seconde phase, celle de la fibrose avec synthèse de collagène par les fibroblastes activés, où la chirurgie des muscles oculomoteurs s’impose devant la persistance des limitations.
Le muscle droit inférieur est le plus fréquemment atteint, ainsi, la limitation la plus fréquente est l’élévation avec diplopie verticale comme c’est le cas pour notre patient (Figure 4).
Cette diplopie est explorée avec un test de Hess-Lancaster (Figure 5).

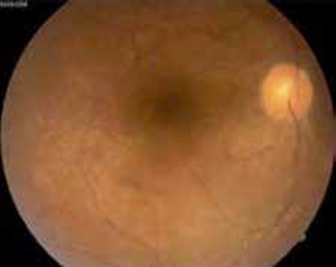
E- Neuropathie optique
Rare, elle représente une menace fonctionnelle majeure. L’augmentation de volume du contenu orbitaire, plus spécifiquement l’élargissement des muscles oculomoteurs à l’apex orbitaire conduit à une véritable neuropathie optique compressive.
Il est intéressant de noter que selon de nombreux auteurs, le risque de survenue d’une neuropathie optique est inversement proportionnel à la présence et la sévérité d’une exophtalmie, qui sont pourtant chacune une réponse à l’augmentation de volume du contenu orbitaire.
En effet, l’exophtalmie permettrait une forme de décompression naturelle vers l’avant, alors que la neuropathie résulte d’une compression à l’apex dans une orbite non extensible.
Le diagnostic repose surtout sur la réalisation d’un examen du champ visuel et d’une OCT papillaire avec mesure de la RNFL (épaisseur de fibres nerveuses parapapillaires).
La présence d’une neuropathie optique compressive représente une indication urgente d’un traitement chirurgical par décompression orbitaire osseuse plus ou moins graisseuse, précédé ou non de bolus de méthylprednisolone (MP) selon le degré de gravité.
Explorations
A- Tomodensitométrie (TDM)
La TDM possède dans l’exploration des OD 3 principaux intérêts :
Elle permet de visualiser l’aspect des muscles oculomoteurs, leur degré d’inflammation et d’infiltration graisseuse.
Du fait de son excellente analyse du cadre osseux, elle permet de mesurer l’index oculo-orbitaire (IOO), pour la classification de l’exophtalmie.
L’exophtalmie est classée selon trois grades de sévérité, après calcul de cet index qui correspond au rapport du segment pré-bicanthal externe (segment perpendiculaire au plan bicanthal externe jusqu’à la ligne tangente au bord antérieur de la cornée) sur la longueur axiale maximale du globe apprécié dans le plan de coupe axiale neuro-oculaire (PNO).
Sa valeur normale moyenne chez l’adulte emmétrope est inférieure à 66 % (seulement 2/3 de la longueur du globe oculaire en avant de la ligne pré-bicanthale).
Ainsi, on définit les trois grades d’exophtalmie axiale [8] :
- Grade 1 : 66,6 % < IOO < 100 % ;
- Grade 2 : IOO = 100 % (pôle postérieur tangent à la ligne pré-bicanthale) ;
- Grade 3 : IOO > 100 % (exophtalmie sévère).
Enfin, elle permet l’étude de l’anatomie des cavités sinusiennes du patient en vue d’une éventuelle décompression chirurgicale de l’orbite.
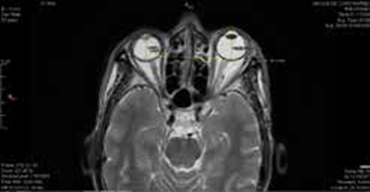
B- Imagerie par résonance magnétique (IRM)
L’examen se fait en pondérations T1 et T2 dans le plan neuro-oculaire (PNO), sans injection de produit de contraste.
Elle permet une analyse fine de la structure musculaire et graisseuse orbitaire, renseignant sur le degré d’infiltration inflammatoire ou de fibrose.
De plus, l’évaluation du risque de compression du nerf optique est plus aisée à l’IRM qu’à la TDM.
Enfin, l’imagerie permet un calcul volumique du contenu musculaire et graisseux qui sera l’un des éléments pris en compte pour le choix de la technique chirurgicale utilisée, décompression osseuse et/ou graisseuse.
L’injection intraveineuse de produit de contraste (gadolinium) est réservée aux formes très inflammatoires où un diagnostic différentiel avec une cellulite orbitaire ou une myosite, doit être éliminée.
Classifications
Avant d’aborder le volet de la prise en charge, il est tout aussi important de définir le degré de sévérité, ainsi que l’activité de la maladie.
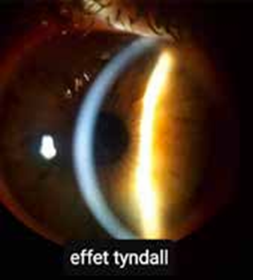
L’European Group on Graves’ Orbitopathy (EUGOGO) reprenant la classification proposée par Mourits en 1989, a proposé un score [9], le « clinical activity score », composé de 7 items cf. Tableau 1, permettant d’apprécier le caractère actif de l’inflammation dans l’OD et d’entamer le traitement approprié, se basant en parallèle sur le degré de sévérité de l’épisode [9] Tableau 2. Ce sont des critères reproductibles, permettant de classer simplement une OD, afin de permettre une prise en charge standardisée des poussées de la maladie.
Chaque item vaut 1 point L’OD étant considérée active si le CAS est ≥ 3 pts
| Score d’activité clinique (CAS score) |
| Douleur rétro-orbitaire spontanée |
| Douleur lors des mouvements oculaires verticaux (Haut/Bas) |
| Rougeur palpébrale |
| Hyperhémie conjonctivale |
| Œdème palpébral |
| Chémosis |
| Œdème de la caroncule/ du repli semi-lunaire |
| Atteinte minime | Rétraction palpébrale mineure(< 2 mm) Atteinte des tissus mous Exophtalmie < 3 mm Diplopie intermittente ou absente Kératite d’exposition répondant aux traitement mouillants |
| Atteinte moderée à sévère | Rétraction palpébrale ≥ 2 mm Atteinte modérée à sévère des tissus mous Exophtalmie ≥ 3 mm Diplopie permanente |
| OD menaçant le pronostic visuel | Neuropathie optique compressive Ulcère de cornée |
Traitement
La prise en charge de l’OD doit être multidisciplinaire, la collaboration ophtalmologiste-endocrinologue est primordiale. L’équilibration des paramètres biologiques s’avère tout aussi importante sur le long terme que le traitement anti-inflammatoire au moment des poussées de la maladie.
Certaines mesures thérapeutiques sont communes à tous les patients, alors que des mesures spécifiques seront proposées selon le degré de sévérité de l’OD.
A- Mesures générales :
Elles comprennent des mesures symptomatiques et le contrôle des facteurs de risque de survenue ou de récidive de l’OD. Les mesures symptomatiques sont représentées par :
- Le port de verres teintés, pour la prévention de la photophobie et la protection de la cornée ;
- L’hygiène palpébrale et conjonctivale (collyres, larmes artificielles) [10,11,12].
- L’injection de toxine botulique dans le releveur de la paupière supérieure afin de combattre la rétraction palpébrale et d’assurer une occlusion complète [13].
- A l’extrême, une tarsorraphie temporaire doit être réalisée. Le contrôle des facteurs de risque vise principalement la restauration d’une euthyroïdie, ceci passe par l’administration d’antithyroïdiens de synthèse et dans les cas réfractaires au traitement médical, la réalisation d’une thyroïdectomie totale ou alors une irradiation par Iode radioactif, avec administration de traitement hormonal substitutif dans les deux cas.
Il faut retenir qu’il faut éviter les passages en hypothyroïdie, cause majeure d’aggravation d’une OD [14].
Le sevrage tabagique est en parallèle un axe essentiel de la prise en charge ; en effet, l’association tabac-poussée d’OD est démontrée par des études de haut niveau de preuves scientifiques [15,16,17].
Par ailleurs, l’intérêt d’un traitement au sélénium, a été démontré, Marcocci et al. recommandent la dose de 200 µg par jour pendant six mois [21], pour l’amélioration de la qualité de vie des patients, ainsi qu’une amélioration de l’atteinte oculaire et une diminution de la progression de la maladie dans l’OD légère.
En cas de recours à une thérapie par iode radioactif, une corticothérapie orale concomitante est prescrite à raison de 0.1- 0.2 mg/kg/j en dose d’attaque, avec dégression progressive sur 6 semaines [18,19].
Chez les patients à haut risque (fumeurs, titre élevé de TRAK, hypothyroïdie sévère), une dose de 0.3- 0.5mg/kg/j est recommandée [20].
B- Corticothérapie
Elle représente la pierre angulaire de la prise en charge de l’OD. Son intérêt est démontré par plusieurs études prouvant son efficacité vs. Placebo [22].
C’est le traitement de première ligne dans les formes actives modérées à sévères.
Bien que la corticothérapie orale soit efficace, les glucocorticoïdes sont préférentiellement administrés par voie intraveineuse [23].
Le protocole de traitement le plus communément utilisé, se base sur des bolus de méthylprednisolone (MP) (Solume-drol©) à une dose cumulée de 4.5 g administrée de façon hebdomadaire sur 12 semaines (six bolus de 0.5 / semaine suivis de six bolus de 0.25 g / semaine) et s’avère très bien toléré par les patients.
La possibilité d’aller à des doses cumulées de 7.5 g (commençant par des bolus de 0.75 g suivis par des doses de 0.5 g) est réservée aux cas très sévères.
Il est à souligner qu’il ne faut pas dépasser des doses cumulées de glucocorticoïdes IV, sous peine de voir se développer des complications, des effets indésirables cardiovasculaires, rénaux, mais surtout hépatiques délétères [24, 25].
Une surveillance de la tension artérielle, de la fonction rénale, mais surtout de la fonction hépatique (dosage des ASLAT et ALAT à la recherche de cytolyse) est essentielle.
En revanche, dans les cas de neuropathie optique compressive, des bolus de MP par voie intraveineuse à fortes doses sont recommandés de façon urgente (0.5 g à 1 g/ jour pendant 3 jours consécutifs) [26].
Et en l’absence de réponse en deux semaines, une décompression orbitaire chirurgicale doit être réalisée.
C- Immunosuppresseurs et Immunomodulateurs
Plusieurs traitements ont été proposés dans le traitement des OD réfractaires à la corticothérapie IV.
De nombreux traitements immunosuppresseurs non spécifiques tels que la cyclosporine, l’azathioprine en association à la radiothérapie externe, le Méthothrexate et le Mycophénolate et les immunomodulateurs de 2e ligne spécifiques comme le Rituximab et plus récemment encore le Tocilizumab et le Teprotumumab, ont ainsi fait l’objet de diverses études avec des résultats plus ou moins concluants.
Dans le rapport de 2021 de l’EUGOGO, appuyé sur des études cliniques contrôlées et renforcées par des études de « vraie vie » [29], le Mycophénolate Mofétil 1g/ jour (ou 0.72 g/ jour de mycophénolate de sodium) pendant 24 semaines, a été retenu pour son efficacité et son profil de sécurité pour l’intégrer dans les protocoles de gestion des OD modérées à sévères [27,28] en tant que traitement de 1ère ligne.
C’est un inhibiteur compétitif de l’inosine monophosphate déhydrogénase, qui a pour effet de réduire la synthèse des anticorps par les lymphocytes B. Il produit également une apoptose des cellules T activées et inhibe le recrutement et l’adhésion d’autres cellules immunes.
Enfin, il possède une action sur les fibroblastes orbitaires en inhibant leur prolifération et leurs actions.
Des « études de vraie vie » menées sur une période d’observation de 04 ans ont également démontré l’efficacité et la sécurité du mycophénolate.
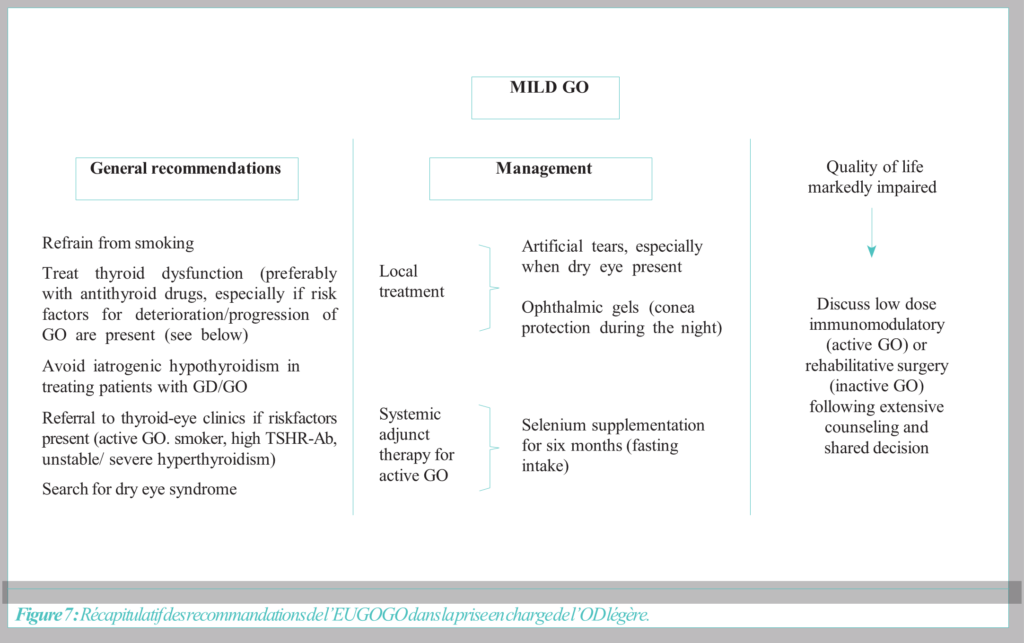
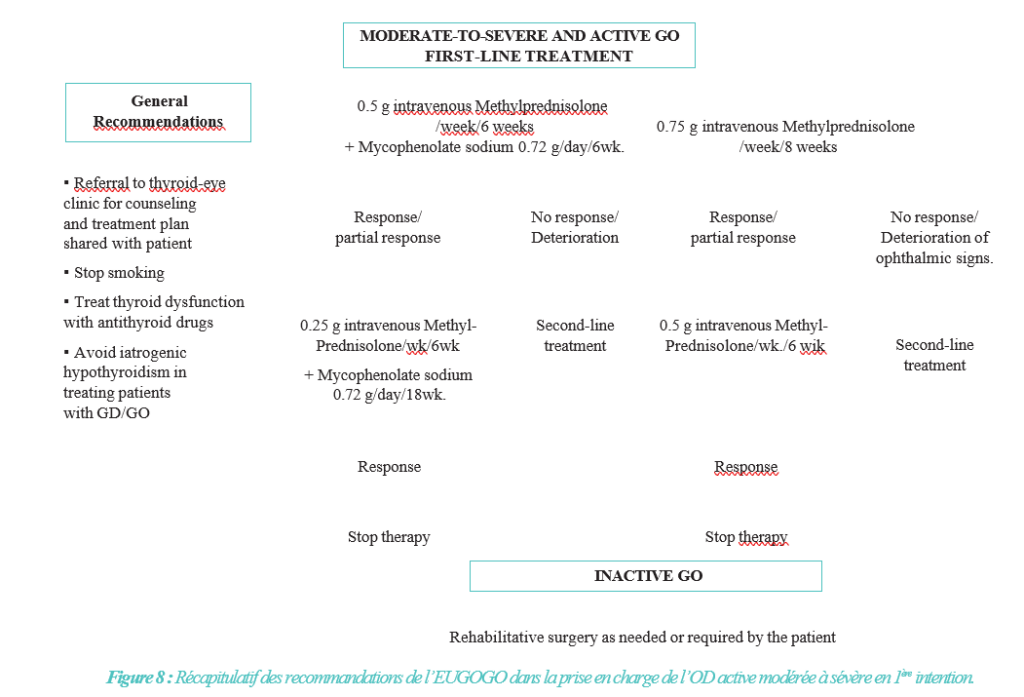
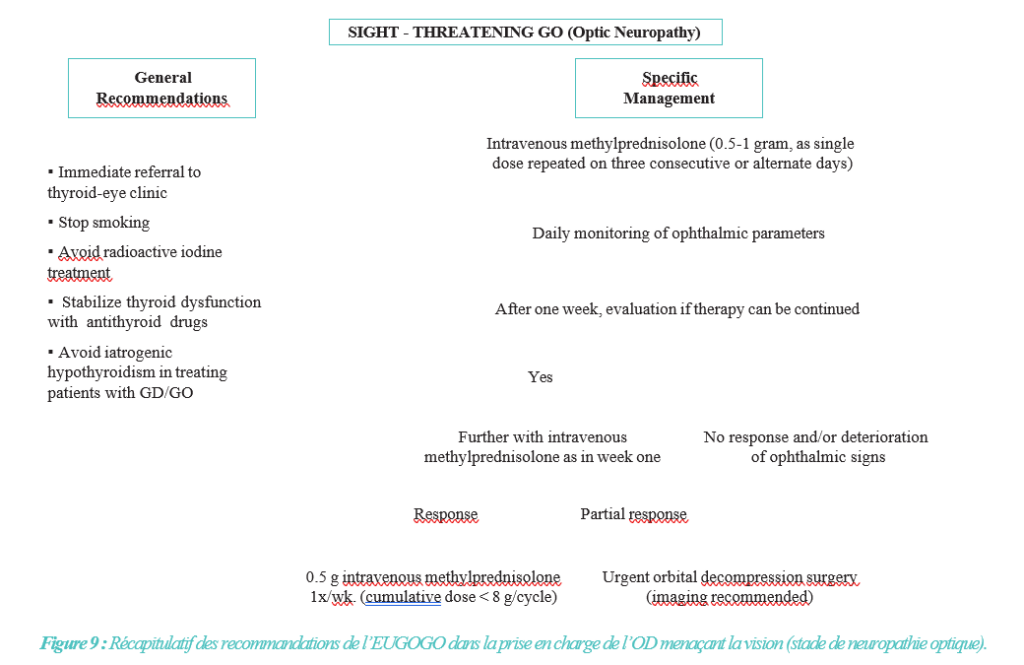
Les récapitulatifs 1, 2 et 3 (Figures 7, 8 et 9) représentent l’ensemble des recommandations retenues par l’EUGOGO pour le traitement des différentes formes d’OD selon le grade de sévérité.
D- Radiothérapie orbitaire externe
Plusieurs études ont prouvé l’efficacité de la radiothérapie orbitaire externe [30,31,32].
En pratique, elle est rarement utilisée seule, elle vient généralement en complément à la corticothérapie, avec une dose cumulée de 20 Gray (Gy) par orbite fractionnée en dix séances sur une période de deux semaines.
Un autre protocole proposant 1 Gy par semaine sur une période de 20 semaines s’avère tout aussi efficace, il a ainsi été retenu par l’EUGOGO [33].
Il semble que la radiothérapie orbitaire externe soit un traitement sûr à long terme, elle présente cependant des contre-indications comme le diabète et l’hypertension artérielle (risque de rétinopathie diabétique et hypertensive) et l’âge inférieur à 35 ans (risque cancérogène accru).
E- Traitements chirurgicaux
La chirurgie est le dernier volet de la prise en charge de l’OD. Elle est indiquée en urgence dans les OD avec menace visuelle, ou plus souvent à la phase séquellaire, lorsque l’inflammation est contrôlée (OD inactive).
- 1ére : Chirurgie de décompression osseuse +/- graisseuse
- 2e : Chirurgie oculomortice
- 3e : Chirurgie de la rétraction palpébrale
- 4e : Chirurgie esthétique du regard
Figure 6 : Chronologie de la prise en charge chirurgicale de l’OD.
4 types d’interventions sont réalisables, suivant un ordre chronologique précis, de crainte que chacune n’interfère avec l’autre.
La décompression orbitaire vise principalement à réduire le degré d’exophtalmie permettant un recul du globe oculaire de 4 à 10 mm en fonction du nombre de parois osseuses effondrées [34] (paroi interne, plancher de l’orbite, paroi externe successivement), elle permet également de lever la compression mécanique du nerf optique par les muscles oculo-moteurs hypertrophiés, réduire le risque d’exposition cornéenne et diminuer le tonus oculaire.
La décompression peut se faire par voie endonasale, trans-faciale ou trans-conjonctivale.
Le délai pour passer à la 2e intervention, à savoir la chirurgie oculomotrice est d’au moins 06 mois.
Cette dernière consiste le plus souvent en un recul musculaire avec re-fixation sclérale [35], les résections sont formellement contre-indiquées.
Le recul est dosé en fonction de la fibrose musculaire et doit souvent être important (6 à 8 mm). Le but à atteindre est la suppression de la diplopie en position primaire et dans le regard vers le bas.
La chirurgie palpébrale, consiste en un allongement palpébral supérieur et/ou inférieur afin de traiter la rétraction ; la rétraction palpébrale supérieure est traitée par Müllerectomie [36]. Quant à la rétraction palpébrale inférieure, elle est corrigée par un recul ou une excision des rétracteurs.
Enfin, une blépharoplastie esthétique supérieure ou inférieure peut être envisagée en dernier lieu. La résection cutanée est toujours la plus économe possible [36].
Conclusion
L’orbitopathie dysthyroïdienne est une affection dysimmunitaire inflammatoire pouvant survenir dans un contexte d’hyperthyroïdie, parfois d’hypothyroïdie, rarement d’euthyroïdie, dont la prise en charge doit être multidisciplinaire.
La symptomatologie s’explique sur le plan physiopathologique par l’interaction entre des lymphocytes T circulants et les fibroblastes orbitaires provoquant la libération de cytokines et la prolifération de fibroblastes, avec au final, accumulation de glycosaminoglycanes dans les muscles oculomoteurs et le tissu conjonctif orbitaire.
La clinique est dominée par l’exophtalmie, la rétraction palpébrale, la diplopie, mais aussi un chémosis, un œdème caronculaire.
Une imagerie orbitaire (TDM et/ou IRM) doit être réalisée. Le traitement qui constitue une longue réhabilitation du regard, revêt plusieurs aspects : médical, chirurgical et mesures associées. Le sevrage tabagique (facteur majeur de sévérité) est essentiel.
L’équilibre thyroïdien doit être obtenu en évitant les passages en hypothyroïdie.
Le traitement préférentiel de la phase aiguë active est la corticothérapie en bolus intraveineux selon les protocoles de l’EU-GOGO. En cas de résistance ou d’intolérance, des traitements immunosuppresseurs peuvent être proposés, comme le Mycophénolate, le Tocilizumab ou le Téprotumumab.
Le traitement chirurgical intervient surtout à la phase séquellaire, rarement en urgence face à une neuropathie op- tique. A cet effet, il est impératif de respecter l’ordre chronologique suivant lorsque les trois types d’intervention sont envisagées : la décompression orbitaire sera réalisée en premier, puis la chirurgie du strabisme puis l’allongement palpébral et enfin éventuellement la blépharoplastie.
Références
- Lehmann GM, Feldon SE, Smith TJ, Phipps R. Immune mechanisms in thyroid eye disease. Thyroid 2008; 18:959–65.
- Smith TJ, Tsai CC, Shih MJ, Tsui S, Chen B, Han R, et al. Unique at- tributes of orbital fibroblasts and global alterations in IGF-1 receptor si- gnaling could explain thyroid-associated ophthalmopathy. Thyroid 2008; 18:983–8.
- Leschik JJ, Diana T, Olivo PD, Konig J, Krahn U, Li Y, Kanitz M & Kahaly GJ. Analytical performance and clinical utility of a bioassay for thyroid-stimulating immunoglobulins. American Journal of Clinical Pa- thology 2013.
- Lanzolla G, Sabini E, Profilo MA, Mazzi B, Sframeli A, Rocchi R, Men- coni F, Leo M, Nardi M, Vitti P et al. Relationship between serum cho- lesterol and Graves’ orbitopathy (GO): a confirmatory study. Journal of Endocrinological Investigation 2018 41 1417–1423.
- Tallstedt L, Lundell G, Torring O, Wallin G, Ljunggren JG, Blomg- ren H & Taube A. Occurrence of ophthalmopathy after treatment for Graves’ hyperthyroidism. The Thyroid Study Group. New England Journal of Medicine 1992 326 1733–1738. (https://doi.org/10.1056/ NEJM199206253262603).
- Bartalena L, Marcocci C, Bogazzi F, Manetti L, Tanda ML, Dell’Un- to E, Bruno-Bossio G, Nardi M, Bartolomei MP, Lepri A et al. Relation between therapy for hyperthyroidism and the course of Graves’ ophthal- mopathy. New England Journal of Medicine 1998 338 73–78.
- Bartalena L, Marcocci C, Bogazzi F, Panicucci M, Lepri A &Pinche- ra A. Use of corticosteroids to prevent progression of Graves’ ophthal- mopathy after radioiodine therapy for hyperthyroidism. New England Journal of Medicine 1989 321 1349–1352. (https://doi. org/10.1056/ NEJM198911163212001).
- Cabanis EA, IbaZizen MT, Abanou A, Salvolini U. Biométrie numéri- sée oculo-orbitaire 3D objective par Scan RX et IRM évaluant exophtal- mie et énophtalmie. J Fr Ophtalmol 2008 ; 31 :46.
- Bartalena L, Kahaly GJ, Baldeschi L, Dayan CM, Eckstein A, Marcocci C, Marinò M, Vaidya B, Wiersinga WM ; EUGOGO †. The 2021 Euro- pean Group on Graves’ orbitopathy (EUGOGO) clinical practice guide- lines for the medical management of Graves’ orbitopathy. Eur J Endocri- nol. 2021 Aug 27;185(4): G43-G67.
- Selter JH, Gire AI &Sikder S. The relationship between Graves’ ophthal- mopathy and dry eye syndrome. Clinical Ophthalmology 2015 9 57–62.
- Ismailova DS, Fedorov AA & Grusha YO. Ocular surface changes in thyroid eye disease. Orbit 2013 32 87–90.
- Vogel R, Crockett RS, Oden N, Laliberte TW, Molina L & Sodium Hyaluronate Ophthalmic Solution Study Group. Demonstration of effi- cacy in the treatment of dry eye disease with 0.18% sodium hyaluronate ophthalmic solution (vismed, rejena) American Journal of Ophthalmolo- gy 2010 149 594–601.
- Uddin JM & Davies PD. Treatment of upper eyelid retraction asso- ciated with thyroid eye disease with subconjunctival botulinum toxin in- jection. Ophthalmology 2002 109 1183–1187.
- Prummel MF, Wiersinga W, Mourits M, Koornneef L, Berghout A & van der Gaag R. Amelioration of eye changes of Graves’ ophthalmopathy by achieving euthyroidism. Acta Endocrinology 1989 121 185–190.
- Wiersinga WM. Smoking and thyroid. Clinical Endocrinology 2013 79 145–151.
- Khong JJ, Finch S, De Silva C, Rylander S, Craig JE, Selva D & Ebe- ling PR. Risk factors for Graves’ orbitopathy; the Australian thyroid-asso- ciated orbitopathy research (ATOR) study. Journal of Clinical Endocrino- logy and Metabolism 2016 101 2711–2720.
- Bartalena L, Piantanida E, Gallo D, Lai A &Tanda ML. Epidemiology, natural history, risk factors, and prevention of Graves’ orbitopathy. Fron- tiers in Endocrinology 2020 11 615993
- Vannucchi G, Covelli D, Campi I, Curro N, Dazzi D, Rodari M, Pepe G, Chiti A, Guastella C, Lazzaroni E et al. Prevention of orbitopathy by oral or intravenous steroid prophylaxis in short duration Graves’ disease patients undergoing radioiodine ablation: a prospective randomized control trial study. Thyroid 2019 29 1828–1833.
- Shiber S, Stiebel-Kalish H, Shimon I, Grossman A & Robenshtok E. Glucocorticoid regimens for prevention of Graves’ ophthalmopathy progression following radioiodine treatment: systematic review and meta-analysis. Thyroid 2014 24 1515–1523.
- Ponto KA, Merkesdal S, Hommel G, Pitz S, Pfeiffer N & Kahaly GJ. Public health relevance of Graves’ orbitopathy. Journal of Clinical Endo- crinology and Metabolism 2013 98 145–152.
- Marcocci C, Kahaly GJ, Krassas GE, Bartanela L, Prummel M, Stahl M, et al. Selenium and the course of mild Grave’s orbitopathy. N Engl J Med 2011; 364:1920–31.
- Van Geest RJ, Sasim IV, Koppeschaar HP, Kalmann R, Stravers SN, Bijls- ma WR &Mourits MP. Methylprednisolone pulse therapy for patients with moderately severe Graves’ orbitopathy: a prospective, randomized, place- bo-controlled study. European Journal of Endocrinology 2008 158 229–237.
- Kahaly GJ, Pitz S, Hommel G & Dittmar M. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. Journal of Clinical Endocrinology and Metabolism 2005 90 5234–5240.
- Bartalena L, Krassas GE, Wiersinga W, Marcocci C, Salvi M, Daume- rie C, Bournaud C, Stahl M, Sassi L, Veronesi G et al. Efficacy and safety of three different cumulative doses of intravenous methylprednisolone for moderate to severe and active Graves’ orbitopathy. Journal of Clinical Endocrinology and Metabolism 2012 97 4454–4463.
- Sisti E, Coco B, Menconi F, Leo M, Rocchi R, Latrofa F, Profilo MA, Mazzi B, Vitti P, Marcocci C et al. Age and dose are major risk factors for liver damage associated with intravenous glucocorticoid pulse therapy for Graves’ orbitopathy. Thyroid 2015 25 846–850.
- Curro N, Covelli D, Vannucchi G, Campi I, Pirola G, Simonetta S, Dazzi D, Guastella C, et al. Therapeutic outcomes of high-dose intrave- nous steroids in the treatment of dysthyroid optic neuropathy. Thyroid 2014 24 897–905.
- Orgiazzi J. Adding the immunosuppressant mycophenolate mofetil to medium-dose infusions of methylprednisolone improves the treatment of Graves’ orbitopathy. Clinical Thyroidology 2018 30 10–14. (https://doi. org/10.1089/ct.2018;30.10-14)
- Lee ACH, Riedl M, Frommer L, Diana T &Kahaly GJ. Systemic safety ana- lysis of mycophenolate in Graves’ orbitopathy. Journal of Endocrinological In- vestigation 2020 43 767–777. (https://doi. org/10.1007/s40618-019-01161-z)
- Quah Qin Xian N, Alnahrawy A, Akshikar R & Lee V. Real-world efficacy and safety of mycophenolate mofetil in active moderate-to-sight-threatening thyroid eye disease. Clinical Ophthalmology 2021
- Prummel MF, Terwee CB, Gerding MN, Baldeschi L, Mourits MP, Blank L, Dekker FW &Wiersinga WM. A randomized controlled trial of orbital radiotherapy versus sham irradiation in patients with mild Graves’ ophthalmopathy. Journal of Clinical Endocrinology and Metabolism 2004 89 15–20. (https://doi.org/10.1210/jc.2003-030809)
- Gorman CA, Garrity JA, Fatourechi V, Bahn RS, Petersen IA, Staf- ford SL, Earle JD, Forbes GS, Kline RW, Bergstralh EJ et al. A prospective, randomized, double-blind, placebo-controlled study of orbital radiothe- rapy for Graves’ ophthalmopathy. Ophthalmology 2001 108 1523–1534. (https://doi.org/10.1016/S0161-6420(01)00632-7)
- Rajendram R, Taylor PN, Wilson VJ, Harris N, Morris OC, Tomlinson M, Yarrow S, Garrott H, Herbert HM, Dick AD et al. Combined immu- nosuppression and radiotherapy in thyroid eye disease (CIRTED): a mul- ticentre, 2 x 2 factorial, double-blind, randomised controlled trial. Lancet: Diabetes and Endocrinology 2018 6 299–309.
- Marquez SD, Lum BL, McDougall IR, Katkuri S, Levin PS, MacMa- nus M & Donaldson SS. Long-term results of irradiation for patients with progressive Graves’ ophthalmopathy. International Journal of Radiation Oncology, Biology, Physics 2001 51 766–774.
- Garrity JA, Fatourechi V, Bergstrath EJ, Bartley JB, Beattly CW,De Santo LW, et al. Results of transantral decompression in 428 patients with severe Grave’s ophthalmopathy. Am J Ophthalmol, 1993; 116:533–47.
- Fells P, Mc Carry B, Allward GW. Ocular muscle surgery in thyroid eye disease. Orbit 1992; 11:169–75.
- Adaenis JP, Lasudry J, Robert PY. Orbitopathie dysthyroïdienne. In: Adenis JP, Morax S, editors. Société française d’ophtalmologie. Pathologie orbitopalpébrale. Paris: Masson; 1998. p. 38-68.