La chirurgie de remplacement prothétique de la hanche est, sans aucun doute, une des opérations les plus réussies en orthopédie. Dans 15 à 25% des cas, les deux hanches sont détériorées. 10% des patients ayant bénéficié d’un remplacement prothétique total d’une hanche sont demandeurs de la même procédure dans les deux ans suivant la première intervention. Le remplacement prothétique de hanche bilatéral en une session opératoire offre les avantages d’un seul séjour hospitalier, d’une seule anesthésie.autres voies d’abord ?
L. Ait El Hadj(1), S. Fourmas(1), A. Benbouzid(1), M. Yakoubi(1), H. Amouri(1), A. Benamirouche(1), H. Mesbah(2),
M. Yakoubi,
(1) Service d’Orthopédie-Traumatologie, EHS Abdelkader Boukhroufa, Ben Aknoun, Alger.
(2) Anesthésie-Réanimation
Date de soumission : 17 Décembre 2020
Abstract: Prosthetic hip replacement surgery is, without a doubt, one of the most successful operations in orthopedics. In 15 to 25% of cases, both hips are damaged. 10% of patients who have had a total hip replacement request the same procedure within two years of the first operation. One-session bilateral hip replacement offers the advantages of a single hospital stay, a single anesthesia. The cost of the operation and the average length of stay in hospital are lower compared to two-stage surgery and rehabilitation is facilitated. The problem of length inequalities of the lower limbs (ILMI) after total hip replacement (THA) persists in about 25% of cases, with a functional impact when it exceeds 10 mm. Hypothesis. Control of length inequality after bilateral THA in one session is better using the direct anterior approach in the supine position on an ordinary table. Materials and methods. This is a retrospective clinical study carried out at the level of the orthopaedics and traumatology department of the Specialized Hospital (EHS) of Ben Aknoun in Algiers. This study included 105 patients diagnosed with bilateral aseptic osteonecrosis of the femoral head (ONTF) operated between January 2016 and January 2019 for simultaneous bilateral THA divided into two groups, group A (25 patients) operated by Hueter’s anterior approach and group B (80 patients) operated by the lateral Hardinge approach. The ILMIs were measured on pre- and postoperative imaging (telemetry). Results. Of the 105 patients, preoperatively 62 patients were isometric (ILMI ≤ 10 mm) and 43 patients had an ILMI> 10 mm. The follow-up found 67 isometric patients (63.8%) and 38 unequal patients (36%). The isometric group included 24 patients from group A, i.e., 96% of the series and 43 patients from group B, i.e., 40%. Of the 38 unequal patients, in group A, only one patient presented an ILMI of 11mm, while in group B (37 patients), 22 patients presented a postoperative ILMI (12 mm on average), 15 patients had an ILMI of 14.9mm. Discussion. In lateral decubitus, palpation of bony landmarks such as patella points or heels through the surgical fields provides limited or even distorted information, due to adduction of the operated limb, especially in patients with a large pelvis. An adduction variation of 10° can have an impact of 17 mm on the length of the lower limb. The main advantage of dorsal decubitus on an ordinary table therefore lies in the presence of both free legs in the operating field. This allows satisfactory control of the lengths by palpation of the two anterosuperior iliac spines and the internal malleoli, legs perpendicular to the pelvis. Conclusion. The anterior approach without an orthopaedic table allows satisfactory control of limb lengths during simultaneous bilateral hip arthroplasty, by precise palpation of anatomical landmarks in the dorsal decubitus position. It thus makes it possible to limit ILMI after THA and improve functional results.
Key words: Total hip replacement, bilateral, anterior approach, lateral approach.
Résumé : La chirurgie de remplacement prothétique de la hanche est, sans aucun doute, une des opérations les plus réussies en orthopédie. Dans 15 à 25% des cas, les deux hanches sont détériorées. 10% des patients ayant bénéficié d’un remplacement prothétique total d’une hanche sont demandeurs de la même procédure dans les deux ans suivant la première intervention. Le remplacement prothétique de hanche bilatéral en une session opératoire offre les avantages d’un seul séjour hospitalier, d’une seule anesthésie. Le coût lié à l’intervention et la durée moyenne de séjour hospitalier sont moindres par rapport à une chirurgie en deux temps et la rééducation est facilitée. Le problème des inégalités de longueur des membres inférieurs (ILMI) après prothèse totale de hanche (PTH) persiste dans environ 25% des cas, avec un retentissement fonctionnel lorsque celle-ci dépasse 10 mm. Hypothèse. Le contrôle de l’inégalité de longueur après PTH bilatérale en une session opératoire est meilleur en utilisant la voie antérieure directe en décubitus dorsal sur table ordinaire. Matériels et méthodes. Il s’agit d’une étude clinique rétrospective réalisée au niveau du service d’orthopédie et de traumatologie de l’Établissement Hospitalier Spécialisé (EHS) de Ben Aknoun à Alger. Cette étude inclue 105 patients avec comme diagnostic ostéonécrose aseptique bilatérale de la tête fémorale (ONTF) opérés entre janvier 2016 et janvier 2019 d’une PTH bilatérale simultanée divisée en deux groupes, le groupe A (25 patients) opérés par voie antérieure de Hueter, et le groupe B (80 patients) opérés par voie latérale d’Hardinge. Les ILMI ont été mesurées sur imagerie (télémétrie) pré- et post-opératoires. Résultats. Sur les 105 patients, en pré-opératoire 62 patients étaient isométriques (ILMI ≤ 10 mm) et 43 patients présentaient une ILMI > 10 mm. Le suivi, retrouvait 67 patients isométriques (63,8%) et 38 patients inégaux (36%).Le groupe isométrique comprenait 24 patients du groupe A soit 96% de la série et 43 patients du groupe B soit 40%. Sur les 38 patients inégaux, dans le groupe A, un seul patient présente une ILMI de 11 mm, tandis que dans le groupe B (37 patients), 22 patients présentaient une ILMI postopératoire (12 mm en moyenne), 15 patients présentaient une ILMI de 14,9mm. Discussion. En décubitus latéral, la palpation des repères osseux tels que les pointes de rotules ou les talons à travers les champs opératoires, offre une information limitée voire faussée, due à l’adduction du membre opéré, en particulier chez les patients avec un bassin large. Une variation d’adduction de 10° peut avoir un retentissement de 17 mm sur la longueur du membre inférieur. L’avantage principal du décubitus dorsal sur table ordinaire réside ainsi dans la présence des deux jambes libres dans le champ opératoire. Ceci permet un contrôle satisfaisant des longueurs par palpation des deux épines iliaques antéro-supérieures et des malléoles internes, jambes perpendiculaires au bassin. Conclusion. La voie antérieure sans table orthopédique permet un contrôle satisfaisant des longueurs des membres lors d’une arthroplastie bilatérale simultanée de hanche, par palpation précise des repères anatomiques en décubitus dorsal. Elle permet ainsi de limiter les ILMI post-PTH et améliorer les résultats fonctionnels.
Mots clés : Prothèse totale de hanche, bilatérale, voie d’abord antérieure, voie d’abord latérale.
Introduction
L’arthrose de la hanche est une des arthroses les plus fréquentes, juste après le genou. Dans 15 à 25% des cas (1), les deux hanches sont détériorées. Une proportion importante de patients ayant bénéficié d’un remplacement prothétique total d’une hanche sont demandeurs de la même procédure dans les deux ans suivant la première intervention (2). Dans l’intervalle entre la première et la deuxième intervention, les patients présentant une pathologie bilatérale ne bénéficient pas du plein potentiel de leur traitement. Le coté non opéré limite la récupération de l’ensemble de la fonction.
Ainsi, lorsque la pathologie est bilatérale, le remplacement prothétique de hanche bilatéral en une session opératoire offre les avantages d’un seul séjour hospitalier, d’une seule anesthésie. Le coût lié à l’intervention et la durée moyenne de séjour hospitalier sont moindres par rapport à une chirurgie en deux temps et la rééducation est facilitée (3). Le problème des inégalités de longueur des membres inférieurs (ILMI) après prothèse totale de hanche (PTH) persiste dans environ 25% des cas, avec un retentissement fonctionnel lorsque celle-ci dépasse 10 mm.
L’inégalité de longueur des membres inférieurs est la troisième cause d’insatisfaction après pose de prothèse totale de hanche en France (4) et la deuxième cause de poursuites judiciaires aux États-Unis (5). C’est donc une complication grave et fréquente dont il faut tenir compte. En pratique, et notamment en décubitus latéral, l’appréciation des longueurs per-opératoires relève souvent plus de l’expérience du chirurgien que de réels repères anatomiques (6,7). La voie d’abord antérieure type Hueter sans table orthopédique permet de s’affranchir de ces difficultés liées à l’installation, et de contrôler cliniquement les longueurs per-opératoires par palpation des malléoles médiales et des épines iliaques, puisque les deux membres inférieurs sont libres dans le champ opératoire.
Notre hypothèse est que le contrôle de l’inégalité de longueur après PTH bilatérale en une session opératoire est meilleur en utilisant la voie antérieure directe en décubitus dorsal sur table ordinaire.
Matériels et méthodes
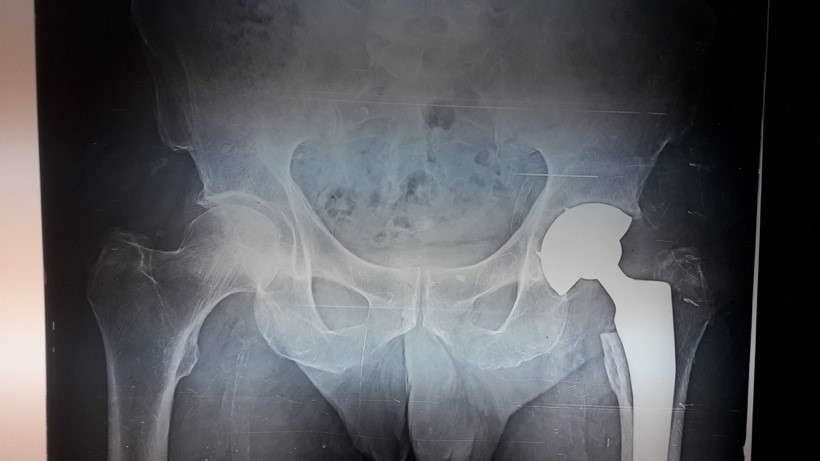
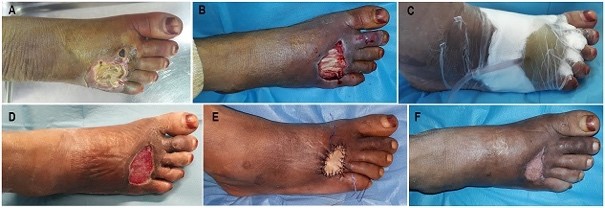
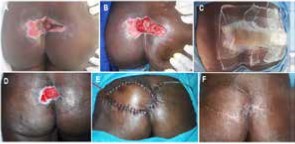
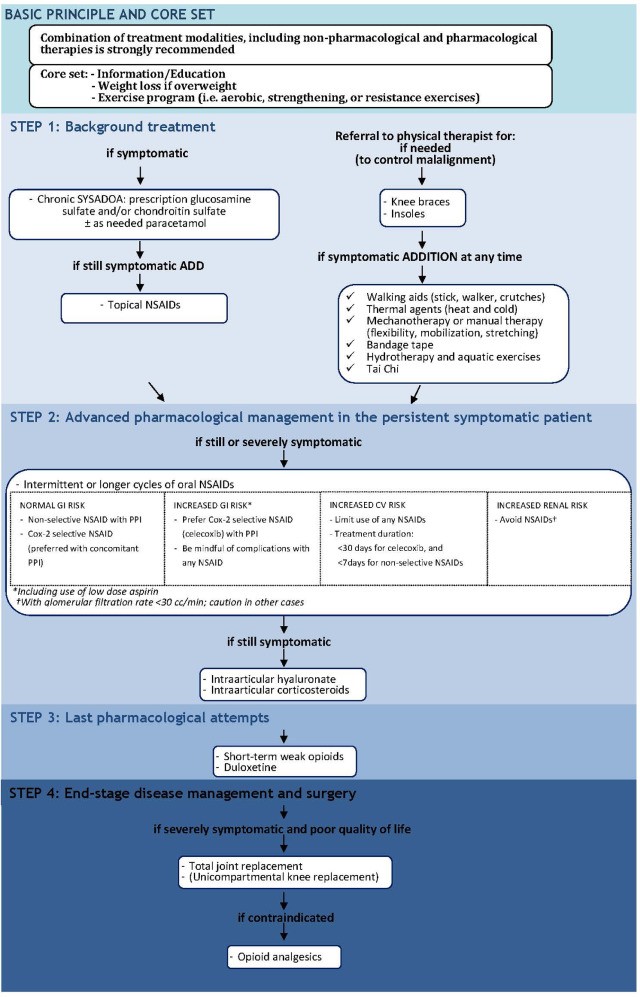
Il s’agit d’une étude clinique rétrospective réalisée au niveau du service d’orthopédie et de traumatologie de l’Établissement Hospitalier Spécialisé (EHS) de Ben Aknoun à Alger. Cette étude inclue 286 patients atteints de coxopathie bilatérale invalidante, soit 572 prothèses totales de hanche. Le diagnostic d’ostéonécrose aseptique bilatérale de la tête fémorale (ONTF) occupe la première place avec 105 cas (37%) (Figure 1). Cinquante-huit patients (20,3%) présentaient des coxites dont la majorité, suivie en rhumatologie pour maladie rhumatismale, entre autres les spondylarthropathies (SPA) (figure 2). Trente-trois cas de dysplasie de hanche (11,53%). Les autres diagnostics étaient représentés par des pseudarthroses bilatérales de l’extrémité supérieure du fémur, la coxarthrose primitive sans étiologie identifiée et les luxations congénitales de hanche “opérées dans l’enfance”.
Description de la série
Les critères d’inclusion étaient les PTH bilatérales réalisées en une session opératoire sur les 105 patients avec comme diagnostic ostéonécrose aseptique bilatérale de la tête fémorale (ONTF) opérés entre janvier 2016 et janvier 2019. Les patients présentant des coxites, dysplasies luxantes, les pseudarthroses bilatérales et les protrusions acétabulaires majeures étaient exclus de l’étude.
L’étude est faite sur des patients divisés en deux groupes, le groupe A (25 patients) opérés par voie antérieure de Hueter et le groupe B (80 patients) opérés par voie latérale d’Hardinge. Toutes les interventions chirurgicales ont été réalisées par le même chirurgien. Les ILMI ont été mesurées sur imagerie (télémétrie) pré- et post-opératoire.
L’âge moyen des patients est de 38,7 ans (17 ans – 52 ans). Nous avons recensé 68 femmes et 37 hommes (37%). Le sexe ratio est donc de 2,3 femmes pour 1 homme. Le score de Devane est adapté à l’évaluation de l’activité physique d’un patient jeune ayant subi une arthroplastie totale de hanche. Il permet d’apprécier les gains apportés par le remplacement prothétique sur les plans social et professionnel. Quarante-neuf pour cent des patients étaient classés semi-sédentaires avec seulement une activité domestique. Les activités quotidiennes sont naturellement perturbées lorsqu’une hanche, à fortiori les deux, a subi un dommage quelconque.
Après la douleur, l’inégalité de longueur des membres inférieurs représente le deuxième problème qui appelle à une solution. Sur les 105 patients, en préopératoire 62 patients étaient isométriques (ILMI ≤ 10 mm), et 43 patients présentaient une ILMI >10 mm. En cas de différence de longueur pré-opératoire, la longueur du membre inférieur le plus long est conservée et le membre le plus court est rallongé de manière à obtenir l’égalité en fin d’intervention.
Le bilan préopératoire comprend une numération formule sanguine, un bilan de coagulation, une radiographie pulmonaire, ainsi qu’un rachis cervical et lombaire, un bilan dentaire récent (pas systématique), et un bilan cardiaque (électrocardiogramme, échocardiographie). Après avoir éclairé tous les patients, la décision de prise en charge par PTH bilatérale en une session opératoire est prise conjointement par le chirurgien et l’anesthésiste.
Méthode
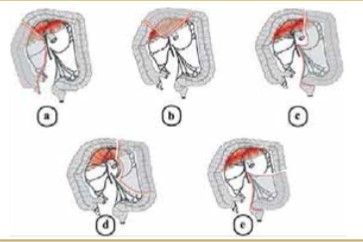
Pour le groupe B, l’intervention s’est déroulée par voie d’Hardinge en décubitus latéral et changement d’installation lors du passage au deuxième coté avec un set nouveau de clampage. Pour le coté initial, a priori, il n’y pas de raison à avantager une hanche avant une autre du moment que lors de la séquence opératoire, les deux hanches vont être opérées selon le même protocole. Cependant, dans le cas d’une inégalité de longueur des membres inférieurs, nous préférons établir une planification préopératoire précise, en usant de calques, afin de déterminer le bon niveau de coupe en vue d’obtenir la longueur voulue. Dans d’autres cas, lorsqu’une hanche est plus douloureuse que l’autre selon les doléances du malade, nous commençons par elle. Car dans le cas où on est appelé à arrêter l’intervention, on aura au moins donné une chance au malade.
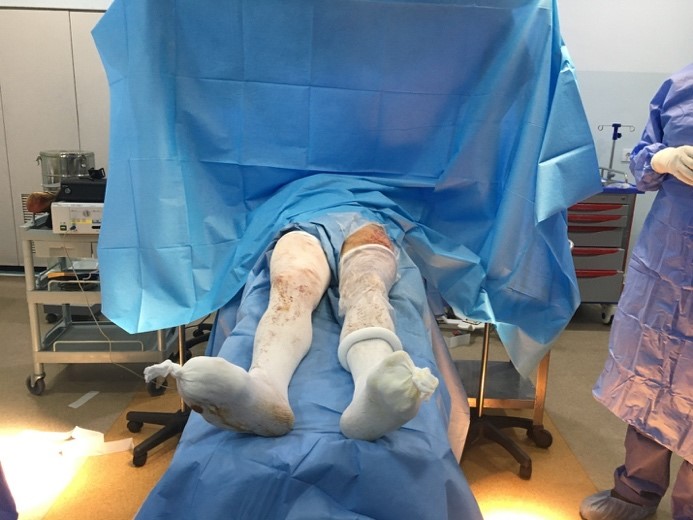
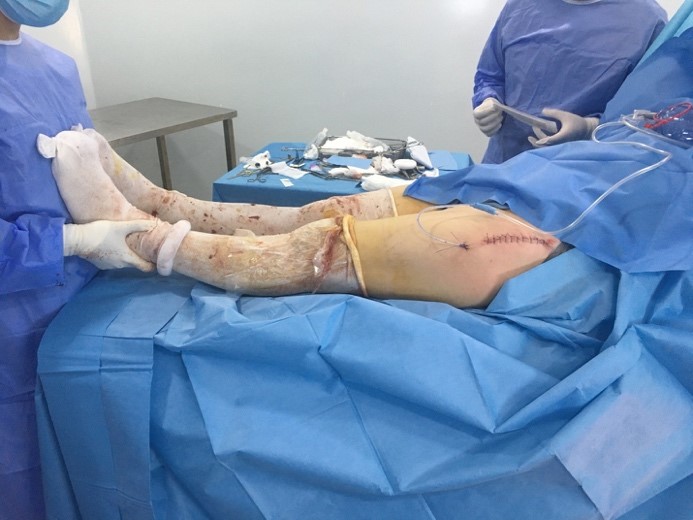
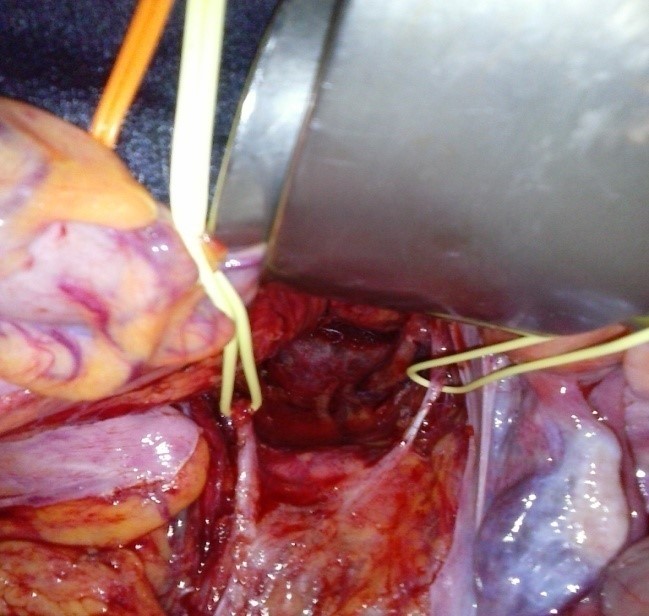
Pour le groupe A l’intervention est réalisée en décubitus dorsal sur table ordinaire, les deux membres inférieurs dans le champ opératoire, incluant les épines iliaques antéro-supérieures. La voie d’abord antérieure de Hueter est utilisée, passant entre tenseur du fascia lata latéralement, et les muscles sartorius et droit antérieur médialement. Après mise en place des implants, un testing complet est réalisé avec contrôle clinique des longueurs par palpation bilatérale et comparative des malléoles médiales (fig. 2), en s’attachant à être reproductible avec les deux membres placés perpendiculairement à la ligne bi-épines iliaques. Un contrôle radioscopique per-opératoire n’est pas réalisé systématiquement pour contrôle du bon positionnement des implants.
Résultats
Méthode de recueil de données : l’ensemble du dossier médical de chaque patient a été soigneusement analysé. Ce qui a permis de recueillir les données concernant l’état civil, les caractéristiques morphologiques (taille et poids), les antécédents et le bilan fonctionnel à chaque visite de contrôle, quand cela a été possible. Une analyse des radiographies a été effectuée.
Les patients ont été revus en consultation à 02 mois, 06 mois (avec télémétrie des membres inférieurs, un pangonogramme), 1 an et 2 ans, afin de faire une évaluation fonctionnelle de leur hanche. Toutes ces données recueillies ont été saisies et traitées avec le logiciel EPI-INFO 7 version 1.0.0.0.
En comparant la télémétrie des membres inférieurs en pré- et post-opératoire, nous avons pu évaluer les ILMI (allongement ou raccourcissement), avant et après pose de prothèses. Deux groupes de patients ont ainsi été constitués : un groupe « isométrique » avec ILMI ≤10 mm et un groupe « ILMI » avec ILMI >10 mm. Le seuil de 10 mm est admis dans la littérature, qu’une inégalité inferieure à ce seuil n’entraîne pas de retentissement clinique fonctionnel (8,9,10).
Le suivi, retrouvait 67 patients isométriques (63,8%) et 38 patients inégaux (36%). Le groupe isométrique comprenait 24 patients du groupe A soit 96% de la série, et 43 patients du groupe B soit 40%. Sur les 38 patients inégaux, dans le groupe A, un seul patient présente une ILMI de 11 mm, tandis que dans le groupe B (37 patients), 22 patients présentaient une ILMI post-opératoire (12 mm en moyenne), 15 patients présentaient une ILMI de 14,9 mm (tableau 1).
Discussion
Ces dernières années, la chirurgie arthroplastique de la hanche mini-invasive est devenue de plus en plus populaire (11). Cependant, certaines interventions chirurgicales mini-invasives ont été caractérisées par un taux de complications très élevé (12).
La voie antérieure directe est une modification de la voie de Smith-Petersen, car seule la partie distale antéro-supérieure est utilisée. Cette technique est devenue pratique courante pour Judet et Judet en 1947 (13,14). Plus récemment, avec l’introduction d’une table orthopédique dédiée. Matta a transformé la procédure chirurgicale en une procédure invasive dans laquelle le patient est également positionné en, décubitus dorsale (15,16). Actuellement, de plus en plus de chirurgiens effectuent cet abord antérieur sans table. Cette variante offre de nombreux avantages : elle n’exige pas la présence de personnel formé pour effectuer des manœuvres sur la table, en outre la longueur des membres, la stabilité de l’implant, et le mouvement de la hanche opérée peut être vérifié plus facilement, car les membres inférieurs sont libres.
Différentes méthodes ont été proposées dans la littérature pour contrôler les longueurs lors d’une arthroplastie de hanche, comme l’évaluation des tensions tissulaires, l’utilisation de pins trans-osseux avec mesure par compas, la planification pré-opératoire 2D ou plus récemment 3D ou encore la navigation. L’étude de Rice et al., (7,17) comparait les différentes méthodes de mesure per-opératoire et retrouvait la meilleure corrélation entre évaluation per-opératoire et radiographies post-opératoires pour la tension des parties molles et le test du piston. Ces tests de tension peuvent néanmoins être limités par l’anesthésie et la curarisation.
En décubitus latéral, la palpation des repères osseux tels que les pointes de rotules ou les talons à travers les champs opératoires, offre une information limitée voire faussée, due à l’adduction du membre opéré, en particulier chez les patients avec un bassin large. Une variation d’adduction de 10° peut avoir un retentissement de 17 mm sur la longueur du membre inférieur. L’avantage principal du décubitus dorsal sur table ordinaire réside ainsi dans la présence des deux jambes libres dans le champ opératoire. Ceci permet un contrôle satisfaisant des longueurs par palpation des deux épines iliaques antéro-supérieures et des malléoles internes, jambes perpendiculaires au bassin.
D’après notre expérience, le contrôle de l’inégalité de longueurs des membres inférieurs est mieux par la voie antérieure en décubitus dorsale sans table orthopédique que dans la voie latérale.
Conclusion
La voie antérieure sans table orthopédique permet un contrôle satisfaisant des longueurs des membres lors d’une arthroplastie bilatérale de hanche simultanée, par palpation précise des repères anatomiques en décubitus dorsal, tels que les épines iliaques antéro-supérieures et les malléoles internes. Elle permet ainsi de limiter les ILMI post PTH et améliorer les résultats fonctionnels.
Date de soumission : 17 Décembre 2020
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts en rapport avec cet article.
Figures
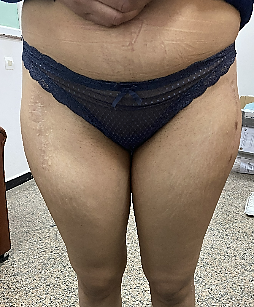
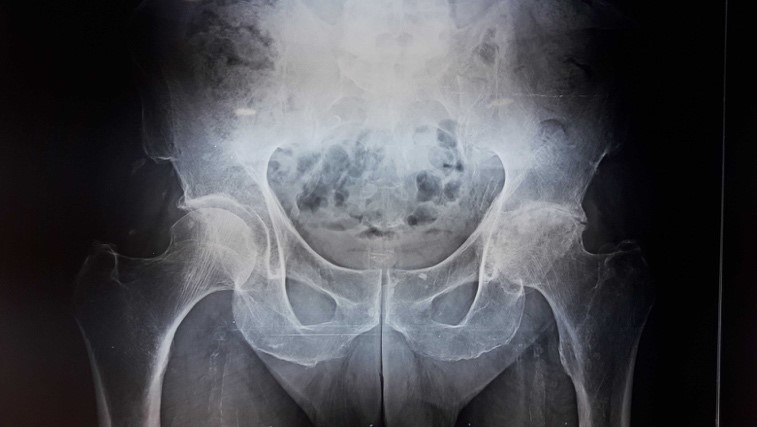
Figure 1 : Patiente de 17 ans présentant une ONTF bilatérale secondaire à une prise prolongée de corticoïdes bénéficiant d’une double prothèse avec couple de frottement alumine-alumine.
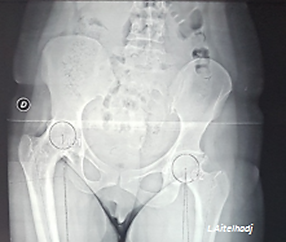
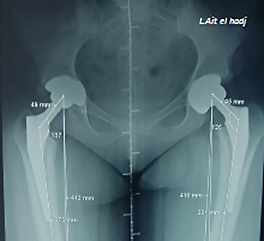
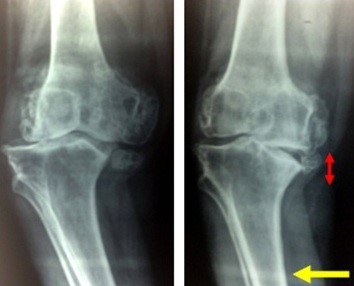
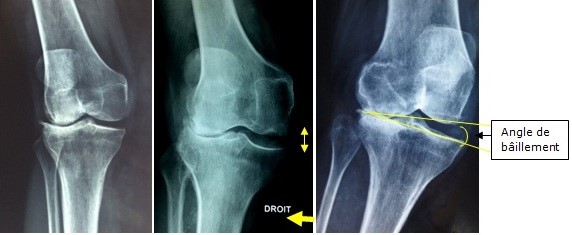
Figure 2 : Patiente de 38 ans présentant une coxarthrose bilatérale sur SPA avec ankylose à droite bénéficiant d’une arthroplastie bilatérale simultanée.
Tableau 1 : Description du type d’inégalités de longueurs pré et postopératoires.
| Préopératoire | Postopératoire | Post-opératoire Voie d’abord antérieure | Post-opératoire Voie d’abord latérale | |
| Isométrique | 62 | 67 | 24 | 43 |
| Inégalité (10 – 12 mm) | 11 | 36 | 1 | 22 |
| Inégalité>13 mm | 27 | 2 | 0 | 15 |
| Total d’inégalité | 38 |
Références
- Melton, Learmonth ID, Young C, Rorabeck C. The operation of the century: total hip replacement. Lancet 2007;370:1508—19
- Alfaro-Adrian J, Bayona F, Reich JA, Murray DW. One-or two-stage bilateral total hip replacement. J Arthroplasty. 1999;14:439—45
- Grégoire Micicoi, Régis Bernard de Dompsure, Laurie Tran, Pascal Boileau, Christophe Trojani. Early morbidity and mortality after one-stage bilateral THA: Anterior versus posterior approach. doi.org/10.1016/j.rcot.2019.09.121
- Marmor S, Farman T. Causes de procédures médicolégales après prothèse totale de hanche. Rev Chir Orthop Traumatol 2011;97:752–7
- Konyve A, Bannister GC. The importance of leg length discrepancy after total hip arthroplasty. J Bone Joint Surg Br 2005;87:155–7.
- Ng VY, Kean JR, Glassman AH. Limb-length discrepancy after hip arthroplasty. J Bone Joint Surg Am 2013; 95:1426–36.
- Rice IS, Stowell RL, Viswanath PC, Cortina GJ. Three intraoperative methods to determine limb-length discrepancy in THA. Orthopedics 2014; 37:488–95.
- Mayr E, Nogler M, Benedetti MG et al. A prospective randomized assessment of earlier functional recovery in THA patients treated by minimally invasive direct anterior approach: a gait analysis study. Clin Biomech (Bristol, Avon) 24:812–818
- Anterior Total Hip Arthroplasty Collaborative Investigators (2009) Outcomes following the single-incision anterior approach to total hip arthroplasty: a multicenter observational study Orthop Clin North Am 40:329–342
- Berend KR, Lombardi AV, Seng BE et al (2009) Enhanced early outcomes with the anterior supine intermuscular approach in primary total hip arthroplasty. J Bone Joint Surg Am 91:107–120
- Lovell TP (2008) Single-incision direct anterior approach for total hip arthroplasty using a standard operating table. J Arthroplasty23:64–68
- Bal BS, Haltom D, Aleto T et al (2005)Early complications of primary total hip replacement performed with a two incision minimally invasive technique. J Bone Joint Surg Am 87:2432–2438
- Judet R, Judet J (1952) Technique and results with the acrylic femoral head prosthesis. J Bone Joint Surg Br 34:173–180
- Judet J, Judet R (1950) The use of an artificial femoral head for arthroplasty of the hip joint. J Bone Joint Surg Br 32:166–173
- Matta JM, Shahrdar C, Ferguson TA (2005) Single-incision anterior approach for total hip arthroplasty on an orthopaedic table. Clin Orthop Relat Res 441:115–124
- Matta JM, Ferguson TA (2005)The anterior approach for hip replacement. Orthopedics 28:927–928
- Paul Lecoaneta, Morgane Vargasa, Julien Pallarob, Thomas Thelena, Clément Ribesa, Thierry Fabrea. Leg length discrepancy after total hip arthroplasty: Can leg length be satisfactorily controlled via anterior approach without a traction table? Evaluation in 56 patients with EOS 3D. Revue de chirurgie orthopédique et traumatologique 104 (2018) 771–776.