Abstract: Introduction: Over 90% of early-stage Hodgkin lymphomas and nearly 80% of advanced stages achieve long-term disease-free survival. Achieving complete remission remains an important prognostic factor. The aim of this work is to assess the predictive factors for obtaining complete remission in Hodgkin lymphoma after a first line treatment. Patients and methods: In this retrospective study, we included adult Hodgkin lymphoma patients, treated with ABVD and or BEACOPP regimens; according to the stages and prognostic groups. Results: two hundred twenty-one patients were included in this study and 70% of them were achieved CR. The response rate was better in the early-stage HL 81,4% versus 55,6 in the advanced stage HL. Performance status according to ECOG greater than or equal 2, achievement of complete remission, B symptoms, bone marrow and spleen involvement and presence of a large tumour mass had a negative impact on complete remission. Lymph nodes low than 3, early-stage Hodgkin lymphoma, favourable early stage and standard risk advanced stage had a positive effect on complete remission. Conclusion: The first therapeutic goal in Hodgkin lymphoma is to achieve the complete remission. It predicts a better long-term survival. Impaired general condition; advanced stage Hodgkin lymphoma, B symptoms and large tumour mass impact the complete remission achievement.
Keys words: Hodgkin Lymphoma; prognosis; treatment response.
Résumé : Introduction : Plus de 90% des lymphomes de Hodgkin localisés et près de 80% des stades étendus atteignent une survie sans maladie à long terme. L’obtention de la rémission complète reste un facteur pronostique primordial. Le but de ce travail est d’évaluer les facteurs prédictifs de l’obtention de rémission compète dans le lymphome de Hodgkin après une seule lignée de traitement. Patients et méthodes : Dans ce travail rétrospectif, nous avons inclus les patients adultes présentant un lymphome de Hodgkin. Les patients ont bénéficié des protocoles thérapeutiques ABVD et BEACOPP selon les stades et les groupes pronostiques. Résultats : Sur 221 patients inclus dans ce travail, 70% des patients ont obtenu la rémission complète. Ce taux a été de 81,4% chez les patients en stade localisé et 55,6% chez patients en stade étendu. Un Performance status supérieur ou égal à 2, l’obtention de la rémission complète, la présence des signes d’évolutivité clinique, une atteinte médullaire, splénique et la présence d’une masse tumorale volumineuse ont un impact négatif sur la rémission complète. Le stade localisé de la maladie, le groupe pronostique favorable pour les stades localisés et de risque standard pour les stades étendus ont un effet positif sur la rémission. Conclusion : le premier objectif thérapeutique des lymphomes de Hodgkin est d’obtenir la rémission complète. Elle prédit une meilleure survie. Un mauvais état général, un lymphome de Hodgkin disséminé, une présence des signes d’évolutivité clinique, et une masse tumorale volumineuse ont un impact sur la réponse au traitement.
Mots clés : Lymphome de Hodgkin, pronostic, réponse au traitement.
Introduction
Le lymphome de Hodgkin (LH) représente 10% des cas de lymphomes nouvellement diagnostiqués. Sur l’ensemble des décès liés aux lymphomes, seulement 5% sont observés dans le LH [1]. En Algérie, l’incidence annuelle est de 1,8 cas/100.000 habitants/an, avec un pic d’incidence entre 16 et 34 ans [2]. Une polychimiothérapie (ABVD / BEACOPP) reste le standard thérapeutique, complétée par une radiothérapie dans les formes localisées de la maladie. Après un protocole de polychimiothérapie, le taux de rémission complète (RC) est de 63% dont 87% pour les groupes pronostiques favorables et 55% pour les groupes défavorables [3]. Dans les formes étendues, le taux de RC est estimé de 51,5% [4]. La survie à long terme dépend des scores pronostiques déjà établis ; le score EORTC [5] pour les stades localisés et IPS [6] pour les stades étendus. Un syndrome tumoral volumineux, une chimio sensibilité et la durée de la RC ont un impact sur la survie globale et la survie sans progression des patients. Dans ce travail, nous avons recherché les facteurs qui permettent de prédire l’obtention de la RC.
Patients et méthodes
Dans ce travail rétrospectif qui s’étale de Janvier 2009 à Décembre 2020, nous avons collecté les données des patients adultes présentant un LH. Le questionnaire de travail établi contient les données civiles, cliniques et biologiques du patient, le score pronostique, le traitement reçu et la réponse au traitement. Le FDG-PET Scan reste l’examen de référence afin d’évaluer la masse tumorale au diagnostic et après le traitement. Puisque seule une minorité de nos patients a pu accéder à cet examen, l’évaluation de la réponse au traitement a été réalisée selon les critères de Cheson 1999 [7] (Tableau 1). Les patients inclus ont bénéficié du traitement classique du LH, soit polychimiothérapie de type ABVD ou BEACOPP. L’analyse des données a été réalisée par le logiciel EPI INFO® version 7. Une variable est considérée comme statistiquement significative si la valeur p est ≤ 0,05 et pour fournir des informations sur la pertinence des résultats, des intervalles de confiances à 95% ont été calculés. La mesure d’une relation entre un éventuel facteur et l’obtention de la RC a été évaluée d’abord par une analyse univariée suivie d’une analyse multivariée, en incluant les variables statistiquement significatives à la valeur ≤ 0,1 en analyse univariée.
Résultats
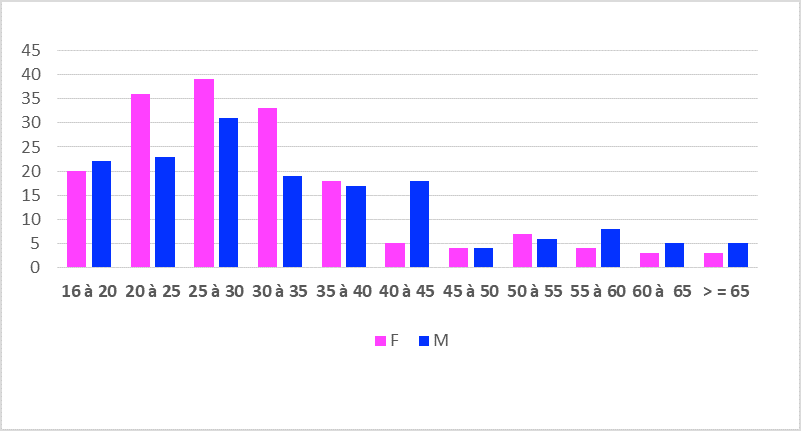
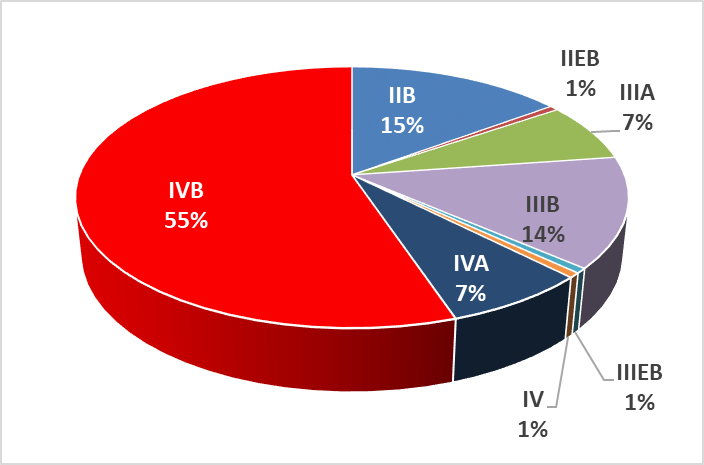
Sur une période de 11 ans nous avons inclus 221 patients. L’âge médian était de 31 ans (16-80 ans), et 54% étaient de sexe masculin. Cent dix-sept patients, soit 80% des cas, avaient un PS ≥ 2. La forme scléro-nodulaire était majoritaire, retrouvée chez 98% des cas. Les stades localisés représentaient 56% des cas, 55% des patients en stade localisé avaient un pronostic favorable selon EORTC, 46% des patients en stades étendus avaient un risque SPI standard.
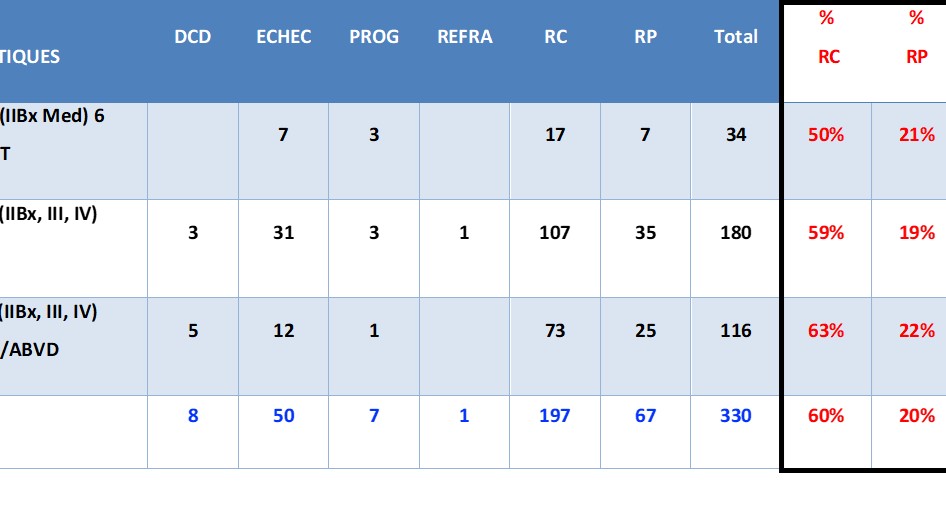
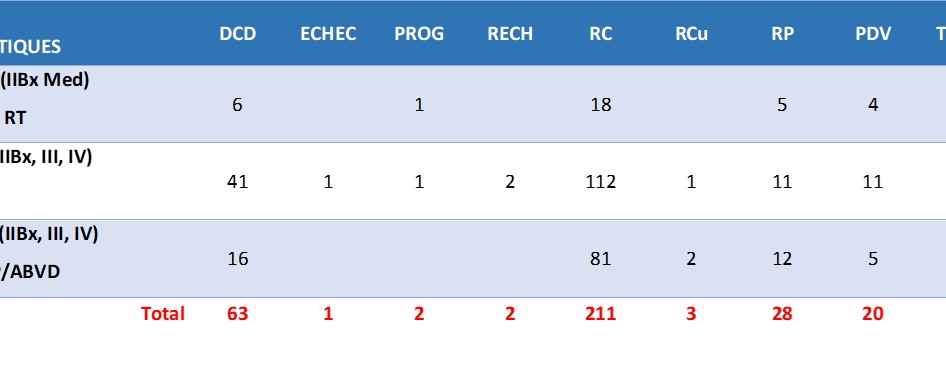
Au total, 190 patients (86%) ont été traités par le protocole ABVD, et 31 patients (14%) par le protocole BEACOPP. La RC a été obtenue chez 70,1% des cas (155 patients), dont 65% (101 patients) présentaient un stade localisé (Tableau 2).
Les patients ont été catégorisés en 2 groupes, le groupe des patients en RC ou RCu, et celui des patients en RP, maladie stable, progression, ou décédés. Nous avons effectué des tests de comparaison sur l’ensemble des variables à tester (Tableau 3). Les paramètres VS (p<0,001), le taux des phosphatases alcaline (p=0,003), le taux des protides sériques (p=0,04) et le taux d’albumine (p<0,001) n’ont pas été inclus dans l’analyse uni et multivariée.
Le résultat de l’impact des facteurs sur l’obtention de la RC est résumé dans le Tableau 4. Dans notre étude, l’âge du patient et le sexe n’avaient pas un impact sur l’obtention de la RC.
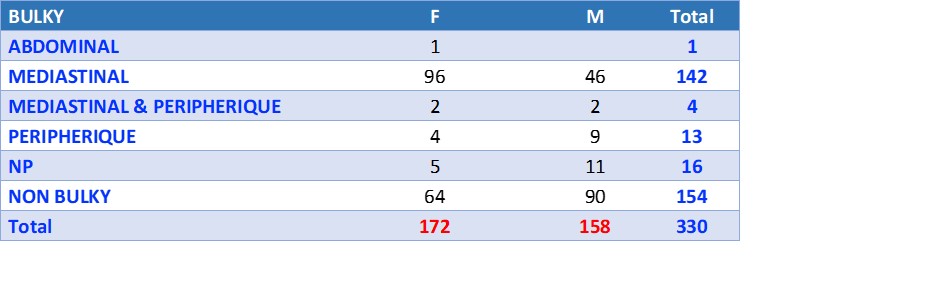
Par contre, le PS selon ECOG [OR 2,8 IC 1,4-5,8 p:0,003], la présence des signes d’évolutivité clinique [OR 3,6 IC 1,7-7,3 p:0,001], la splénomégalie [OR 2,2 IC 1,07-4,7 p:0,029], l’atteinte médullaire [OR 4,1 IC 1,5-10,4 p:0,004] et la présence d’une masse tumorale volumineuse (index : masse médiastinale/ thorax >0,33 et/ou une adénopathie >10 cm) [OR 2,2 IC 1,2-4,2 p:0,015] réduisaient les chances d’avoir une RC après un traitement standard de première ligne.
L’atteinte de moins de trois aires ganglionnaires [OR 0,8 IC 0,6-1,2 p:0,05], un stade localisé de la maladie ; I et II selon la classification de ANN ARBOR [OR 0,28 IC 0,15-0,5 p<0,001], un score pronostique favorable dans les stades localisés [OR 0,2 IC 0,06-0,63 p:0,006], et un score standard pour les formes étendues de la maladie [OR 0,7 IC 0,3-0,82 p:0,005] augmentaient la probabilité d’obtenir une RC.
Discussion
L’évaluation de l’état général des patients par le PS selon ECOG est primordiale lors de leur prise en charge. Les auteurs d’une étude des années 1980 ont constaté qu’une chimiothérapie administrée aux patients ayant un PS selon ECOG médiocre diminue le taux de réponse au traitement, la survie et augmente la toxicité [8,9]. Ainsi, l’American society of clinical oncology (ASCO) déconseille l’utilisation de la chimiothérapie chez les patients atteints d’un cancer solide et ayant un PS supérieur ou égal à 3 [10]. Dans notre travail, 25% des patients ayant un PS ≥ 2 ont des signes d’évolutivité clinique et 30% d’entre eux ont un stade avancé de la maladie.
L’atteinte splénique dans le LH peut prendre plusieurs formes, une splénomégalie homogène, une infiltration diffuse, des lésions miliaires ou des atteintes nodulaires uniques ou multiples [11]. Ainsi, une rate de taille normale peut être le siège d’une localisation lymphomateuse. Par ailleurs, il est difficile de préciser la taille réelle d’une rate [12]. Cheson et al., proposent un diamètre vertical supérieur à 13 cm pour définir une splénomégalie [12]. L’atteinte splénique est mieux déterminée par le PET-FDG [11]. Dans une étude de la relation entre atteinte splénique et obtention de la RC U. Rueffer et al., en 2003, constatent que la présence d’une splénomégalie diminue le taux de la RC, en effet, 61,6% des patients n’ayant pas obtenue la RC, ont eu une splénomégalie au diagnostic [13].
La présence d’une masse tumorale volumineuse aggrave le pronostic des LH de stade localisé [14,15]. De ce fait, actuellement, il est suggéré de traiter les LH de stade II B Bulky selon le même protocole que les stades avancés [16,17]. Dans notre série, parmi les 93 patients classés en stade II, 25% (24 patients) étaient des II B Bulky et la RC n’a été obtenue que chez 42% d’entre eux, avec un odds ratio (OR) significatif [OR 3, IC 1,1-8,4 p:0,03].
L’infiltration de la moelle osseuse témoigne d’une maladie disséminée, elle est rare chez les patients atteints de LH, son incidence varie entre 4% et 14% selon les séries rapportées au cours des trente dernières années [18,19]. Son implication s’avère être un marqueur de mauvais pronostic indépendant pour prédire à la fois la résistance au traitement, la survie sans progression, et la survie globale [20].
Le taux estimé de RC dans les stades localisés est de 63%, il est nettement meilleur dans les groupes favorables selon le score de l’EORTC, avec un taux de RC estimé de 87% versus 55% de RC dans les groupes défavorables, cette différence a été rattrapée par la radiothérapie [3]. Dans les formes étendues du LH le taux de RC a été estimé à 51,4% [4].
Actuellement le traitement des formes localisées dépend du score pronostique. Les groupes favorables reçoivent 3 cycles d’ABVD suivi d’une radiothérapie de consolidation, et les groupes défavorables bénéficient de 4 cycles d’ABVD plus radiothérapie. L’évaluation par FDG-PET scan est proposée après deux cycles d’ABVD [21]. Dans les stades localisés, les patients ayant reçu une combinaison chimiothérapie et radiothérapie. La survie globale a été de 97% et la survie sans évènement de 93% [22]. Le SPI est un score pronostique validé pour estimer la survie sans progression et la survie globale des LH de stade avancé [6]. Chez les patients qui ne présentent aucun facteur de risque, la survie sans progression après une RC est de 84%, alors qu’elle est de 42% chez les patients avec 7 facteurs de risques [23].
Conclusion
Après le diagnostic d’un LH, le premier objectif de la prise en charge thérapeutique est d’avoir une RC avec le minimum de toxicité et de décès. Dans cette optique, l’identification des facteurs pouvant interférer avec l’obtention de la RC est donc primordiale, ceci afin de mieux adapter le traitement à visée curative et symptomatique chez ces patients, ce qui peut augmenter les chances de survie des patients et leur taux de guérison.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- RL Siegel, KD Miller, A Stacy, Fedewa, J Dennis, A Jemal, et al. Cancer statistics, 2017. CA Cancer J Clin. 2017; 67:7-30.
- MT Aabad, S Taoussi, Lamraoui F, Oukid S, Benlabiod M, Bouchakor Y et al. Épidémiologie de la maladie de Hodgkin en Algérie Période 2008-2012. Revue Algérienne d’Hématologie, 2015, (10-11) ; 6-11
- F Tensaout, N Ait Amer, F Belhadri, N Abdennebi, H Moussaoui, F Boukhamia, et al. Résultats thérapeutiques du protocole ABVD-Platine. Revue Algérienne d’Hématologie, 2015, (10-11) ; 12-17.
- F Talbi, K Djouadi, SE Belkhal, Y Ghassoul, MR Abadi, S Boudjalida, et al. Résultats de l’ABVD dans les stades étendus de la maladie de Hodgkin. Revue Algérienne d’Hématologie, 2015, (10-11) ; 18-22.
- EM Noordijk, P Carde, N Dupouy, A Hagenbeek, ADG Krol, JC Kluin-Nelemans, et al. Combined-modality therapy for clinical stage I or II Hodgkin’s lymphoma: long-term results of the European Organisation for Research and Treatment of Cancer H7 randomized controlled trials. J Clin Oncol 2006; 24: 3128–3135.
- D Hasenclever, V Diehl, JO Armitage, D Assouline, M Björkhlom, E Brusamolino, et al. A prognostic score for advanced Hodgkin’s disease. International prognostic factors project on advanced Hodgkin’s disease. N Engl J Med. 1998; 339:1506-14.
- BD Cheson, SJ Horning, B Coiffier, MA Shipp, RI Fisher, JM Connors, et al: Report of an International Workshop to standardize response criteria for non-Hodgkin’s lymphomas. J Clin Oncol 1999; 17:1244-1253.
- KE Stanley. Prognostic factors for survival in patients with inoperable lung cancer. J Nat Cancer Instit. 1980; 65(1):25-32.
- JL Pater, M Loeb. Nonanatomic prognostic factors in carcinoma of the lung: a multivariate analysis. Cancer. 1982; 50(2):326-331.
- LE Schnipper, TJ Smith, D Raghavan, BW Blayney, PA Ganz, TM Mulvey, et al. American Society of Clinical Oncology identifies five key opportunities to improve care and reduce costs: the top five list for oncology. J Clin Oncol. 2012; 30(14):1715-1724.
- SS Saboo, KM Krajewski, KN O’Regan, A Giardino, JR Brown, N Ramaiya, et al: Spleen in haematological malignancies: Spectrum of imaging findings. Br J Radiol2012; 85:81-92.
- BD Cheson, RI Fisher, SF Barrington, F Cavalli, H Chwatrz, E Zucca, et al. Recommendations for Initial Evaluation, Staging, and Response Assessment of Hodgkin and Non-Hodgkin Lymphoma: The Lugano Classification. J Clin Oncol 2014 ; 32:3059-3067.
- Rueffer, M Sieber, M Stemberg, A Gossmann, A Josting, T Koch, et al. Spleen involvement in Hodgkin_s lymphoma: assessment and risk profile. Ann Hematol 2003 ; 82:390–396.
- Fermé, H. Eghbali H, JH. Meerwaldt, C. Rieux, J. Bosq, F. Berger, et al. Chemotherapy plus involved-field radiation in early-stage Hodgkin’s disease. N Engl J Med 2007;357(19):1916-1927.
- Diehl, J. Franklin, M. Pfreundschuh, B. Lathan, U. Paulus, D. Hasenclever et al. Standard and increased-dose BEACOPP chemotherapy compared with COPP-ABVD for advanced Hodgkin’s disease. N Engl J Med 2003; 348(24):2386-2395.
- Engert, H. Haverkamp, C. Kobe, J. Markova, C. Renner, A. Ho, et al. Reduced- intensity chemotherapy and PET-guided radiotherapy in patients with advanced stage Hodgkin’s lymphoma (HD15 trial): a randomised, open-label, phase 3 non-inferiority trial. Lancet 2012; 379(9828):1791-1799.
- Borchmann P, Kreissl S, Diehl V, Engert A. Treatment of Advanced-Stage Hodgkin Lymphoma: Let Us Face the Facts. Journal of Clinical Oncology 2013; 31(24):3045-3046.
- Alsuliman, A. Bekadja, A. Arabi, H. Touhami, F. Touhami, Z. Zouaoui et al, Hodgkin Lymphoma in the West of Algeria: Panorama of Characteristics, Initial Work-up, Survival and Risk Factors Distribution J Blood Lymph 2014, 4 (2): 1-7
- Howell, M. Grey, J. Chang, GR. Morgenstern, R.A. Cowan, D.P Deakin, J.A Radford et al. The value of bone marrow examination in the staging of Hodgkin’s lymphoma: a review of 955 cases seen in a regional cancer centre. Br J Haematol 2002; 119: 408-411.
- Mangla MBBS, M. Umair Mushtaq, R. Kumar, N. Agarwal, S. Gull Chaudhary, R. Catchatourian et al. Prognostic Significance of Bone Marrow Involvement in Hodgkin Lymphoma. Blood 2016;128 (22): 5370.
- RT Hoppe, RH Advani, WZ Ai, RF Ambinder, P Armand, CM Bello, et al. Hodgkin Lymphoma, Version 2.2020. J Natl Compr Canc Netw 2020; 18(6):755–781.
- E Andeas, J Raemaekers. Treatment of early favorable and early unfavorable hodgkin lymphoma – combined modality therapy? seminhematol.2016; 05.004.
- AA Moccia, J Donaldson, M Chhanabhai, PJ Hoskins, RJ Klasa, KJ Savage, et al. International Prognostic Score in advanced- stage Hodgkin’s lymphoma: altered utility in the modern era. J. Clin. Oncol. 2012; 30, 3383–3388.
| Tableau 4. L’analyse uni et multivarié de l’impact des facteurs sur l’obtention de la rémission complète.
OR : Odds Ratio, PS : Performance status selon ECOG, IC: Intervalle de confiance, EORTC : European organization for research and treatment of cancer. SPI: Système prognostic international. |
| Tableau 1. Les critères de réponse au traitement.
RC : rémission complète, RCu : rémission complète incertaine, RP : réponse partielle |
| Tableau 3. Caractéristiques clinico-biologique et les résultats des tests de comparaisons.
RC : Rémission complète, PS : Performance status selon ECOG, Symptôme B : signes d’évolutivités cliniques, Bulky : adénopathie > 10 cm de diamètre et ou IMT > 0,33. LDH : Lactate dyshydrogénèse. P : P value.* : Test de Chi 2. ** : Test de Student |
| Tableau 2. Répartition de la réponse au traitement en fonction du stade de la maladie.
N : nombre des patients |