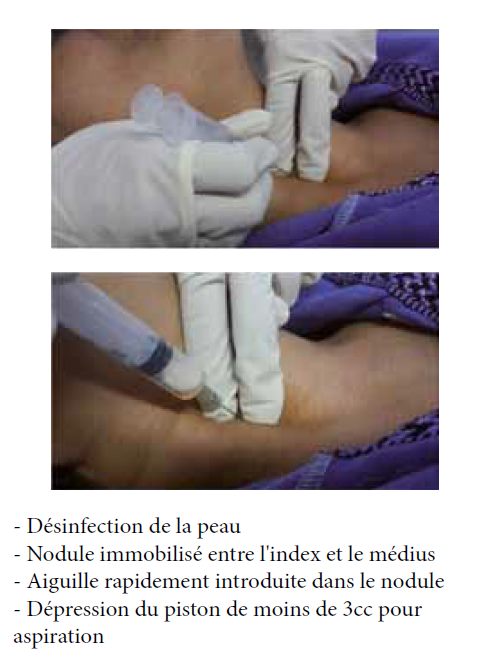
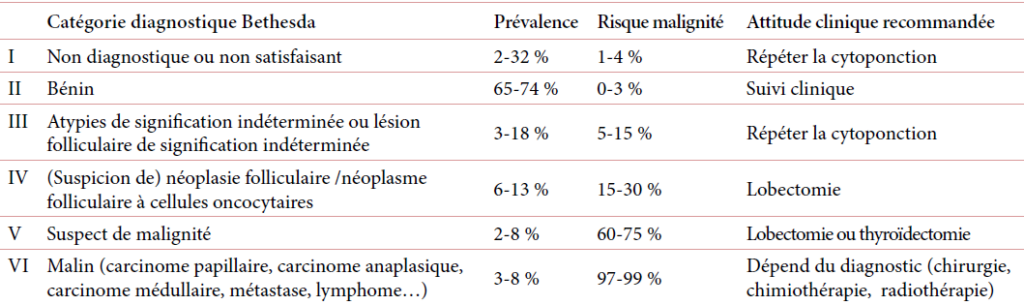
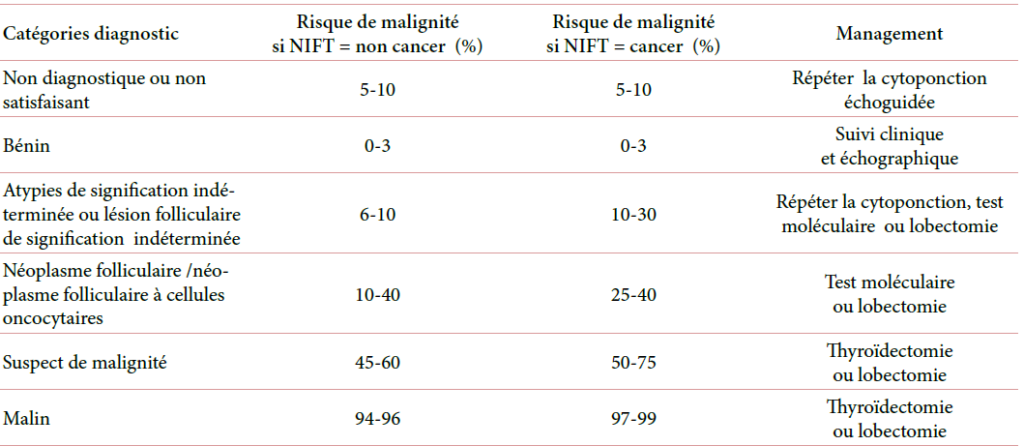
L. RABEHI, Service d’Endocrinologie et Maladies Métaboliques, CHU Lamine Debaghine, Bab El Oued, Alger.
Abstract : Hypoparathyroïdism results from the absence or insufficiency of PTH secretion, the main regulating hormone of calcium homeostasis. The clinical picture reflects the consequence of hypocalcemia in short and medium term and its mode of installation. These etiologies are multiple most often acquired, rarely hereditary, improved by advances in molecular biology. Its positive diagnosis is biological, evoked in the presence of hypocalcemia compared to inappropriate low or normal PTH rate. Diagnosis approach aims to link or not a parathyroid origin to this hypocalcemia. A lesion assessment should be performed especially in chronic or syndromic hypoparathyroïdism to adapt its management. Treatment of hypoparathyroïdism involves vitamino calcium hormonal substitution, which must be regularly monitored and meet the therapeutic objectives to avoid iatrogenesis including hypercalciuria. It can be a challenge for the clinician to find the right balance between the discomfort of hypocalcemia, hypercalciuria risk and hyperphosphatemia. Hormone replacement therapy with recombinant or native PTH may be an alternative to overcome the stand-alone treatment disadvantages.
Key-words : Hypoparathyroïdism, PTH, hypocalcemia, CaSR, hypercalciuria.
Résumé : L’hypoparathyroïdie résulte de l’absence ou de l’insuffisance de la sécrétion de l’hormone parathyroïde (PTH), principale hormone régulatrice de l’homéostasie calcique. Le tableau clinique traduit la conséquence de l’hypocalcémie à court, à moyen terme et de son mode d’installation. Ces étiologies sont multiples le plus souvent acquises, rarement héréditaires dont le diagnostic a été amélioré par les progrès de la biologie moléculaire. Son diagnostic positif est biologique évoqué devant la constatation d’hypocalcémie en regard d’un taux de PTH inappropriée bas ou normal. La démarche diagnostique vise à rattacher l’origine parathyroïdienne ou non de cette hypocalcémie. Un bilan lésionnel doit être réalisé surtout dans les hypoparathyroïdies chroniques ou syndromiques, pour adapter la prise en charge. Le traitement de l’hypoparathyroïdie fait appel à la substitution hormonale vitamino-calcique qui doit être régulièrement surveillée et répondre aux objectifs thérapeutiques pour éviter l’iatrogénie notamment l’hypercalciurie. Il peut constituer un challenge pour le praticien afin de trouver le juste équilibre entre l’inconfort de l’hypocalcémie, le risque de l’hypercalciurie et l’hyperphosphatémie. L’hormonothérapie substitutive par la PTH recombinante ou native peut constituer une alternative pour pallier aux inconvénients du traitement standard.
Mots-clés : Hypoparathyroïdie, PTH, hypocalcémie, CaSR, hypercalciurie
Introduction :
L’hypoparathyroïdie est l’ensemble des manifestations cliniques et paracliniques diverses dues à une diminution ou absence de la sécrétion de l’hormone parathyroïde la « PTH ». Ce qui aura comme conséquence biologique une hypocalcémie exposant le patient à court terme aux risques de crise de tétanie et convulsive, au long terme aux troubles trophiques. Les hypothyroïdies sont d’origines multiples, rarement héréditaires, le plus souvent acquises, dont la chirurgie cervicale est la cause la plus fréquente.
2. Physiopathologie
Le corps humain d’un adulte de 70Kg contient environ 1Kg de calcium et 700 g de phosphore, élément dont l’immense majorité (99% du Ca+ et 85 % du PO4-) est localisé dans le cristal d’hydroxyapatite du squelette.
0,1 % du calcium extra osseux se retrouve en extracellulaire mesuré en tant de calcémie totale (40 % est liée aux protéines principalement l’albumine, 10 % liée à des anions, 50% libre sous forme de calcium ionisé).
La calcémie varie étroitement entre 2,15-2,55 mmol/l (86- 102 g/l).
Le maintien de la balance calcique est assuré par trois organes l’intestin, l’os, le rein et un système régulateur représenté par les hormones calcitropes la PTH et le calcitriol (1-25(OH)D3).
A. PTH :
C’est une protéine de 84 AA synthétisée continuellement et stockée dans les vésicules des cellules parathyroïdes. Elle est secrétée en réponse immédiate à l’hypocalcémie, mais aussi à plus long terme à la carence en calcitriol, l’hyperphosphatémie et la résistance à la FGF23.
Cette sécrétion est finement régulée par le Ca+ plasmatique via le récepteur sensible au calcium « CaSR » exprimé à la surface des cellules parathyroïdes. Une augmentation de la calcémie ionisée active le CaSR, ce qui induit la dégradation de la PTH et la sécrétion de fragments inactifs. Au contraire, la baisse de la calcémie ionisée entraine une inactivation du CaSR et une stimulation de la sécrétion de la PTH intacte la quelle va :
- Stimuler la libération du Ca+ de l’os vers le plasma via le récepteur da la PTH « PTHR1 ».
- Augmenter la réabsorption rénale du Ca+ principalement au niveau du tube contourné distal.
- Diminuer la réabsorption rénale du phosphate, ce qui augmente la phosphaturie.
- Stimuler, au niveau rénal, la synthèse et l’activité de 1-ahydroxylase qui catalyse la transformation du 25(OH)D3 en 1-25(OH)D3 ou calcitriol, qui à son tour augmentera l’absorption intestinale du Ca+.
B. La vitamine D
La vitamine D calciférol (D3 Cholécalciférol, D2 ergo- calciférol) va subir deux hydroxylation. La 1ère au niveau du foie, en position 25 pour former la 25(OH)D3. La 2ème au niveau rénal, en position 1 pour former la 1-25 (OH)D3 ou calcitriol. Cette hydroxylation rénale est régulée et stimulée principalement par la PTH, une hypophosphatémie, une hypocalcémie.
Le calcitriol agit via un récepteur cytosolique le VDR présent dans de nombreux tissus cibles (parathyroïde, rein, os, tube digestif) mais également d’autres organes. Le calcitriol permet l’absorption intestinale et rénale du Ca+ et du PO4-, permettant un environnement phosphocalcique favorable à la minéralisation osseuse. En retour le calcitriol diminue la synthèse de la PTH et la prolifération des cellules parathyroïdes.
- Au cours de l’hypoparathyroïdie L’hypocalcémie est expliquée par la diminution de la résorption osseuse et de la réabsorption tubulaire rénale de Ca+.
L’hyperphosphatémie est en rapport avec une augmentation de la réabsorption tubulaire rénale. De plus, la diminution de la sécrétion de PTH et l’hyperphosphatémie entrainent la diminution de la synthèse rénale du calcitriol, qui est à l’origine d’une diminution de l’absorption intestinale du Ca+.
Clinique
La symptomatologie liée à l’hypocalcémie est variable, Elle peut être modérée et latente, en règle générale bien tolérée. Elle peut être sévère et menaçant le pronostic vital. L’expression du tableau clinique dépendra du degré de l’hypocalcémie, son mode d’installation (aigu, chronique), l’étiologie et l’âge du patient. Les symptômes sont d’autant plus sévères que l’hypocalcémie est de survenue brutale et de début précoce dans la vie. Ils surviennent même chez des patients qui maintiennent des concentrations de Ca+ dans les objectifs thérapeutiques.
A. Manifestations paroxystiques
• La Crise de Tétanie :
Elle est fréquente dans l’hypocalcémie aigue, se caractérise par une contraction musculaire spontanée et persistante secondaire à une augmentation de l’excitabilité neuronale.
Elle débute par des paresthésies et fourmillement des extrémités et de la région péribuccale, suivies par des fasciculations musculaires, puis surviennent les contractures généralisées ou localisées aux membres supérieurs réalisant « la main d’accoucheur ». À la face « le museau de carpe ».
Aux membres inférieurs l’aspect en « varus équin ». Les contractures peuvent se généraliser à tous les muscles et entrainer des spasmes gastriques, intestinaux, bronchospasmes, et des formes majeures avec spasmes laryngés et crises convulsives généralisées chez le nourrisson.
- Signes d’hyperexcitabilité neuromusculaire Ces signes existent en dehors de la crise de tétanie. Ils sont fréquents et variables selon la gravité et la chronicité de l’hypocalcémie, ils se traduisent par : Paresthésies distales et péribuccales, spontanées ou déclenchées par la compression ou l’effort.
- Signe de Chvosteck : ce signe peu spécifique se traduit par une contracture reflexe de la lèvre supérieure, à la percussion de la joue à mi-distance entre le lobule de l’oreille et la commissure.
- Signe de Trousseau : se traduit par la contracture de la main et des doigts en main d’accoucheur, provoquée par la compression du bras par un brassard gonflé à 20 mmHg au-dessus de la PAS pendant 2-3mn.
B. Manifestations chroniques
L’hypocalcémie chronique provoque moins de manifestations neuromusculaires mais plutôt des manifestations diverses et peu spécifiques.
- Troubles trophiques : cutanéomuqueux et phaneriens, existent à différents niveaux. Peau sèche désquamante, siège de lésions infectieuses surtout mycosiques. Cheveux fins et secs. Les ongles sont striés et cassants. Émail dentaire striée et dépoli avec caries nombreuses et à répétition. Chez les enfants hypocalcémiques, les dents sont fréquemment dysplasiques voire absentes.
- Troubles neurologiques : peuvent exister des signes extrapyramidaux, syndromes parkinsoniens, mouvements anormaux choréiques ou athétosiques, des crises comitiales généralisées ou focalisées, résistantes au traitement antiépileptique et régressant après correction de l’hypocalcémie.
- Troubles digestifs : les patients peuvent se plaindre de constipation et de coliques abdominales, d’une stéatorrhée avec malabsorption possible par atrophie des villosités intestinales.
- Troubles psychiques : ils sont variés et trompeurs, allant du simple changement d’humeur, insomnie et agitation, aux états dépressifs et mélancoliques, névrose s’améliorant après correction de la calcémie.
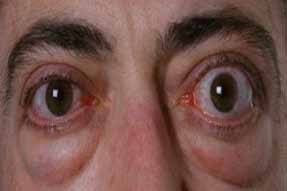
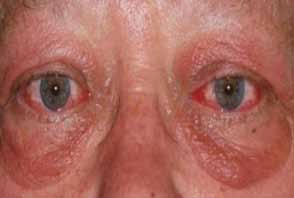
- Manifestations oculaires : la cataracte est la manifestation la plus caractéristique et de topographie évocatrice. Sous capsulaire antérieure ou surtout postérieure, épargnant le noyau du cristallin. Elle est retrouvée chez 28% des patients souffrant d’hypocalcémie depuis plus de 4 ans.
- Manifestations osseuses : une déminéralisation du squelette, avec plus au moins au long terme une ostéopénie, des fractures, des tassements vertébraux.
- Manifestations cardiaques : lors d’hypocalcémie sévère, des patients peuvent subir des épisodes d’arythmie, troubles de conduction, ou insuffisance cardiaque congestive. Ces troubles ne sont contrôlés qu’après correction de l’hypocalcémie.
- Calciflcations des parties molles : l’hyperphosphatémie chronique observée au cours de l’hypoparathyroïdie, favorisée par le traitement substitutif, va conduire à la formation de dépôts calciques, liés à l’augmentation du produit phosphocalcique et à l’expression locale de molécules ostéogéniques. Ces calcifications sont classiquement localisées au niveau cérébral (syndrome de Fahr) et rénal mais peuvent s’observer au niveau cutané, articulaire, oculaire et vasculaire.
- Altération de la qualité de vie : près de 80% des patients rapportent une fatigue ou une fatigabilité. Beaucoup de patients se plaignent de troubles de la mémoire et de la concentration. La qualité de vie des patients est diminuée. Cependant, aucun lien avec le contrôle biologique, l’étiologie, la durée de la maladie ou encore les traitements instaurés n’a pu être clairement établi.
- Morbidité : Le risque d’hospitalisation pour infection est augmenté, même en excluant les infections du tractus urinaire. Cette sensibilité aux infections pourrait être expliquée par le fait que le Ca+ est un second messager important pour les cellules immunitaires.
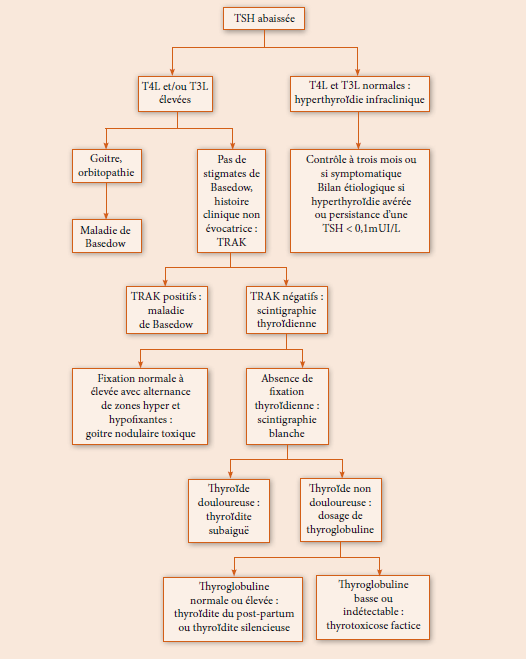
Diagnostic biologique
A. Biologie
Le diagnostic positif de l’hypoparathyroïdie est biologique. Il est posé devant une hypocalcémie associée à une valeur plasmatique de PTH inappropriée non élevée (basse ou normale) contrôlée à deux semaines d’intervalle. Le tableau biologique associe :
- PTH : basse ou normale.
- Hypocalcémie : inférieur à 2,10 mml/l (84 mg/l). Pour être correctement interprétée, elle doit toujours être confrontée à la protidémie.
Il convient de calculer la calcémie corrigée par les formules suivantes :
Ca+ corrigée = Ca+ (mg/l) – [0,689 x (protidémie+50,6)] ou Ca+ (mg/l) – [0,689 x (albumine+40)].
- Hypocalciurie : inférieur à 100 mg/24 h chez le patient non traité, en raison de la diminution de la charge filtrée du calcium, (alors qu’elle est normale voir élevée dans l’hypocalcémie autosomique dominante).
- Hyperphosphatémie : par augmentation de la réabsorption tubulaire rénale
- Hypophosphatémie : par diminution de l’excrétion tubulaire rénale.
- Calcitriol : est bas en raison de l´absence de stimulation de la 1α hydroxylase rénale par la PTH.
Les indices de remodelage osseux sont diminués. Il est rare de recourir au test dynamique. Le dosage de l’APMc urinaire avant et après injection de PTH est réservé au diagnostic différentiel entre l’hypoparathyroïdie et pseudo-hypoparathyroïdie.
Où l’APMc augmente dans l’hypoparathyroïdie vraie et non dans la pseudo-hypoparathyroïdie.
A. Paraclinique
- ECG : trouble de repolarisation à type d’allongement de l’espace QT et segment ST.
- EEG : Images en doublet, triplet ou multiple.
- Radiologie : calcifications des noyaux gris de la base. Épaississement des corticales chez l’enfant.
- DMO : la diminution de la sécrétion de PTH entraine une diminution du remodelage osseux, accompagnée d’une augmentation de la minéralisation de l’os cortical ou trabéculaire. Ainsi, chez des patients atteints d’hypoparathyroïdie, il a été constaté une augmentation de la densité minérale osseuse au niveau des sites d’os trabéculaire, avec une diminution de la perte minérale osseuse physiologique au niveau des sites d’os cortical.
Orientation étiologique
A. Sur le plan clinique
Lors de l’exploration d’un patient se plaignant de symptômes évocateurs d’hypocalcémie, et en l’absence d’insuffisance rénale sévère, le diagnostic est avant tout guidé par l’interrogatoire, l’enquête familiale et l’examen clinique. En effet, une chirurgie thyroïdienne oriente vers une hypoparathyroïdie post chirurgicale. L’existence d’autres cas familiaux d’hypocalcémie peut orienter vers le diagnostic d’hypocalcémie autosomique dominante ou d’hypoparathyroïdie héréditaire.
L’examen clinique recherchera des anomalies secondaires à la résistance à d’autres hormones que la PTH et des signes malformatifs fréquemment associées aux syndromes de résistance héréditaire à la PTH (pseudo-hypoparathyroïdies).
B. Sur le plan biologique
Devant la constatation d’une hypocalcémie, le dosage de la PTH est un élément d’orientation étiologique qui permet de distinguer :
Les hypocalcémies « parathyroïdiennes » où la sécrétion de PTH est inappropriée (basse ou normale) représentées par les hypoparathyroïdies et l’hypocalcémie autosomique dominante.
Les hypocalcémies « extra parathyroïdiennes », où la sécrétion de la PTH est appropriée (élevée) représentées par les pseudo-hypoparathyroïdies et la carence ou la résistance à la Vitamine D.
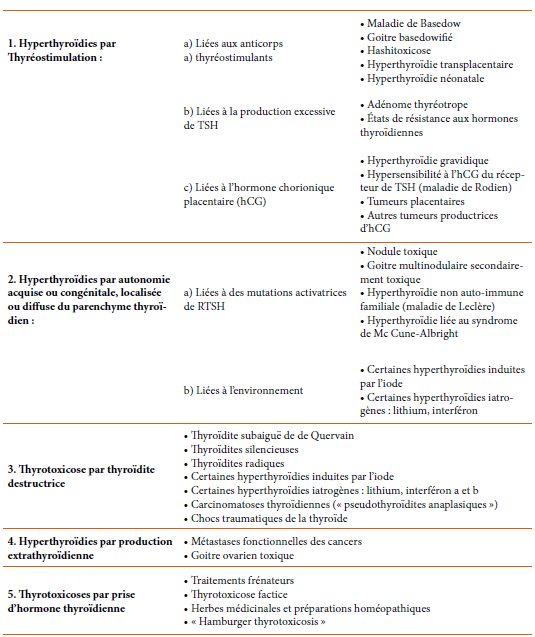
Étiologies des hyperparathyroïdies
A. Hypoparathyroïdie acquise
- Iatrogène : La chirurgie cervicale reste l’étiologie la plus fréquente de l’hypoparathyroïdie (75 % des causes). Pratiquée pour cancer thyroïdien ou laryngé, maladie de Basedow ou goitre multi nodulaire, interventions répétées sur les parathyroïdes. Ou la conséquence d’un œdème ou d’hémorragies altérant la vascularisation des glandes parathyroïdes. Cette hypoparathyroïdie peut être précoce habituellement transitoire, ou tardive généralement définitive.
- Secondaire à la destruction des glandes : lors d’irradiation cervicale externe, traitement par l’iode radioactif, infiltration granulomateuse (tuberculose, sarcoïdose), néoplasique (métastases d’un cancer), fibro-inflammatoire (thyroïdite de Riedel), maladie de surcharge (Wilson et hémochromatose).
- Fonctionnelle : le CaSR est sensible à la magnésémie et sa baisse chronique inhibe la sécrétion de la PTH et entraîne une résistance tubulaire à la PTH. Les désordres du métabolisme du magnésium (hyper ou hypomagné- sémie profonde ou chronique) peuvent entrainer une hypoparathyroïdie fonctionnelle.
B. Hypoparathyroïdie génétique
1. Hypoparathyroïdie auto-immune
C’est la seconde cause d’hypoparathyroïdie bien que son diagnostic soit souvent retenu par défaut devant une hypoparathyroïdie idiopathique. Elle peut être sporadique ou familiale avec mode de transmission indéterminé lorsqu’elle est isolée. L’hypoparathyroïdie peut être la composante du syndrome APECED (Poly Endocrinopathie Auto-immune, Candidose, Dystrophie Ectodermique). Ce syndrome héréditaire, de transmission autosomique récessive par mutation du gène AIRE localisé en 21 q22.3 est caractérisé par la triade une candidose cutanéomuqueuse qui est la manifestation la plus précoce, suivi de l´hypoparathyroïdie puis de l´insuffisance surrénalienne.
1. Hypoparathyroïdie Congénitale
Les hypoparathyroïdies congénitales peuvent se révéler en période néonatale par des hypocalcémies permanentes. La PTH est indosable et le traitement par dérivés actifs de la vitamine D ne peut être arrêté sans récidive de l’hypocalcémie. Plusieurs gènes résumés dans le tableau ont été identifiés. Impliqués dans la genèse des parathyroïdes (GCMB, GATA3, TBX1, TBCE 1-2), la transmission du signal calcique au niveau de la cellule parathyroïdienne (CaSR, GNA11), ou dans les cellules cibles.
- Le syndrome de Di George : (syndrome vélocardiofacial) : est la principale étiologie de l’hypoparathyroïdie génétique. Il s’agit d’une hypoparathyroïdie syndromique dans laquelle le tableau clinique est très variable d’un enfant à l’autre et l’hypocalcémie peut parfois être le seul symptôme et s’améliorer durant l’enfance. La micro délétion est présente dans plus de 95% des cas mais est rarement détectée chez les parents (mutation de novo).
- Les mutations activatrices du gène du récepteur sensible au calcium (CaSR) : est la deuxième étiologie d’hypoparathyroïdie congénitale, par ordre de fréquence. En cas de mutation activatrice un gain de fonction et un faux signal d’hypercalcémie est transmis et donc la sécrétion de PTH est freinée. Comme ce récepteur existe également au niveau du tubule rénal, la caracté- ristique de cette hypoparathyroïdie de transmission au- tosomique dominante est qu’elle associe hypocalcémie et hypercalciurie. La prise en charge doit être prudente, du fait du risque majeur de néphrocalcinose.
Traitement
A. Hypocalcémie chronique
1. Objectif
Le traitement d’une hypoparathyroïdie chronique doit essayer de répondre à plusieurs objectifs : prévenir les symptômes de l’hypocalcémie, maintenir la calcémie dans les limites inferieures de la normale (ou juste en dessous de la normale), maintenir le produit phosphocalcique (calcémie × phosphorémie) < 55 mg2/dl2, éviter l’hypercalciurie et l’apparition de calcifications rénales. Le traitement vise aussi l’amélioration de la qualité de vie des patients, qui doit être évaluée avant, après l’introduction du traitement, et au cours du suivi. Il doit impliquer le patient lui-même par l’éducation notamment quant au signes indiquant un sous ou un surdosage.
2. Moyens thérapeutiques et dose
- Calcium : Carbonate de calcium en comprimé ou sachet à 500 mg. À raison de 1 à 6 g/jour en 2 à 4 prises à prendre au cours du repas car mieux absorbé avec l’acidité gastrique et permet d’avoir un effet chélateur du phosphore.
- Vitamine D active
- Calcitriol (Rocaltrol®), capsule de 0,25 μg. À raison de 0,25 à 1,5μg /jour.
- Alfacalcidol (1α(OH)D3), sous forme de gouttes à 0,10 μg, ou capsule de 0,25 ; 0,5 ou 1 μg. À raison de 1 à 3 μg /jr.
Diurétiques thiazidiques (DT), en cas d’hypercalciurie, ce traitement doit être combiné à un régime hyposodé. Hydrochlorothiazide : 12,5 à 100 mg/j. Indapamide : 1,25 à 5 mg/j.
- Supplémentation en Mg+. Si hypomagnésémie (mutation activatrice du CaSR, traitement par IPP, DT, malabsorption). Ampoule MAG2 122 mg. Comprimé effervescent, 150mg ; ou à avaler, 100mg. À raison de 300 à 400mg/jour en 2 à 3 prises.
- Hygiène de vie : en cas d’hyperphosphatémie il faut réduire la vitamine D active et augmenter la dose du Ca+. Prescrire un régime alimentaire (éviction des viandes, abats, charcuteries, poissons, crustacés, fruits secs, légumes à bouillir). Conseiller un apport alimentaire optimal en Ca+.
3. Surveillance du traitement
Pendant la mise en place du traitement la calcémie peut être mesurée plusieurs fois par semaine, puis toutes les semaines. Une fois la stabilisation obtenue un bilan tous les 3 à 6 mois, voire annuellement selon l’équilibre du patient sera réalisé. Il comprendra calcémie, phosphatémie, magnésium, urée, créatinémie.
Il faut vérifier en périodes d’ajustement thérapeutique la calciurie qui doit être ensuite recontrôlée au moins une fois par an pour atteindre l’objectif celui d’une calciurie < 4 mg/kg/24h.
B. Hypocalcémie aigue (crise de tétanie)
Les hypocalcémies symptomatiques ou sévères (< 70 mg/L ou < 1,8 mmol/L), nécessitent un traitement intraveineux.
Il faut préférer l’ampoule de gluconate de Ca+ à 10 % (10 ml contenant 90 mg de Ca+ élément).
Plutôt que le chlorure de Ca+ 10% (10 ml contenant 272 mg de Ca+) car veino-toxique. Ce traitement comporte :
- Administration en urgence en IV lente sur 15 minutes de deux à trois ampoules de gluconate de calcium 10 % dilués dans 50 à 100 ml de SG5 %. A répéter jusqu’à disparition des signes de gravité.
- Ensuite relayer par une perfusion IV apportant 0,5 à 2 mg/kg/h de (moyenne de 1 mg/kg).
- Exemple : pour un sujet pesant 80 kg (1 mg de Ca+ x 80 poids) x 24h = 1920 mg de Ca+/24h.
- 1920/90 = 21 amp/24h → soit 7 ampoules /8h dans diluées dans 500ml de SGI 5%.
- Passage à la voie per os quand la calcémie est supérieure à 80 mg/l.
Une hypomagnésémie associée doit être recherchée et supplémentée par une à deux ampoules de sulfate de magnésium 10 % par 24 heures. Pouvant être portées à 5 ampoules par 24 heures en cas d’hypomagnésémie sévère (< 0,7 mmol/l).
A. Perspectives thérapeutiques
L’absence de réabsorption tubulaire du Ca+ médiée par la PTH, conduit à l’augmentation de la filtration rénale de Ca+ et au risque de néphrocalcinose, de lithiase rénale et d’insuffisance rénale.
Le traitement conventionnel vitamino-calcique ne permet pas de remplacer l’effet hypophosphorémiant de la PTH via l’excrétion tubulaire proximale. Ceci expose au risque de déports ectopiques de PO4- dans les tissus notamment le cerveau. Ainsi le médecin doit jongler entre l’inconfort de l’hypocalcémie et le risque de l’hypercalciurie et hyperphosphatémie. Pour y remédier, la PTH recombinante initialement utilisée pour le traitement de l’ostéoporose a prouvé son efficacité dans l’hypopara- thyroïdie. Deux présentations sont disponibles en forme injectable en sous cutané. PTH (1-34) tériparatide (FORSTEO®). La PTH (1-84) (Natpara®) qui correspond à la forme native. La tolérance est globalement bonne sur une durée de suivi de 6 ans. Cependant il n’a pas été démontré si ce traitement permettait de prévenir les complications de l’hypoparathyroïdie chronique notamment le risque de néphrocalcinose. Ce traitement reste couteux et ne devrait être proposé qu’aux patients mal équilibrés sous traitement vitamino-calcique standard.
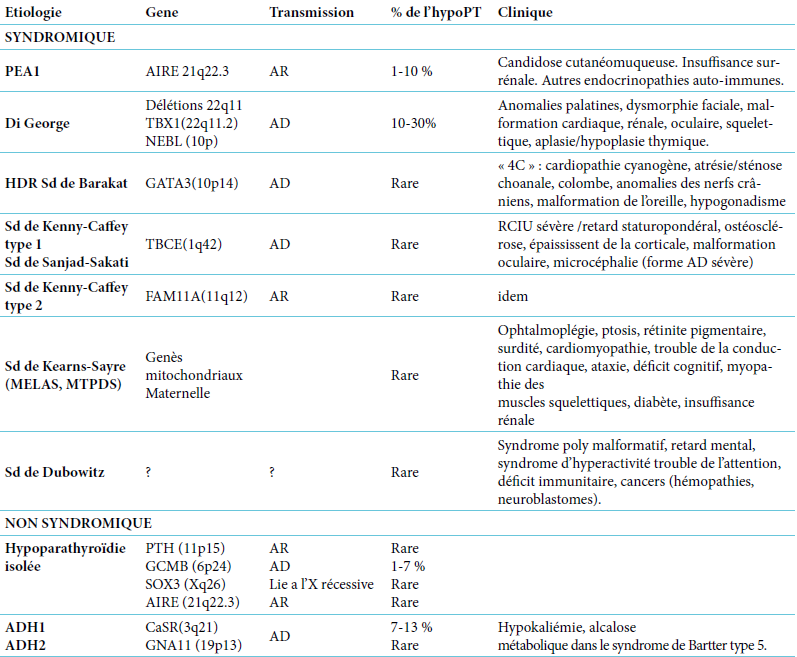
Sd : syndrome ; AR : autosomique récessif ; AD : autosomique dominant ; ADH : autosomal dominant hypoparathyroïdisme.
Conclusion
L’hypoparathyroïdie est une cause rare d’hypocalcémie qui se traduit dans les situations aigues ou chroniques par des signes variés. Elle affecte le fonctionnement de plusieurs organes et par conséquent la qualité de vie. Son diagnostic positif est biologique, et repose sur la mise en évidence d’une hypocalcémie associée à un taux de PTH inapproprié (bas ou normal).
La démarche diagnostique devant une hypocalcémie vise à rechercher son origine parathyroïdienne ou extra parathyroïdienne.
L’hypoparathyroïdie relève d’étiologies multiples dont les causes acquises demeurent les plus fréquentes. Une fois le diagnostic posé, l’étape suivante consistera à faire un bilan lésionnel pour répertorier les complications de l’hyperparathyroïdie chronique surtout dans les formes syndromiques.
Son traitement fait appel à la substitution vitamino-calcique avec les formes actives de vitamine D.
Ce traitement sera régulièrement et périodiquement suivi afin de prévenir l’hyper calciurie et l’hyperphosphatémie. La PTH recombinante peut constituer dans le futur une alternative thérapeutique pour pallier aux inconvénients de ce traitement standard surtout pour les patients mal contrôlés.
Références :
- P. Houillier. Physiologies des parathyroïdes. Encycl Méd Chir, Endocrinologie-Nutrition,10-011-C-10, 2008.
- Eladari D, Maruani G, Paillard M et Houillier P. Hypoparathyroïdie (à l’exclusion des syndromes de résistance à l’hormone parathyroïdienne). Encycl Méd Chir, Endocrinologie-Nutrition, 10-012-A-10, 2002, 9 p.
- Clarke BL, Brown EM, Collins MT, Juppner H, Lakatos P, Levine MA, et al. Epidemiology and diagnosis of hypoparathyroidism. J Clin Endocrinol Metab 2016 ;101 :2284-99.
- Champigny MA. Hypoparathyroïdie de l’enfant en France : aspects diagnostiques et étiologiques. Étude multicentrique. Thèse pour le diplôme de doctorat de médecine. Université de Limoges, 2016.
- S. Espiarda, M.-C. Vantyghema, R. Desailloud. Actualisation sur l’hyperparathyroïdie : un peu de théorie, beaucoup de pratique. An- nales d’Endocrinologie 78 (2017) S1-S10.
- Houillier P, Campone C, Maruani G, Paillard M. Traitement de l’hyperparathyroïdie de l’adulte. Med Clin Endocrinol Diabete, 2002, 1 : 53-56.
- Bilezikian JP, Brandi ML, Cusano NE, Mannstadt M, RejnmarkL, Rizzoli R, et al. Management of Hypoparathyroidism : Present and Future. J Clin Endocrinol Metab 2016 ;101 :2313-24.
- Rubin MR, Cusano NE, Fan WW, Delgado Y, Zhang C, Costa AG, et al. Therapy of hypoparathyroidism With PTH (1-84) : A Prospective six year Investigation of efficacy and safety. J Clin Endocrinol Metab 2016 ;101 :2742-5