M. DJENNANE (1), L. IGUENI (1),A. TIBICHE (2), Service de Rhumatologie, Service d’Épidémiologie, CHU Mohamed Nedir, Tizi Ouzou.
Abstract : Objectifs. L’ostéoporose est une complication fréquente de la spondyloarthrite (SA). L’ostéoporose dans la SA augmente significativement le risque de fractures par compression vertébrale dans les 5 ans suivant le diagnostic de SA. L’objectif de ce travail est d’estimer la prévalence des fractures vertébrales au cours de la spondyloarthrite en utilisant la Vertebral Fracture Assessment (VFA). Méthodes. Notre étude a inclus 132 patients avec SA. Les données cliniques, l’évaluation radiographique des fractures vertébrales (VFA) de T4 à L4 dans le rachis thoracique et lombaire, la densité minérale osseuse (DMO) et le statut en vitamine D ont été analysées. Résultats. Des fractures vertébrales ont été observées chez dix-sept (17) FV, soit chez 13% des 132 patients atteints de SA. La prévalence de l’ostéoporose était significativement plus élevée chez les patients avec FV, comparés aux patients sans FV (35% contre 24%). L’analyse multivariée a montré que la présence de fracture vertébrale était indépendamment associée à l’âge, à la durée de la maladie, à l’activité élevée de la maladie, au faible taux de vitamine D. Conclusion. L’ostéoporose est une comorbidité retrouvée dans la SA, souvent sous-diagnostiquée et non traitée. L’âge avancé, le fardeau de la maladie, son activité et l’immobilisation causée par la formation de syndesmophytes et les paramètres de l’inflammation sont des facteurs de risque élevé d’ostéoporose. Ces résultats suggèrent un dépistage précoce de cette comorbidité afin d’initier une prise en charge efficace. Néanmoins, des études longitudinales avec des effectifs plus importants sont nécessaires pour confirmer ces résultats.
Key-words : Spondyloarthritis, vertebral fracture, vertebral fracture assessment, Osteoporosis, bone mineral density, vitamin D.
Résumé : Objectifs. L’ostéoporose est une complication fréquente de la spondyloarthrite (SA). L’ostéoporose dans la SA augmente significativement le risque de fractures par compression vertébrale dans les 5 ans suivant le diagnostic de SA. L’objectif de ce travail est d’estimer la prévalence des fractures vertébrales au cours de la spondyloarthrite en utilisant la Vertebral Fracture Assessment (VFA). Méthodes. Notre étude a inclus 132 patients avec SA. Les données cliniques, l’évaluation radiographique des fractures vertébrales (VFA) de T4 à L4 dans le rachis thoracique et lombaire, la densité minérale osseuse (DMO) et le statut en vitamine D ont été analysées. Résultats. Des fractures vertébrales ont été observées chez dix-sept (17) FV, soit chez 13% des 132 patients atteints de SA. La prévalence de l’ostéoporose était significativement plus élevée chez les patients avec FV, comparés aux patients sans FV (35 % contre 24 %). L’analyse multivariée a montré que la présence de fracture vertébrale était indépendamment associée à l’âge, à la durée de la maladie, à l’activité élevée de la maladie, au faible taux de vitamine D. Conclusion. L’ostéoporose est une comorbidité retrouvée dans la SA, souvent sous-diagnostiquée et non traitée. L’âge avancé, le fardeau de la maladie, son activité et l’immobilisation causée par la formation de syndesmophytes et les paramètres de l’inflammation sont des facteurs de risque élevé d’ostéoporose. Ces résultats suggèrent un dépistage précoce de cette comorbidité afin d’initier une prise en charge efficace. Néanmoins, des études longitudinales avec des effectifs plus importants sont nécessaires pour confirmer ces résultats.
Mots-clés : Spondyloarthrite, fracture vertébrale, évaluation des fractures vertébrales, ostéoporose, densité minérale osseuse, vitamine D.
Introduction :
L’ostéoporose est une complication fréquente de la spondyloarthrite (SA), avec une incidence comprise entre 18,7 % et 62 % (1).
La prévalence de l’ostéoporose est plus élevée chez les hommes et augmente avec l’âge et la durée de la maladie. L’ostéoporose est également plus fréquente chez les patients présentant des syndesmophytes, de fusion cervicale avec atteinte articulaire périphérique.
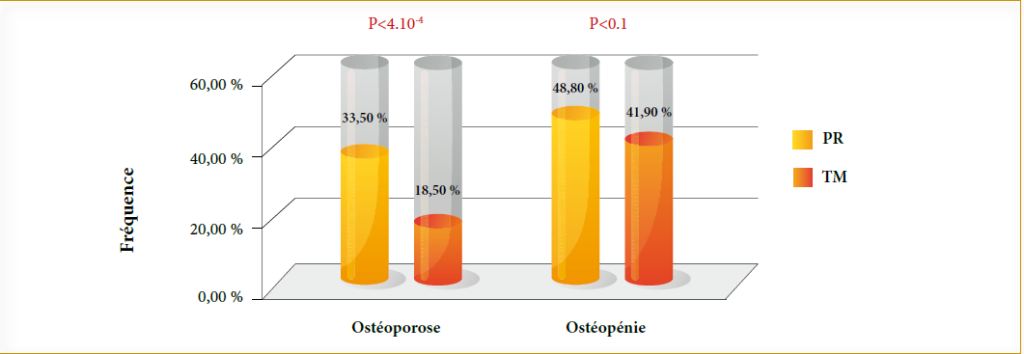
Chez les patients atteints de SA, l’ostéoporose est en grande partie limitée au squelette axial, contrairement à celui observé dans la polyarthrite rhumatoïde (2). L’ostéo-densitométrie osseuse (DMO) au rachis lombaire et au col fémoral peut être sévèrement réduite.
Le développement de syndesmophytes dans la SA peut entraîner des difficultés à utiliser le scanner DEXA pour déterminer la densité minérale osseuse lombaire, car ces derniers peuvent masquer les vertèbres ostéoporotiques.
L’ostéoporose dans le SA augmente significativement le risque de fractures par compression vertébrale dans les 5 ans suivant le diagnostic de SA. Le risque de fracture par compression vertébrale survenant sur une période de 30 ans suivant le diagnostic de SA est de 14 %, contre 3,4 % pour les témoins de la population (3).
Les cytokines telles que le TNF-alpha et l’IL-6 peuvent jouer un rôle important dans la pathogenèse de l’ostéoporose au début de la SA, et les taux d’IL-6 ont été corrélés avec les marqueurs de l’activité et de la sévérité de la maladie (4).
Bien que la radiographie standard de la colonne vertébrale soit considérée comme le gold-standard dans la détection des fractures vertébrales (FV), la Vertebral Fracture Assessment (VFA) offre certains avantages (5) comme la faible irradiation (3 micro-Sieverts au lieu de 600 pour un rachis dorsolombaire de profil), la mesure simultanée de la densitométrie osseuse, le moindre coût avec une valeur prédictive négative élevée de 95,5 % entre D7 et L4. Elle a également certains inconvénients comme une lisibilité de l’image insuffisante particulièrement au rachis dorsal supérieur (D4-D7) avec une sensibilité insuffisante (50 %) pour les FV de grade 1 (6).
La Vertebral Fracture Assessment (VFA) est une nouvelle méthode permettant l’évaluation et le diagnostic des fractures vertébrales (6).
C’est un outil pratique important pour la détection de ces déformations vertébrales. Malgré la prévalence élevée de l’ostéoporose et des fractures vertébrales dans la SA, ceci contraste avec le peu d’études dans la littérature portant sur l’évaluation du risque fracturaire (7).
L’objectif de ce travail est d’estimer la prévalence des fractures vertébrales au cours de la spondyloarthrite en utilisant la VFA.
Objectifs :
Objectif principal : Estimer la prévalence des fractures vertébrales au cours de la spondyloarthrite. Objectifs secondaires : identifier les facteurs de risque des fractures vertébrales et évaluer le statut vitaminique D.
Patients et Méthodes :
Population d’étude : C’est une étude prospective transversale ayant concerné une cohorte de patients atteints de SA recrutés au niveau de l’hôpital universitaire de Tizi Ouzou. Ont été inclus les patients remplissant les critères de New York de 1984.
N’ont pas été inclus les patients présentant une insuffisance rénale, une affection retentissant sur le métabolisme phosphocalcique, les patients ayant pris un traitement biologique, des corticoïdes, des anticonvulsivants et du calcium depuis moins de trois mois ainsi ceux chez lesquels les données étaient manquantes ou bien les résultats de la VFA étaient ininterprétables.
Tous les patients ont donné leur consentement éclairé.
Protocole de l’étude
Les données démographiques des patients ont été colligées, telles que l’âge, la taille, le poids, l’IMC. De même que les caractéristiques cliniques de la maladie ont été recueillies telles que la durée de la maladie, l’activité de la maladie par la mesure du BASDAI (Bath AS Disease Activity Index), Bath Indice fonctionnels (BASFI), le Bath AS Index de radiologie (BASRI).
Le bilan Biologique comportant essentiellement la CRP et la vitesse de sédimentation (VS), le dosage de la 25OHD totale.
Évaluation des fractures vertébrales
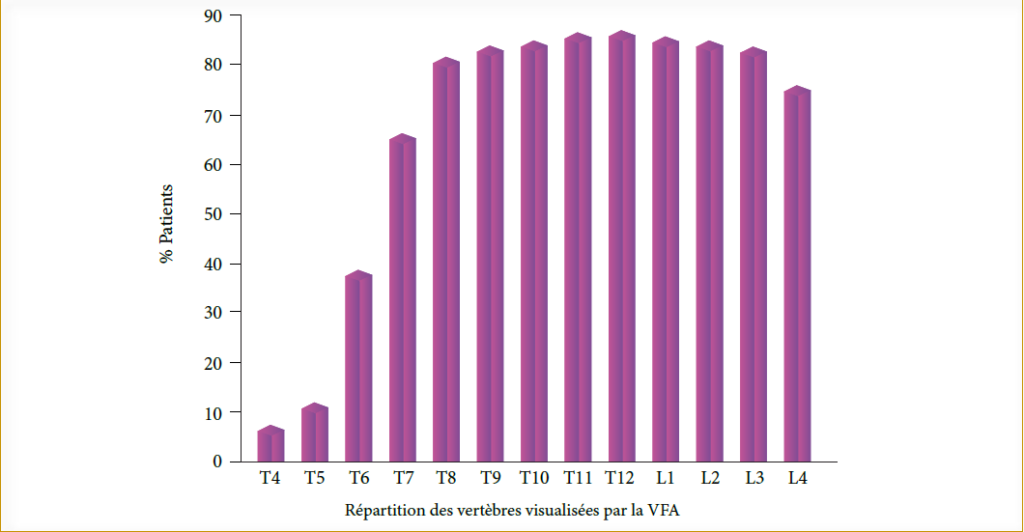
L’analyse de la morphologie vertébrale de T4 à L4 a été réalisée avec la VFA sur des images de profil obtenues avec l’appareil d’absorptiométrie biphotonique en positionnant le patient en décubitus latéral (Hologic Discovery).
Une analyse qualitative et semi quantitative a été réalisée selon la classification de Genant (8).
Selon cette méthode, les fractures sont classées en trois types en fonction des déformations (cunéiforme, biconcave ou en galette), et en trois degrés selon l’importance de la réduction d’une hauteur (antérieure, moyenne, postérieure) de la vertèbre considérée par rapport à sa hauteur postérieure ou à la hauteur postérieure d’une vertèbre adjacente en cas de galette. Le degré 1 correspond à une réduction de hauteur de 20 à 25 %, le degré 2 de 25 à 40 %, et le degré 3 de plus de 40 %.
Mesure de la Densitométrie osseuse : BMD
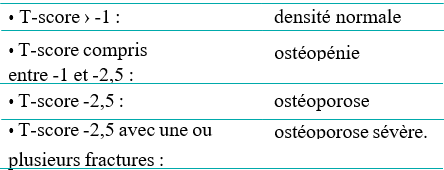
La mesure se fait au niveau de la colonne lombaire de L1-L4 en antéro-postérieur et au niveau fémoral par un technicien formé au niveau de l’unité d’ostéodensitométrie osseuse. La DMO a été réalisée avec un appareil Hologic, QDR 2000. La définition de l’ostéoporose est basée sur la classification de l’organisation mondiale de la santé en normal quand le T-score > -1, ostéopénie si T-score est compris entre -1 et -2,5 et ostéoporose si T-score ≤ -2,5.
Analyses statistiques
Les analyses statistiques ont été réalisées par le logiciel SPSS (Statistical Package for Social Sciences)
L’Analyse descriptive
- Estimation de la moyenne, de l’écart type, de la médiane (valeur minimale et maximale), pour les variables quantitatives
- Estimation des pourcentages pour les variables qualitatives
- Comparaison des fréquences a été faite avec le test de chicarré L’Analyse des facteurs de risques potentiels
- L’association entre les FV et les facteurs de risques potentiels a été obtenue par le calcul des Odds-ratios
- Un seuil de significativité de p=0,05 a été défini pour chaque test.
Résultats
Caractéristiques des patients
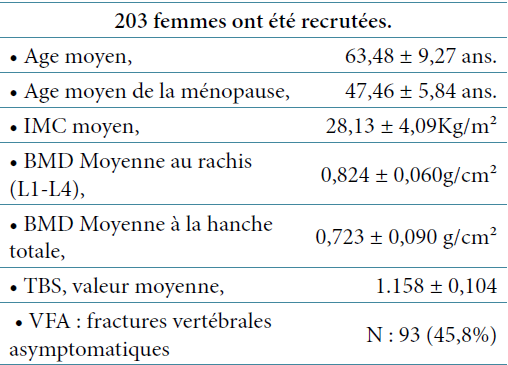
Cent trente deux patients (108 hommes et 24 femmes) ont été inclus dans l’étude. L’âge moyen des patients est de 41,7± 9,6 ans, la durée moyenne de la maladie est de 9,7± 4,2. Le BASDAI moyen est de 47,3 ± 20,4. La CRP moyenne est de 31,5 ± 40,6. Les caractéristiques démographiques et cliniques de la population d’étude sont présentées dans le tableau 1.
| Caractéristiques | Moyenne | Intervalle | ||
| Age, moyenne (SD), ans | 41,7 (9,6) | 20 | 62 | |
| Taille, moyenne (SD), cm | 153 (4,5) | 141 | 163 | |
| Poids, moyenne (SD), Kg | 66,8 (10,7) | 45 | 95 | |
| BMI, moyenne (SD), Kg/m2 | 24,1 (3,8) | 13 | 29,2 | |
| Durée de la maladie, moyenne (SD), ans | 10,3(6,4) | 3 | 25 | |
| CRP, moyenne (SD), mg | 12,8(12,5) | 3 | 65 | |
| VS, moyenne (SD) | 29,5(11,2) | 8 | 63 | |
| BASDAI | 47,3(20,4) | 2,4 | 90 | |
| BASRI Spine | 3,1 ± 2,8 | 0 | 12 | |
| BASRI Hip | 1,6 ± 1,5 | 0 | 4 | |
| BASFI | 51,5 ± 19,5 | 0 | 93 | |
| 25 OHD Totale | 20,4 ± 6,2 | 11 | 31 | |
| T-score rachis lombaire, moyenne(SD) | -1,68(1,2) | – 4,00 | 1,40 | |
| T-score col fémoral, moyenne (SD) | -1,15(0,8) | -3,60 | 1,10 | |
| OP, touts sites, n (%) | 27 (21%) | |||
| FV, n (%) | 17 (12,87) |
Prévalence des fractures vertébrales
Dix sept (17) FV soit 13 % des 132 patients atteints de SA ont été identifiées. Douze (12) patients avaient au moins une fracture vertébrale et cinq (5) patients avaient au moins deux ou plusieurs FV identifiées par la VFA. Les caractéristiques de la population d’étude selon la présence ou l’absence de la fracture vertébrale sont décrites dans le tableau 2. Les patients présentant une FV sont dans la grande majorité des cas, des hommes avec un âge moyen de 42,2 (4,8), et ont une maladie plus active (61,6 ± 10,7) par rapport aux patients sans FV. L’ostéoporose est plus importante chez les patients fracturés par rapport aux patients non fracturés.
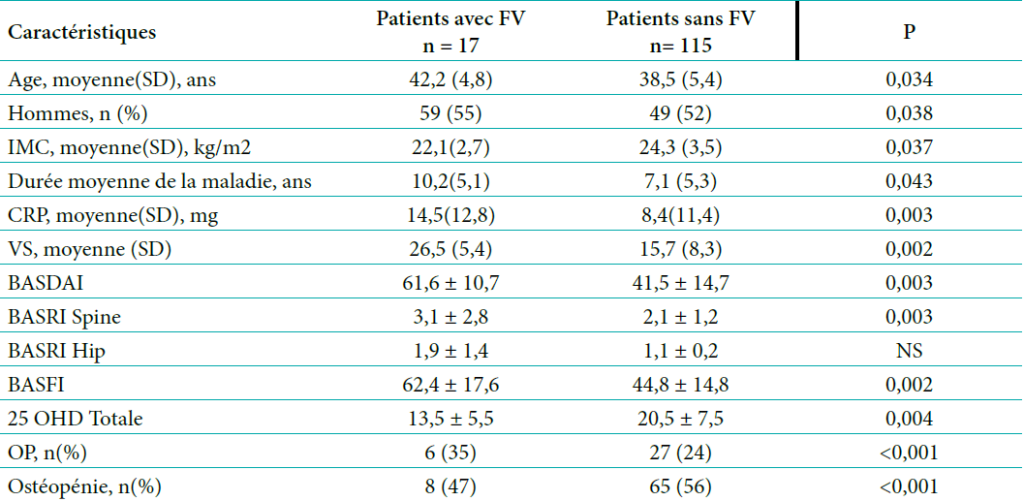
Facteurs de risque des fractures vertébrales
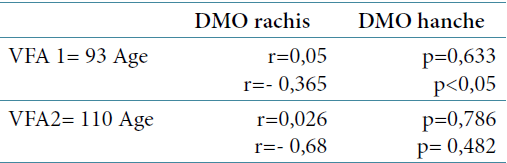
L’analyse de régression multi variée a montré que la présence de la fracture vertébrale était indépendamment associée à la durée longue de la maladie, à l’activité élevée de la maladie, à la BMD basse au rachis lombaire et au statut vitaminique D bas. Les autres paramètres tels que l’âge élevé, le bilan inflammatoire et l’indice fonctionnel de fatigue ne ressortent pas de façon indépendante (Tableau 3).
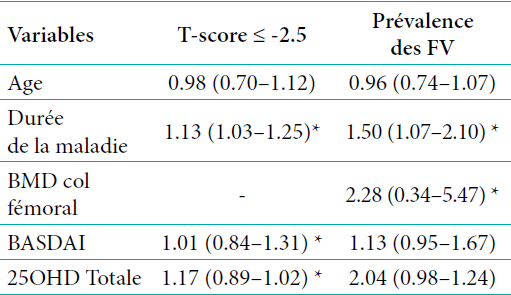
Tableau 3 : Analyse multi variée des facteurs de risque associés aux fractures vertébrales
Discussion
Dans notre travail, la prévalence des fractures vertébrales de grade 2 et 3 est de 13 %. Plusieurs travaux de la littérature ont rapporté des taux de prévalence variables. Geusens et al. ont, dans une étude réalisée en Belgique, ayant concerné 390 patients âgés de 50 ans, retrouvé une prévalence de FV de l’ordre 11,8 % (8).
Ralston et al. a décrit, dans une étude faite en population de FV ayant concerné 111 patients atteints de SA, une prévalence de FV de 16 % (9).
Une autre étude réalisée à l’est de Londres par Donnelly S et al. chez 87 patients avec SA, a rapporté une prévalence de 10,3 % de FV (10).
Mitra D, dans un travail sur 66 patients avec SA, a trouvé une prévalence de FV de 17 % (12).
De même qu’un travail réalisé par Vosse et al. sur 59 patients avec SA âgés de 46 à 54 ans a trouvé une prévalence de FV de 17 % (12).
Ces différences de taux de prévalence de FV s’expliqueraient en partie aux biais de recrutement des populations (population sélectionnée d’âge variable, le nombre variable de patients recrutés, de même que le sex-ratio ainsi que l’activité de la maladie, différents d’une étude à une autre).
l’activité de la maladie, différents d’une étude à une autre). L’étude qui, à notre avis, a déterminé une prévalence de FV la plus exacte semble être celle de Cooper et al. (13), qui, dans une cohorte initiale de 158 patients réalisée dans l’état de Minnesota (USA), a rapporté une augmentation du risque de FV cliniques avec un Odds Ratio de 7,7 (intervalle de confiance de 95 %, 4,3-12,6) ; ainsi qu’une incidence cumulée de FV cliniques plus élevée chez les hommes (OR 10,7 contre 4,2 femmes) ; qui augmente les 5 premières années, culminant à 17 % entre la 20ème et la 30ème année après le diagnostic initial. Le tableau N°4 résume les principaux travaux.
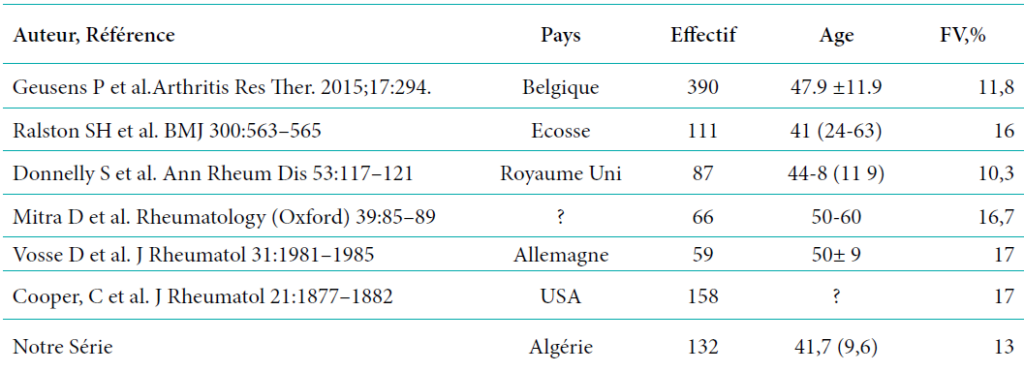
Dans notre étude, l’ostéoporose est retrouvée dans 21 % de l’échantillon dans les sites selon les critères de l’OMS. Cette relative faible prévalence contraste avec les différentes données de la littérature. En effet, dans une revue de la littérature réalisée par Van Der Weijden (14), la prévalence de l’OP est comprise entre 13 et 16 %.
Dans une autre revue récente de la littérature, incluant plus de 55 études, la prévalence de l’OP est comprise entre 3 et 47% (15). La différence dans la prévalence de l’OP observée dans ces études est peut être liée aux caractéristiques différentes des populations étudiées ainsi que les critères utilisés dans la définition de la SA (critères ASAS ou bien New York modifiés). La prévalence élevée des syndesmophytes chez les patients a contribué à la fausse interprétation de la BMD au niveau lombaire. La BMD au niveau du col fémoral serait dans ce cas le meilleur reflet du statut densitométrique de nos patients.
Dans notre étude, les facteurs de risque (FDR) retrouvés sont l’âge élevé, l’IMC bas, la durée élevée de la maladie, le bilan inflammatoire élevé, l’activité élevée de la mala- die ainsi qu’un statut vitaminique D bas. Les facteurs de risques qui ressortent de manière indépendante en ana- lyse multi variée sont l’âge, la durée de la maladie, l’acti- vité de la maladie, le statut vitaminique D bas. Dans un travail réalisé par B. Mermerci sur 100 patients avec SA, il n’a pas été observé de corrélation positive entre un statut vitaminique D bas et un statut densitométrique bas (16).
Nous n’avons pas trouvé de corrélation significative entre la BMD basse au rachis lombaire et les paramètres élevés de l’inflammation (VS et CRP) contrairement à d’autres études (17-20). Par contre la corrélation a été retrouvée au niveau du col fémoral comme suggéré dans pas mal d’études (21).
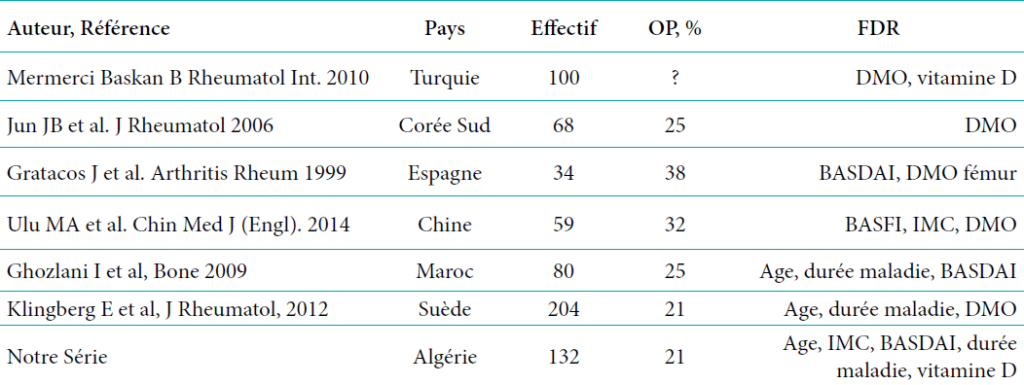
Nos résultats se rapprochent des travaux réalisés en Corée du Sud, en Suède et au Maroc ; et ce, en raison d’une méthodologie de travail presque identique malgré une certaine disparité des effectifs étudiés.
En conclusion, l’ostéoporose est une comorbidité retrouvée dans la SA, elle est souvent sous-diagnostiquée donc non traitée. L’âge avancé, le fardeau de la maladie de par son activité et l’immobilisation engendrée, la formation de syndesmophytes et les paramètres de l’inflammation élevés contribuent au risque élevé d’ostéoporose.
Ces résultats suggèrent un dépistage précoce de cette comorbidité afin d’initier une prise en charge effective. Néanmoins des études longitudinales avec des effectifs conséquents sont nécessaires pour confirmer ces résultats.
Références :
- Sinigaglia, L., Varenna, M., Girasole, G. and Bianchi, G. (2006) Epidemiology of osteoporosis in rheumatic diseases. Rheum Dis Clin North Am 32: 631–658.
- Vosse, D., Van Der Heijde, D., Landewe, R., Geusens,P., Mielants, H., Dougados, M. et al. (2006) Determinants of hyperkyphosis in pa- tients with ankylosing spondylitis. Ann Rheum Dis 65: 770–774
- Lange, U., Kluge, A., Strunk, J., Teichmann, J. and Bachmann, G. (2005) Ankylosing spondylitis and bone mineral density-what is the ideal tool for measurement? Rheumatol Int 26: 115–120.
- Visvanathan, S., van der Heijde, D., Deodhar, A., Wagner, C., Baker, D.G., Han, J. et al. (2009) Effects of infliximab on markers of inflam- mation and bone turnover and associations with bone mineral density in patients with ankylosing spondylitis. Ann Rheum Dis 68: 175–182.
- Wasnich RD, Ross PD, Davis JW, Vogel JM (1989) A comparison of single and multi-site BMC measurements for assessment of spine fracture probability. J Nucl Med 30:1166–1171
- Lentle BC et al. Recognizing and reporting vertebral fractures: reducing the risk of future osteoporotic fractures. Can Assoc Radiol J 2007;58:27-36
- Johansson C et al. Reproductive factors as predictors of bone den- sity and fractures in women at the age of 70. Maturitas 1993; 17:39-50
- Geusens P, Vosse D, van der Linden S (2007) Osteoporosis and vertebral fractures in ankylosing spondylitis. Curr Opin Rheumatol .19:335–339
- Ralston SH, Urquhart GD, Brzeski M, Sturrock RD (1990) Preva- lence of vertebral compression fractures due to osteoporosis in anky- losing spondylitis. BMJ 300:563–565
- Donnelly S, Doyle DV, Denton A, Rolfe I, McCloskey EV, Spector TD (1994) Bone mineral density and vertebral compression fracture rates in ankylosing spondylitis. Ann Rheum Dis 53:117–121
- Mitra D, Elvins DM, Speden DJ, Collins AJ (2000) The prevalence of vertebral fractures in mild ankylosing spondylitis and their rela- tionship to bone mineral density. Rheumatology (Oxford) 39:85–89
- Vosse D, Feldtkeller E, Erlendsson J, Geusens P, van der Linden S (2004) Clinical vertebral fractures in patients with ankylosing spon- dylitis. J Rheumatol 31:1981–1985
- Cooper, C., Carbone, L., Michet, C.J., Atkinson, E.J., O’Fallon, W.M. and Melton, L.J., 3rd. (1994) Fracture risk in patients with ankylosing spondylitis: a population based study. J Rheumatol 21:1877–1882.
- Van Der Weijden MA, Claushuis TA, Nazari T, Lems WF, Dijk- mans BA, van der Horst-Bruinsma IE. High prevalence of low bone mineral density in patients within 10 years of onset of ankylosing spondylitis: a systematic review. Clin Rheumatol. 2012;31:1529–35.
- Kilic E, Ozgocmen S. Bone mass in axial spondyloarthritis: a lite- rature review. World J Orthop. 2015;6:298–310
- Mermerci Baskan B et al, The relation between osteoporosis and vitamin D levels and disease activity in ankylosing spondylitis. Rheu- matol Int. 2010 Jan;30(3):375-81
- Jun JB, Joo KB, Her MY, Kim TH, Bae SC, Yoo DH, Kim SK: Fe- moral bone mineral density is associated with vertebral fractures in patients with ankylosing spondylitis: a cross-sectional study. J Rheu- matol 2006, 33:1637-1641
- Gratacos J, Collado A, Pons F, Osaba M, Sanmarti R, Roque M, Larrosa M, Munoz-Gomez J: Significant loss of bone mass in patients with early, active ankylosing spondylitis: a followup study. Arthritis Rheum 1999, 42:2319-2324
- Ulu MA et al, Prevalence of osteoporosis and vertebral fractures and related factors in patients with ankylosing spondylitis. Chin Med J (Engl). 2014;127(15):2740-7
- Ghozlani I et al, Prevalence and risk factors of osteoporosis and vertebral fractures in patients with ankylosing spondylitis. Bone. 2009 May;44(5):772-6
- Klingberg E et al, Vertebral fractures in ankylosing spondylitis are associated with lower bone mineral density in both central and peri- pheral skeleton. J Rheumatol. 2012 Oct;39(10):1987-95