S. BERKANE, Service de Gastro-entérologie, CHU Mustapha Bacha, Alger
Abstract : Hepatitis B virus (HBV) is a global health problem and a major cause of liver cirrhosis and hepatocellular carcinoma. HBV infection can be efficiently prevented by vaccination and many treatments are available, however, optimal timing as well as modalities and duration of treatment remain a real challenge. So far, there is no reliable cure for patients chronically infected by HBV. Currently approved drugs, pegylated interferon and nucleos(t)ide analogues, can only achieve viral suppression as clearance of HBsAg is rare and lifelong therapy is needed in most cases. Hepatitis B surface antigen (HBsAg) level quantification with HBV DNA measurement could help predict the likelihood of response to treatment, particularly for pegylated interferon. New treatments targeting sustained clearance of HBV DNA and HBsAg are expected.
Key-words : Hepatitis B, Guidelines, antiviral therapy, peginterferon alfa-2a, entecavir, tenofovir, resistance.
Résumé : L’infection chronique par le virus de l’hépatite B (VHB) pose un problème de santé publique à l’échelle planétaire, et est à l’origine de la majorité des cirrhoses du foie et du carcinome hépatocellulaire. La vaccination est efficace, des traitements sont disponibles, cependant, le véritable défi reste : qui traiter et quand, les modalités ainsi que la durée du traitement. À ce jour, il n’y a pas de guérison définitive de l’hépatite B. Les traitements actuellement approuvés sont l’interféron pégylé et les analogues nucléos(t) idiques permettant la suppression virale, la clairance de l’AgHBs restant rare. Un traitement à vie par les analogues est nécessaire dans la majorité des cas. La quantification de l’AgHbs combiné au DNA du VHB peut prédire la probabilité de réponse au traitement, en particulier pour l’interféron pégylé. De nouveaux traitements plus efficaces sont attendus.
Mots-clés : Hépatite B, recommandations, traitement antiviral, interféron pégylé alfa-2a, tenofvir, résistance.
Introduction :
infection chronique par le virus de l’hépatite B pose un problème de santé publique, elle concerne près de 350 millions de personnes dans le monde [1].
C’est la principale cause de mortalité par cirrhose et par carcinome hépatocellulaire (CHC), à l’origine de près de 600.000 décès par an [1,2].
30 à 40% de porteurs chroniques du VHB développeront une altération hépatique progressive évoluant vers la cirrhose et le carcinome hépatocellulaire.
Le traitement antiviral repose actuellement sur les analogues nucléos(t)idiques (AN) et l’interféron pégylé (INF-PEG).
Le problème est d’identifier les patients à risque de développer ces complications et les traiter à temps.
Les facteurs viraux influençant l’évolution de l’hépatopathie sont le statut AgHbe, le DNA VHB sérique, le génotype et les variants VHB[3,4].
Qui traiter ?
Tout patient porteur chronique d’une infection virale B ne nécessite pas obligatoirement un traitement. Celui-ci est indiqué en cas d’hépatopathie active avec une réplication virale et des lésions hépatiques.
Le candidat au traitement est défini selon le taux du DNA VHB et des ALT sériques[5-13].
Tous les patients AgHbe positif ou négatif, avec un DNA du VHB >2000UI/mL et des ALT élevées, doivent être traités après confirmation d’une fibrose ou d’une inflammation hépatique modérée à sévère. En l’absence de fibrose évidente, un suivi par le dosage du DNA VHB et des ALT tous les 3 à 6 mois est indiqué, puis tous les 6-12 mois les années suivantes[5,8].
Les patients en phase de tolérance immunitaire et les porteurs inactifs ne doivent pas être traités[5,7,14-19]. Cependant, une fibrose significative peut se voir avec des ALAT normales persistantes, si la charge virale reste élevée[20,21].
L’indication thérapeutique repose également sur d’autres facteurs tels que l’âge, les antécédents familiaux de cirrhose et de CHC, les comorbidités, les coinfections, la génétique, le désir du patient, l’efficacité du traitement et ses effets secondaires. Le profil de résistance du VHB, le coût et la disponibilité des traitements interviennent aussi dans la décision thérapeutique[22].
Objectifs du traitement :
La perte de l’AgHbs est l’objectif majeur du traitement. Comme cet objectif est rarement atteint, voire jamais, avec un traitement de durée définie, la perte de l’AgHbs ne constitue plus l’objectif primordial mais le facteur prédictif de bon pronostic de l’infection VHB à long terme [23].
Les traitements actuels ne peuvent pas éradiquer l’infection virale B mais seulement entrainer, par une virosuppression, un état de porteur inactif persistant, pouvant aboutir ensuite à la perte de l’AgHbs[24].
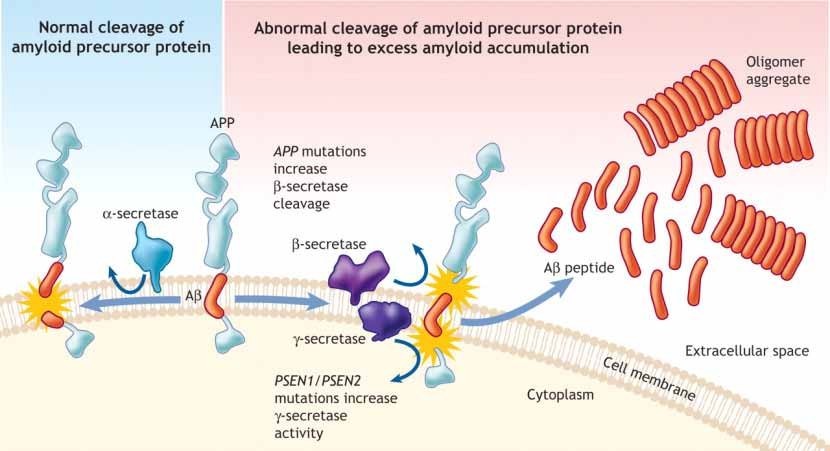
L’absence d’éradication virale est liée à la persistance, au niveau du foie, du cccDNAviral résiduel[25].
La perte de l’AgHbs n’est cependant pas synonyme d’une régression des lésions histologiques hépatiques ou de la prévention du CHC.
Choix du traitement :
Deux approches thérapeutiques sont disponibles pour les patients AgHBe positif et négatif :
Un traitement de durée définie par l’INF et un traitement suppressif au long cours par les AN.
L’objectif de la première stratégie est une suppression soutenue de la réplication virale à la fin du traitement par l’induction de l’état de porteur inactif du VHB (des ALAT normales, un ADN du VHB inférieur à 2000 UI/mL), et, en particulier pour les patients AgHBe positif, une séroconversion anti-HBe. C’est la stratégie de l’INF-PEG pendant 48 semaines, avec une seule dose 180µg/s en sous cutanée, indépendamment du statut AgHbe, positif ou négatif[5,6].
L’avantage de l’INF-PEG alpha est l’absence de développement d’une résistance du VHB et un taux élevé de séroconversion HBe et HBs. Cependant, il requiert une injection sous-cutanée, il est associé à des effets secondaires (fatigue, syndrome pseudo grippal, anémie, pancytopénie, et dépression) et il est contre-indiqué en cas de cirrhose avancée.
Les facteurs de bonne réponse au traitement par l’INF-PEG sont : une faible charge virale et des ALT élevées>2xLSN[5,6] ; les génotypes A et B[26,27] ; l’absence de cirrhose et de mutants VHB C ou pré-C et un polymorphisme IL28B CC[7]. D’autres facteurs peuvent influencer le choix thérapeutique en faveur de l’interferon, notamment le sujet jeune, une jeune femme projetant une grossesse dans un futur proche, l’absence de comorbidités, les préférences du patient en cas de coinfection VHC.
Chez les patients AgHBe négatif, le jeune âge, le sexe féminin, un taux sérique élevé des ALAT et un faible taux sérique de DNA VHB ont été associés à une meilleure réponse virologique soutenue[28].
L’autre option thérapeutique est de débuter par un AN qui a l’avantage d’être bien toléré, per os, avec peu ou pas de contre-indications, sans risque en cas de cirrhose décompensée et chez les patients transplantés. Les inconvénients sont le risque de résistance virale, le modeste taux de séroconversion Hbe et la séroconversion Hbs qui reste rare.
Les analogues oraux sont représentés par des médicaments de première génération, la lamivudine et l’adéfovir, tandis que l’entécavir (ETV), la telbivudine et le ténofovir (TDF) constituent les analogues de la nouvelle génération. Le traitement par les AN est de durée indéfinie, voire à vie [22,29-31].
Traitement par IFN-PEG alpha :
Dans un essai de 814 patients AgHBe positif, ayant reçu l’INF-PEG seul, la lamivudine seule ou la combinaison des deux durant 48 semaines, avec un suivi de 24 semaines post-traitement, la séroconversion Hbe était significativement plus élevée sous INF-PEG seul, comparativement à la lamivudine (32% vs 19% ; P <0,001) et au traitement combiné (27% v 19%, p=0,02)[32].
Concernant la durée du traitement, l’essai randomisé NEPTUNE a montré, chez 544 patients AgHBe positif, une réponse élevée associée à l’INF-PEG, à la dose de 180 µg une fois par semaine pendant 48 semaines, comparativement à 180 µg ou 90 µg durant 24 semaines (25,8% et 14,1%, respectivement)[33].
Dans un autre essai contrôlé et randomisé, 128 patients AgHBe négatif, dont 94% de génotype D, ont été traités pendant 48 semaines par INF-PEG (180µg/semaine ; n=51),96 semaines par INF-PEG (48 semaines à 180 µg/semaine, puis 48 semaines à 135µg/semaine ; n=52), 48 semaines par INF-PEG (180µg/semaine) et lamivudine (100 mg/jour) ou 48 semaines par interféron pégylé seul (135µg/semaine) (n=25). À 1 an post-traitement, le taux de réponse virologique (DNA < 2000 UI/ml) était significativement plus marqué chez les patients traités 96 semaines par l’INF-PEG seul par rapport à ceux traités pendant 48 semaines (28,8% v 11,8% ; P = 0,03)[34].
L’addition de lamivudine au cours des 48 premières semaines de traitement n’a pas apporté de bénéfice supplémentaire par rapport à l’INF seul.
L’INF peut, par le biais de son mode d’action immunologique, induire un contrôle soutenu du VHB post-traitement entraînant une perte de l’AgHbs chez 20 à 30% des patients traités[29,30,35-38]. Une sélection appropriée des patients peut augmenter ce pourcentage jusqu’à 40%[39].
Chez le sujet AgHBe négatif, l’INF-PEG a-2a à 180µg par semaine durant 48 semaines entraîne une normalisation des ALAT post-traitement dans 59% des cas, une réduction du DNA VHB < 2000UI/mL dans 43%, et la perte de l’AgHbs chez 3% des patients[40]. Dans une étude de 230 patients suivis à long terme, une réponse
virologique soutenue (ADN du VHB <2000UI/mL) a été observée chez 21% des patients à 5 ans post-traitement, et la clairance de l’AgHBs était de 5% à 1an et 12% à 5 ans après le traitement [41].
Si la combinaison Lamivudine-IFN-PEG permet une meilleure suppression du DNA du VHB, il n’y a cependant pas de différence en termes de réponse soutenue[42].
Traitement par les analogues :
Parmi les AN disponibles pour le traitement du VHB, notamment la lamivudine, l’adéfovir, la telbivudine, l’entécavir et le ténofovir, seuls l’ETV et le TDF sont recommandés en première ligne chez les patients naïfs par les guidelines internationaux. Ces deux médicaments sont généralement bien tolérés, avec peu d’effets indésirables. Chez les sujets AgHbe négatif traités 48 semaines par l’ETV ou le TDF, la perte du DNA du VHB sérique (< 60 à 80UI/mL) a été notée dans 90 et 93% des cas respectivement[43,44].
Ces deux analogues entraînent une rémission virologique biochimique avec une amélioration de l’activité nécrotico-inflammatoire et de la fibrose hépatique, voire une réversion de la cirrhose[45,46].
Le traitement par ces AN, puissants antiviraux à forte barrière génétique à la résistance, a permis d’obtenir, à long terme (5-6 ans), une régression significative de la fibrose et de la cirrhose, avec une amélioration histologique continue[45,46]. La perte de l’AgHBs à 12 mois de traitement était cependant négligeable[43,44,47-49].
Lequel choisir en première ligne, ETV ou TDF ? En réalité, il n’ya pas de différence significative chez les sujets AgHbe positif ou négatif sur la séroconversion et la perte de l’AgHbs[50].
Entecavir :
Dans un essai contrôlé randomisé de 715 patients AgHBe positif, l’ETV augmentait la proportion de patients avec un ADN du VHB indétectable (67% vs 36% ; P <0,001) et entraînait une normalisation des ALAT (68% vs 60% ; P = 0,02) [51].
Les effets indésirables comprenaient la diarrhée, la fatigue, les douleurs abdominales et la toux.
Dans un autre essai contrôlé de 648 patients AgHBe négatif, randomisés sous ETV ou lamivudine, l’ETV a considérablement augmenté la proportion de patients avec un taux de DNA du VHB indétectable (90% vs 72% ; P <0,001) et induit une normalisation des ALAT (78% vs 71% ; P = 0,045)[43].
Les effets secondaires étaient similaires entre les deux groupes (fatigue, céphalées, nausées). Ces résultats ont été confirmés dans un essai contrôlé randomisé, comparant la lamivudine et l’ETV chez 709 patients AgHBe positif sur 96 semaines, montrant une supériorité de l’ETV dans la réduction du DNA du VHB (80% vs 39% ; P <0,001) et dans la normalisation des ALAT (87% vs 79% ; P = 0,005), bien que le taux cumulatif de séroconversion AgHbe soit similaire entre les deux groupes[52].
Concernant les patients AgHBe négatif, un essai contrôlé randomisé de 648 patients a montré que l’ETV augmentait de manière significative la proportion de patients avec un DNA du VHB indétectable par rapport à la lamivudine (90% vs 72% ; P <0,001) et la normalisation des ALAT (78% vs 71% ; P = 0,045)[53].
Après un suivi de 5 ans, un seul cas de résistance était détecté, une séroconversion HBe était obtenue chez 23% des patients et une perte de l’AgHbs dans 1,4% des cas[53].
L’incidence cumulative à 3 ans de la résistance à l’ETV est de 1,2% chez le patient naïf AgHBe positif[54].
Une étude rétrospective a identifié 5 cas d’acidose lactique chez 16 patients en cirrhose avancée, traités par ETV, présentant tous un MELD égal ou supérieur à 22. Dans deux études ultérieures de patients avec cirrhose décompensée, aucun cas d’acidose lactique n’était rapporté[55,56].
Ténofovir :
Les essais randomisés contrôlés, comparant le ténofovir disoproxil fumarate (TDF) à l’adéfovir chez 846 patients AgHBe positif et 603 patients AgHBe négatif, ont montré que le TDF augmentait de manière significative la normalisation des ALAT (68% vs 54% ; P = 0,03) et la perte de l’AgHBs (3% vs 0% ; P=0,02) sans preuve de résistance au TDF[44].
Après un suivi de 8 ans, aucune mutation de résistance n’a été détectée chez les patients AgHBe positif ou négatif [57].
Un essai randomisé de 379 patients naïfs, comparant l’ETV en monothérapie à la combinaison ETV-TDF chez les patients naïfs AgHbe positif et négatif, montrait que l’entécavir était aussi efficace que le traitement combiné [58].
D’autres études ont montré que le TDF en monothérapie avait une efficacité comparable au TDF combiné à l’emtricitabine (Truvada), à la fois chez le naïf et chez les patients préalablement traités par la lamivudine[59,60]. Dans la vraie vie, le TDF et l’ETV représentent le traitement de choix, non seulement pour la grande majorité des patients AgHBe négatif, mais aussi pour les sujets AgHbe positif non actifs ou inéligibles à l’INF-PEG et les patients au stade de cirrhose, indépendamment de leur statut AgHBe[6,7,61].
L’AASLD, L’APASL et l’EASL recommandent à long terme les analogues pour les patients AgHBe négatif[5,7]. Dans un essai prospectif, randomisé et contrôlé, la perte de l’AgHbs à 72 semaines de traitement était meilleure sous traitement combinant TDF et INF-PEG alfa-2a, durant 48s (groupe A), que dans les groupes traités par TDF + INF-PEG durant 16s, suivi de TDF durant 32s (groupe B), par TDF seul durant 120s (groupe C), ou par INF-PEG seul durant 12 mois (groupe D). Elle était de 9,1%, 2,8%, 0% et 2,8% dans les groupes A, B, C et D respectivement. Il y avait une différence significative entre le groupe A et les groupes C et D. Elle n’était pas significative entre le groupe B et les groupes C et D. Dans le groupe A, la perte de l’AgHbs survenait aussi bien chez les patients AgHbe positif que chez les patients AgHbe négatif. L’incidence des effets secondaires et le taux d’arrêt du traitement pour effets secondaires étaient similaires dans tous les groupes[62].
Une étude rétrospective de patients AgHBe positif et négatif, cirrhotiques ou non, avec biopsie hépatique avant et après 5 ans de traitement par le TDF (N=348), a montré qu’il y avait une réponse virologique, sérologique et histologique indépendamment de l’existence de cirrhose à l’état basal[63].
Un traitement de durée définie est réservé aux sujets AgHbe positif, avec un taux de séroconversion Hbe faible[22,29,30]. À long terme, le TDF est devenu le traitement de choix de la cirrhose, indépendamment du statut AgHBe[6,7].
Le problème des analogues au long cours chez les sujets AgHBe négatif est le faible taux de perte de l’AgHbs, limité à seulement 1-2% par année [64].
Traitement combiné :
Le traitement combiné n’a pas montré plus d’efficacité sur la suppression virale, ni un taux plus élevé de réponse virologique à long terme par rapport à la monothérapie, il ne peut, dans ce cas, être recommandé en première ligne [65].
Le traitement combiné de 2 analogues a été évalué dans une étude de superiorité portant sur 379 patients AgHBe positif ou négatif, après 96 semaines de traitement. Le groupe sous ETV seul avait un taux de DNA du VHB < 50 UI/mL similaire à celui sous traitement combiné ETV-TDF (83% vs 76%)[58].
Aucune différence dans l’efficacité entre le traitement combiné INF-PEG-Analogues et INF-PEG ou analogues seuls n’a été démontrée [66].
En raison du faible taux de perte de l’AgHbs sous analogues et le faible taux de réponse soutenue suite à leur arrêt après une durée définie, la tendance a été de rajouter l’INF-PEG alpha 2a, pour une durée variable, au traitement par analogues[67-69].
Chez les patients en immunotolérance, le traitement combiné TDF-emtricitabine permet une meilleure suppression virale par rapport auTDF seul. Dans une étude de 126 patients AgHBe positif avec un taux de DNA du VHB > 1,7x 107 UI/mL et un taux normal des ALAT, 55% des patients ayant reçu le TDF en monothérapie et 76% des patients ayant reçu TDF+emtricitabine ont eu un DNA VHB <69 UI/mL après 192 semaines de traitement [13]. Cependant, la séroconversion HBe a été obtenue chez seulement 3 patients (5%), tous sous TDF seul. La combinaison lamivudine-INF-PEG alfa n’a pas eu un impact virologique ou sérologique sur la réponse au traitement par rapport à l’INF-PEG seul[32].
L’ajout de la telbivudine à l’INF-PEG alfa est à éviter, en raison du risque accru de polyneuropathies sévères[70].
Résistance antivirale :
Les études cliniques à long terme avec ETV en monothérapie ont montré un risque de résistance très faible, de 1,2 % après 6 ans de traitement [71].
Aucun cas de résistance n’a été décrit à 6 ans chez 585 patients ni à 8 ans chez 412 patients sous TDF [44].
Une élévation du taux du DNA du VHB sous traitement d’au moins 1 log10 UI/ml par rapport au nadir à la réponse initiale chez un patient adhérant, suggère le développement de la résistance.
La résistance à l’un des analogues confère une résistance aux autres analogues. Les patients résistants à la lamivudine présentent un risque de résistance sous ETV de près de 51% à 5 mois ans de traitement[72].
En cas de résistance à la lamivudine, la telbivudine ou le TDF seul est suffisant ; ils n’ont pas de résistance croisée[60].
Le TDF ou l’ETV peuvent être suffisants en cas de résistance à l’adéfovir[73,74].
Malgré le risque rare de survenue de résistance à l’ETV, le traitement de substitution est le TDF en monothérapie, son efficacité est identique au traitement combiné TDF-ETV, avec 71% et 73% des patients obtenant un taux d’ADN du VHB indétectable à 48 semaines[75].
Initiation du traitement :
– En présence d’une cirrhose :
Idéalement, tous les patients atteints de cirrhose avec une charge virale détectable sont à traiter, quel que soit le taux des ALAT. On prescrit l’ETV (0,5 mg), ou le TDF (300 mg) ou l’INF-PEG avec prudence (Child- Pugh A).
La durée du traitement doit être prolongée, en raison du risque de rebond virologique après arrêt du traitement[5,7]. En cas de cirrhose décompensée, le traitement devrait être initié rapidement par un analogue, sans tenir compte des ALAT ou du DNA du VHB. Les analogues sont parfois insuffisants, justifiant l’évaluation simultanée de ces patients pour une transplantation hépatique. On prescrit l’ETV (1 mg/j) ou le TDF (300mg). L’INF- PEG est contre-indiqué. Le traitement à long terme est recommandé[5,7].
– Hépatite Chronique Active AgHBe(+) :
Tout patient présentant un DNA VHB >20000UI/mL et des ALAT > LSN (limite supérieure de la normale) persistantes doit être traité. En l’absence de signe d’hépatopathie avancée, il est licite d’attendre 3 à 6 mois une séroconversion AgHbe spontanée [5,8].
– Hépatite Chronique Active AgHBe(-):
Les patients avec un DNA du VHB supérieur à 2000UI/ mL et des ALAT supérieures à 2 fois la normale doivent être traités, la ponction biopsie hépatique (PBF) reste facultative. Un taux d’ALAT > LSN et/ou un DNA VHB entre 2000 et 20000UI/ml ou un Fibroscan> 6Kpa[76] justifient une biopsie hépatique et un traitement si nécessaire[6,8,76].
Quantification de l’AgHbs :
Elle reflète la concentration intra-hépatique du DNA du VHB et la productivité virale. Il existe une corrélation positive entre la concentration de l’AgHBs et la charge virale B, indépendamment de l’expression de l’antigène HBe[77]. Deux tests sont disponibles pour la quantification de l’AgHbs : le test architecte AgHbs (Abbott Diagnostics)[78] et le dosage quantitatif Elecsys HBsAg II (Roche Diagnostics)[79].
La quantification permet de distinguer les porteurs chroniques AgHbe négatif des patients en activité, les porteurs inactifs ayant des niveaux inférieurs à 1000 UI/ml [80]. Elle pourrait également prédire la réactivation chez les patients AgHBe négatifs asymptomatiques [81,82]. Un taux d’AgHbs>à 1000UI/ml et un DNA VHB> 2000 UI/ml prédisent la réactivation de la maladie, définie par un taux de DNA VHB >2000 UI/mL et une augmentation des taux d’ALAT avec une sensibilité de 92%, une spécificité de 51%, une valeur prédictive négative de 96% et une valeur prédictive positive de 30%[81].
La quantification de l’AgHbs et du DNA VHB est importante pour la décision et le suivi thérapeutique.
Évaluation des traitements :
– Évaluation de la réponse à l’interféron pégylé : La durée du traitement par l’INF-PEG alpha 2a est de 12 mois et la posologie est de 180µg une fois par semaine, quel que soit le statut AgHbe. L’évaluation de la réponse au traitement repose sur le taux de DNA du VHB et la quantification de l’AgHbs avant traitement, puis 3 et 6 mois après traitement[22,30].
Pour les patients AgHbe(+), la réponse à l’INF-PEG est définie par la perte de l’AgHbe, la séroconversion Ac anti-Hbe + et un DNA VHB < 2 000UI/mL, 6 mois après arrêt du traitement.
Pour les patients AgHBe (-) : la réponse au traitement correspond à la suppression soutenue du DNA VHB< 2 000UI/mL et la normalisation des ALAT, 12 mois après arrêt du traitement[5,6,83].
Chez le patient AgHbe(+), l’absence de réduction du taux d’AgHbs à S12 de traitement est un bon facteur prédictif de non réponse. Dans une analyse de 803 patients, le taux de réponse était bas, en l’absence de réduction à S12 de l’AgHbs, pour les génotypes A ou D (VPN de 97–100%), et si à S12, l’AgHbs était>20,000 UI/mL pour les génotypes B ou C (VPN 92–98%). À S24 de traitement, pratiquement tous les patients avec un AgHbs>20,000UI/mL ne répondront pas au traitement, quel que soit le génotype (VPN pour la réponse et la perte de l’AgHbs 99% et 100%). Il est recommandé d’arrêter le traitement dans de tels cas[83,84].
Chez le sujet AgHbe(-), l’absence de réduction de l’AgHbs et une réduction <2log du DNA du VHB à S12 de traitement réduisent considérablement les chances d’obtenir une réponse virologique soutenue[85,86].
Basée sur ces facteurs d’évaluation, la non réponse à l’interféron incite à switcher vers les analogues.
Les guidelines internationaux recommandent[5,8] l’arrêt du traitement, ou le switch vers un autre traitement en l’absence de réduction du DNA VHB à S12 supérieur à 2 logs. L’APASL 2012, quant à elle, préconise la poursuite du traitement pendant 12 mois sans tenir compte de la réponse du DNA VHB[5].
– Évaluation de la réponse virologique aux analogues :
– Durée du traitement par les analogues :
AgHbe (+) : poursuite du traitement jusqu’a négativation du DNA VHB sérique et séroconversion AgHbe ; consolidation en poursuivant le traitement 12 mois après apparition des anticorps anti-Hbe.
AgHbe (-) : si l’AASLD et l’EASL recommandent les analogues indéfiniment, du moins jusqu’à la perte de l’AgHbs chez le non cirrhotique, l’APASL préconise son arrêt si le DNA VHB sérique devient indétectable durant 3 tests consécutifs à 6 mois d’intervalle[5,7].
L’évaluation doit distinguer la non adhérence, la résistance et la réponse partielle. Avec les nouveaux anti-viraux actuellement recommandés en première ligne (ETV et TDF), la résistance chez les patients naïfs est rare, la plupart des cas d’échappement étant liés à la non adhérence[87]. L’évaluation se fait par Ia mesure du taux de DNA du VHB à 12 semaines pour identifier la non réponse primaire et à 24 semaines pour évaluer la suppression virologique soutenue, puis tous les 3-6 mois lors de la première année, pour confirmer la suppression virale maintenue et détecter un échappement viral.
- Échec ou non réponse primaire au traitement
Elle se définit par une réduction <1 log10UI/mL à 3 mois de traitement ; elle est rare avec l’ETV et le TDF. L’adhérence doit être vérifiée chez tout patient sans réponse à S12 ou S24. Si elle est confirmée, il est nécessaire de réaliser les tests de résistance à S24 et de proposer une stratégie thérapeutique adaptée[6].
- Echappement viral
Il se définit par une augmentation du DNA du VHB > 1log par rapport au nadir ou un ADN du VHB>100UI/mL chez des patients indétectables sous analogues.
- Réponse virologique partielle ou inadéquate Lorsque l’ADN VHB >2000 UI/mL à 24 semaines ou positif à 48 semaines de traitement, l’adhérence doit être vérifiée.
- Virémie persistante
Elle se définit par une réduction en plateau du DNA VHB et/ou l’échec à obtenir un taux indétectable après 96 semaines de traitement. La prise en charge optimale
des patients avec un DNA VHB détectable après 48 semaines de traitement par ETV ou TDF est inconnue. En cas de réduction progressive de l’ADN du VHB sérique, on peut poursuivre le traitement, et il y a amélioration progressive des taux de réponse et un faible risque de résistance[88]. En cas de réponse partielle à 1an de traitement par ETV, si le DNA du VHB est <1000 UI/mL, une suppression virale est souvent obtenue en poursuivant, au moins pendant 2 ans, le traitement [88]. Si, par contre, le taux de DNA reste élevé (> 1000UI/ML), il est licite de switcher vers le TDF ou combiner TDF et ETV[89].
En cas de réponse partielle à l’ETV à 0,5 mg par jour, l’augmentation de la dose à 1 mg par jour ne semble pas aboutir à une suppression virale complète[87].
- Évaluation de la toxicité rénale
À l’exception de la Telbivudine, une altération de la fonction rénale a été rapportée avec tous les analogues. Il est recommandé de faire systématiquement une clairance à la créatinine (eGFR) et la phosphatémie chez les patients à risque rénal. Pour les patients sous TDF, il est recommandé de faire la créatinine sérique, la phosphaturie et la chimie des urines avant traitement, puis tous les 3 mois la première année de traitement, ensuite tous les 6 mois s’il n’y a pas d’anomalie rénale[7,90]. Un ajustement des doses pourrait s’avérer nécessaire.
- Évaluation de la densité osseuse
Durant les premières années de traitement sous TDF, une réduction de la densité osseuse a été rapportée.
Certains recommandent, avant de débuter un traitement par un analogue, une DMO et un suivi du taux de la 25-hydroxy vitamine D sous traitement avec supplémentation en cas de déficit[8].
Quand arrêter le traitement par analogues ?
– Sujet AgHbe négatif
La durée du traitement des sujets AgHbe négatif est indéterminée pour les analogues. Il est néanmoins recommandé de poursuivre le traitement jusqu’à la perte de l’AgHBs[5,7]. Son arrêt prématuré peut entraîner une réactivation de la charge virale B dans la majorité des cas. À long terme, les analogues exposent au risque de la résistance et leur coût reste élevé. L’arrêt du traitement pourrait être une option chez certains patients, la décision doit prendre en considération la réponse virale et la sévérité des lésions hépatiques. Le traitement ne doit pas être arrêté en cas de cirrhose avancée, du fait du risque fatal de poussées hépatitiques et de décompensation hépatique.
L’arrêt peut être considéré après 2 ans de traitement si l’ADN du VHB est indétectable en trois occasions distinctes et à six mois d’intervalle [5]. Cette stratégie est indiquée en particulier chez les patients avec un DNA du VHB basal faible ≤ 20000 UI/ml.
Le suivi par les ALT et le DNA du VHB à intervalles réguliers est nécessaire pour détecter à temps les rechutes. Il est recommandé d’évaluer le DNA VHB sérique à intervalle mensuel les 3 premiers mois, puis tous les 3 mois pendant la première année, ensuite tous les 3-6 mois. L‘intervalle le plus court est recommandé en cas de cirrhose[91].
La quantification de l’AgHbs pourrait avoir un rôle prédictif du contrôle de l’infection VHB après arrêt du traitement[82]. Un taux d’AgHbs≤ 200 IU/ml sous traitement et une réduction de l’AgHbs> 1 log10 IU/ml par rapport au taux basal, a une forte valeur prédictive de réponse soutenue au traitement. L’arrêt du traitement peut alors être considéré, car le risque de récidive est minime.
– Sujet AgHbe positif
L’arrêt des analogues nucléos(t)ides peut être envisagé après 12 mois de consolidation succédant à la sérocon- version anti-HBe.[5,7]
Cas particuliers :
– Co-infection VHB-VHC
Il n’y a pas d’interaction entre le TDF ou l’ETV et les agents antiviraux directs du VHC. Habituellement, l’un des virus prime, c’est le VHC, qui sera traité quel que soit le stade de fibrose par les nouveaux DAA durant 3 mois. Le VHB sera surveillé et traité selon l’indication, comme pour les mono infectés par des antiviraux[8].
– Co-infection HIV
Parmi les 40 millions de personnes infectées par le VIH à travers le monde, 2 à 4.000.000 sont coinfectés par le VHB. L’infection HIV aggrave l’évolution naturelle de l’infection VHB en altérant les réponses immunitaires innées et adaptées au virus[92]. Cela va induire une augmentation des taux d’hépatite B chronique et la baisse des taux de séroconversion HBe ou de perte de l’AgHBs sous traitement[93].
Dans l’étude multicentrique de cohorte de 5.293 homosexuels, la mortalité liée au foie était plus élevée chez les coinfectés que chez les mono infectés, surtout quand le taux de CD4 basal était faible[94].
Si les deux infections VHB-VIH doivent être traitées, la combinaison TDF-emtricitabine est recommandée [5,6].
– Hépatite delta (VHD)
Le traitement de l’infection VHD repose sur l’interféron. Dans un essai randomisé, comparant l’interféron pégylé seul (n=29), l’adéfovir seul (n=30) ou leur combinaison (n=31), l’INF-PEG, avec ou sans adéfovir, a permis une clairance soutenue du VHD chez 28% des patients, 24 semaines après traitement [95]. Cependant, à long terme, la moitié des répondeurs soutenus récidivent avec un RNA VHD positif [96].
Dans un autre essai randomisé en double aveugle, évaluant un traitement prolongé par l’INF-PEG (n=59) avec ou sans TDF (n=61), durant 96 semaines, l’efficacité était identique pour la réponse soutenue, 24 semaines après traitement (23-30%) [97].
– Grossesse
Chez la femme en âge de procréer, le traitement vise à réduire la transmission mère-enfant du VHB. L’immunoprophylaxie active-passive réduit la transmission mère-enfant de 95% [98].
Elle consiste en l’administration au nouveau-né des immunoglobulines anti-Hbs dans les 12 heures suivant la naissance et la vaccination anti-VHB à la naissance, à 1 mois et 6 mois.
La transmission peut se produire même après immuno-prophylaxie, si le taux de DNA du VHB chez la mère est supérieur à 106UI/mL (200000 UI/mL, 1million de copies/mL) [99].
Une femme enceinte, avec un DNA du VHB ≥ 106UI/mL au 3ème trimestre, doit être traitée afin de prévenir la transmission au fœtus, à partir de 26 à 28 semaines de gestation jusqu’à 4 semaines du post partum [7]. Les analogues nucléos(t)ides préférées sont la lamivudine, la telbivudine ou le TDF ; l’administration de ces molécules aux mères très virémiques induit un risque de transmission du VHB de 0% au fœtus, tandis que ce risque est de 8% dans le groupe contrôle [100].
Les mères AgHbs(+) requièrent plus d’attention durant la grossesse et le post partum, en raison du risque de poussée hépatique lié aux modifications immunologiques ; une surveillance rigoureuse est ainsi recommandée (ALAT toutes les 12 semaines durant la grossesse, à 4–6 semaines du post partum, puis tous les 3-6mois). Le traitement doit être arrêté en post-partum chez les mères qui vont allaiter [101], et l’interféron est contre-indiqué [102].
Chez la femme enceinte ou planifiant une grossesse dans un proche avenir, les analogues nucléos(t)ides doivent être utilisés avec prudence, en raison du risque de toxicité mitochondriale. En cas de fibrose ou de cirrhose avancée, il a été suggéré d’initier le traitement et de le maintenir durant la grossesse [103].
– Réactivation du VHB :
Les patients infectés par le VHB, sous traitement immunosuppresseur, sont à risque de réactivation virale. Cette dernière peut survenir après une greffe de la moelle osseuse ou de cellule souche, de transplantation d’organes solides, après une chimiothérapie ou après prise d’anti-corps anti-CD20 ou d’agents biologiques (anti TNF alpha) [104].
La symptomatologie varie d’une légère hypertransaminasémie à une hépatite fulminante.
La réactivation est prévenue par le dépistage et un traitement approprié. Tous les patients doivent être testés pour les anticorps anti HBc, l’AgHbs, et le taux du DNA du VHB s’il est positif, avant de débuter un traitement immunosuppresseur [105].
Le traitement antiviral sera introduit plusieurs semaines avant l’immunosuppression et maintenu durant 12 mois après arrêt de l’immunosuppression.
– Patients AgHbs(+)
Tous les patients AgHBs positif devraient bénéficier d’un traitement par analogues nucléos(t)idiques avant l’immunosuppression. Il sera maintenu 12 semaines après l’arrêt du traitement immunosuppresseur, quel que soit le taux du DNA du VHB [5,7,106].
La lamivudine est appropriée et rentable, en particulier si le traitement est de courte durée. L’ETV ou le TDF sont recommandés si le traitement immunosuppresseur est prescrit pour une durée indéterminée [107].
Le suivi reposera sur le dosage du DNA VHB tous les 3 mois, son augmentation devancera celle des ALAT.
– Patients AgHbs(-) et anti-HBc positif
Ces patients peuvent prétendre à un traitement prophylactique par les analogues nucléos(t)ides, même si le risque de réactivation est plus faible par rapport aux patients AgHBs(+), et variable selon le type d’immuno-suppresseur (de 5% à 20%). Néanmoins, le ritixumab augmente ce risque [108]. Le traitement prophylactique est recommandé en cas de DNA VHB détectable.
Si le DNA VHB est indétectable, un suivi seul est nécessaire, sauf dans certains cas (rituximab), où la prophylaxie est recommandée.
– Carcinome Hépatocellulaire :
La réplication virale B est un facteur important du développement du CHC [109]. Le traitement antiviral a pour but de réduire son incidence [110]. La Lamivudine a entraîné une réduction du développement du CHC chez les patients cirrhotiques et non cirrhotiques, son efficacité était cependant limitée par le développement de la résistance au traitement [111-113].
Une étude cas-témoins a montré une incidence cumulative à 5 ans du CHC inférieure chez les patients traités par ETV par rapport au groupe témoin (3,7% vs 13,7%, P <0,001), avec un moindre risque de CHC dans le groupe ETV (HR = 0,37, IC à 95% : [0,15 -0,91], P=0,30) [114].
Des méta-analyses ont montré les avantages du traitement antiviral pour réduire le taux de développement du CHC [115,116]. Cependant, le traitement ne supprime pas complètement le risque de CHC, en particulier en cas de cirrhose établie où le foie est déjà sujet à la cancérogenèse, même en l’absence de réplication virale [117]. Une fois le CHC développé, le traitement anti-VHB dépendra du stade de la maladie. Idéalement, tous les patients doivent être sous analogues du fait de la cirrhose sous jacente. L’APASL recommande d’introduire le traitement antiviral chez tous les patients avec CHC si l’ADN du VHB est > 2000UI/mL avant et/ou après un traitement curatif, et le traitement doit être débuté en préemptif pour tous les patients subissant une chimio-embolisation transartérielle (TACE) [5].
– Transplantation hépatique :
Les indications de la transplantation hépatique (TH) comprennent les poussées graves, les formes chroniques décompensées et le développement du CHC [118].
Le traitement antiviral par l’ETV ou le TDF est important avant la TH pour contrôler l’infection VHB et empêcher la récidive post-TH [119-121].
Après la TH, le traitement est associé aux immunoglobulines anti-Hbs (HBIG) pour éviter la récidive de l’infection VHB et prévenir la perte du greffon [122]. En combinant les HBIG et la lamivudine, plus de 95% de récidives ont pu être évitées [123].
Grâce à la disponibilité de puissants analogues, avec un faible taux de résistance, un régime seul par ETV ou TDF sans les HBIG s’est avéré suffisant [124,125].
Chez les patients DNA VHB négatif lors de la TH, il est recommandé de faire une courte cure d’HBIG (6–12 mois), associée à un traitement au long cours par ETV, TDF ou la combinaison des deux [126].
Chez les patients à haut risque de récidive, on associe les HBIG à l’ETV ou au TDF à long terme [121,127].
Le traitement anti viral du VHB est recommandé à vie après une TH.
Suivi à long terme :
Il est recommandé chez tous les porteurs chroniques du VHB. Le suivi des patients non traités est trimestriel, tous les 3 mois la première année, puis tous les 3 mois pour l’AgHBe(+) et tous les 6 mois pour l’AgHbe(-) l’année suivante.
Les patients AgHbe(-) avec un DNA VHB > 20000 UI/ ml et des ALAT normales persistantes nécessitent un contrôle tous les 3 mois [8].
Une surveillance étroite, tous les 3 mois au moins, est recommandée chez les sujets à risque élevé de réactivation par le taux du DNA VHB et des ALAT. Le dépistage du CHC s’effectue tous les 6 mois, par une échographie avec ou sans dosage de l’AFP ; chez l’homme de plus de 40 ans et la femme de plus de 50 ans, en présence d’une cirrhose hépatique ou d’antécédents familiaux de CHC [3].
Une surveillance du CHC reste recommandée même après une réponse virologique au traitement de l’hépatite B, car le risque de développer un CHC, même faible, persiste [117].
Une endoscopie digestive haute pour la surveillance des varices œsogastriques en vue d’une prophylaxie primaire par bêtabloquants en cas de varices de grade 2 à 3. En l’absence de varices, un contrôle tous les 2 à 3 ans doit être instauré.
Nouveaux traitements anti VHB :
Des traitements visant à inhiber les différentes étapes du cycle de vie du VHB sont en développement.
Plusieurs cibles thérapeutiques potentielles existent, comprenant l’inhibition de l’entrée virale dans l’hépatocyte, la perturbation de la nucléocapsidation virale, la dégénérescence de l’ADN circulaire et les thérapies immunes incluant des agonistes et des récepteurs.
D’autres traitements sont à différents stades de développement, comprenant :
- Les analogues anti-VHB phosphonatés, similaires à l’Adefovir, le TDF et les dérivés de TDF, avec des propriétés pharmacologiques améliorées ;
- Des molécules d’ADN anti-sens,
- Des molécules d’insertion à l’ARN,
- Les inhibiteurs de l’absorption du VHB par les hépatocytes,
- Les inhibiteurs de la formation de la capside,
- Les inhibiteurs de la RNase H,
- Les inhibiteurs de modification de l’histone [27,31,64,128-131].
Conclusion :
L’infection chronique par le VHB représente un fardeau pour la santé à l’échelle mondiale. Elle est associée à une morbidité et une mortalité élevées en l’absence de traitement. Les stratégies thérapeutiques comprennent l’interféron pégylé pendant une durée définie ou un traitement suppressif à long terme par les analogues. Le traitement combiné n’a pas démontré son efficacité. Les analogues offrent une excellente suppression du DNA VHB et la régression de la fibrose, mais de faibles taux de séroconversion HBe et un risque élevé de rechute à l’arrêt du traitement. La surveillance par quantification de l’AgHbs est utile pour prédire la réponse au traitement, en attendant le développement de nouvelles thérapies. Le traitement antiviral n’élimine pas le risque de survenue du CHC.
À long terme, le taux de perte de l’AgHbs est rare, estimé à 1-2% par an, incitant de ce fait à un traitement de longue durée, voire à vie.
Références:
- Kew MC. Epidemiology of chronic hepatitis B virus infection, hepatocellular carcinoma, and hepatitis B virus-induced hepatocellular carcinoma. PatholBiol (Paris) 2010; 58: 273–277.
- Hadziyannis SJ, Vassilopoulos D, Hadziyannis E. The natural course of chronic hepatitis B virus infection and its management. Adv Pharmacol 2013; 67:247–291.
- Chen CJ, Yang HI, Su J, et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. JAMA 2006;295:65–73.
- Tseng TC, Liu CJ, Yang HC, et al. Serum hepatitis B surface antigen levels help predict disease progression in patients with low hepatitis B virus loads. Hepatology2013;57:441–50.
- Liaw YF, Kao JH, Piratvisuth T, Chan HLY, Chien RN, et al. Asian-Pacific consensus statement on the management of chronic hepatitis B: a 2012 update. Hepatol Int 2012; 6: 531-561.
- European Association for The Study of The Liver. EASL clinical practice guidelines: Management of chronic hepatitis B virus infec- tion. J Hepatol 2012; 57: 167-185.
- Terrault NA, Bzowej NH, Chang K-Mi, Hwang JP, Jonas MM, Murad MH. AASLD Guidelines for Treatment of Chronic Hepatitis B. Hepatology 2015.
- MartinP, Lau DTY, Nguyen MH, Janssen HLA, Dieterich DT, Peters MG, Jacobson IM. A Treatment Algorithm for the Manage- ment of Chronic Hepatitis B Virus Infection in the United States: 2015 Update. Clinical Gastroenterology and Hepatology 2015;13:2071–2087.
- Prati D, Taioli E, Zanella A, et al. Updated definitions of healthy ranges for serum alanine aminotransferase levels. Ann Intern Med 2002;137:1–10.
- Yuen M-F, Yuan H-J, Wong DK-H, et al. Prognostic determi- nants for chronic hepatitis B in Asians: therapeutic implications. Gut 2005;54:1610–1614.
- Perrillo RP, Lai C-L, Liaw Y-F, et al. Predictors of HBeAgloss after lamivudine treatment for chronic hepatitis B. Hepatology 2002;36:186–194.
- Lok AS, McMahon BJ. Chronic hepatitis B. Hepatology 2007; 45:507–539.
- Chan HLY, Chan CK, Hui AJ, et al. Effects of tenofovirdiso- proxilfumarate in hepatitis B e antigen-positive patients with normal levels of alanine aminotransferase and high levels of hepatitis B virus DNA. Gastroenterology 2014; 146:1240–1248.
- Kumar M, Sarin SK, Hissar S, et al. Virologic and histologicfea- tures of chronic hepatitis B virus-infected asymptomaticpatients with persistently normal ALT. Gastroenterology 2008;134:1376–1384
- Hu K-Q , Schiff ER, Kowdley KV, et al. Histologic evidence ofactive liver injury in chronic hepatitis B patients with normalrange or minimally elevated alanine aminotransferase levels. J Clin Gastroen- terol 2010;44:510–516.
- Chao DT, Lim JK, Ayoub WS, et al. Systematic review withmeta- analysis: the proportion of chronic hepatitis B patientswith normal alanine transaminase <40 IU/L and significant hepatic fibrosis. Ali- ment Pharmacol Ther 2014;39:349–358.
- Nguyen LH, Chao D, Lim JK, et al. Histologic changes in liver- tissue from patients with chronic hepatitis B and minimal increasesin levels of alanine aminotransferase: a meta-analysis and systematic review. Clin Gastroenterol Hepatol 2014;12:1262–1266.
- Park BK, Park YN, Ahn SH, Lee KS, Chon CY, Moon YM, Park C, Han KH. Long-term outcome of chronic hepatitis B based on his- tological grade and stage. J Gastroenterol Hepatol 2007; 22: 383-388.
- Tai DI, Lin SM, Sheen IS, Chu CM, Lin DY, Liaw YF. Longterm outcome of hepatitis B e antigen-negative hepatitis B surface antigen carriers in relation to changes of alanine aminotransferase levels over time. Hepatology2009; 49: 1859-1867.
- Fung J, Lai CL, But D, Wong D, Cheung TK, Yuen MF. Preva- lence of fibrosis and cirrhosis in chronic hepatitis B: implications for treatment and management. Am J Gastroenterol 2008; 103: 1421- 1426.
- Kim HC, Nam CM, Jee SH, Han KH, Oh DK, Suh I. Normal serum aminotransferase concentration and risk of mortality from liver diseases: prospective cohort study. BMJ 2004; 328: 983.
- Santantonio TA, Fasano M. Chronic hepatitis B: Advances in treatment. World J Hepatol 2014;6:284–292.
- Hadziyannis SJ, Sevastianos V, Rapti I, Vassilopoulos D, Had- ziyannis E. Sustained responses and loss of HBsAg in HBeAg-nega- tive patients withchronic hepatitis B who stop long-term treatment with adefovir. Gastroenterology 2012;143:629–636.
- Hadziyannis SJ. Update on Hepatitis B Virus Infection: Focus on Treatment. Journal of Clinical and Translational Hepatology 2014;2: 285–291.
- Rehermann B, Bertoletti A. Immunological aspects of antiviral therapy of chronic hepatitis B virus and hepatitis C virus infections. Hepatology 2014, July 21.26-
- Lau GK, Piratvisuth T, Luo KX, Marcellin P, et al. Peginterferon Alfa-2a, lamivudine, and the combination for HBeAg-positive chronic hepatitis B.N Engl J Med. 2005; 352: 2682-2695.
- Flink HJ, et al. Am J Gastroenterol. 2006;101:297-303.
- Bonino F, Marcellin P, Lau GK, Hadziyannis S, et al. Predicting response to peginterferon alpha-2a, lamivudine and the two combi- ned for HBeAg-negative chronic hepatitis B. Gut 2007; 56: 699-705.
- Liaw YF. Impact of therapy on the long-term outcome of chronic hepatitis B. Clin Liver Dis 2013;17:413–423.
- Yuen MF, Lai CL. Treatment of chronic hepatitis B: Evolution over two decades. J Gastroenterol Hepatol 2011; 26:138–143.
- Tujios SR, LeeWM. Update in the management of chronic hepa- titis B. Curr Opin Gastroenterol 2013;29:250–256.
- Lau GK, Piratvisuth T, Luo KX, et al. Peginterferon alfa-2a, lami- vudine, and the combination for HBeAg-positive chronic hepatitis B. N Engl J Med 2005;352:2682-95.
- Liaw YF, Jia JD, Chan HL, et al. Shorter durations and lower doses ofpeginterferon alfa-2a are associated with inferior hepatitis B e antigenseroconversion rates in hepatitis B virus genotypes B or C.Hepatology 2011;54:1591-9.
- Lampertico P, Vigano M, Di Costanzo GG, et al. Randomiseds- tudycomparing 48 and 96 weeks peginterferon alpha-2a therapy in genotype DHBeAg-negative chronic hepatitis B. Gut 2013;62:290-8.
- Dusheiko G. Treatment of HBeAg positive chronic hepatitis B: interferon or nucleoside analogues. Liver Int 2013;33:137–150.
- Vigano M, Mangia G, Lampertico P. Results of treatment of chro- nic hepatitis B with pegylated interferon. Clin Liver Dis 2013;17:425– 443.
- Marcellin P, Bonino F, Yurdaydin C, Hadziyannis S, Moucari R, Kapprell HP et al. Hepatitis B surface antigen levels: association with 5-year response to peginterferon alfa-2a in hepatitis B e-antigen-nega- tive patients. Hepatol Int 2013;7:88–97.
- Brunetto MR, Marcellin P, Cherubini B, Yurdaydin C, Farci P, Hadziyannis SJ, et al. Response to peginterferon alfa-2a (40KD) in HBeAg-negative CHB: ontreatment kinetics of HBsAg serum levels vary by HBV genotype. J Hepatol 2013;59:1153–1159.
- Lampertico P, Liaw YF. New perspectives in the therapy of chro- nic hepatitis B. Gut 2012; 61: i18–i24.
- Marcellin P, Lau GKK, Bonino F, Farci P, et al. Peginterferon alfa- 2a alone, lamivudine alone, and two in combination in patients with HBeAG-negative chronic hepatitis B. N Engl J Med 2004; 351:1206– 1217.
- Marcellin P, Bonino F, Lau GK, Farci P, et al. Sustained response of hepatitis B e antigen-negative patients 3 years after treatment with peginterferon alpha-2a. Gastroenterology 2009; 136: 2169-2179.
- Papatheodoridis GV, Dimou E, Dimakopoulos K, et al. Outcome of hepatitis B e antigen-negative chronic hepatitis B on long-term nucleos(t)ide analog therapy starting with lamivudine. Hepatolo- gy2005; 42: 121-129.
- Lai CL, Shouval D, Lok AS, Chang TT, et al. Entecavir versus lamivudine for patients with HBeAg-negative chronic hepatitis B. N Engl J Med 2006; 354: 1011-1020.
- Marcellin P, Heathcote EJ, Buti M, Gane E, et al. Tenofovirdiso- proxilfumarate versus adefovirdipivoxil for chronichepatitis B. N Engl J Med 2008; 359: 2442-2455.
- Marcellin P, Gane E, Buti M, Afdhal N, Sievert W, Jacobson IM, et al. Regression of cirrhosis during treatment with tenofovirdisoproxil- fumarate for chronic hepatitis B: a 5-year open-label follow-up study. Lancet 2013; 381:468–475.
- Chang TT, Liaw YF, Wu SS, Schiff E, Han KH, Lai CL et al. Long-term entecavir therapy results in the reversal of fibrosis/cirrho- sis and continued histologicalimprovement in patients with chronic hepatitis B. Hepatology 2010;52:886–893.
- Marcellin P, Lau GK, Bonino F, Farci P, et al. Peginterferon alfa- 2a alone, lamivudine alone, and the two in combination in patients with HBeAg-negative chronic hepatitis B. N Engl J Med 2004; 351: 1206-1217.
- Lai CL, Gane E, Liaw YF, Hsu CW, et al. Telbivudine versus lamivudine in patients with chronic hepatitis B. N Engl J Med 2007; 357: 2576-2588.
- Hadziyannis SJ, Tassopoulos NC, Heathcote EJ, et al. Adefovir- dipivoxil for the treatment of hepatitis B e antigen-negative chronic hepatitis B. N Engl J Med 2003; 348: 800-807.
- Lok ASF. Drug Therapy: Tenofovir. Hepatology. 2010; 52:743-747.
- Chang TT, Gish RG, de Man R, et al. A comparison of entecavir and lamivudine for HBeAg-positive chronic hepatitis B. N Engl J Med 2006;354:1001-10.
- Gish RG, Lok AS, Chang TT, et al. Entecavir therapy for up to 96 weeks in patients with HBeAg-positive chronic hepatitis B. Gastroen- terology 2007; 133: 1437-44.
- Chang TT, Lai CL, Kew Yoon S, et al. Entecavir treatment for up to 5 years in patients with hepatitis B e antigen-positive chronic hepatitis B. Hepatology 2010;51:422-30.
- Yuen MF, Seto WK, Fung J, Wong DK, Yuen JC, Lai CL. Three years of continuous entecavir therapy in treatment-naive chronic hepatitis Bpatients: VIRAL suppression, viral resistance, and clinical safety. Am J Gastroenterol 2011;106:1264-71.
- Liaw YF, Sheen IS, Lee CM, et al. Tenofovirdisoproxilfumarate (TDF), emtricitabine/TDF, and entecavir in patients with decompen- sated chronichepatitis B liver disease. Hepatology 2011;53:62-72.
- Shim JH, Lee HC, Kim KM, et al. Efficacy of entecavir in treat- ment-naïve patients with hepatitis B virus-related decompensated cir- rhosis. J Hepatol 2010;52:176-82.
- Corsa AC, Liu Y, Flaherty JF, et al. No detectable resistance to tenofovirdisoproxilfumarate (TDF) in HBeAg+ and HBeAg− patients with chronichepatitis B (CHB) after eight years of treatment. Hepa- tology 2014;1707.
- Lok ASF, Trinh H, Carosi G, et al. Efficacy of entecavir with or without tenofovirdisoproxilfumarate for nucleos(t)ide-naive patients with chronic hepatitis B. Gastroenterology 2012;143:619-28.
- Chan HL, Chan CK, Hui AJ, et al. Effects of tenofovirdisoproxil- fumarate in hepatitis B e antigen-positive patients with normal levels of alanine aminotransferase and high levels of hepatitis B virus DNA. Gastroenterology 2014;146:1240-8
- .Fung S, Kwan P, Fabri M, et al. Randomized comparison of ten of ovirdisoproxilfumaratevsemtricitabine and tenofovirdisoproxil- fumarate inpatients with lamivudine-resistant chronic hepatitis B. Gastroenterology 2014;146:980-8.
- Chen CH, Chiu YC, Lu SN, Lee CM, Wang JH, Hu TH, et al. Serum hepatitis B surface antigen levels predict treatment response to nucleos(t)ide analogues. World J Gastroenterol 2014;20:7686–7695.
- Marcellin P, Ahn SH, Ma X, Caruntu FA. & al. Combination of TenofovirDisoproxilFumarate and Peginterferon alfa-2a Increases Loss of Hepatitis B Surface Antigen in Patients with Chronic Hepa- titis B On behalf of the Study 149 Investigators. Gastroenterology 2015;1–11.
- Buti M, Fung S, Gane E, Afdhal NH et al. Long-term clinical outcomes in cirrhotic chronic hepatitis B patients treated with tenofo- virdisoproxilfumarate for up to 5 years. Hepatol Int 2015; 9:243–250.
- Tang CM, Yau TO, Yu J. Management of chronic hepatitis B infection: current treatment guidelines, challenges, and new develop- ments. World J Gastroenterol 2014;20:6262–6278.
- Kumar M, Sarin SK. Systematic review: combination thera- pies for treatment-naïve chronic hepatitis B. Aliment Pharmacol Ther2008; 27: 1187-1209.
- Li MY, Yuan XL, Zhang DZ. Comparison of peg-interferon monotherapy to peg-interferon and nucleoside analogue combina- tion therapy for hepatitis B: a meta-analysis of randomized controlled trials. ZhonghuaGanZang Bing ZaZhi 2012; 20: 442–447.
- Ouzan D, Penaranda G, Joly H, et al. Add-on peginterféron leads to loss of HBsAg in patients with HBeAg-negative chronic hepatitis and HBV DNA fully suppressed by long-term nucleotide analogs. J Clin Virol 2013; 58:713–717.
- Barone M, Iannone A, Di Leo A. HBsAg clearance by Peg-inter- feron addition to a long-term nucleos(t)ide analogue therapy. World J Gastroenterol 2014; 20:8722–8725.
- Kittner JM, Sprinzl MF, Grambihler A, et al. Adding pegylated interferon to a current nucleos(t)ide therapy leads to HBsAgserocon- version in a subgroup of patients with chronic hepatitis B. J Clin Virol 2012;54:93–95.
- Marcellin P, Avila C, Wursthorn K et al. Telbivudine (LDT) plus peg-interferon (PEGIFN) in HBeAg-positive chronic hepatitis B: very potent antiviral efficacy but risk of peripheral neuropathy (PN). J Hepatol 2012;52:S6–S7.
- Tenney DJ, Rose RE, Baldick CJ, Pokornowski KA, et al. Long- term monitoring shows hepatitis B virus resistance to entecavir in nu- cleoside-naïve patients is rare through 5 years of therapy. Hepatology 2009; 49: 1503-1514.
- Sherman M, Yurdaydin C, Sollano J, Silva M, Liaw YF, et al. Entecavir for treatment of lamivudine-refractory, HBeAg-positive- chronic hepatitis B. Gastroenterology 2006; 130: 2039-2049.
- Berg T, Zoulim F, Moeller B, et al. Long-term efficacy and safety of emtricitabine plus tenofovir DF vstenofovir DF monotherapy in adefovir-experienced chronic hepatitis B patients. J Hepatol 2014; 60: 715–722.
- Reijnders JG, Deterding K, Petersen J, et al. Antiviral effect of en- tecavir in chronic hepatitis B: influence of prior exposure to nucleos(t) ideanalogues. J Hepatol 2010;52:493-500.
- Lim YS, Byun KS, Yoo BC, et al. Tenofovirmonotherapy versus tenofovir and entecavir combination therapy in patients with enteca- vir-resistantchronic hepatitis B with multiple drug failure: results of a randomised trial. Gut 2016; 65: 852-60.
- NICE guidance VHB. National institute for health and care excel- lence 2013.Jaroszewicz J., BC Serrano, K Wursthorn, et al. Hepatitis B sur- face antigen (HBsAg) levels in the natural history of hepatitis B virus (HBV)-infection: A European perspective Journal of Hepatology 2010; 52: 514–522.
- Yamashita N, Kagita M, et al. Quantitation of hepatitis B surface antigen by an automated chemiluminescentmicroparticle immunoas- say. J Virologic Methods 2004;115:217-22.
- Zacher BJ, Moriconi F, Bowden S, et al. Multicenter evaluation of the Elecsys hepatitis B surface antigen quantitative assay. Clin Vaccine Immunol 2011;18:1943-50.
- Brunetto MR, Oliveri F, Colombatto P, et al. Hepatitis B surface antigen serum levels help to distinguish active from inactive hepatitis B virusgenotype D carriers. Gastroenterology 2010;139:483-90.
- Martinot-Peignoux M, Lapalus M, Laouénan C, et al. Prediction of disease reactivation in asymptomatic hepatitis B e antigen-negative chronic hepatitis B patients using baseline serum measurements of HBsAg and HBV-DNA. J Clin Virol2013; 58: 401-407.
- Martinot-Peignoux M, Lapalus M, Asselah T, Marcellin P. HBsAg quantification: useful for monitoring natural history and treatment outcome. Liver Int2014; 34 Suppl 1: 97-107.
- Sonneveld MJ, Hansen BE, Piratvisuth T, et al. Responseguide- dpeginterferon therapy in hepatitis B e antigen-positive chronic he- patitis B using serum hepatitis B surface antigen levels. Hepatology 2013;58:872–880.
- Sonneveld MJ, Rijckborst V, Boucher CAB, et al. Prediction of sustained response to peginterferon alfa-2b for hepatitis B e antigen- positive chronic hepatitis B using on-treatment hepatitis B surface antigen decline. Hepatology 2010;52:1251–1257.
- Rijckborst V, Hansen BE, Cakaloglu Y, et al. Early on-treatment prediction of response to peginterferon alfa-2a for HBeAgnegative chronic hepatitis B using HBsAg and HBV DNA levels. Hepatology 2010;52:454–461.
- Rijckborst V, Hansen BE, Ferenci P, et al. Validation of a stopping rule at week 12 using HBsAg and HBV DNA for HBeAg negative pa- tients treated with peginterferon alfa-2a. J Hepatol 2012;56:1006–1011.
- Ha NB, Ha NB, Garcia RT, et al. Medication nonadherence with long-term management of patients with hepatitis B e antigennegative chronic hepatitis B. Dig Dis Sci 2011;56:2423–2431.
- Zoutendijk R, Reijnders JGP, Brown A, et al. Entecavir treat- ment for chronic hepatitis B: adaptation is not needed for the majority of naïve patients with a partial virological response. Hepatology 2011;54:443–451.
- Lu L, Yip B, Trinh H, et al. Tenofovir-based alternate therapies for chronic hepatitis B patients with partial virologicalresponsetoen- tecavir. J Viral Hepat 2015; 22: 675–681.
- Liaw YF, Sheen IS, Lee CM, et al. Tenofovirdisoproxilfumarate (TDF), emtricitabine/TDF, and entecavir in patients with decompen- sated chronichepatitis B liver disease. Hepatology 2011;53:62-72.
- Chan WK, Tan SS, Mohamed R. Stopping Therapy in HBeAg Negative Disease. Current Hepatitis Reports 2013; 12: pp 105-111.
- Phung BC, Sogni P, Launay O. Hepatitis B and human immuno- deficiencyvirus co-infection. World J Gastroenterol 2014;20:17360-7.
- Thio CL. Hepatitis B and human immunodeficiency virus coin- fection. Hepatology 2009;49:S138-45.Thio CL, Seaberg EC, Skolasky R, Jr., et al. HIV-1, hepatitis B virus, and riskof liver-related mortality in the Multicenter Cohort Study (MACS). Lancet 2002;360:1921-6.
- Wedemeyer H, Yurdaydin C, Dalekos GN, et al. Peginterferon plus adefovir versus either drug alone for hepatitis delta. N Engl J Medic 2011; 364: 322-31.
- Heidrich B, Yurdaydin C, Kabacam G, et al. Late HDV RNA relapse after peginterferon alpha-based therapy of chronic hepatitis delta. Hepatology 2014;60:87-97.
- 97-Wedermeyer H, Yurdaydin C, Ernst S, et al. Prolonged therapy of hepatitis delta for 96 weeks with pegylated-interferon-a-2a plus tenofoviror placebo does not prevent HDV RNA relapse after treat- ment: the HIDIT-2study. 49th European Association for the Study of the Liver International Liver Congress (EASL 2014). London, April 9-13, 2014. Abstract O4.
- US Department of Health and Human Services. MMWR: a comprehensive immunization strategy to eliminate transmission of hepatitis B virus infection in the United States. 2005.
- www.cdc.gov/ mmwr/preview/.Zou H, Chen Y, Duan Z, et al. Virologic factors associated with failure to passive-active immunoprophylaxis in infants born to HB- sAg-positive mothers. J Viral Hepatitis 2012;19:18-25.
- Han G-R, Cao M-K, Zhao W, et al. A prospective and open- label study for the efficacy and safety of telbivudine in pregnancy for the prevention of perinatal transmission of hepatitis B virus infection. J Hepatol 2011;55:1215–1221.
- Ehrhardt S, Xie C, Guo N, Nelson K, Thio CL. Breastfeeding while taking lamivudine or tenofovirdisoproxilfumarate: a review of the evidence. Clin Infect Dis 2015;60:275-8.
- Patton H, Tran TT. Management of hepatitis B during pregnan- cy. Nat Rev Gastroenterol Hepatol 2014;11:402-9.Peginterferon alfa-2b pregnancy and breastfeeding warnings. www.drugs.com/pregnancy/peginterferon-alfa-2b.html.Di Bisceglie AM, Lok AS, Martin P, et al. Recent US Food and Drug Administration warnings on hepatitis B reactivation with im- mune suppressing and anticancer drugs: just the tip of the iceberg? Hepatology 2015;61:703-11.
- Reddy KR, Beavers KL, Hammond SP, et al. American gas- troenterological association institute guideline on the prevention and treatment of hepatitis B virus reactivation during immunosuppressive drug therapy. Gastroenterology 2015;148:215-9.
- Saab S, Dong MH, Joseph TA, et al. Hepatitis B prophylaxis in patients undergoing chemotherapy for lymphoma: a decision analysis model. Hepatology 2007; 46: 1049-56.Hwang JP, Lok AS. Management of patients with hepatitis B who require immunosuppressive therapy. Nat Rev Gastroenterol Hepatol 2014;11:209-19.
- Hsu C, Tsou HH, Lin SJ, et al. Chemotherapy-induced hepatitis B reactivation in lymphoma patients with resolved HBV infection: a prospective study. Hepatology 2014;59:2092-100.Fung J, Lai CL, Yuen MF. Hepatitis B and C virus-related carci- nogenesis. Clin Microbiol Infect 2009; 15: 964-970.
- Lai CL, Yuen MF. Prevention of hepatitis B virus-related he- patocellular carcinoma with antiviral therapy. Hepatology2013; 57: 399-408.
- Yuen MF, Seto WK, Chow DH, et al. Long-term lamivudine therapy reduces the risk of long-term complications of chronic hepa- titis B infection even in patients without advanced disease. Antivir Ther 2007; 12: 1295-1303.
- Liaw YF, Sung JJ, Chow WC, et al. Management of severe chro- nic hepatitis B DF, Sabbat J. Lamivudine for patients with chronic hepatitis B and advanced liver disease. N Engl J Med 2004; 351: 1521-1531.
- Kurokawa M, Hiramatsu N, Oze T, et al. Long-term effect of lamivudine treatment on the incidence of hepatocellular carcinoma in patients with hepatitis B virus infection. J Gastroenterol2012; 47: 577-585.
- Hosaka T, Suzuki F, Kobayashi M, Seko Y, Kawamura Y, Sezaki H, Akuta N, Suzuki Y, Saitoh S, Arase Y, Ikeda K, Kobayashi M, Kumada H. Long-term entecavir treatment reduces hepatocellular carcinoma incidence in patients with hepatitis B virus infection. He- patology2013; 58: 98-107.
- Sung JJ, Tsoi KK, Wong VW, Li KC, Chan HL. Meta-analysis: Treatment of hepatitis B infection reduces risk of hepatocellular carcinoma. Aliment Pharmacol Ther2008; 28: 1067-1077.
- Papatheodoridis GV, Lampertico P, Manolakopoulos S, Lok A. Incidence of hepatocellular carcinoma in chronic hepatitis B patients receiving nucleos(t)ide therapy: a systematic review. J Hepatol 2010; 53: 348-356.
- Papatheodoridis GV, Manolakopoulos S, Touloumi G, et al. Vi- rological suppression does not prevent the development of hepatocel- lular carcinoma in HBeAg-negative chronic hepatitis B patients with cirrhosis receiving oral antiviral(s) starting with lamivudine monothe- rapy: results of the nationwide HEPNET. Greece cohort study. Gut 2011; 60: 1109-1116 [PMID: 21270118]
- Fung J. Managing hepatitis B: Before and after liver transplanta- tion. Ind J Transplant 2011; 5: 77-80
- Yasunaka T, Takaki A, Yagi T, et al. Serum hepatitis B virus DNA before liver transplantation correlates with HBV reinfection rate even under successful low-dose hepatitis B immunoglobulin prophylaxis. Hepatol Int 2011; 5: 918-926.
- Chun J, Kim W, Kim BG, et al. High viremia, prolonged Lami- vudine therapy and recurrent hepatocellular carcinoma predict post- transplant hepatitis B recurrence. Am J Transplant 2010; 10: 1649-1659.
- Marzano A, Gaia S, Ghisetti V, Carenzi S, et al. Viral load at the time of liver transplantation and risk of hepatitis B virus recurrence. Liver Transpl 2005; 11: 402-409.
- Samuel D, Muller R, Alexander G, Fassati L, Ducot B, Benha- mou JP, Bismuth H. Liver transplantation in European patients with the hepatitis B surface antigen. N Engl J Med 1993; 329: 1842-1847.
- Lo CM, Cheung ST, Lai CL, Liu CL, Ng IO, Yuen MF, Fan ST, Wong J. Liver transplantation in Asian patients with chronic hepatitis B using lamivudine prophylaxis. Ann Surg 2001; 233: 276-281.
- Angus PW, Patterson SJ, Strasser SI, McCaughan GW, Gane E. A randomized study of adefovirdipivoxil in place of HBIG in combination with lamivudine as post-liver transplantation hepatitis B pro- phylaxis. Hepatology 2008; 48: 1460-1466.
- Fung J, Chan SC, Cheung C, et al. Oral nucleoside/nucleotide analogs without hepatitis B immune globulin after liver transplanta- tion for hepatitis B. Am J Gastroenterol2013; 108: 942-948.
- Ku W, Wang U, Nguyen MH. Hepatitis B immunoglobu- lin (HBIG) for post-transplant HBV. Expert Opin Biol Ther 2015; 15:665–677.Fung J, Chan S-C, Cheung C, et al. Oral nucleoside/nucleotide analogs without hepatitis B immune globulin after liver transplantation for hepatitis B. Am J Gastroenterol 2013; 108:942–948.
- Fletcher SP, Delaney WE. New therapeutic targets and drugs for the treatment of chronic hepatitis B. Semin Liver Dis 2013;33:130–137.
- Wang XY, Chen HS. Emerging antivirals for the treatment of hepatitis B. World J Gastroenterol 2014;20:7707–7717.
- Qiu LP, Chen L, Chen KP. Antihepatitis B therapy: a review of current medications and novel small molecule inhibitors. Fundam- ClinPharmacol 2014;28:364–381.
- Glebe D, Konig A. Molecular virology of hepatitis B virus and targets for antiviral intervention. Intervirology 2014;57:134–140.