Category: Uncategorized
Acute Articular Rheumatism: Better to prevent than to cure
Is umbilical hernia a simple condition?
Screening for hearing loss in at-risk newborns using evoked otoacoustic emissions and early brainstem auditory evoked potentials: A prevalence study of 231 cases
Iron Deficiency in Children With or Without Anemia: What’s New?
Epidemiology of ovarian cancer
Ch.MAZOUZI1,R.BENYAHIA2,E.KERBOUA3,B.BELLOUZE4; (1) Service d’Oncologie Médicale, CHUBéjaïa, (2) Service de Radiologie, CPMC Alger, (3) Service d’Oncologie Médicale, CPMC
Abstract
Ovarian cancer represents approximately 4 % of female can- cers and is responsible for more than 5 % of cancer deaths. White women or women living in developed countries are most at risk. Incidence and mortality rates, stable between 1980 and 2000, tend to decrease with the advent of oral contraception and therapeutic progress. Hereditary forms of ovarian cancer represent 5 to 10 % of cases: epithelial carcinomas alone or associated with breast cancers (BRCA 1 and 2 mutations) or Lynch syndrome associating ovarian cancer with colon or endometrial cancers. More than 90 % of epithelial ovarian cancers are sporadic. All situations al- lowing a reduction in the number of ovulations during hor- monal and gynecological reproductive life play a protective role. Thus, a high number of pregnancies, the use of breast- feeding and a long duration of oral contraception reduce the risk of ovarian cancer. Conversely, risk factors are readily associated with relative hyperestrogenism: hormonal treat- ment for menopause, endometriosis, infertility, polycystic ovary syndrome, obesity, diabetes. On an environmental and toxic level, occupational exposure to certain aromatic compounds has a deleterious role, while the protective ef- fect of sun exposure and vitamins A and D is mentioned. Many other factors probably also have a positive or negative impact on the risk of ovarian cancer but remain debated. The objective of this work is to analyze data from the litera- ture on the risk factors for ovarian cancer. A bibliographic search was carried out on PubMed using a search algorithm containing the keywords: ovary, ovarian, exposure, work, oc- cupation. Relevant articles were selected based on their title and abstract. Interesting articles cited in the bibliography of the selected studies were also considered.
Keywords : Ovarian cancer, descriptive epidemiology, risk factors, BRCA 1, 2.
Résumé
Le cancer de l’ovaire représente environ 4 % des cancers fémi- nins et est responsable de plus de 5 % des décès par cancer. Les femmes de couleur blanche ou vivant dans des pays dévelop- pés sont les plus exposées. Les taux d’incidence et de mortalité, stables entre 1980 et 2000, tendent à diminuer avec l’avène- ment de la contraception orale et les progrès thérapeutiques. Les formes héréditaires des cancers de l’ovaire représentent 5 à 10 % des cas : carcinomes épithéliaux seuls ou associés à des cancers du sein (mutations BRCA 1 et 2) ou syndrome de Lynch associant cancer ovarien aux cancers du côlon ou de l’endomètre. Plus de 90 % des cancers épithéliaux ovariens sont sporadiques. Toutes les situations permettant de dimi- nuer le nombre d’ovulations au cours de la vie reproductive hormonale et gynécologique jouent un rôle protecteur. Ainsi, un nombre élevé de grossesses, le recours à l’allaitement ma- ternel et une longue durée de contraception orale diminuent le risque de cancer de l’ovaire. Inversement, les facteurs de risque sont volontiers associés à une hyperoestrogénie relative : trai- tement hormonal de la ménopause, endométriose, infertilité, syndrome des ovaires polykystiques, obésité, diabète. Sur le plan environnemental et toxique, l’exposition professionnelle à certains composés aromatiques a un rôle délétère, alors que l’effet protecteur de l’exposition solaire et des vitamines A et D est évoqué. De nombreux autres facteurs ont probablement aussi un impact positif ou négatif sur le risque de cancer ova- rien, mais restent discutés. L’objectif de ce travail est d’analyser des données de la littérature sur les facteurs de risque du can- cer de l’ovaire. Une recherche bibliographique a été effectuée sur PubMed en utilisant un algorithme de recherche conte- nant les mots-clés : ovary, ovarian, exposure, work, occupa- tion. Les articles pertinents ont été sélectionnés selon leur titre et résumé. Les articles intéressants cités dans la bibliographie des études retenues ont également été pris en compte.
Mots-clés :Cancer de l’ovaire, épidémiologie descriptive, facteurs de risques, BRCA 1, 2.
Introduction
Les tumeurs de l’ovaire sont caractérisées par plusieurs types histologiques et des potentiels de malignité variables. Les tu- meurs épithéliales ou tumeurs du revêtement ovarien repré- sentent environ 65 % de l’ensemble des tumeurs et plus de 85 % des tumeurs malignes de l’ovaire de l’adulte. Les types histo- logiques sont séreux, mucineux, endométrioïdes, à cellules claires, à cellules transitionnelles (Brenner) ou indifférenciés. Les tumeurs séreuses, mucineuses et de Brenner peuvent être bénignes, malignes ou à malignité atténuée. Les tumeurs en- dométrioïdes, à cellules claires ou indifférenciées, sont classi- quement malignes. Les tumeurs germinales représentent 15 à 20 % des tumeurs de l’ovaire. Ces tumeurs malignes sont sur- tout diagnostiquées dans l’enfance. Les tératomes kystiques, classiquement bénins, sont les plus fréquents. Les autres types ont un profil malin : dysgerminomes (séminomes), tumeurs du sinus endodermique, carcinomes embryonnaires, chorio- carcinomes et tératomes immatures. Les tumeurs du mésen- chyme et des cordons sexuels représentent 6 % des tumeurs de l’ovaire. Elles sont hormono-sécrétantes. Les tumeurs fémi- nines se composent des tumeurs stromales et de la granulo- sa. Les tumeurs mâles correspondent aux tumeurs de Serto- li-Leydig ou androblastomes. Ces tumeurs évoluent de façon maligne, hormis les fibromes et thécomes de l’ovaire guéris par la chirurgie. Enfin, l’ovaire peut héberger des tumeurs de type lymphome, sarcome ou mélanome.
Épidémiologie descriptive
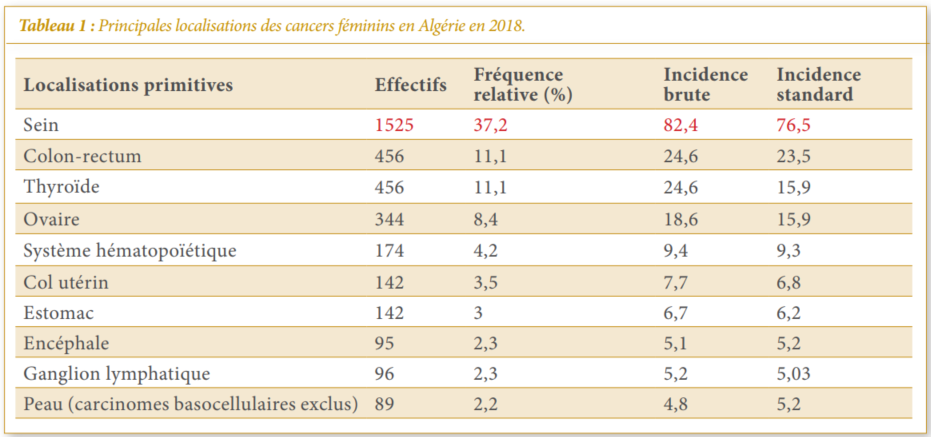
Le cancer de l’ovaire est le sixième cancer le plus fré- quent chez les femmes (et le 18e au total des cancers les plus fréquents) dans le monde entier. Environ 239 000 cas ont été enregistrés en 2012, soit près de 4 % de tous les nouveaux cas de cancer chez les femmes (2 % au to- tal) et le cancer de l’ovaire représente la huitième cause la plus fréquente de décès par cancer chez les femmes dans le monde (14e au total) [1]. En Algérie (Tableau 1), il représente le troisième cancer gynécologique chez la femme après le cancer du sein et du col utérin [1]. Par- tout dans le monde, des taux d’incidence normalisés se- lon l’âge varient de plus de 11 pour 100 000 femmes en Europe centrale et orientale à moins de 5 pour 100 000 dans certaines parties de l’Afrique. Les taux d’incidence sont de : 11,7 pour 100 000 au Royaume-Uni, 8,0 pour 100 000 aux États-Unis, 5,2 pour 100 000 au Brésil et 4,1 pour 100 000 en Chine. Une évaluation épidémio- logique globale montre que le cancer de l’ovaire touche surtout les femmes entre 60 et 70 ans mais la possibi- lité d’atteintes plus précoces est reliée à une prédis- position héréditaire chez des patientes avec des liens de parenté au premier degré [2]. Selon les dernières données de l’OMS publiées en 2020, les décès par Cancer des ovaires en Algérie ont atteint 611 ou 0.33 % des décès totaux [3].
Épidémiologie Analytique
A- Génétique
Environ 90 % des cancers ovariens sont sporadiques [5]. Ils retrouvent leur genèse le plus souvent dans la perte de gènes suppresseurs de tumeurs ou dans le gain d’un oncogène. Les formes héréditaires des cancers de l’ovaire représentent 5 à 10 % des cas : elles se regroupent d’une part sous la forme de carcinomes épithéliaux seuls ou associés à des cancers du sein (Breast Research Cancer Antigen BRCA 1 et 2) et d’autre part dans le cadre d’un syndrome associant des cancers du côlon ou de l’endomètre (syndrome de Lynch). Ces deux maladies sont caractérisées par une transmission autosomique dominante, avec une forte pénétrance. En dehors de ces deux syndromes, un antécédent personnel de cancer du sein ou familial de can- cer de l’ovaire est associé à un risque accru d’un facteur 3 à 5.
B- Breast Research Cancer Antigen (BRCA) 1 et 2
La mutation de deux gènes suppresseurs de tumeurs BRCA 1 et BRCA 2, localisés respectivement en 17q21 et 13q14, est responsable de 80 % et 15 % de ces prédispositions lorsqu’une histoire familiale est retrouvée. Ces deux gènes codent pour des protéines impliquées dans les mécanismes de réparation de lésions de l’ADN, de contrôle du cycle cellulaire et de la transcription d’autres gènes. La probabilité chez les femmes porteuses de ces mutations de développer un carcinome ovarien est entre 10 % et 63 % et la probabilité de dévelop- per un cancer du sein entre 56 % et 87 %, notamment pour les BRCA 1. Plus de 800 mutations de ces deux gènes ont été identifiées, compliquant les recherches au niveau de chaque famille. Certains groupes de population, comme les femmes juives Ashkénazes ou les Islandaises, présentent des mutations récurrentes connues des gènes BRCA 1 et BRCA 2, avec une prévalence estimée à 2,5 % chez les femmes juives Ashké- nazes. Chez ces patientes déclarant un cancer de l’ovaire, une des mutations est retrouvée chez 26 à 41 % d’entre elles [6 – 7]. La survenue d’un carcinome ovarien dans un contexte gé- nétique est souvent plus précoce que dans les cas sporadiques, quoique rare avant 40ans. L’implicationpotentielle desgènesBRCA 1 et BRCA 2 dans les cancers sporadiques du sein et de l’ovaire n’est pas encore clarifiée. En pratique, lorsqu’une mutation d’un gène BRCA est diagnostiquée au niveau personnel, au décours d’un traitement pour cancer ou dans le cadre d’un dépistage familial, une surveillance clinique et paraclinique rigoureuse est recommandée [8]. Concernant le risque ovarien, une échographie pelvienne est réalisée annuellement à partir de l’âge de 35 ans. Compte tenu de la performance limitée de l’échographie pour le dépistage du cancer de l’ovaire, une an- nexectomie prophylactique est recommandée à partir de 40 ans après validation pluridisciplinaire. L’âge de l’intervention peut être modulé en fonction du gène altéré, de l’histoire fa- miliale et de la demande de la patiente. L’analyse histologique des trompes et des ovaires doit être complète afin de faire le diagnostic d’un cancer occulte, présent dans 5 % des cas. Cette annexectomie bilatérale prophylactique permet de réduire de 85 à 96 % le risque de cancer de l’ovaire, de la trompe ou du péritoine [9, 10]. 10 % environ d’altérations histologiques (dysplasies, lésions précancéreuses) sont découvertes sur les pièces d’annexectomies prophylactiques. Le risque résiduel de cancer est estimé à 5 % [11, 12].
C- Syndrome des cancers colorectaux non polypoïdes héréditaires ou syndrome de Lynch II
Il s’agit de formes familiales de cancer du côlon volontiers droit, parfois associé à des cancers de l’endomètre, des ovaires ou du tractus urogénital. Le syndrome de Lynch est impliqué dans 2 % des cancers ovariens. Trois gènes ont pu être incriminés : hMLH1 (Human Mutant Homologue 1), hMSH2, hMSH6; il s’agit de gènes du système MMR (MisMatch Repair). La perte de fonction de ces gènes favorise l’accumulation de mutations favorables à l’évolution maligne des processus tumoraux. Ce syndrome est défini par les critères d’Amsterdam II en 1999 [13] :
- Au moins trois sujets atteints de cancers appartenant au spectre étroit du syndrome HNPCC (côlon, rectum, endo- mètre, intestin grêle, voies urinaires) et histologiquement prouvés ;
- Unis deux à deux par un lien de parenté au premier degré sur au moins deux générations ;
- Un des cancers au moins s’étant révélé avant l’âge de 50 ans. Lorsqu’un gène du système MMR est découvert. La patiente bénéficie d’un temps de réflexion et doit être accompagnée de façon pluridisciplinaire dans la formulation de sa demande et dans sa décision finale. Les modalités de surveillance va- rient entre l’abstention et la surveillance échographique et biologique selon les pays. Les tests génétiques restent limités à certaines indications qui tiennent compte de l’histoire per- sonnelle et familiale des patientes, dans le cadre d’une consul- tation d’oncogénétique. Les dernières recommandations françaises précisent que l’hystérectomie avec annexectomie prophylactique peut être envisagée chez les femmes porteuses d’une mutation d’un gène MMR après accomplissement du projet parental [14]. L’indication de cette intervention est validée dans le cadre d’une réunion de concertation pluridisciplinaire spécifique. La patiente bénéficie d’un temps de réflexion et doit être accompagnée de façon pluridisciplinaire dans la for- mulation de sa demande et dans sa décision finale.
D- Vie reproductive, hormonale et gynécologique
- Ménarche et ménopause
L’âge d’apparition des premières règles ou l’âge de survenue de la ménopause n’ont pas pu être clairement impliqués comme des facteurs de risque indépendants, tant la genèse de ces tu- meurs apparaît multifactorielle. Concernant la ménopause, deux visions s’affrontent : en considérant qu’un taux élevé de gonadotrophines est un facteur d’exposition au cancer ova- rien, une ménopause précoce est donc à risque; mais selon la théorie de « l’ovulation incessante », une ménopause tardive l’est aussi par le biais de l’augmentation des traumatismes de surface du parenchyme ovarien liés aux ovulations, potentiel- lement mutagènes [19].
- Parité
La grossesse est un facteur protecteur. Le risque relatif de can- cer ovarien chez une femme ayant eu un enfant par rapport à une nullipare est de 0,4 – 0,6 avec un bénéfice s’accroissant à chaque naissance [20, 21]. Ce bénéfice est notamment retrou- vé lorsque la dernière grossesse a lieu tardivement dans la vie génitale, période où le parenchyme ovarien présente souvent des lésions précancéreuses qui pourraient régresser à l’arrêt des ovulations [22].
- Grossesses non menées à terme
Le rôle des grossesses non menées à terme est discuté, tant le recueil précis de chaque histoire obstétricale est difficile. Certaines interruptions volontaires de grossesse ne sont pas évoquées par pudeur et des avortements spontanés précoces peuvent ne pas être détectés ou inconnus du médecin. Par ailleurs, les données les plus récentes sont contradictoires, fac- teur de protection ou d’exposition selon les séries [23 – 24].
- Allaitement
L’allaitement n’est un élément protecteur que si sa durée est prolongée. L’hypothèse avancée est celle du principe de la di- minution du nombre d’ovulations et du taux de gonadotro- phines circulantes. En effet, dans la cohorte NHS (Nurse Health Study), le risque de cancer ovarien n’est pas réduit en population globale dont l’allaitement était en moyenne de 9 mois. La réduction significative du risque (0,66) n’est obser- vée que dans le sous-groupe des femmes ayant allaité plus de 18 mois par rapport à celles qui n’ont pas allaité. Ces résultats sont valables pour les tumeurs séreuses et endométrioïdes. Les tumeurs mucineuses ne semblent pas bénéficier de cet effet protecteur, à l’inverse des tumeurs à cellules claires [25 – 26].
- Infertilité et inducteurs de l’ovulation
L’infertilité est un facteur de risque. Le risque relatif de déve- lopper un carcinome ovarien pour une femme infertile depuis plus de cinq ans est de 2,7 % par rapport à une femme décla- rant une grossesse en moins d’un an de tentatives. Concernant les inducteurs de l’ovulation, une augmentation du risque était retrouvée dans les années 1990 [28 – 29]. Les données récentes se montrent plus rassurantes [29]. Cependant, des incertitudes de- meurent sur le citrate de clomiphène pour lequel un surrisque de cancer utérin et mammaire est évoqué, en l’absence d’asso- ciation démontrée avec le cancer ovarien. L’interprétation doit tenir compte de l’âge de prise en charge des patientes, de la du- rée de traitement, du type d’infertilité et du délai à l’obtention d’une grossesse, sources de biais dans l’analyse des résultats.
- Contraception oestroprogestative
L’effet protecteur des oestroprogestatifs sur le risque de surve- nue d’un cancer ovarien est connu depuis longtemps. Il s’ex- plique par la baisse du nombre d’ovulations et de l’effet muta- gène des proliférations cellulaires engendrées, la baisse du taux circulant des gonadotrophines, facteur de risque notamment en péri-ménopause et le rôle bénéfique de la progestérone. En effet, certaines études ont observé un effet apoptotique de la progestérone sur des cellules ovariennes malignes humaines. Chez les femmes non porteuses de mutations BRCA, le risque relatif est de 0,4 à 0,6 % après cinq ans de prise, avec une dimi- nution du risque de 6 % à chaque année supplémentaire. Le rôle de la contraception chez les patientes porteuses de muta- tions BRCA est discuté, mais un bénéfice semble être observé
sur la prévention des cancers ovariens [30]. La difficulté d’in- terprétation est liée à l’effet contraire induit par la contracep- tion sur le cancer du sein chez les patientes mutées. Comme pour la grossesse, l’effet protecteur des oestroprogestatifs ne concerne que les tumeurs épithéliales non mucineuses.
E- Syndrome des ovaires polykystiques
Son implication est évoquée dans différentes études, sans ce- pendant l’identifier comme facteur de risque indépendant [31]. L’étiopathogénie est discutée : surrisque lié au syndrome par l’augmentation des concentrations ovariennes locales d’hor- mones stéroïdiennes et de facteurs de croissance type EGF ou IGF; effet iatrogène des traitements inducteurs de l’ovu- lation prescrits dans cette indication. Les résultats des études sont discordants, certaines rapportant un risque relatif de 2,5, d’autres ne retrouvant pas d’association [32]. Ces discordances peuvent s’expliquer par des biais de sélection des populations étudiées et certains facteurs de confusion (obésité associée, in- duction de l’ovulation, grossesses). Il n’y a pas de corrélation entre les signes cliniques d’hyperandrogénie (hirsutisme, ir- régularités menstruelles, acné) et le risque de cancer ovarien.
F- Traitement hormonal de la ménopause (THM)
L’étude randomisée Women’s Health Initiative (WHI) est la première en 2003 à évoquer l’impact du THM sur le risque de survenue des cancers gynécologiques [41]. Dans cette co- horte, les femmes substituées par un traitement combiné (0,625 mg d’œstrogènes équins associés à 2,5 mg d’acétate de médroxyprogestérone) ou un placebo sont suivies pendant 5,6 ans. Le risque relatif de développer un cancer ovarien et, plus globalement, une tumeur maligne annexielle est respec- tivement de 1,6 et 1,9 [42]. Les autres grandes études de cohorte anglo-saxonnes Nurse Health Study (NHS) et MWS (Million Women Study) révèlent une augmentation significative du risque relatif de cancer ovarien (1,2 à 1,4) chez les femmes mé- nopausées sous THM au moment de l’événement par rapport aux femmes ménopausées non substituées. La durée du THM augmente à la fois le risque de survenue du cancer et d’en décéder. Chez les femmes ayant un antécédent de THM, la durée a également une influence négative. Le risque relatif est de 1,5 chez les femmes substituées pendant plus de cinq ans, alors qu’aucune augmentation du risque n’est observée chez les femmes traitées en moyenne pendant 3,3 ans. Le risque de cancer ovarien est doublé chez les femmes traitées par estro- gènes seuls en comparaison avec celles sous oestroprogestatifs. Parmi les oestroprogestatifs, aucune différence n’est observée selon la molécule, la forme galénique, la voie d’administra- tion et le schéma de prescription [47]. Le risque est augmenté pour les tumeurs séreuses ou endométrioïdes par rapport aux autres formes histologiques [33]. L’influence délétère du THM dans ces études anglo-saxonnes n’est pas observée dans la co- horte française E3N, où le traitement se compose essentielle- ment d’estrogènes et de progestérone naturels.
G- Endométriose
L’endométriose touche 5 à 15 % des femmes en période d’ac- tivité hormonale. Des études ont montré un lien entre la pré- sence d’endométriose et la survenue d’un cancer de l’ovaire, principalement de type endométrioïde et à cellules claires. La fréquence de survenue varie de 0,7 à 8 % [34]. Une large co- horte japonaise confirme l’augmentation du risque chez les patientes ayant des endométriomes, surtout si leur taille est importante et l’âge élevé au moment du diagnostic [35]. Ceci s’explique par les similitudes étiopathogéniques de l’endomé- triose et du cancer ovarien qui partagent les mêmes facteurs de risque. Le pronostic du cancer est toutefois meilleur dans ce contexte. L’augmentation du risque est d’autant plus impor- tante que l’endométriose s’associe à une infertilité primaire.
H- Hystérectomie, ligature de trompes
Les femmes ayant subi une ligature tubaire ont un risque diminué de cancer ovarien de 32 à 39 %, indépendamment de l’effet bénéfique de la grossesse, de l’allaitement et de la contraception oestroprogestative. Certains auteurs ont sug- géré l’hypothèse de l’origine tubaire de certains cancers de l’ovaire [36]. Cet effet protecteur se retrouve notamment chez les porteuses de mutations BRCA1. Les explications physio- pathologiques sont nombreuses : diminution de la vascu- larisation ovarienne, diminution du risque inflammatoire ovarien par voie rétrograde, diminution de l’ascension vers l’ovaire d’agents potentiellement cancérigènes comme le talc, l’amiante et les gels contraceptifs. L’hystérectomie avec conser- vation annexielle agirait par le même biais, avec une diminu- tion du risque évaluée à 36 % [37].
Au total, beaucoup de ces situations cliniques sont en rap- port avec le retentissement qu’elles engendrent sur le nombre d’ovulations. La théorie de « l’ovulation incessante » est le terme consacré pour tous les cas où le nombre élevé d’ovula- tions au cours de la vie génitale semble impliqué dans l’histoire naturelle du cancer de l’ovaire.
I- Facteurs généraux et médicamenteux
- Âge
L’âge moyen au moment du diagnostic est de 60 ans. Cepen- dant, le cancer de l’ovaire n’est pas exclusivement une maladie de la femme ménopausée. Il est observé chez les femmes en période d’activité génitale dans 22 à 29 % des cas. Ces notions doivent être présentes à l’esprit lors du diagnostic d’une masse annexielle en préménopause.
- Race
Bien que les femmes de race blanche vivant dans des pays dé- veloppés soient plus exposées au cancer ovarien que les autres femmes, des études essentiellement nord-américaines ont montré que l’obésité et les antécédents familiaux de cancers gy- nécologiques exposaient plus les femmes afro-américaines au cancer ovarien que les femmes américaines blanches. D’autres
facteurs comme le taux de ligature tubaire, le nombre de gros- sesses, influent vraisemblablement sur les différences obser- vées. Par ailleurs, le pronostic plus sombre du cancer ovarien chez les femmes afro-américaines serait plus en rapport avec les difficultés d’accès aux soins qu’avec des mécanismes biolo- giques différents [38].
- Morphologie
Un risque relatif de cancer ovarien de 2,2 est rapporté dans la littérature chez les femmes de plus de 175 cm, par rapport aux femmes de moins de 160 cm. L’obésité ne semble pas influen- cer le risque de cancer ovarien en préménopause. Après la mé- nopause, le risque relatif de cancer est compris entre 1,2 et 1,3 chez les femmes ayant un indice de masse corporelle (IMC) supérieur à 30 par rapport à celles ayant un IMC inférieur à 25. De façon surprenante, l’absence de THM apparaît délétère. Chez les femmes non substituées, le risque relatif est de 1,8 pour les obèses par rapport aux non obèses, alors que chez les femmes substituées, il n’y a pas de différence selon l’IMC [40]. De même, l’accroissement de l’IMC de 2 kg/m2 n’augmente le risque relatif de cancer ovarien (1,05) que chez les femmes sans THM [64]. Il est classique d’expliquer la prolifération des cellules épithéliales ovariennes par l’effet anti-apoptotique des fortes concentrations plasmatiques d’androgènes, d’œstro- gènes et d’insuline (IGF) chez les femmes obèses. Cependant, l’influence non négative du THM n’est pas expliquée et pour- rait être liée à des facteurs de confusion.
- Activité physique et diététique
Une activité physique régulière paraît réduire le risque de can- cer séreux invasif, mais pas celui des autres sous-types histo- logiques et des tumeurs à malignité atténuée. Le recueil de ces données est soumis à de nombreux biais, notamment sur l’in- terprétation des différents types d’activité physique [61, 66]. Une large consommation de fibres alimentaires est classiquement associée à une diminution du taux d’œstrogènes circulants et du risque de cancer hormonodépendant. Une étude nutri- tionnelle associée à l’étude WHI retrouve un effet bénéfique au-delà de quatre ans de régime riche en fibres, fruits et lé- gumes, donc d’une manière générale pauvre en graisses. Ce- pendant, ce rôle prophylactique n’a pas été observé dans une autre série prospective.
- Diabète
Les dysrégulations glycémiques ont été identifiées comme des facteurs de risque indépendant de cancer, notamment dans les pays occidentaux où elles s’associent à de mauvaises habitudes alimentaires. L’hyperglycémie constituerait un milieu de dé- veloppement favorable aux cellules tumorales par des méca- nismes cellulaires complexes. La régulation de la glycémie des femmes diabétiques permet de prévenir le cancer de l’ovaire [41].
- Inflammation et anti-inflammatoires
Le cancer de l’ovaire pourrait être lié à une inflammation pelvienne chronique classiquement induite par les infections génitales hautes. L’inflammation jouerait un rôle mutagène sur l’épithélium de surface ovarien [42]. Elle entraînerait une augmentation des mitoses, des lésions de l’ADN, un stress oxydatif et des concentrations élevées de cytokines et de pros- taglandines. Ainsi, les anti-inflammatoires non stéroïdiens (AINS) ont été évoqués en chimioprévention du carcinome ovarien. Les résultats sont cependant discutés. Les études sont polymorphes et soumises à de nombreux biais d’interpréta- tion : multiples AINS utilisés avec des différences de biodis- ponibilité et de pharmacocinétique selon les molécules; mo- dalités de recueil des informations chez les patientes sources d’erreurs et d’imprécisions (auto-questionnaires) concernant des médicaments en vente libre et d’usage large. Une mé- ta-analyse ne rapporte aucune action préventive des AINS, ni de l’aspirine. L’absence d’association significative entre AINS et prévention du cancer ovarien est confortée par les résultats de deux grandes cohortes prospectives.
- Paracétamol [43]
Les résultats des premières séries publiées étaient contradic- toires, mais en 2006 une méta-analyse a attribué un rôle pro- tecteur au paracétamol pour des consommations régulières (30 prises par mois sur au moins six mois en moyenne) avec un risque relatif à 0,7. Ces résultats sont à interpréter avec la même prudence et les mêmes réserves que pour les AINS et l’aspirine, notamment au niveau des modalités de recueil et des circonstances de prescription de la molécule. De plus, les études n’ont pas la même définition des consommations « régulières ». La physiopathologie de cette protection reste à préciser, car le paracétamol n’agit pas sur le cycle des prosta- glandines par mécanisme anti- inflammatoire.
- Antidépresseurs, benzodiazépines [44]
Un risque accru de carcinome ovarien et de tumeurs à mali- gnité atténuée a été observé chez les femmes traitées par anti- dépresseurs et benzodiazépines. Les antidépresseurs agissant par les voies dopaminergiques et de la norépinéphrine sont accusés, alors que les données sont plus rassurantes pour les molécules agissant par inhibition de recapture de la séro- tonine. Certaines prescriptions associées (amphétamines) semblent influencer le risque. Concernant les benzodiazé- pines, les études sont majoritairement en faveur d’une absence de risque.
J- Facteurs environnementaux et toxiques
- Exposition solaire et vitamine D [45]
L’exposition solaire est bénéfique et liée à la localisation géo- graphique. Une incidence plus élevée de carcinomes ovariens est observée dans les hautes latitudes de chaque hémisphère, où l’exposition solaire est moindre. L’effet positif de la produc- tion accrue de vitamine D est avancé. En effet, les patientes ayant un cancer ovarien ont 3,7 fois plus de chance d’avoir un taux faible de vitamine D sérique circulante (< 23 ng/dl) que la population générale. Certains polymorphismes du récep- teur à la vitamine D sont retrouvés chez des patientes avec un cancer ovarien de meilleur pronostic. L’hypothèse est que la présence cellulaire accrue de vitamine D et de sa forme active (1,25 dihydroxyvitamine D) induirait une augmentation des phénomènes apoptotiques dans les cellules épithéliales trans- formées en cellules néoplasiques. Cependant, la relation entre polymorphisme génétique des récepteurs à la vitamine D, taux de vitamine D circulante et pronostic de la maladie n’est pas encore bien établie [46].
- Vitamine A
La dysrégulation du métabolisme de la vitamine A est impli- quée dans la carcinogenèse ovarienne. L’effet protecteur de la consommation régulière de caroténoïdes riches en vitamine A (alpha-carotène, bêta-carotène) est discuté. Le fenrétinide (analogue synthétique de la vitamine A) donné en traitement adjuvant du cancer du sein a montré qu’il réduisait l’incidence des cancers ovariens chez ces patientes. L’effet est réversible à l’arrêt du traitement [47].
- Profession [48]
Certaines substances comme les herbicides, les amines aro- matiques, les hydrocarbures aromatiques et aliphatiques, l’amiante et le talc augmenteraient le risque de cancer ovarien. Ces deux derniers agiraient par l’inflammation chronique créée par leur présence au niveau du tractus génital haut. Ain- si, les femmes exposées travaillant dans les pressings ou dans l’imprimerie industrielle sont à risque de cancer ovarien, in- dépendamment de leur vie gynécologique et hormonale. Les professions exposées à des doses cumulées importantes de gaz d’échappement de moteurs diesel et de solvants contenant des hydrocarbures aromatiques, sont également à risque. En effet, les particules diesel inhalées pourraient avoir un effet œstro- gène-like, à l’inverse des essences sans plomb.
- Tabac
Les femmes fumeuses régulières ont un risque accru de déve- lopper une tumeur mucineuse, mais l’implication du tabac sur les autres types histologiques de tumeurs invasives et à mali- gnité atténuée n’est pas établie [49].
- Café
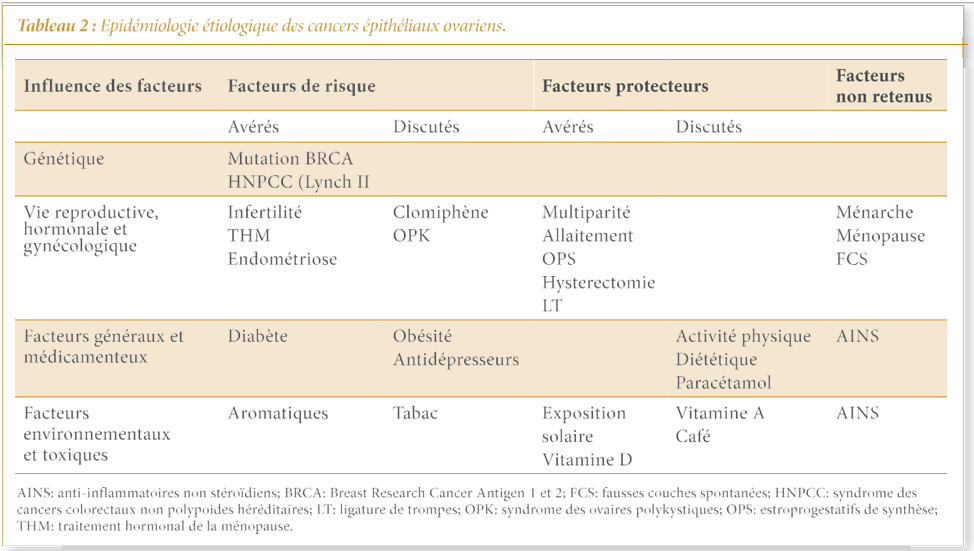
La prise régulière de café montre un bénéfice après la méno- pause, notamment chez les femmes sans traitement hormonal substitutif. La protection concerne les patientes consommant au moins 2,5 tasses par jour [50]. La caféine modulerait le taux d’hormones sexuelles de façon différente en pré et post-mé- nopause. Elle serait efficace en abaissant leur taux et le traite- ment hormonal de la ménopause pourrait s’opposer à ces ef- fets favorables. Le polymorphisme des gènes impliqués dans le métabolisme de la caféine est actuellement étudié. Au total, les études préliminaires ontsuggéré que plusieurs facteurs pouvaient protéger ou exposer les femmes aucancer de l’ovaire. Certains ont été validés par les données épidémiologiques les plus récentes, d’autres restent discutés ou ne sont plus retenus (Tableau 2).
Conclusion
Le cancer de l’ovaire n’est pas, à la différence du cancer du sein un cancer très fréquent, en revanche, c’est un cancer caracté- risé par une extrême gravité. En termes d’incidence, il est en augmentation continue. La mortalité par cancer de l’ovaire continue de croître aussi en Algérie, essentiellement chez les femmes âgées de plus de 60 ans, Le premier facteur de risque du cancer de l’ovaire est un facteur de risque génétique sur lequel aucun moyen de prévention direct n’existe. Les gènes associés à un surrisque de cancer du sein et de l’ovaire sont les gènes BRCA 1 et 2. Ainsi, les femmes ayant des antécédents personnels ou familiaux de cancer du sein ou de l’ovaire, sur- venu à un âge jeune, se verront rechercher cette mutation génétique afin qu’une prise en charge spécialisée leur soit proposée.
Références
- GLOBOCAN 2008 (IARC). Section of Cancer Information. http://globocan.iarc.fr.
- Ferlay J, Shin HR, Bray F, Forman D, Mathers C, Parkin DM. Estimates of worldwide burden of cancer in 2008: GLOBOCAN 2008. Int J Cancer 2010; 127: 2893–917.
- Jemal A, Siegel R, Ward E, Hao Y, Xu J, Thun MJ. Cancer statistics,2020. CA Cancer J Clin 2020; 59: 225–49.
- Herbst AL. The epidemiology of ovarian carcinoma and the current status of tumor markers to detect disease. Am J Obstet Gynecol; 170: 1099–105.
- Moslehi R, Chu W, Karlan B, Fishman D, Risch H, Fields A, et al. BRCA1 and BRCA2 mutation analysis of 208 Ashkenazi Jewish women with ovarian cancer. Am J Hum Ge- net 2000; 66: 1259–72.
- Struewing JP, Hartge P, Wacholder S, Baker SM, Berlin M, McA-dams M, et al. The risk of cancer associated with specific mutations of BRCA1 and BRCA2 among Ashkenazi Jews. N Engl J Med 1997 ; 336:1401–8.
- INCA. Principales recommandations de prise en charge des femmes porteuses d’une mutation de BRCA 1 ou BRCA 2 (2009) www.e-cancer.fr.
- Friebel TM, Domchek SM, Neuhausen SL, Wagner T, Evans DG, Isaacs C, et al. Bila- teral prophylactic oophorectomy and bilateral prophylactic mastectomy in a prospective cohort of unaffected BRCA1 and BRCA2 mutation carriers. Clin Breast Cancer 2007; 7:875–82.
- Vasen HF, Haites NE, Evans DG, Steel CM, Moller P, Hodgson S, et al., European Familial Breast Cancer Collaborative Group. Current policies for surveillance and ma- nagement in women at risk of breast and ovarian cancer: a survey among 16 European family cancer clinics. Eur J Cancer 1998; 34:1922–6.
- Piek JM, van Diest PJ, Zweemer RP, Jansen JW, Poort-Keesom RJ Menko FH, et al. Dysplastic changes in prophylactically removed Fallopian tubes of women predisposed to developing ovarian cancer. J Pathol 2001; 195: 451–6.
- Chene G, Penault-Llorca F, Le Bouedec G, Mishellany F, Dauplat MM, Jaffeux P, et al. Ovarian epithelial dysplasia and prophylactic oophorectomy for genetic risk. Int J Gyne- col Cancer 2009; 19: 65–72.
- Adami HO, Hsieh CC, Lambe M, Trichopoulos D, Leon D, Persson I, et al. Parity, age at first childbirth, and risk of ovarian cancer. Lancet 1994; 344: 1250–4.
- Dick ML, Siskind V, Purdie DM, Green AC, Australian Cancer Study Group (Ova- rian Cancer); Australian Ovarian Cancer Study Group. Incomplete pregnancy and risk of ovarian cancer: results from two Australian case-control studies and systematic review. Cancer Causes Control 2009; 20: 1571–85.
- Danforth KN, Tworoger SS, Hecht JL, Rosner BA, Colditz GA, Hankinson SE. Breastfeeding and risk of ovarian cancer in two prospective cohorts. Cancer Causes Control 2007; 18:517–23.
- Ness RB, Cramer DW, Goodman MT, Kjaer SK, Mallin K, Mosgaard BJ, et al. Infer- tility, fertility drugs, and ovarian cancer: a pooled analysis of case control studies. Am J Epidemiol 2002; 155:217–24.
- Rossing MA, Daling JR, Weiss NS, Moore DE, Self SG. Ovarian tumors in a cohort of infertile women. N Engl J Med 1994; 331: 771–6.
- Brinton LA, Lamb EJ, Moghissi KS, Scoccia B, Althuis MD, Mabie JE, et al. Ova- rian cancer risk after the use of ovulation-stimulating drugs. Obstet Gynecol 2004; 103: 1194–203.
- Rossing MA, Tang MT, Flagg EW, Weiss LK, Wicklund KG. A case control study of ovarian cancer in relation to infertility and the use of ovulation-inducing drugs. Am J Epidemiol 2004; 160:1070–8.
- Calderon-Margalit R, Friedlander Y, Yanetz R, Kleinhaus K, Perrin MC, Manor O, et al. Cancer risk after exposure to treatments for ovulation induction. Am J Epidemiol 2009; 169: 365–75.
- Bosetti C, Negri E, Trichopoulos D, Franceschi S, Beral V, Tzonou A, et al. Long-term effects of oral contraceptives on ovarian cancer risk. Int J Cancer 2002; 102: 262–5.
- Whittemore AS, Balise RR, Pharoah PD, Dicioccio RA, Oakley Girvan I, Ramus SJ, et al. Oral contraceptive use and ovarian cancer risk among carriers of BRCA1 or BRCA2 mutations. Br J Cancer 2004; 91: 1911–5.
- De Franc ⁎a Neto AH, Rogatto S, Do Amorim MM, Tamanaha S, Aoki T, Aldrighi JM. Oncological repercussions of polycystic ovary syndrome. Gynecol Endocrinol 2010; 26: 708–11.
- Schildkraut JM, Schwingl PJ, Bastos E, Evanoff A, Hugues C. Epithelial ovarian cancer risk among women with polycystic ovary syndrome. Obstet Gynecol 1996; 88: 554–9.
- Anderson G, Judd H, Kaunitz A, Barad D, Beresford S, Pettinger M, et al. Effects of estrogen plus progestin on gynecologic cancers and associated diagnostic procedures: the Women’s Health Initiative randomized trial. JAMA 2003; 290: 1739–48.
- Beral V, Bull D, Green J, Reeves G. Ovarian cancer and hormone replacement therapy in the Million Women Study. Lancet; 369:1703–10.
- Kobayashi H. Ovarian cancer in endometriosis: epidemiology, natural history, and clinical diagnosis. Int J Clin Oncol 2009; 14: 378–82.
- Kindelberger DW, Lee Y, Miron A, Hirsch MS, Feltmate C, Medeiros F, et al. Intrae- pithelial carcinoma of the fimbria and pelvic serous carcinoma: Evidence for a causal relationship. Am J Surg Pathol 2007; 31: 161–9.
- Green A, Purdie D, Bain C, Siskind V, Russell P, Quinn M, et al., Survey of Women’s Health Study Group. Tubal sterilisation, hysterectomy and decreased risk of ovarian can- cer. Int J Cancer 1997.
- Lukanova A, Kaaks R. Endogenous hormones and ovarian cancer: epidemiology and current hypotheses. Cancer Epidemiol Biomarkers Prev 2005; 14: 98–107.
- Brun JL, Feyler A, Chêne G, Saurel J, Brun G, Hocké C. Long-term results and pro- gnostic factors in patients with epithelial ovarian cancer. Gynecol Oncol 2000; 78:21–7.
- Nagle CM, Bain CJ, Green AC, Webb PM. The influence of reproductive and hormonal factors on ovarian cancer survival. Int J Gynecol Cancer 2008; 18: 407–13.
- Brun JL, Rouzier R, Uzan S, Daraï E. External validation of a laparoscopic-based score to evaluate resectability of advanced ovarian cancers: clues for a simplified score. Gynecol Oncol 2008; 110: 354–9.
- Schouten LJ, Goldbohm RA, van den Brandt PA. Height, weight, weight change, and ovarian cancer risk in the Netherlands cohort study on diet and cancer. Am J Epidemiol 2003; 157:424–33.
- Lahmann PH, Cust AE, Friedenreich CM, Schulz M, Lukanova A, Kaaks R, et al. An- thropometric measures and epithelial ovarian cancer risk in the European Prospective Investigation into Cancer and Nutrition. Int J Cancer 2010; 126: 2404–15.
- Leitzmann MF, Koebnick C, Danforth KN, Brinton LA, Moore SC, Hollenbeck AR, et al. Body mass index and risk of ovarian cancer. Cancer 2009; 115: 812–22.
- Lahmann PH, Friedenreich C, Schulz M, Cust AE, Lukanova A, Kaaks R, et al. Physi- cal activity and ovarian cancer risk: the European Prospective Investigation into Cancer and Nutrition. Cancer Epidemiol Biomarkers Prev 2009; 18: 351–4.
- Rossing MA, Cushing-Haugen KL, Wicklund KG, Doherty JA, Weiss NS. Recreatio- nal physical activity and risk of epithelial ovarian cancer. Cancer Causes Control 2010; 21: 485–91.
- Prentice R, Thomson C, Caan B, Hubbell F, Anderson G, Beresford S, et al. Low-fat dietary pattern and cancer incidence in the Women’s health initiative dietary modifica- tion randomized controlled trial. J Natl Cancer Inst 2007; 99: 1534–43.
- Kellenberger LD, Bruin JE, Greenaway J, Campbell NE, Moorehead, Holloway AC, et al. The role of dysregulated glucose metabolism in epithelial ovarian cancer. J Oncol 2010; 2010: 514310.
- Ness RB, Cottreau C. Possible role of ovarian epithelial inflammation in ovarian can- cer. J Natl Cancer Inst 1999; 91: 1459–67.
- Rodríguez-Burford C, Barnes MN, Oelschlager DK, Myers RB, Talley LI, et al. Ef- fects of nonsteroidal anti-inflammatory agents (NSAID) on ovarian carcinoma cell lines: preclinical evaluation of NSAID as chemopreventive agents. Clin Cancer Res 2002; 8: 202–9.
- [42] Fairfield KM, Hunter DJ, Fuchs CS, Colditz GA, Hankinson SE. Aspirin, other NSAID, and ovarian cancer risk (United States). Cancer Causes Control 2002; 13: 535– 42.
- Merritt MA, Green AC, Nagle CM, Webb PM, Australian Cancer Study (Ovarian Cancer); Australian Ovarian Cancer Study Group. Talcum powder, chronic pelvic in- flammation and in relation to risk of epithelial ovarian cancer. Int J Cancer 2008; 122: 170–6.
- Bonovas S, Filioussi K, Sitaras NM. Do non-steroidal anti-inflammatory drugs affect the risk of developping ovarian cancer? Ameta-analysis. Br J Clin Pharmacol 2005; 60: 194–203.
- Pinheiro SP, Tworoger SS, Cramer DW, Rosner BA, Hankinson SE. Use of non-ste- roidal anti-inflammatory agents and incidence of ovarian cancer in 2 large prospective cohorts. Am J Epidemiol 2009; 169: 1378–87.
- Bonovas S, Filioussi K, Sitaras NM. Paracetamol use and risk of ovarian cancer: a meta-analysis. Br J Clin Pharmacol 2006; 62: 113–21.
- Dublin S, Rossing MA, Heckbert SR, Goff BA, Weiss N. Risk of epithelial ovarian cancer in relation to use of antidepressants, benzodiazepines, and other centrally acting medications. Cancer Causes Control 2002; 13: 35–45.
- Tamez S. Vitamin D receptor polymorphisms and prognosis of patients with epithe- lial ovarian cancer. Br J Cancer 2009; 101: 1957–60
- Bertone ER, Hankinson SE, Newcomb PA, Rosner B, Willet WC, Stampfer MJ, et al. A population-based case-control study of carotenoid and vitamin A intake and ovarian cancer (United States). Cancer Causes Control 2001; 12: 83–90.
- Guo J, Kauppinen T, Kyyronen P, Heikkila P, Lindbohm ML, PukkalaE. Risk of eso- phageal, ovarian, testicular, kidney and bladder cancers and leukaemia among Finnish workers exposed to diesel or gasoline engine exhaust. Int J Cancer 2004; 111: 286–92.
Hepatic tuberculosis: report of a case
A.BELKHATIR1,W.MOKHDAR1,H.KIES 2,A.SARIHASSOUN3 ; (1) Service de Gastro-entérologie, CHU Dr Tidjani Damerdji, Tlemcen, (2) Service d’Anatomopathologie, CHU Dr Tidjani Damerdji, Tlemcen.
Abstract
Hepatic tuberculosis is rare, the interest of its knowledge lies in the diagnostic problems it poses in particular in its primitive form. The clinical, biological and radiological aspects are often misleading. We report the case of an immunocompetent 38-year-old patient single housewife, with no notion of tuberculosis contagion, whose initial clinical, biological and radiological picture was non-specific. Operated for cholecystitis, followed for the appearance of cervical ADP, in whom the anatomopathological examination of liver biopsies and lymph node areas performed respectively during cholecystectomy and transparietal puncture, confirmed the diagnosis. During a laparoscopy for cholecystitis and preoperatively, discovery of multiple whitish nodules disseminated over the entire the surface of the liver, a biopsy was performed on one of these granulations associated with a cholecystectomy. The anatomopathological examination came back in favor of chronic cholecystitis in acute post-lithiasis attack while the anatomopathological examination of the hepatic granuloma showed an epithelial-giganto-cellular infiltrate without caseous necrosis bathed in a steatotic parenchyma. Four months after the appearance of cervical lymphadenopathy, excisional biopsy of one of these lymphadenopathies corrected the diagnosis, confirming the histological study of the tuberculous nature of the lymphadenopathy and hepatic granulations. Once the diagnosis was made, antituberculosis treatment was started for 6 months.
Keywords : Laparoscopy, hepatic granulations, caseous necrosis.
Résumé
La tuberculose hépatique est rare, l’intérêt de sa connaissance réside dans les problèmes diagnostiques qu’elle pose notamment dans sa forme primitive. Les aspects cliniques, biologiques et radiologiques sont souvent trompeurs. Nous rapportons le cas d’une patiente immunocompétente âgée de 38 ans, femme au foyer célibataire, sans notion de contagion tuberculeuse, dont le tableau clinique, biologique et radiologique initial était aspécifique. Opérée d’une cholécystite, suivie de l’apparition d’une ADP cervicale, chez qui l’examen anatomo-pathologique des biopsies hépatiques et des zones ganglionnaires, réalisées respectivement au cours de la cholécystectomie et de la ponction transpariétale, a confirmé le diagnostic. Lors d’une laparoscopie pour cholécystite et en préopératoire, découverte de multiples nodules blanchâtres disséminés sur toute la surface du foie, une biopsie a été réalisée sur l’une de ces granulations, associée à une cholécystectomie. L’examen anatomopathologique est revenu en faveur d’une cholécystite chronique en crise aiguë post-lithiasique tandis que l’examen anatomopathologique du granulome hépatique montrait un infiltrat épithélial-giganto-cellulaire sans nécrose caséeuse baignant dans un parenchyme stéatosique. Quatre mois après l’apparition de l’adénopathie cervicale, la biopsie exérèse d’une de ces lymphadénopathies a permis de confirmer le diagnostic, confirmant l’étude histologique du caractère tuberculeux de l’adénopathie et des granulations hépatiques. Une fois le diagnostic posé, un traitement antituberculeux a été instauré pendant 6 mois.
Mots-clés : Laparoscopie, granulations hépatiques, nécrose caséeuse.
Introduction
Dans le cadre de la maladie tuberculeuse, l’atteinte hépatique est souvent associée aux autres localisations abdominales. La forme primitive de la tuberculose hépatique, plutôt rare, réalise des aspects souvent trompeurs. Son diagnostic est histologique et/ou bactériologique. Son traitement ne se dissocie guère des autres formes de tuberculose, son évolution sous traitement est généralement favorable.
Observation
La patiente I. S. âgée de 38 ans, a consulté aux urgences pour des douleurs aiguës de l’hypochondre droit. Dans ses antécédents, nous avions retrouvé une déficience psychologique modérée dès l’enfance, la patiente n’a suivi aucun traitement. Elle avait présenté de façon épisodique des douleurs abdominales spontanément résolutives, isolées, sans syndrome fébrile ou ictérique, avec absence de notion de contage tuberculeux.
La douleur avait débuté 24 heures avant son admission aux urgences. L’examen clinique mettait en évidence une défense douloureuse à la palpation de l’hypochondre droit, un signe de Murphy positif, une température de 37,2, un poids de 92 Kg, un BMI à 36. Elle n’avait pas de cicatrice BCG visible au niveau des deltoïdes.
Sur le plan biologique, il a été retrouvé une élévation de la CRP à 48 mg/l, pas d’hyperleucocytose ou d’anémie ni cholestase ou cytolyse, sérologie HIV négative.
L’échographie abdominale réalisée objectivait une vésicule à paroi fine siège de plusieurs mini-calculs (Figures 1, 2).
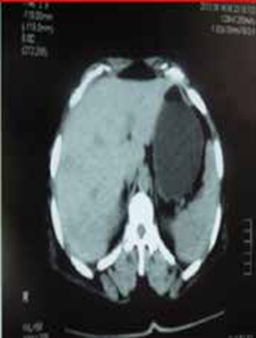
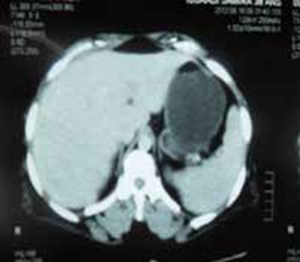
La tomodensitométrie abdominale avec opacification confirmait cette cholécystite avec un foie hétérogène, siège de multiples microlésions arrondies hypodenses, rehaussées légèrement après injection de produit de contraste (Figures 3, 4).
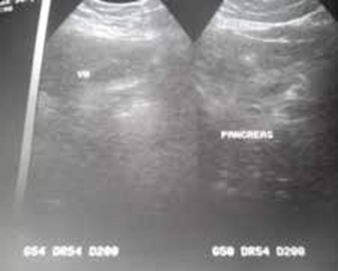
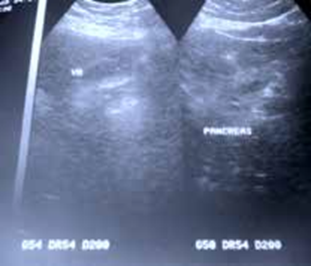
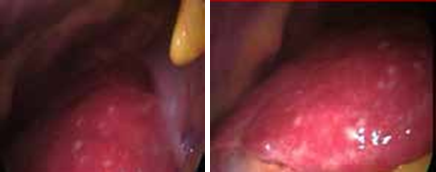
Une cœlioscopie réalisée a montré de multiples granulations blanchâtres disséminées dans la totalité du foie, le reste de l’exploration était sans particularité (Figures 6 ,7). Une cholé-cystectomie associée à une biopsie hépatique objectivant une granulation blanchâtre, ont été réalisées.
L’examen histologique de la pièce opératoire est celui d’une cholécystite chronique en poussée aiguë post-lithiasique, alors que la biopsie hépatique montrait un parenchyme hépatique siège d’une surcharge stéatosique modérée avec la présence de 3 follicules épithélio-giganto-cellulaires sans nécrose caséeuse (Figure 8).
Le bilan étiologique de la granulomatose hépatique comportant : les Ac anti-HVC, les Ac anti-mitochondries M2, une électrophorèse des protéines, un dosage de l’enzyme de conversion, une radiographie pulmonaire, une endoscopie digestive, était négatif.
L’intradermoréaction à la tuberculine était positive (phlycténulaire) à 12 mm. La recherche du BK par l’examen direct et culture sur les biopsies et liquides gastriques, était négative.
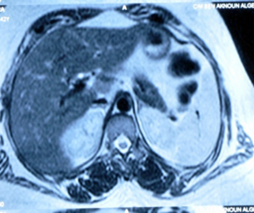
L’IRM abdominale objectivait des micronodules hépatiques iso-intenses T1-T2 évocateurs des séquelles tuberculeuse, sarcoïdose, autres.
Après l’intervention, nous avions constaté l’apparition d’adénopathies cervicales bilatérales ovalaires, dures et indolores dont la cytoponction confirmait la nature tuberculeuse des granulations hépatiques (Figure 8). La patiente a été mise sous traitement antituberculeux avec une surveillance clinique et biologique mensuelle. Nous avions constaté la disparition du syndrome inflammatoire au bout de quelques semaines, suivie de la disparition des adénopathies et des nodules hépatiques plus tard.

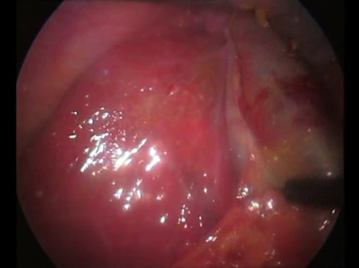
Discussion
La tuberculose hépatique est retrouvée souvent dans le cadre d’atteinte multi-viscérale, rarement sous la forme isolée surtout chez un patient immunocompétent [1, 2]. Elle pose un véritable problème diagnostic même en zone d’endémie à cause de son aspect aspécifique, des signes cliniques, biologiques et radiologiques [3].
Elle associe habituellement fièvre, altération de l’état général, amaigrissement, parfois hépatomégalie avec ou sans ictère [4, 5]. Chez notre patiente la découverte était fortuite.
Sur le plan biologique, le syndrome inflammatoire est présent dans 50 % des cas et peut être associé à une cholestase anictérique dans 29 % des cas [3, 4, 6]. Les réactions tuberculiniques sont souvent positives. La mise en évidence de BK sur les biopsies par l’examen direct ou par culture est positive dans 50 % des cas [7], alors que l’amplification du BK par PCR au sein des prélèvements en matière de tuberculose hépatique n’est pas encore décrite dans la littérature. Dans notre cas, le syndrome inflammatoire est associé seulement à une réaction tuberculinique fortement positive.
L’apport de l’imagerie est intéressant, mais peu spécifique et la forme micronodulaire ou la miliaire hépatique (petits nodules hypo-échogènes hypodenses avec et sans prise de contraste) est la forme radiologique la plus fréquente [7]. À l’échographie, les nodules ne sont pas toujours visualisés. Dans notre observation, les lésions étaient peu comparables à celles décrites dans la littérature.
L’histologie est centrée par la présence de granulomes épithélioïdes et gigantocellulaires, dont l’aspect n’est pas spécifique. La caséification est présente dans la quasi-totalité des cas [8]. Chez notre patiente la caséification est absente et les follicules épithélio-giganto-cellulaires baignent dans un parenchyme stéatosique.
Le diagnostic est donc histologique et/ou bactériologique. Par ailleurs, le diagnostic est souvent posé sur la coexistence de la granulomatose hépatique avec une autre localisation évocatrice, en particulier pulmonaire. C’est celui que nous avons rencontré, mais la localisation évocatrice était ganglionnaire et non pulmonaire. Enfin, l’existence d’une hépatite granulomateuse isolée, en particulier s’il existe des manifestations générales, peut conduire à un traitement d’épreuve qui confirme le diagnostic.
Selon les recommandations de l’OMS, le traitement des localisations extra-pulmonaires sans atteinte du SNC repose sur une quadrithérapie antituberculeuse pendant 02 mois, suivi d’une bithérapie pendant 04 mois dont l’utilisation incite à une vigilance particulière dans le contexte de perturbation biologique hépatique [9, 10].
Conclusion
La Tuberculose Hépatique Primitive est rare, son diagnostic repose essentiellement sur l’examen histopathologique des fragments biopsiques obtenus par biopsie hépatique, réalisé lors de la laparoscopie ou la ponction transpariétale guidée. Son évolution est généralement favorable sous traitement médical spécifique..
Références
- Ilboudo D, Sawadogo A, Drabo Y. (2004) La tuberculose hépatique. A propos d’un cas chez un sujet immuno-compétent. Med Afr Noire 51: 524–6
- Pelletier G. (1998) La tuberculose hépatique. Hépato-Gastro5: 409–14.
- Sanchez-Tapias JM. Tuberculose hépatique. In: Benhamou JP, Bircher J, Mc Intyre N, Rizzeto M, Rodes J eds. Hépatologie clinique. Paris: Flammarion, 1993: 688-689.
- Patanakar T, Prasad S, Armao D, Mukherji S. Tuberculous abscesses of the liver. AJR 2000, 174 : 1 166-7.
- Kok Kyy Yapp SKS. Isolated hepatic tuberculosis: report of five cases and review of the literature. j Hepatobiliary Pancreat Surg 1999, 6 :195-8.
- Cherki S, Cotte E, Boibieux A, Baulieux J, Adham M. (2006) Tuberculose hépatique un cas à forme pseudo-tumorale. Gastroenterol Clin Biol 11:1317– 20 chez un malade immunocompétent. Aspect clinique et radiologique. Gas- troenterol Clinbiol1996; 20 :913-4.
- Amaris J, Kardache M, Soyer P, Lalande F, Boudiaf M, Scherrer A, et al. Aspects radiologiques du tuberculome hépatique. Gastroenterol Clin Biol 1997; 21 :888-92.
- Jorge AD. Peritoneal tuberculosis. Endoscopy 1984; 16:10-2.
- Maher D, Chaulet P, Spinaci S, Harries A. Le traitement de la tuberculose: principes à l’intention des programmes nationnaux. 2nd. Genève, Suisse: WHO/TB /97.220.
- Bouvet E, Abiteboul D, Antoun F, Bessa Z, Billy C, Dautzenberg B, et al. Prévention et prise en charge de la tuberculose en France. Synthèse et recom- mandations du groupe de travail du Conseil Supérieur d’Hygiène Publique de France (2002-2003). Rev Mal Respir 2003; 20 :7S1-105
Post-surgical functional prognosis of open fractures of the distal femur: Experience of the Orthopedic and traumatology surgery department, Yopougon University Hospital, Abidjan, Ivory Coast
. V. FEIGOUDOZOUI 1, T. MEMPANOU 2, K. D. SOUMARO 1,P. DOGOSSOU 1, E. V. M. AKA KOUAME 1, J.-B. SIE-ESSOH 1 ;Service de Chirurgie Orthopédique et Traumatologie, CHU Yopougon, Abidjan, Côte-d’Ivoire,Département d’Epidémiologie, Université de Maryland, Ecole de Médecine, Etats-Unis.
Abstract
Objective : Contribute to improving the prognosis of open fractures of the distal femur. Methods : This is a 5 years retrospective study from January 2017 to December 2021. Were included all open fractures of the distal femur. Before 2018, 10 osteosynthesis of fractures were performed by Kirschner wires, simple condylar plate and external fixator. As of 2018, 6 osteosynthesis of fractures were performed by LCP and DCS condylar screw-plate. The fracture line was classified according to Chiron. The skin opening was classified according to Gustillo. The results were evaluated according to the score of the Association for the Study and the Application of the Method of Ilizarov (ASAMI). Results: Sixteen patients were retained including 11 men. The average age was 35.5 years (range: 18 and 72 years). According to Gustillo’s classification, there were 10 type II lesions. Three fractures were classified type I-4 and type II-5 according to the Chiron classification. Osteosynthesis were first performed using an external fixator (8) then osteosynthesis were performed by LCP (5) or DCS condylar screw-plate (1). According to the ASAMI score, 8 patients functionally performed very well. Conclusion: The functional prognosis of open fractures of the distal femur was influenced by the type of fracture line, the skin opening, and the quality of the implant used. The functional results were improved with the use of AO system implants.
Keywords : Abidjan, femur, fracture, prognosis, open.
Résumé
Objectif : Contribuer à l’amélioration du pronostic des fractures ouvertes du fémur distal. Méthodes : Il s’agit d’une étude rétrospective s’étalant sur une période de 5 ans allant de janvier 2017 à décembre 2021. Etaient incluses, toutes les fractures ouvertes du fémur distal. Avant 2018, 10 ostéosynthèses de fractures étaient réalisées par broches de Kirschner, plaque condylienne simple et fixateur externe. A partir de l’année 2018, 6 ostéosynthèses de fractures étaient réalisées par LCP et visplaque condylienne DCS. Le trait de fracture était classé selon Chiron. L’ouverture cutanée était classée selon Gustillo. Les résultats étaient évalués selon le score de l’Association for the Study and the Application of the Method of Ilizarov (ASAMI). Résultats : Seize patients étaient retenus dont 11 hommes. L’âge moyen était de 35,5 ans (extrêmes : 18 et 72 ans). Selon la classification de Gustillo, il y avait 10 lésions de type II. Trois fractures étaient classées type I-4 et type II-5 selon la classification de Chiron. Les ostéosynthèses étaient d’abord réalisées par fixateur externe (8) puis par LCP (5) ou visplaque condylienne DCS (1). Selon le score de l’ASAMI, au plan fonctionnel, 8 patients avaient un excellent résultat. Conclusion : Le pronostic fonctionnel des fractures ouvertes du fémur distal était influencé par le type de trait de fracture, l’ouverture cutanée et la qualité de l’implant utilisé. Les résultats fonctionnels étaient améliorés grâce à l’utilisation des implants du système AO.
Mots-clés : Abidjan, fémur, fracture, pronostic, ouverte.
Introduction
Le fémur distal est le segment du fémur compris entre le tiers inférieur en haut et les condyles en bas [1]. Une fracture ouverte est une solution de continuité associée à une plaie cutanée qui communique avec le foyer de cette fracture. Les fractures du fémur distal sont souvent complexes et peu fréquentes [2, 3]. L’existence d’une ouverture cutanée constitue un facteur de gravité. Les fractures du fémur distal représentent un grand challenge [4]. Le traitement est un parage suivi d’ostéosynthèse par fixation externe, clou ou plaque. L’intérêt du traitement chirurgical est de permettre une rééducation précoce. Les implants tels la plaque à compression de Judet-Letournel et ceux du système AO (LCP-Locking Condylar Plate, la Vis-plaque DCS-Dynamic Condylar Plate) ont permis à d’autres praticiens selon leur plateau technique d’obtenir des résultats satisfaisants [1, 5]. Le pronostic fonctionnel dépend de la quali- té du montage et des résultats de la rééducation [6]. Mais une infection locale peut retarder le démarrage de la rééducation. De même, une réduction imparfaite influence les résultats de la rééducation à travers la mauvaise qualité de la consolidation qui s’en suit [7]. La récupération des mouvements du genou garantit un excellent résultat et ainsi un meilleur avenir socio-professionnel. Le pronostic fonctionnel concerne les sujets jeunes. Chez les sujets âgés, le pronostic est vital [6, 8]. Le but de cette étude était de contribuer à l’amélioration du pronostic des fractures ouvertes du fémur distal.
Méthodes
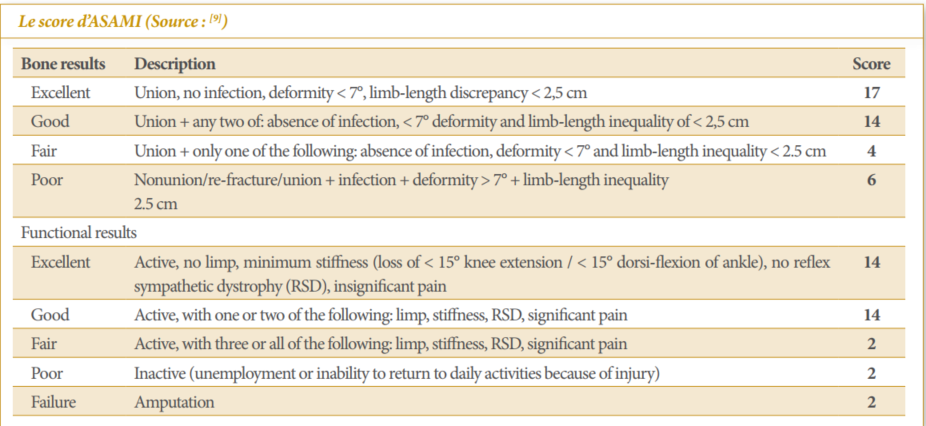
Cette étude rétrospective et monocentrique couvrait la période allant de janvier 2017 à décembre 2021. Elle portait sur tous les dossiers des patients traités dans le service pour fractures ouvertes du fémur distal. Les dossiers incomplets et les patients perdus de vue n’étaient pas inclus. L’ouverture cutanée était classée selon Gustillo-Anderson et le trait de fracture selon Chiron [1]. Tous les patients avaient subi un parage suivi d’ostéosynthèse. La reprise chirurgicale n’était pas nécessaire dans tous les cas. La durée de l’étude était répartie en deux périodes. La première période s’étalant de janvier 2017 à décembre 2018 durant laquelle, 10 ostéosynthèses de fractures étaient réalisées par broches de Kirschner, plaque visée et fixateur externe. La seconde période s’étalant de janvier 2019 à décembre 2021 pendant laquelle 6 ostéosynthèses de fractures étaient réalisées par LCP ou vis-plaque condylienne DCS. Les interventions chirurgicales s’étaient déroulées sans difficultés particulières. Le recul minimum retenu était de 34 mois. Les résultats étaient évalués selon le score de l’Association for the Study and the Application of the Method of Ilizarov (ASAMI) [9, 10]. Le score de l’ASAMI est un score américain d’évaluation du genou qui est constitué de 2 composantes : la consolidation et la fonction du membre. Cette étude expose seulement les résultats de la composante fonctionnelle du membre. Le Logiciel Epi Info avait servi à l’analyse des données.
Résultats
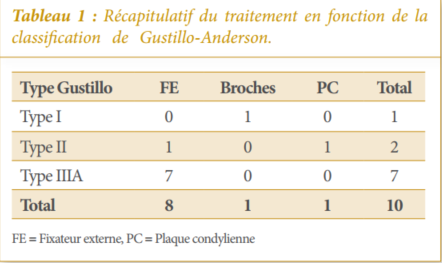
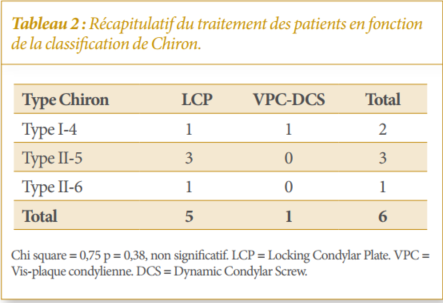
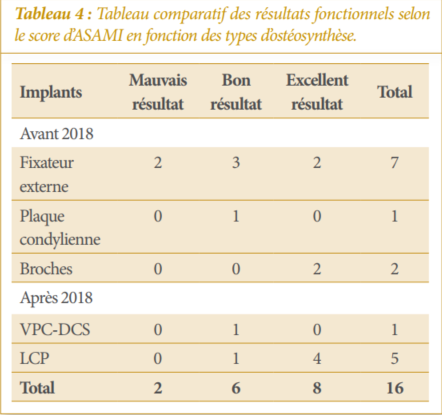
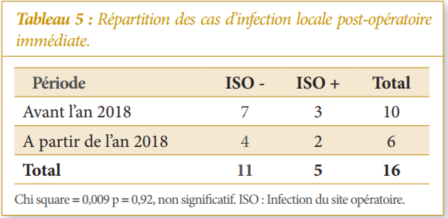
Seize patients avec 16 fractures ouvertes du fémur distal étaient retenus dont 11 hommes et 5 femmes, d’âge moyen de 35,5 ans (extrêmes : 18 et 72 ans). Les résultats pertinents sont exposés dans les Tableaux 1, 2, 3 et 4 et illustrés par les Figures 1, 2 et 3.
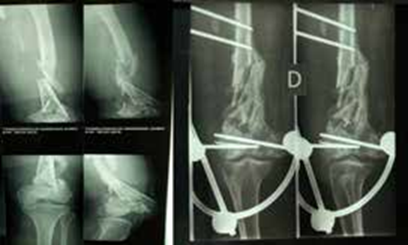
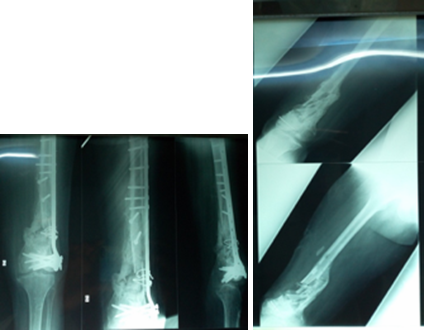


Discussion
Dans cette étude, la taille de l’échantillon était petite. Elle n’avait donc pas permis de tirer des conclusions convaincantes. Toutefois, devant la rareté des études sur le sujet, cette étude garde son importance de manière spécifique.
Dix patients avaient une lésion type II de Gustillo. La violence des traumatismes était à l’origine de ce type d’ouverture cutanée. Plusieurs auteurs avaient également retrouvé dans leurs études des fractures ouvertes dues à un traumatisme de haute énergie [4, 11-13]. L’ouverture cutanée serait due à un traumatisme de haute vélocité. Cependant, cette étude avait relevé que l’ouverture cutanée était à l’origine de l’infection du site opératoire (ISO) en cas d’un parage insuffisant. Une fracture ouverte peut s’accompagner de perte de substance cutanée. En fonction de son étendue, la perte de substance cutanée peut également exposer l’os à un problème de couverture cutanée. Dans cette étude, 3 patients du groupe IIIA de Gustillo s’étaient retrouvés avec une perte de substance cutanée après le parage. La récupération était obtenue par cicatrisation dirigée (2) et lambeau fascio-cutané (1) sous fixateur externe.
Les infections du site opératoire (ISO) incluent toute infection sur le site opéré, survenant dans les 30 jours suivant l’intervention ou dans l’année s’il y a eu mise en place d’un implant ou d’une prothèse [14]. En servant de porte d’entrée pour les germes, l’ouverture cutanée favorise l’installation d’une ISO. Du fait du retard dans le délai de parage, l’éventuel germe présent dans la plaie peut alors se multiplier. Après le parage, le germe peut parfois persister entrainant une ISO. Cinq patients avaient développé une ISO. Ces infections étaient jugulées grâce à des pansements avec lavages au sérum physiologique. Néanmoins, un prélèvement du pus suivi de culture et antibiogramme étaient réalisés chez 2 patients. La bactérie retrouvée était inhabituelle dans le service (Pseudomonas aeruginosa).
Afin d’obtenir la guérison de l’ISO, certains praticiens étaient contraints de reprendre leurs patients au bloc [4, 15], voire procéder à une amputation transfémorale [16]. Dans cette étude, l’ISO avait indirectement influencé le pronostic fonctionnel des fractures ouvertes du fémur distal en retardant le démarrage de la rééducation. Cette situation avait favorisé le développement des 2 cas de légère raideur du genou. L’intensification de la rééducation avait permis de récupérer les amplitudes anatomiques des genoux.
Avant l’an 2018, les implants utilisés étaient les broches, la plaque condylienne ou le fixateur externe. Avec ces implants, les résultats du traitement n’étaient pas assez satisfaisants. Ainsi, l’idée était de choisir en première intention les Vis-plaque condyliennes DCS et les LCP. Les résultats étaient alors très satisfaisants chez les 6 patients opérés. Plusieurs auteurs avaient également obtenu des résultats satisfaisants avec les implants du système AO [11, 12, 17]. Dans cette étude, faute de moyens financiers, les 10 premiers patients ne pouvaient pas acheter les implants AO. Cette particularité exceptionnelle expliquait pourquoi les résultats de cette étude étaient moins satisfaisants avant l’an 2018. En outre, il importe de souligner l’efficacité des implants du système AO dans la réduction peropératoire des fractures. Cette efficacité était également confirmée par les résultats de cette étude. Cependant, les complications à type de raideur du genou existent [18]. Dans cette étude, 4 patientsavaientcommencé leurrééducationaprès le premier mois du post-opératoire. Quatre autres avaient commencé la rééducation durant la première semaine du post-opératoire. Les résultats de la rééducation des 2 cas de raideur du genou étaient proches de ceux de Manou et al. [19]. Pour une raideur légère du genou l’attitude était de tenter une récupération par la rééducation [7].
Conclusion
L’ISO et la raideur du genou sont des facteurs qui influencent le pronostic fonctionnel des fractures ouvertes du fémur distal au CHU de Yopougon, Abidjan, Côte d’ivoire. Ces deux facteurs sont liés au trait comminutif et l’ouverture cutanée de la fracture. Le pronostic est bon lorsque la prise en charge est rigoureuse et devant l’utilisation d’implants du système AO. La mise en évidence de l’amélioration des résultats fonctionnels dans cette étude était une expérience pertinente. Cette expérience permet d’évoquer la possibilité d’une autre étude avec un échantillon suffisant afin de démontrer l’efficience de ces nouveaux implants au fémur distal.
Références
- P. Chiron. Fractures de l’extrémité inférieure du fémur de l’adulte. EMC (Elsevier Masson SAS, Paris), Ap- pareil locomoteur. 2009; 14-080 : A-10.
- M.L. Kanoun, M. Chebil, M. Ben Maitig, H. Ayadi, N. Haddad, N. Shimi, et al. Results of unicondylar femoral fractures: a review of 28 patients. Tunis Méd. 2007; 85: 586–590.
- S.M. Holmes, D. Bomback, M.R. Baumgaertner. Coronal fractures of the femoral condyle: a brief report of five cases. J Orthop Trauma 2004; 18 :316–319.
- G. Lamraski, D. Toussaint, J. Bremen. Traitement chirurgical des fractures de l’extrémité inférieure dufémur par ostéosynthèse extra-médullaire. Acta Orthopaedica Belgica. 2001 ; 67(1) : 32 – 41.
- E.J.B. Sié, C.A. Mobiot, A. Traoré, Y. Lambin. Distal femoral fractures treated with condylar buttress plate in West African hospital. J Clin Orthop Trauma. 2012 ; 3 : 98-102.
- L. Béguin, F. Chalençon, M.H. Fessy. Fracture de l’extrémité distale du fémur : place du traitement orthopé- dique. Springer. 2005. 6 : 143-146.
- G. Le Blay. Raideur après fractures autour du genou. Traitement non chirurgical (ou conservateur) et pré- vention : Conduite à tenir devant les raideurs postopératoires du genou. Rev Chir Orthop et Rép App Loc. 2002 ; 88(5) : 39-41.
- M. Ehlinger, G. Ducrot, P. Adam, F. Bonnomet. Fractures du fémur distal : technique chirurgicale et revue de la littérature. RCOT. 2013 ; 99 : 304-312.
- S. Patil, R. Montgomery. Management of complex tibial and femoral nonunion using the Ilizarov tech- nique, and its cost implications. J Bone Joint Surg [Br]. 2006; 88-B : 928-932.
- B. J.-D. Tekpa, A. Doui-Doumgba, H.V. Feigoudozoui, L. Nghario, P.A Issa-Mapouka, M.N. Nali. Epi- démiologie et prise en charge des pseudarthroses diaphysaires de jambe à propos de 104 cas traités selon un algorithme précis en milieu précaire. RCOT. 2018; 104 :193-7.
- J.-C. Bel, C. Court, A. Cogan, C. Chantelot, G. Piétu, E. Vandenbussche et coll. Les fractures uni-condy- liennes du fémur distal. 2014; 100 : 628-632.
- W. Bouaziz, Z. Ellouze, R. Guidara, A. Abid1, M. Zribi1, H. Keskes. Fractures uni-condylienne du fémur : étude rétrospective de 26 cas. J.I. M. Sfax. 2018 30 : 39-48.
- Jerbi, Sabri M, Msakni A, Khalil H, Hédi A, Trabelsi M. Prise en charge chirurgicale des fractures sus et intercondyliennes du fémur : à propos de 150 cas. Rev Chir orthop Trauma. 2016. 102:797-798.
- O. Abdoulaye, M. L. Harouna Amadou, O. Amadou, O. Adakal, H. M. Larwanou, L. Boubou, D. Ou- marou, M. Abdoulaye, S. Mamadou. Aspects épidémiologiques et bactériologiques des infections du site opératoire (ISO) dans les services de chirurgie à l’Hôpital National de Niamey (HNN). Pan Afr J. 2018 ; 31 :33 doi: 10.11604/pamj. 2018.31.33.15921.
- H. Redouane, B.A. Mohamed, B. Moncef, K. Mohamed, S.B. Mohamed. Intérêt du clou rétrograde dans les fractures dufémur distal : àpropos de 07 cas. PanAfricanMedical Journal. 2018; 31 :73.
- B.J.L.N. Sery, J.E. Kouassi, L.B. Yao, K.I. M’Bra, A.N.A. Kouassi, M. Kodo. Fractures du fémur distal : Ré- sultats des traitements. Rev int sc méd Abj. 2019; 21,4 :342-345.
- P. Hoffmeyer, R. Peter, D. Fritschy. Fracture de l’extrémité inférieure dufémur de l’adulte. Encycl Méd Chir (Editions Scientifiques et Médicales Elsevier SAS, Paris, tous droits réservés), Techniques chirurgicales – Or- thopédie – Traumatologie, 44-800, 2001, 11 p.
- E. Vandenbussche, M. LeBaron, M. Ehlinger, X. Flecher, G. Pietu, La SOFCOT. La lame-plaque pour l’ostéosynthèse des fractures supra-, sus- et intercondyliennes du fémur de l’adulte : une étude cas-témoin Blade-plate fixation for distal fractures : A case-control study. Rev Chir Orthop Trauma. 2018; 100 : 413-417.
- B. Manou K, D. Alloh A., B. Nandjui M., A.M. Datie, J. Bombo, B. Soumahila S. Conséquences fonc- tionnelles et socio-professionnelles des fractures des membres inférieurs vues en médecine physique et de réadaptation d’Abidjan. J. Réadapt. Méd. 2004; 24(1-2) : 32-34.
Centralized reconstitution unit for cytotoxic drugs: what organization?
Y. BOUYAKOUB1, N. MOUSSAOUI2 ;Faculté de Médecine de Tlemcen, Université Abou Bekr Belkaid, Faculté de Médecine d’Oran, Université Oran 1, Centre Hospitalo-Universitaire d’Oran.
Abstract
Cytotoxic drugs may present potential risks to the health staff called to manipulate them without special precautions. Exposure to these substances can occur at all steps of use in hospital, especially during preparation, waste management and administration to the patient. The success of cancer treatment will depend largely on the important phase that’s the reconstitution of cytotoxic drugs before administration to the patient. This step is very important to the guarantee of sterility of injected products and the preservation of the quality of these highly reactive products. Based on biblio- graphic data, we try to propose a typical scheme of different investments (structure, staff, training …) that can be set up to create a centralized reconstitution unit of cytotoxic drugs in order to guarantee stable, effective and safe preparations.
Keywords : Cytotoxic drugs, centralized reconstitution unit, quality, security.
Résumé
Les médicaments cytotoxiques peuvent présenter des risques potentiels pour le personnel de santé appelé à les manipuler sans précautions particulières. L’exposition à ces substances peut se produire à toutes les étapes d’utilisation à l’hôpital, no- tamment lors de la préparation, la gestion des déchets et l’ad- ministration au patient. Aussi, le succès d’un traitement contre le cancer dépendra largement d’une phase importante qui est celle de la reconstitution des médicaments cytotoxiques avant leur administration au patient. Cette étape est très importante pour la garantie de stérilité des produits injectés et la préservation de la qualité de ces produits hautement réactifs. À partir de données bibliographiques, nous tentons de propo- ser un schéma type de différents investissements (structure, personnel, formations…) pouvant être mis en place afin de créer une unité de reconstitution centralisée des médicaments cytotoxiques dans le but de garantir des préparations stables, efficaces et sûres.
Mots-clés : Cytotoxiques, unité de reconstitution centralisée, qualité, sécurité.
Introduction
La chimiothérapie connaît un développement considérable dans le traitement des cancers depuis quelques décennies grâce à une meilleure maîtrise des protocoles et à la découverte de molécules innovantes [1]. Face à cette augmentation, les effets constatés lors de la manipulation de ces substances
hautement réactives ont été largement décrits. Aussi, la reconstitution des anticancéreux constitue un enjeu de santé publique à la fois en termes de protection du personnel, de l’environnement et de la sécurité du patient, par la qualité de la préparation administrée [1].
Contexte
Les agents anticancéreux sont des molécules à haut risque, qui présentent des dangers particuliers; en effet, ces médicaments ont généralement une marge thérapeutique étroite avec une toxicité élevée; de plus, les protocoles de chimiothérapie sont souvent complexes et leur administration nécessite parfois le recours à des voies d’injection à risque (intrathécale, intra-ar- térielle) sans toutefois oublier le fait que les patients souffrant de cancer représentent une population fragile avec une faible tolérance [2]. Ainsi, les erreurs de médicaments en oncologie ont souvent des répercussions sérieuses, c’est pourquoi, des protections supplémentaires doivent être mises en place au niveau des sites de manipulation des agents anticancéreux [3]. La centralisation de la reconstitution des anticancéreux au niveau de la pharmacie d’un établissement de santé, précisé- ment dans des zones de travail confinées et stériles, s’impose comme la pratique de référence pour limiter les risques d’une contamination chimique pour le personnel soignant qui les manipule, mais surtout afin d’éviter la iatrogénie médicamen- teuse vis-à-vis des patients traités ; cette pratique aboutira à une augmentation de la qualité du produit délivré sans éven- tuelles contaminations microbiennes et qui permettra de plus, de mutualiser les ressources nécessaires à la production des chimiothérapies en milieu hospitalier [2].
Risques iatrogènes liés à la préparation des médicaments anticancéreux à l’hôpital.
Une étude française a enregistré 115 prescriptions comportant une ou plusieurs erreurs sur un total de 5000 ordonnances [4]. Par ailleurs, une étude américaine met en évidence un taux global de non-conformité de 9 %, dont 2 % d’erreurs graves (conséquences cliniques potentielles). Ces dernières concernent la dose du médicament (69 % et 37 % des ano- malies avec des seuils respectifs de 5 à 10 % de la dose) [5]. Le calcul de la dose et la préparation de la dose adéquate sont des étapes cruciales.
Une étude espagnole, portant sur 4734 préparations de cytos- tatiques montre un taux global d’erreurs de 1,99 %, dont 47 % concernent l’étiquetage [6]. Très récemment, l’incidence des erreurs en fabrication est estimée respectivement à 10,6 % (4 % hors présence bulles d’air) et 3,1 % par deux équipes françaises indépendantes [7, 8].
Médicaments cytotoxiques : quelles condi- tions de sécurité ?
En pratique et en ce qui concerne les médicaments cyto- toxiques, il existe un regroupement de deux classifications, aboutissant à trois niveaux d’exposition à prendre en termes de locaux, d’équipements, de matériels et de protections individuelles. Il est possible de les classer par des critères subjectifs mais également par calcul de l’indice de contact cytotoxique (ICC) [1] :
- Le niveau I : ICC < 1 correspond à la préparation et l’admi- nistration occasionnelles. Dans ce cas, un ensemble de pré- cautions minimales doit, faute de mieux, être mis en place.
- Le niveau II : 1 < ICC < 3 correspond à la préparation et l’ad- ministration de niveau modéré. Dans ce cas, une unité de re- constitution centralisée des cytotoxiques est souhaitable. Faute de mieux, la reconstitution doit être faite dans des locaux iso- lés, spécialement prévus à cet effet. Ces dispositions s’ajoutent aux recommandations minimales prévues pour le niveau I.
- Le niveau III : ICC > 3 correspond à la préparation et à l’admi- nistration de façon intensive et de routine. Ce niveau justifie une unité de reconstitution centralisée équipée soit d’un isolateur, soit d’une ou de plusieurs hottes à flux d’air laminaire vertical.
La physiopathologie des rhinosinusites repose sur l’œdème de la muqueuse qui au début est le résultat d’une implication multifac- torielle : l’inflammation – l’infection virale ou bactérienne – l’al- lergie nasosinusienne – la pollution de l’environnement – le taba- gisme actif surtout mais passif également. Cet œdème entraine un blocage et une obstruction des ostiums sinusiens (orifices de drainage). Ceblocage anatomo-fonctionnel entraîne une hypoxie muqueuse qui génère à sontour un œdème contribuant ainsi à la pérennisation de l’œdème de la muqueuse rhinosinusienne.
Préparation centralisée des chimiothérapies : quelle approche ?
La mise en place d’une unité centralisée de fabrication de chimiothérapie est une démarche complexe, qui nécessite une approche par processus, de la prescription à l’administration. Un groupe de travail multidisciplinaire doit être créé afin de décider de l’organisation du circuit, qui doit répondre à trois critères : qualité, sécurité et efficience [2].
La démarche consiste àcartographier et àséquencer les processus en vue de réaliser une analyse de risque. Cette analyse permet de déterminer, de prioriser et de sécuriser les points critiques [2].
La non-diffusion d’anticancéreux dans l’environnement doit être l’idée clé guidant la mise en place de matériels, de procé- dures, d’une démarche de qualité afin de prévenir ce risque [3].
A- Les locaux
L’unité, qui constituera un noyau indépendant, pourra se situer dans les services de soins spécialisés, ou mieux, au sein du service de la Pharmacie Hospitalière, à condition que la gestion du transport des thérapeutiques soit organisée dans le respect des règles d’hygiène et de confidentialité [10].
La préparation proprement dite, puisque aseptique, devra être ef- fectuée dans une zone à atmosphère contrôlée (ZAC) : isolateur ou salle protégée munie d’une ou de plusieurs hottes à flux laminaire vertical [11, 12].
Un investissement en locaux se traduit tout d’abord par une architecture appropriée, devant rassembler plusieurs locaux contigus [3] (Figure 1), notamment :
- Le local de travail externe : ce local est réservé à l’acte pharmaceutique et comprend entre autres la documentation (thésaurus des protocoles de chimiothérapie, bibliographie, manuel assurance qualité…), le dossier patient et le système informatique. Un SAS de communication doit être aménagé entre le local des préparations et le local de travail externe per- mettant le transfert des produits finis tout en évitant la conta- mination des locaux ;
- Le local de stockage : qui sert au stockage des matières ;
- Le SAS des matières : dédié au transfert des produits entre le local de stockage et le local de préparation et inversement ;
- Le SAS du personnel : ce dernier est divisé en deux zones et sert pour la zone « sale » au déshabillage et au lavage des mains et pour la zone « propre » à l’habillage stérile. Un SAS doit être aménagé et est équipé d’un point de lavage avec alimentation par commande fémorale ou coude voire à déclenchement au- tomatique ;
- Le SAS des déchets : ce local est dédié à l’évacuation des dé- chets du local de préparation vers l’extérieur du secteur ;
- Le local de préparation : est réservé à la préparation stérile proprement dite, soit sous hotte à flux vertical ou bien en isola- teur. L’aménagement de ce local doit être conforme aux lignes directrices des bonnes pratiques en vigueur et comprend no- tamment :
- Des surfaces lisses, inertes chimiquement, des angles arron- dis; toutes les surfaces (murs et sols, plans de travail, etc…) sont conçues pour éviter les risques d’adsorption ou de fixation des produits à risque, ainsi que pour faciliter leur nettoyage;
- La cascade de pression entre ces différents locaux est de 12,5 à 15 Pa permettant d’éviter la contamination des autres locaux de travail et de garantir la stérilité du produit fini;
– Les contaminations microbienne et particulaire sont contrôlées. La hotte à flux d’air laminaire doit être dotée d’un schéma de ventilation correspondant à celui des postes de sécurité micro- biologique (PSM) de type II avec un système de régulation des débits avec alarme [13].
Il faut souligner que, l’atmosphère contrôlée est de classe A sous la hotte et sous isolateur [3].
En ce qui concerne les SAS et la salle de préparation, la zone d’atmosphère contrôlée doit être de classe C et pour ce qui est du local de travail externe et le local de stockage, les atmosphères ne sont pas obligatoirement contrôlées [3, 14].
| Local de travail externe | Local de stockage | SAS personnel | |
| SAS matière | |||
| Local de préparation muni de : . Une ou plusieurs hottes à flux vertical . Un ou plusieurs isolateurs | SAS déchets | ||
| Figure 1 : Proposition de l’architecture d’une unité de reconstitution centralisée des médicaments cytotoxiques. | |||
B- Le personnel
La maîtrise des flux (personnel, produits et informations) participe à cette gestion des risques [3].
Ces opérations, en tant que préparations magistrales, sont réglementairement placées sous la responsabilité du pharma- cien hospitalier [9].
Le nombre de personnes en ZAC doit être limité; le mouve- ment des opérateurs doit être mesuré et méthodique [3].
Tout le personnel travaillant dans de telles unités doit avoir droit à une formation continue et à des contrôles médicaux périodiques. Son habillage et son comportement au sein de l’unité de reconstitution centralisée des cytotoxiques doivent être réglementés, excluant le port de montre, bijoux, maquil- lage et lui interdisant de manger et de fumer [15].
C- La préparation proprement dite
Elle doit répondre en tout point aux normes mentionnées dans le guide des Bonnes Pratiques de Préparation et en par- ticulier au chapitre 6 « Préparations de médicaments stériles » et au chapitre 7 « Préparations de médicaments contenant des produits à risque ou particulièrement dangereux pour le personnel ou l’environnement » [3, 14].
En effet, il est recommandé de séparer les préparations dange- reuses des préparations non dangereuses, soit dans des locaux différents, soit sur des appareils différents, soit en fonctionnant par campagne de préparation (Bonnes Pratiques de Prépara- tion – Chapitre 7.3. Locaux) [3, 14].
D- La gestion des déchets
Les déchets produits à la fin de la chaîne de préparation sont constitués principalement des flacons et ampoules de cyto- toxiques entamés ou utilisés, des seringues, des compresses et champs de préparation, c’est pourquoi, après la préparation, les déchets ne doivent pas stationner plus de 24 heures en salle de reconstitution; ils sont déposés à l’issue de chaque manipu- lation dans des conteneurs spéciaux, à fermeture inviolable [15]. Selon les recommandations de l’OMS, les déchets cyto- toxiques requièrent une destruction par incinération à une température > 1200°C[15].
Les excrétas des malades tels que urines et vomissures, peuvent être une source conséquente de contamination par ces médicaments hautement réactifs, ainsi les malades et leur entourage doivent être sensibilisés dans ce sens; le personnel de nettoyage à l’hôpital doit être vêtu correctement de manière à lui éviter tout risque de contamination [16].
Conclusion
La reconstitution des médicaments anticancéreux constitue un enjeu de santé publique. L’optimisation de la gestion de ces substances hautement réactives passe obligatoirement par l’établissement d’un plan de gestion des risques, qui permettra la sécurisation du circuit de leur préparation jusqu’à leur administration.
La centralisation de ces unités paraît faire partie intégrante de ce plan, afin de proposer un produit qui réponde aux normes qualité / sécurité. Cela permettra aussi de lutter contre le gaspillage de ces produits onéreux en effectuant une économie notable, par l’éviction ou la diminution du jet de flacons entamés.
La présence du pharmacien au sein du staff des unités cen- tralisées est indispensable afin d’atteindre les objectifs suscités.
Références
- Bouley M. Mémoire de l’école nationale de santé publique. RENNE : 2002.
- Carrez L, and al. Organisation et sécurisation du circuit des chimiothérapies : Exemple de la pharmacie des Hôpitaux Universitaires de Genève, 2014.
- Réseau régional de cancérologie de Lorraine. Cahier des charges des Unités Centrali- sées en Pharmacie pour la préparation des agents anticancéreux dans les sites du réseau, 2009.
- AUGRY F, RAVAUD R, LOPEZ I et al. Erreurs de prescription des médicaments cyto- toxiques : étude prospective de 5000 ordonnances. J Pharm Clin 1998; 17(1): 20-4.
- FLYNN E, PEARSON R, BARKER K. Observational study of accuracy in compoun- ding IV admixtures at five hospitals. Am J Health Syst Pharm 1997; 54: 904-12.
- ESCOMS M, CABANAS M, OLIVERAS M et al. Errors evolution and analysis in antineoplastic drug preparation during one year. Pharm World Sci 1996, 18(5): 178-81.
- QUACH V, HERNANDO V, COMBEAU D et al. Control evaluation of cytotoxic infusion preparations in isolator. Proc Eur Assoc Hosp Pharm 2000 : 24 (abstract 55).
- BORDET F, CRAUSTE-MANCIET S, BROSSARD D. Analyse des préparations non conformes d’une unité de préparation de cytostatiques. Proc Hopipharm 2000 : 61 (abs- tract 69).
- Basteri M.J, Dani J., Fity S. Mise en place d’une unité centralisée de préparation des cytotoxiques sous hotte à flux laminaire. Expérience de deux centres Hospitaliers du sud- est. Centre hospitalier de Bastia, Centre hospitalier de brignoles, 2002.
- Circulaire DHOS/E1 n°265 du 12 juin 2001 relative aux modalités des dispositions réglementaires applicables aux pharmacies à usage intérieur.
- Norme AFNOR-NFX 44-101. Définition et classification de la propreté particulaire de l’air et d’autres gaz.
- Norme Pr. NF EN ISO 14644-4. Salles propres et environnements contrôlés apparen- tés : conception et construction.
- Beretta M. Les postes de sécurité pour la manipulation des médicaments cyto- toxiques. Tech Hosp. 1998 ; 623 : 21-24.
- Agence nationale de sécurité du médicament. Bonnes pratiques de fabrication, Déci- sion et annexe : décembre 2013.
- Gabarda M. L’élimination par incinération des déchets liés à l’utilisation de médica- ments anticancéreux. Techniques hospitalières 1999; 633 : 32-33.
- CCLIN Sud-Ouest. Recommandations pour la manipulation des médicaments cy- totoxiques, 2002.
Acute and chronic rhinosinusitis in adults and children
S. KHAROUBI ; Service ORL et Chirurgie de la Face et du Cou, CHU Ibn Rochd, Faculté de Médecine,
Abstract
Acute and chronic rhinosinusitis are an inflammation of the mucosa of the sinus cavities, viral but especially bacterial and sometimes mycotic, evolving between 4 (acute) and 12 (chronic) weeks. It is a frequent pathology in daily medical practice and the diagnosis is based on anamnestic history and clinical examination (nasal endoscopy). Imaging (CT-scan) is a very important procedure in the diagnosis of crude, complicated forms and in the preoperative evaluation. Treatment is essentially based on probabilistic (acute forms) or specific (recurrent and chronic forms) antibiotic therapy. Minimally invasive surgery is an interesting and safety alternative (balloon plasty) in some anatomoclinical forms. It is necessary to collect the global data in relation to this pathology and to converge on a strategy of recommendations in good practices from treatment more efficient and to contain the expenses in health care.
Keywords : Rhinorrhea, rhinoscopy, facial pain, facial CT-scan, orbital complications.
Résumé
Les rhinosinusites aiguës et chroniques correspondent à une inflammation de la muqueuse des cavités sinusiennes, virale mais surtout bactérienne et parfois mycosique, évoluant entre 4 (aiguës) et 12 (chroniques) semaines. C’est une pathologie fréquente en pratique médicale quotidienne dont le diagnostic repose sur une anamnèse bien dirigée et un examen clinique précis (endoscopie nasale). L’imagerie (scanner) occupe une place importante dans le diagnostic des formes frustes, compliquées et dans l’évaluation préopératoire. Le traitement repose essentiellement sur une antibiothérapie probabiliste (formes aiguës) ou dirigée (formes récidivantes et chroniques). La chirurgie mini-invasive est une alternative intéressante (balloon plasty) pour solutionner quelques formes anatomocliniques. Il est nécessaire de colliger les données globales en rapport avec cette pathologie et de converger vers une stratégie de recommandations de bonnes pratiques pour rendre plus efficiente la prise en charge et contenir les dépenses en soins de santé.
Mots-clés : Rhinorrhée, rhinoscopie, douleurs faciales, scanner massif facial, complications orbitaires.
Introduction
Les sinus de la face sont des cavités pneumatiques creusées dans les os de la face située au pourtour de la cavité orbitaire. Chaque sinus est tapissé d’une muqueuse de type respiratoire et communique avec les fosses nasales par un ostium propre. A la naissance, seul l’ethmoïde est présent sous forme de cellules de 2 à 3 mm de diamètre au scanner. Le sinus maxillaire (opacité 3 à 4 mm) atteint ou se rapproche de celui de l’adulte vers l’âge de 10 ans, le sinus frontal : 7 à 8 ans et le sinus sphénoïdal : 6 à 7 ans.
La physiopathologie des rhinosinusites repose sur l’œdème de la muqueuse qui au début est le résultat d’une implication multifactorielle : l’inflammation l’infection virale ou bactérienne l’allergie nasosinusienne la pollution de l’environnement le tabagisme actif surtout mais passif également. Cet œdème entraine un blocage et une obstruction des ostiums sinusiens (orifices de drainage). Ceblocage anatomo-fonctionnel entraîne une hypoxie muqueuse qui génère à sontour un œdème contribuant ainsi à la pérennisation de l’œdème de la muqueuse rhinosinusienne.
Les rhinosinusites (aiguës en particulier) constituent un motif très fréquent en consultation et sont à l’origine d’une prescription importante d’antibiotiques et d’arrêt de travail. L’omnipraticien occupe une place importante dans le dispositif de prise en charge primaire (première ligne) de cette pathologie.
Le spécialiste (ORL) intervient devant les formes résistantes, récurrentes, compliquées, chroniques ou celles qui nécessitent une expertise en vue d’une solution chirurgicale (Tableau 1). Le diagnostic est simple dans les formes communes et repose sur une symptomatologie nasale plus ou moins bruyante associée à un syndrome infectieux modéré et la constatation d’une
suppuration du méat moyen à l’endoscopie. L’imagerie est indiquée dans les formes torpides, trainantes et compliquées ou chroniques comme prélude à une chirurgie.
Le traitement médical est essentiel devant toute pathologie sinusienne. Il repose essentiellement sur l’antibiothérapie probabiliste dans les formes aiguës et dirigée dans les formes chroniques (prélèvement et antibiogramme). Les soins rhinologiques (lavage des fosses nasales) sont systématiquement associés.
La chirurgie, rarement proposée en premier, n’est indiquée (en dehors des formes compliquées) qu’après une analyse détaillée des données de l’examen clinique et de l’imagerie (scanner).
PALIER 1 : Prise en charge omnipraticien
- Evaluer la symptomatologie
Fièvre, obstruction nasale, rhinorrhée unilatérale, douleurs.
- Examen clinique
Douleurs points sinusiens, examen nasal (spéculum manuel) : pus.
- Traitement
Amoxicilline 50 à 80 mg/kg/j pendant 7 à 10 jours ou Amoxicilline-Acide clavulanique 1,5 gr à 2gr/j Allergie : pristinamycine 500 mg 4 fois/j pendant 7 jours.
Paracétamol 1 à 2 gr/j. Lavage des fosses nasales.
- Contrôle 48 à 72 heures
En présentiel ou par téléphone. Bonne évolution, poursuivre le traitement (7 à 10 jours). Stagnation ou aggravation….. PALIER 2.
PALIER 2 : Prise en charge spécialisée (ORL)
- Examen endoscopique + prélèvements bactériologiques
- Ajuster le traitement (observance, ajustement).
- Contrôle 48 heures
En présentiel ou par téléphone. Bonne évolution, poursuivre le traitement (7 à 10 jours).
- Stagnation ou aggravation………………….. IMAGERIE (scanner).
Admission milieu hospitalier.
Tableau 1 : Niveaux de prise en charge des rhinosinusites par l’omnipraticien et le médecin spécialiste.
Rappels anatomo-physiologiques
Les cavités nasales ont une structure anatomique complexe, se développent au cours de l’embryogenèse et poursuivent leur développement jusqu’à l’âge adulte.
Le sinus maxillaire se développe vers le 70e jour de grossesse. A la naissance il mesure 7 x 4 x 4 mm et atteint son anatomie normale vers 15 ans.
Le sinus ethmoïdal débute son développement entre 3 et 5 mois in utéro et atteint son volume définitif vers 12 ans.
Le sinus frontal est absent à la naissance et débute son développement vers 2 ans et atteint sa taille définitive vers l’âge de 20 ans. Le sinus sphénoïdal est visible radiologiquement vers 4 ans et atteint son volume final vers 10 et 12 ans.
Le rôle des cavités sinusiennes est diversement apprécié, elles interviennent notamment dans l’amélioration, le réchauffement et l’humidification de l’air. Ces cavités augmentent la résonance de la voix, amortissent les traumatismes crânio-faciaux et contribuent à alléger le poids du massif crânien [1].
Explorations des cavités nasales et paranasales
Les cavités sinusiennes ou paranasales comportent 3 sinus pairs : maxillaires, frontaux, ethmoïdaux et un sinus impair et médian, le sinus sphénoïdal. Ces cavités sinusiennes sont tapissées d’une muqueuse de type respiratoire et se drainent dans les fosses nasales par le méat moyen (maxillaire, ethmoïde, frontal) et un orifice propre pour le sinus sphénoïdal.
Seul le sinus frontal comporte un canal propre expliquant par ailleurs la spécificité pathologique et thérapeutique de ce sinus. L’examen clinique et l’exploration de ces cavités nasosinusiennes nécessite une instrumentation et un équipement adapté.
A- Endoscopie
L’endoscopie nasale est l’examen primordial et fondamental dans le bilan diagnostique et évolutif des rhinosinusites aiguës et chroniques. Elle est réalisée au mieux par une optique rigide à 0° (4 mm pour l’adulte et 2,7 mm pour l’enfant) après une anesthésie locale (xylocaïne naphazolinée à 5 % – patients âgés de plus de 15 ans). L’endoscopie permet de voir l’état de la muqueuse (lisse, pale, hypertrophiée), la présence de polypes, la présence de sécrétions muco-purulentes, purulentes ainsi que des anomalies morphologiques (cloison nasale, cornets inférieurs et moyens).
B- Imagerie
L’imagerie occupe une place importante dans les rhinosinusites mais son indication reste codifiée et loin d’être systématique. Les radiographies standard ne sont plus de mise, elles sont irradiantes, peu précises et rarement exploitables.
Lescanner dumassif facial sans injection de contraste est l’examen de choix.
Au cours des rhinosinusites aiguës, le scanner est réalisé devant une suspicion de complications. La rhinosinusite aiguës se traduit par un niveau liquidien, une opacité totale homogène ou un épaississement muqueux supérieur à 4 mm. L’IRM est plutôt indiquée pour évaluer les complications neuro-méningées. La séquence T1 permet le diagnostic des suppurations cérébrales et les extensions extra sinusiennes. La séquence T2 est utile pour différencier une inflammation muqueuse d’une hypertrophie.
Les séquences avec injection de contraste permettent le diagnostic d’une thrombose du sinus caverneux.
Pour évaluer les complications orbitaires et crâniennes, nous avons recours au scanner avec contraste et l’IRM non injectée. Le Cone Beam peut apporter des informations intéressantes pour analyser la responsabilité dentaire dans la genèse, les récidives ou la pérennisation des rhinosinusites. Il est indiqué également pour évaluer les rhinosinusites maxillaires (Figure 1). Les rhinosinusites chroniques nécessitent un scanner non injecté surtout à titre d’évaluation pré-opératoire. Le Cone Beam renseigne sur les rapports odontogéniques et l’état du sinus maxillaire.
Les sinusites fungiques non invasives sont explorées au mieux par un scanner, tandis que les formes allergiques relèvent d’un scanner (image en double densité) ou l’IRM avec un épais- sissement fungique mucineux entouré d’une hyperplasie muqueuse. Le scanner et l’IRM injectés sont utilisés dans les formes invasives.
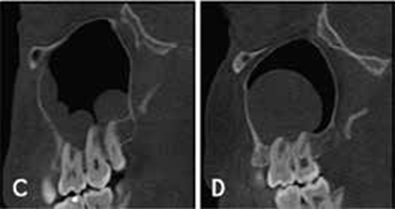
Cliché C : Polypes du sinus maxillaire. Cliché D : Pseudokyste du sinus maxillaire. (Cliché ROSADO L. )
C- Etude de la fonction mucociliaire
Le transport mucociliaire est la première ligne de défense non spécifique. L’étude de la fonction mucociliaire trouve son indication dans les rhinosinusites chroniques notamment de l’enfant.
- Etude de la clairance mucociliaire nasale : un colorant où des particules radioactives évaluent le transport mucociliaire qui doit rester inférieur à 35 minutes.
- Etude des battements ciliaires : le battement ciliaire est évalué après une biopsie de la muqueuse nasale avec examen anatomopathologique entre lame et lamelle. La fréquence est évaluée par des techniques spécialisées (stroboscopie électronique).
- Etude de l’ultrastructure des cils : examen sous microscopie électronique.
- Etude des propriétés du mucus : glycoprotéines.
D- Etude de la flore bactérienne et mycologique
- Bactériologie
Etude des prélèvements au niveau du méat moyen sous optique dans les rhinosinusites résistantes au traitement, chez un immunodéprimé, compliquées ou en cas de poussée de réchauffement des formes chroniques (Figure 2).
- Mycologie nasale
Les prélèvements sont essentiellement réalisés en peropératoire.
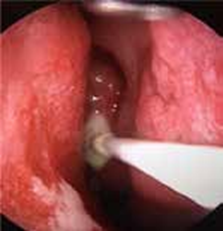
Rhinosinusites aiguës
A- Rhinosinusites aigües de l’adulte
C’est un processus inflammatoire des cavités nasales et une ou plusieurs cavités paranasales, causé par un agent externe (d’origine virale, bactérienne, fongique) pour une durée inférieure à quatre semaines.
Les rhinosinusites aiguës sont responsables de 3 millions de consultation par an aux Etats-Unis et seules 2 % sont d’origine bactérienne et nécessitent donc une antibiothérapie.
Le grand dilemme à résoudre actuellement est de pouvoir poser le diagnostic d’une rhinosinusite aiguë bactérienne afin de sélectionner les patients à placer sous antibiothérapie et éviter les résistances bactériennes (surconsommation d’antibiotiques). Cet objectif est retenu dans les recommandations des sociétés savantes sur la prise en charge des rhinosinusites aiguës (Tableau 2).
| Critères diagnostiques des rhinosinusites – Présence de deux (2) critères majeurs – Ou présence d’un (1) critère majeur et deux (2) critères mineurs |
| Critères majeurs – Présence de pus au niveau du méat sinusien moyen à l’examen (raie purulente) – Obstruction nasale – Rhinorrhée antérieure ou postérieure – Anosmie, Hyposmie – Fièvre – Douleurs ou sensation de pesanteur faciale – Rougeur de la face |
| Critères mineurs – Douleurs ou sensation de pression oreille (irritation de la trompe d’Eustache par les sécrétions nasales et nasopharyngées) – Toux – Douleurs dentaires – Asthénie – Haleine fétide – Fièvre – Céphalées |
C’est la forme la plus fréquente souvent secondaire à un coryza ou un bain surtout en piscine.
- Bactériologie : Haemophilus influenzae – Pneumocoque – Staphylocoque doré (Tableau 3).
- Signes cliniques : la symptomatologie associe deux ou plusieurs signes suivants :
- Une douleur faciale unilatérale, sous-orbitaire, pulsatile, augmentée par la position penchée en avant et les efforts de toux, accompagnée d’une céphalée diffuse.
- Une obstruction nasale unilatérale (plus significative) est souvent observée, associée à une rhinorrhée purulente parfois striée de sang du côté de la douleur.
| Bactériologie des rhinosinusites aiguës | Bactériologie des rhinosinusites chroniques |
| – Streptococcus Pneumoniae – Haemophilus Influenzae – Staphylococcus aureus – Branhamella catarrhalis – Streptocoque – Enterocoque – Anaérobies : rares (0 à 10 %) | – Staphylococcus aureus – Pseudomonas Aeruginosa ETUDES 2019 : – Pseudomonas Aeruginosa – Klebsiella species – Enterobacter species |
- L’examen clinique
La palpation déclenche une douleur à la pression de la région sous-orbitaire.
La rhinoscopie montre une muqueuse pituitaire inflam- matoire avec des cornets tuméfiés et du pus siégeant électivement dans le méat moyen (Figure 3).
Radiographie standard : en incidence Blondeau montre une opacité totale du sinus maxillaire parfois un niveau liquide. Le scanner montre une opacité totale ou surtout un niveau liquidien. L’IRM (non recommandée dans une forme aiguë) montre une image d’hypersignal du sinus maxillaire (Figures 4, 5, 6).
L’évolution sous traitement est habituellement favorable avec le retour à la normale sur le plan anatomique et fonctionnel en 3 à 6 semaines.
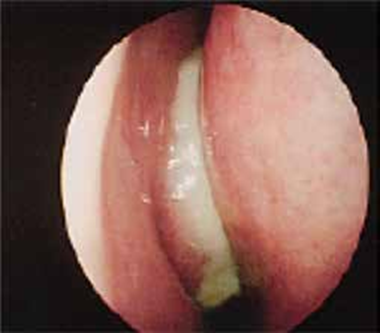
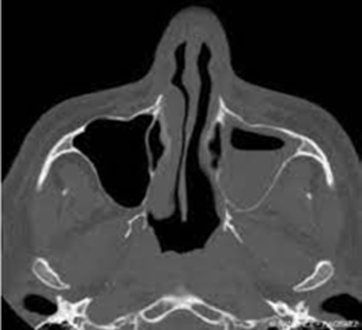
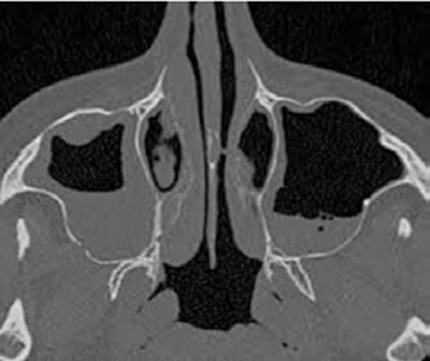
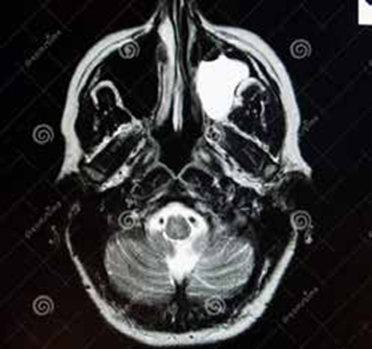
- Traitement : Il est médical et se résume essentielle- ment à l’antibiothérapie.
1- Antibiothérapie :
Elle est de type probabiliste et agit sur au moins 3 germes (Haemophilus -Pneumocoque – Moraxella) pendant 8 à 10 jours.
Dans les cas les plus habituels, on prescrit de l’amoxicilline (80 mg/Kg/j) ou l’association Amoxicilline + acide Clavulanique : 1,5 – 2 g en 3 prises pendant 10 jours. On peut recourir également à une Céphalosporine de 1ére génération : Céfadoxime, Céfixime. En cas d’allergie aux céphalosporines, on utilise les macrolides, Clari- thromycine, ou Pristinamycine [3] (Tableau 4).
| Antibiothérapie et rhinosinusites aiguës : Option 1 : Amoxicilline : Adulte 4 x 1g/j pendant 10 jours. Enfant : 70 – 80 mg/kg/ jour. Option 2 : En cas d’antibiothérapie récente ou de non-réponse au bout de 72 heures : Amoxicilline – Acide clavulanique : Adulte : 2 x 2 g/j pendant 10 jours. Enfant : 40 – 50 mg/kg/jour. Ou Céfuroxime – axétil : Adulte : 3 x 500 mg/j pendant 10 jours Enfant : 30 – 50 mg/j (dose maximale 1,5 g /j) Option 3 : En cas d’allergie on utilise les macrolides : Azithromycine Adulte 500 mg/J pendant 3 jours ou 5 jours (500 mg 1x + 250 mg 4x) Enfant : 10 mg/j (dose max. 500 mg/j). Télithromycine 800 mg/j pendant 5 jours en une prise pour adultes et enfants > 12 ans Les fluoroquinolones (Moxifloxacine, Lévofloxacine) sont administrés exceptionnellement dans cette indication. Antibiothérapie et rhinosinusites chroniques : Quinolones respiratoires Lévofloxacine 500 mg : 1 comp/jour (7 jours). Moxifloxacine 400 mg : 1 comp/j (7 jours). Amoxicilline-Acide clavulanique Fortes doses 80 mg/10 mg/kg/j. Ceftriaxone : amp 500 et 1 gr. 1 à 2 gr/j (IV). Nourrissons et Enfants 50 mg/kg/j. Amoxicilline Fortes doses 100 mg/kg/j. Cefpodoxime proxétil Adulte comp 100 mg 1 à 2 comp/j. Enfant: 8 mg/kg/j en 2 prises. Céfuroxime axétil (comp 250, 500 mg) 250 – 500 mg/j en deux prises. Enfant 10 mg/kg 2 fois/j. Cefdinir 7 mg/kg en 2 prises ou 14 mg/kg en une prise Sulfaméthoxazole – Triméthoprime comp 200/40 400/80 800/160 mg Adulte : 1 comp chaque 12 heures. Enfant : 30 mg/kg/j en 2 prises. Doxycycline comp 100 mg Adulte : plus 60 kg :100 mg 2 comp/j. Moins de 60 kg 2 comp/j le premier jour puis 1 comp/j. Enfant plus de 8 ans 4 mg/kg en 2 prises. Télithromycine 800 mg/ jour (5 jours). Macrolides Clarithromycine 250, 500 mg Adultes : 1 à 2 comp/j. |
Corticothérapie : Elle accélère la guérison en agis- sant sur l’œdème muqueux et réduit les douleurs. On utilise généralement la voie orale (prednisone 1 mg/Kg/j en cure courte 5 à 6 jours (en respectant les contre-indications habituelles).
Traitement local : Il se résume au lavage des fosses nasales au sérum physiologique (ce qui facilite le drainage des sécrétions purulentes).
Les vasoconstricteurs locaux permettent d’ouvrir les orifices méatiques sinusiens et aider donc au drainage des sécrétions. L’administration de vasoconstricteurs locaux ne doit pas dépasser 5 à 6 jours (Tableau 5).
| Soins rhinologiques : sérums -Sérum isotonique (osmolarité identique à celle du sérum sanguin) Eau distillée + chlorure de sodium 0,9 % -pour les rhinorrhées. Eau de mer isotonique (mêmes propriétés que le sérum isotonique). Eau de mer hypertonique Chlorure de sodium hypertonique à 2,3 g, Hyaluronate de sodium à 0,06 %, Eau purifiée q.s.p.100ml -contre obstruction nasale. -Sérum soufré (régénération cellulaire) Eau de mer 31,82 ml, sel de soufre, Eau purifiée qsp 100 ml. -Préparation « maison » : 1 litre d’eau (robinet) faire bouillir 3 minutes puis ajouter 10 ml (2 cuillères à thé) de sel et 2,5 ml (1/2 cuillère thé) de bicarbonate de sodium. |
| Soins rhinologiques : antiseptiques Hexamidine di-isétionate Désomédine 0,1 %* 4 à 6 pulvérisations/j. Benzalkonium chlorure Humex* 1à 2 pulvérisations 4 à 6 fois/j. Ritiométane magnésien Nécyran sol nasal 4 à 6 pulvérisations/j. Benzododécinium, Polysorbate 80 Prorhinel* 1 à 3 lavages /j. Benzododécinium bromure Rhinédrine* 2 pulvérisations 3 à 4 fois. Acide ténoique sel d’éthanolamine Rhinotrophyl* 1 pulvérisation 4 à 6 fois/j. |
| Soins rhinologiques : vasoconstricteurs Oxymétazoline chlorydrate Aturgyl* 1 pulvérisation 2 à 3 fois/j. Tuaminoheptane, acétylcystéine, benzalkonium Rhinofluimucil* 2 pulvérisations 3f. Oxymétazoline Respibien* 0,5 mg/ml 1 pulvérisation 3 fois/j. |
| Soins rhinologiques : corticoïdes Mométasone Nasonex* 2 pulvérisations/j. Budésonide Rhinocort* 4 pulvérisations/j. Triamcinolone Nasacort* 2 pulvérisations/j. Béclométasone Béconase* 4 à 8 pulvérisations/j. Fluticasone Flixonase* 2 pulvérisations/j. Flunisolide Nasalide* 4 pulvérisations 2 fois/j. Tixocortol Pivalone* 1 à 2 pulvérisations 4 fois/j. |
Les aérosols (sérum et corticoïdes) sont parfois pres- crits 2 fois/j pendant une semaine notamment chez la femme enceinte avec le même effet (drainage).
Les ponctions de sinus : Elles sont de moins en moins utilisées en raison de l’efficacité des traitements utilisés. Elles sont indiquées classiquement au cours des sinusites hyperalgiques, des sinusites bloquées, des sinusites nosocomiales (HIV mycose, pyocyanique) et des sinusites résistantes au traitement médical ou traînantes. Ces ponctions permettent d’évacuer les sécrétions purulentes, de faire des prélèvements si- nusiens utiles pour une étude microbiologique et de réaliser des lavages sinusiens (sérum isotonique associé à des antiseptiques ou des antibiotiques).
- Sinusite frontale aiguë
La douleur est intense, toujours unilatérale, dans la région sus-orbitaire, déclenchée par la pression de la paroi antérieure du sinus frontal. Il s’y associe une obstruction nasale, une rhinorrhée antérieure purulente, un larmoiement et une photophobie.
La rhinoscopie montre la présence de pus dans le méat moyen.
La radiographie standard montre une opacité frontale et souvent ethmoïdale associée (Figure 7).
La sinusite frontale est considérée comme une localisation à risque avec la possibilité d’extériorisation à la peau et surtout des complications encéphalo-méningées.
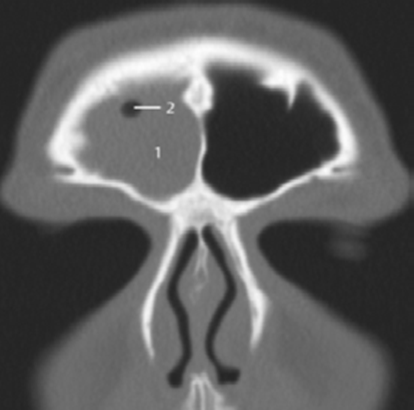
Figure 7 : Scanner massif facial coupe coronale : opacités sinus frontal
(1) avec une clarté (2) réalisant une sinusite frontale aiguë droite (cliché MEDICINE. KEY).
- Sinusite ethmoïdale aiguë
Elle est (rare) peu fréquente chez l’adulte et rarement isolée (tableau de pansinusite). L’imagerie est un examen essentiel pour le diagnostic positif, l’évaluation de son extension (ethmoïde antérieur, postérieur ou total) et surtout pour diagnostiquer les complications par contiguïté (globe oculaire).
- Sinusite sphénoïdale aiguë
Elle est souvent associée à une atteinte inflammatoire des autres sinus et passe longtemps inaperçue. Elle prend surtout l’allure d’un tableau neurologique (céphalées intenses, profondes et rebelles, centro-crâniennes ou rétro-oculaires irradiant au vertex) ou ophtalmologiques (troubles visuels) et le diagnostic est facilité par l’imagerie (scanner). Le traitement médical est efficace mais parfois il y a nécessité de recourir à un drainage par voie endoscopique [5].
B- Rhinosinusites aiguës de l’enfant
Les sinusites de l’enfant posent deux ordres de problèmes :
- Diagnostic : Surtout chez l’enfant avant l’âge de 6 ans où la sinusite est le plus souvent indissociable de la rhinopharyngite, ce qui est à l’origine du retard dia- gnostique.
- Thérapeutique : Par leur caractère tenace et les risques de complications graves. La chirurgie a une place limitée [4].
- Ethmoïdite aiguë
C’est l’atteinte inflammatoire d’origine infectieuse du labyrinthe ethmoïdal.
L’ethmoïdite aiguë de l’enfant passe généralement par deux stades consécutifs : une ethmoïdite aiguë non extériorisée puis extériorisée.
Ethmoïdite aiguë non extériorisée (EANE)
Elle réalise le tableau clinique d’une rhinopharyngite mucopurulente banale que caractérise surtout l’im- portance des signes généraux avec une fièvre élevée à 39°C, une asthénie de l’enfant et des céphalées fronto-orbitaires vives.
L’examen clinique à ce stade montre une douleur à la pression de l’angle interne de l’œil avec un œdème des deux paupières qui prédomine au niveau de l’angle interne de l’œil. Nous notons également des secrétions purulentes surtout du côté atteint.
La radiographie standard montre une asymétrie des cellules ethmoïdales avec une opacité du côté atteint. La prescription fréquente et précoce d’antibiotiques souvent motivée par l’importance de la fièvre ou l’existence d’une otite associée évite l’évolution vers l’extériorisation et les complications oculaires.
Ethmoïdite aiguë extériorisée (EAE)
Les signes généraux sont marqués par une fièvre entre 39 et 40°C, des frissons et des céphalées fron- to-orbitaires extrêmement vives.
Les anomalies cliniques prédominent à l’angle interne de l’œil avec un œdème ou une collection de la pau- pière supérieure et inférieure, une douleur intense à la pression de l’unguis ou du globe oculaire.
Au stade de cellulite, il y a un chémosis avec une rou- geur conjonctivale mais sans exophtalmie. L’acuité visuelle et le fond d’œil sont normaux.
Dans le stade collecté, il existe toujours une exophtal- mie qui est directe, irréductible, empêchant la fermeture de la paupière avec un chémosis énorme faisant hernie par la fente palpébrale. La mobilité oculaire est réduite (Figure 8).
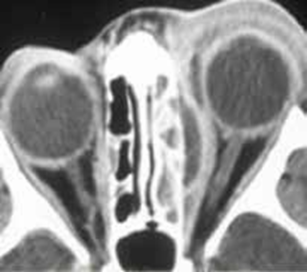
Trois signes doivent être recherchés systématiquement et la présence de l’un d’entre eux impose le drainage chirurgical en urgence, à savoir une immobilité du globe oculaire, une mydriase paralytique ou une anesthésie cornéenne.
L’absence ou le retard de traitement engendre des complications graves sur le plan vital et fonctionnel :
- Oculaires : Kératite, atteinte du nerf optique, nerfs ocu- lo-moteurs (III-IV- VI), rétiniennes.
- Neurologiques : Thrombophlébite du sinus caverneux, méningite, encéphalite ou abcès cérébral (Figure 9).
- Générales : Septicémie ou localisations secondaires.
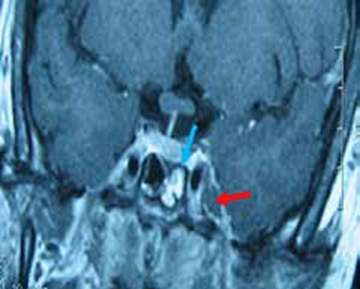
Sur le plan bactériologique, on retrouve surtout Haemo- philus Influenzae, Pneumocoque, Staphylocoque doré, Streptocoque du groupe A.
Le diagnostic positif d’une ethmoïdite et son évaluation (stade clinique) repose sur l’examen clinique et le scanner du massif facial. L’IRM est indiquée en cas de complica- tions neuro-méningées.
La bactériologie toujours nécessaire est un véritable moyen thérapeutique qui permet d’ajuster ou de réajuster une antibiothérapie face à une affection gravissime pouvant occasionner une mortalité et une grande morbidité.
L’anamnèse, l’examen clinique et l’imagerie permettent d’éliminer une dacryocystite, un furoncle des paupières, un érysipèle ou les tumeurs primitives de l’orbite.
Traitement :
Au stade d’ethmoïdite aiguë non extériorisée, nous prescrivons une antibiothérapie per os de type amoxicilline-acide cla- vulanique 50 mg/Kg/j en 4 prises. Nous associons un traitement local sous forme d’une désinfection nasale (lavages répétés au sérum). Un contrôle est réalisé au bout de 24 heures. En cas d’évolution favorable, il est poursuivi durant 15 jours. Cependant dans le cas d’un état stationnaire ag- gravation, nous basculons vers un traitement par voie parentérale calqué sur le schéma de l’ethmoïdite extériorisée : ATB voie générale schéma E.A.E.
Au stade d’ethmoïdite aiguë extériorisée, une hospitalisa- tion s’impose avec une antibiothérapie par voie parentérale. Nous utilisons une céphalosporine 3e génération : Céfotaxime 100 mg/Kg 4 fois avec un anti staphylococcique fosfomy- cine 100 mg/Kg en 2-3 fois, un imidazolé (flagyl) 30 mg/Kg en 2 fois et une quinolone durant 5 jours nétilmicine 6-7.5 mg/Kg/j en 2 fois. Nous associons une désinfection rhino- pharyngée, une corticothérapie (lutter contre l’œdème et les douleurs) et un collyre antiseptique. Ce traitement est prolongé 3 à 6 semaines avec un relais par voie orale selon l’évolution clinique et les résultats bactériologiques.
La chirurgie est indiquée dans le cas d’un abcès de l’orbite devant la constatation d’un seul signe sur la triade sémiologique de collection orbitaire par voie externe (canthale interne) ou endonasale endoscopique.
Autres formes de sinusites chez l’enfant
Les autres sinusites (frontales, maxillaires ou sphénoïdales) sont rares chez l’enfant et sont observées sur terrains par- ticuliers (mucoviscidose) ou sous formes de tableaux cli- niques mixtes (ethmoïdo-maxillaire, ethmoïdo-sphénoi- dale, ethmoïdo-frontale, pansinusites).
C. Rhinosinusites aiguës récidivantes
La rhinosinusite aiguë récidivante est définie par la consta- tation de quatre (4) ou plus d’épisodes de rhinosinusite aiguë par an avec une rémission totale (7 et 10 jours de ré- mission) entre les différentes poussées.
Ces rhinosinusites sont observées surtout chez la femme à partir de 40 ans.
Les germes retrouvés sont identiques à ceux des rhinosi- nusites aiguës.
Un examen endoscopique permet un bilan local (anato- mique). L’imagerie se résume à un examen tomodensitométrique du massif facial sans injection de contraste uniquement en cas d’anomalies anatomiques, de complications ou si nous programmons une thérapie à base de balloon sinuplasty.
Le traitement repose sur l’antibiothérapie au cours des poussées aiguës.
Les rhinosinusites aiguës récidivantes sont une indication des traitements locaux : topiques corticoïdes ou antihistaminiques locaux.
La thérapie par balloon sinuplasty assimilée à une technique mini-invasive trouve pleinement ses indications dans ces formes récidivantes.
Une septoplastie (déviation impactant le fonctionnement du méat moyen) associée à une méatotomie (plus ou moins couplée à une ethmoïdectomie antérieure) est une option recommandée par plusieurs auteurs.
Rhinosinusites chroniques
A- Rhinosinusites chroniques de l’adulte
Les sinusites chroniques correspondent à l’inflammation ou l’infection d’une ou plusieurs des cavités sinusiennes de la face qui dure plus de douze semaines. Elles sont ca- ractérisées par la persistance de signes fonctionnels rhino- logiques, des signes endoscopiques et scannographiques après un traitement médical adapté et bien conduit [6].
Sinusites chroniques bactériennes d’origine nasale
Elles sont habituellement bilatérales et indolores en dehors des poussées de surinfection. L’atteinte touche surtout les sinus maxillaires. Parfois elle est diffuse réalisant une pan-sinusite chronique.
Sur le plan bactériologique, on retrouve Hémophilus influenzae, streptocoque, staphylocoque, anaérobies.
La symptomatologie clinique est dominée par une rhinor- rhée postérieure purulente trainante avec un mouchage qui survient particulièrement le matin au lever. L’obstruction nasale est bilatérale. Les douleurs sont observées surtout au cours des poussées et les dysosmies sont au second plan.
Il faut aussi penser à une sinusite chronique en présence de signes indirects à type de gène pharyngée permanente, enroulement matinal, otite séro-muqueuse, ou dyspepsie, ou parfois devant des signes généraux inexpliqués à type de fébricule matinal récurrent, asthénie, courbatures, nausées permanentes, plénitude de la face.
La rhinoscopie montre une muqueuse inflammatoire, une hypertrophie des cornets avec une suppuration du méat moyen de même que du muco-pus sur la paroi postérieure du pharynx.
L’imagerie est essentielle dans le diagnostic d’une rhinosi- nusite chronique. Elle permet de rattacher aux sinus une symptomatologie souvent non spécifique, trainante ou de voisinage (irido-cyclite). Elle repose essentiellement sur l’examen tomodensitométrique du massif facial en coupes axiales, coronales et reconstructrices millimétriques sans injection de produit de contraste. Il n’y a pas d’image spé- cifique mais on constate surtout le caractère diffus, multi- focal et parfois mutant des lésions. On peut ainsi observer une opacité totale ou localisée, des images de niveaux liquides (poussées aiguës), une tonalité inhomogène avec images arrondies, un épaississement en cadre de la muqueuse, une déminéralisation osseuse diffuse ou une ostéo condensation. Une étude spécifique des rapports sinuso-dentaires est ha- bituelle soit par Denta-scan ou un examen en mode Cone beam.
Un bilan biologique est habituel en fonction des résultats anamnestiques et recherchera un déficit immunitaire localisé ou général. Une étude de la cinétique cellulaire et de la viscosité des sécrétions muqueuses peut orienter vers certains syndromes (immobilité ciliaire, mucoviscidose, vascularites).
Ce bilan comportera une numération formule sanguine avec frottis, une exploration de la fonction rénale, une gly- cémie, une VS et une CRP, un test à la sueur, une électro- phorèse des protéines, un dosage du fer sanguin, une TSH. Le traitement médical est toujours de mise et basé sur une antibiothérapie dirigée après identification du germe en cause et un antibiogramme.
Cette antibiothérapie fait souvent appel à une association amoxicilline + acide clavulanique ou à une fluoroquino- lone. En cas d’échec, on bascule vers des régimes associant amoxicilline-acide clavulanique + fluoroquinolones pen- dant 10 jours ou fluoroquinolones + céphalosporine 3e génération.
Une corticothérapie en cure courte est habituelle (1 mg/ Kg/j) avec vasoconstricteurs et aérosols. La chirurgie est généralement réalisée par voie endoscopique sous forme d’une méatotomie moyenne de drainage associée si né- cessaire au traitement des lésions associées, septoplastie et concha bullosa.
Sinusites chroniques d’origine dentaire
Le sinus en cause est le sinus maxillaire en raison des rap- ports étroits entre 2 prémolaires, 1ére et 2e molaires avec le fond du sinus maxillaire.
Les signes fonctionnels se résument à un mouchage pu- rulent unilatéral et fétide. L’anamnèse retrouve la notion de douleurs dentaires au froid ou au chaud.
Il faut souligner l’intérêt d’un examen stomatologique avec un bilan radiologique adapté (Dentascan).
Le traitement est double, celui de la dent causale et un curetage du sinus avec méatotomie moyenne par voie endoscopique.
Les mycoses sinusiennes
La truffe ou balle fongique est la forme la plus fréquente. Elle touche surtout les sinus maxillaires (89 %). C’est une sinusite fongique localisée extra muqueuse peu ou pas agressive survenant chez les immunocompétents. Sur le plan clinique, elle se traduit par des douleurs minimes, une obstruction nasale, une rhinorrhée (mouchage noirâtre), une cacosmie et plus rarement un œdème de la face ou palpébral.
L’endoscopie peut être normale ou montrer notamment des sécrétions purulentes, un œdème polypoïde voire des fragments de truffe extériorisés.
L’imagerie montre un aspect de corps étranger pseudo-mé- tallique dans une cavité sinusienne.
L’examen mycologique direct peut montrer des filaments mycéliens. L’analyse anatomopathologique montre une masse solide friable brun-noirâtre avec un enduit crémeux. Le traitement est chirurgical avec extraction de la balle fongique et drainage large du sinus par méatotomie.
Chez les sujets immunodéprimés, l’aspergillose peut revêtir une forme grave aiguë douloureuse avec lyse osseuse, extension orbitaire et endocrânienne de pronostic grave qui néces- site un large débridement par voie externe (parfois avec exentération orbitaire) et un traitement antifongique par voie générale (Figure 10).
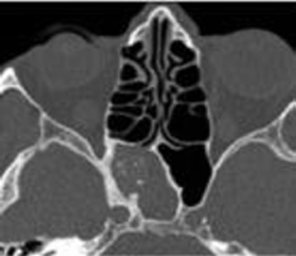
B- Rhinosinusites chroniques de l’enfant
C’est une entité étiopathogénique, clinique, radiologique et évolutive dont le substratum étant une inflammation chronique de la muqueuse naso-sinusienne.
Elles s’organisent en deux groupes : les rhinosinusites chro- niques sans polypose et les rhinosinusites chroniques aves polypose et constituent 5 % des cas avec une prévalence entre 7 et 8 ans.
Sur le plan pathogénique, il y a les rhinosinusites chro- niques essentielles et les formes secondaires (mucovis- cidose, déficit immunitaire, dyskinésie ciliaire, intolérance à l’aspirine). Les formes dentaires ou associées à une sar- coïdose, une maladie auto immune, sont exceptionnelles. La symptomatologie associe surtout une obstruction na- sale rebelle avec une rhinorrhée antérieure (mouchage fré- quent) et postérieure, fluide ou épaisse.
Un examen ORL complet est réalisé en particulier une en- doscopie qui recherchera des polypes, des sécrétions pu- rulentes et un œdème du méat moyen. La muqueuse peut être normale, pâle, délavée ou œdématiée. Un bilan allergologique (plus de 3 ans) peut être utile (adapté à l’âge et à l’anamnèse), une PH-métrie à la recherche d’un reflux gastro-œsophagien et la recherche d’un asthme associé. La rhinosinusite chronique de l’enfant nécessite dans certains cas une exploration spécialisée pour asseoir un cadre nosologique. Elle doit se faire en concertation (pédiatre, pneumologue, immunologiste, allergologue). Cette exploration est graduelle et toujours intégrée dans le contexte anamnestique et familial.
Ce bilan comporte une imagerie, un scanner et une IRM (opacité totale ou partielle à intégrer dans le contexte clinique au scanner, dépôts cellulaires ou lipidiques et fibrose à l’IRM), un bilan immunitaire (NFS, sérologie vaccinale, sérologie post-infectieuse, dosage pondéral des Immuno- globulines), test de la sueur, examens microbiologiques à la recherche d’une dyskinésie ciliaire primitive ou une intolé- rance à l’aspirine.
La prise en charge thérapeutique est complexe et nécessite une observance et une hygiène de vie particulière. L’apprentissage du mouchage est essentiel (éviter le reniflement) avec un lavage des fosses nasales au sérum plusieurs fois par jour pendant plusieurs semaines. L’antibiothérapie est indiquée lors des poussées.
Sur le plan chirurgical, nous évitons toute chirurgie agres- sive des sinus. Une adénoïdectomie peut être indiquée voire une méatoplastie au ballonnet.
En présence d’une polypose, il faut privilégier le traitement médical : corticothérapie en cure courte (3 cures par an) et soins rhinologiques.
Complications des rhinosinusites
Elles doivent être recherchées systématiquement et métho- diquement lors du diagnostic initial et surtout au cours de l’évolution et la surveillance des patients atteints de rhino- sinusites aiguës.
Il faut accorder une attention particulière à une sympto- matologie nouvelle ou une aggravation rapide du tableau clinique jusqu’à la stabilité.
Il peut s’agir d’une fièvre persistante ou qui réapparait, une altération de l’état général, des céphalées tenaces et persistantes ou récidivantes après une accalmie, des vomis- sements, une altération de la conscience, une confusion mentale.
Le diagnostic repose sur un examen clinique précis notam- ment la recherche d’un syndrome méningé, un syndrome neurologique localisé et surtout sur l’imagerie (TDM, IRM).
Les prélèvements bactériologiques (ponction lombaire, ponction stéréotaxique d’un abcès) sont essentiels car ils permettent une antibiothérapie ciblée.
- La complication la plus fréquente des sinusites aiguës étant le passage à la chronicité.
- Les mucocèles ethmoïdo-frontaux : Ce sont des forma- tions kystiques secondaires à l’obstruction chronique post-traumatique ou idiopathique du canal naso-frontal. Sa surinfection entraîne une pyomucocèle.
- Les complications ophtalmologiques surtout dans les ethmoïdites à type de cellulites orbitaires, uvéites et la névrite optique rétro bulbaire.
- Les complications méningo-encéphaliques sous forme de méningites purulentes, d’abcès sous duraux, intra-céré- braux, extraduraux et les thrombophlébites du sinus caver- neux, crises épileptiques (Figure 8).
- L’ostéomyélite surtout pour les formes frontales.
- Les septicémies et localisations secondaires (septiques) La prise en charge thérapeutique est médico-chirurgicale associant une antibiothérapie (bithérapie ou trithérapie), mesures générales (réhydratation, antipyrétiques, antal- giques, anti-convulsivants, corticoïdes, solutés osmolaires). La chirurgie est indiquée en cas de suppuration collectée sous forme de drainage.

Conclusion
Les rhinosinusites constituent toujours une pathologie fréquente et problématique compte tenu des mutations bactériologiques (antibiothérapies abusives et écologie bactérienne), des atypies de présentation clinique (sé- miologie décapitée par les traitements, des dysmorphies anatomo-fonctionnelles) et des défis posés en matière de prise en charge et de santé publique en général [7].
Il est important de mener une véritable veille sani- taire pour cette pathologie, d’organiser un suivi ciblé et d’émettre des recommandations de pratique médicale afin d’harmoniser l’encadrement de ces affections (Tableau 6).

Références
- Delmas. J, Radulesco. T, Varoquaux. A, Thomassin. JM, Dessi. P, Michel. J Anatomie des cavités nasosinusiennes EMC ORL 2017 20-265-A-10 Paris 20 pages.
- Aring. AM, Chan. MM Current Concepts in Adult Acute Rhinosinusitis. Am Fam Physician. 2016 Jul 15; 94 (2): 97-105.
- Lemiengre MB, van Driel ML, Merenstein D, Liira H, Mäkelä M, De Sutter.AI Antibiotics for acute rhinosinusitis in adults. Cochrane Database Syst Rev. 2018 Sep 10; 9 (9): CD006089. doi: 10.1002/14651858.CD006089.
- Nocon CC, Baroody FM. Acute rhinosinusitis in children. Curr Allergy Asthma Rep. 2014 Jun; 14 (6): 443. doi: 10.1007/s11882-014-0443-7.
- Esposito S, Marchisio P, Tenconi R, Tagliaferri L, Albertario G, Patria MF, Principi. N. Diagnosis of acute rhinosinusitis. Pediatr Allergy Immunol. 2012 Aug; 23 Suppl 22: 17-9. doi: 10.1111/j.1399-3038.2012.01319.x.
- Cho SH, Ledford D, Lockey RF. Medical management strategies in acute and chronis rhinosinusitis. J Allergy Clin Immunol Pract. 2020 May; 8 (5): 1559-1564. doi: 10.1016/j. jaip.2020.02.020.
- Teeters J, Boles M, Ethier J, Jenkins A, Curtis LG Acute rhinosinusitis: new gui- delines for diagnosis and treatment. JAAPA. 2013 Jul; 26(7):57-9. doi: 10.1097/01. jaa.0000431519.28443.5e

