Pr H. Djoudi Service de rhumatologie, EHS Douéra.
Remerciements à tous les investigateurs qui ont participé à la réalisation de l’étude.
Abstract :
Introduction : The management of rheumatoid arthritis has considerably increased during the last few years. This evolution is due to the emergence of a more effective therapeutic arsenal, to an early management strategy with a tight control and specific and ambitious goals. We only have little information on the actual practices of the management of the AR in Algeria. The only clinical studies conducted on this disease locally are very often limited to patients followed in one rheumatology department. The main objective of this study is to describe the medicinal treatment (symptomatic treatment and Disease-Modifing Drugs (DMARDs) used in AR progressing since less than two years.
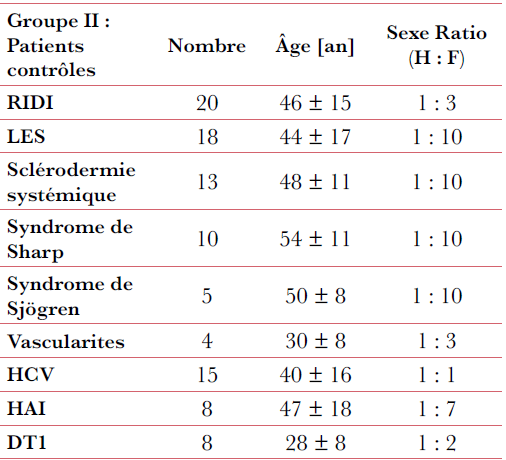
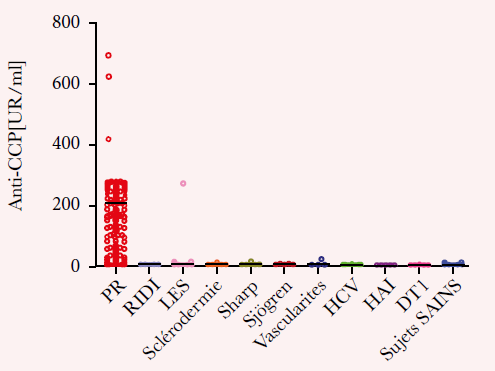
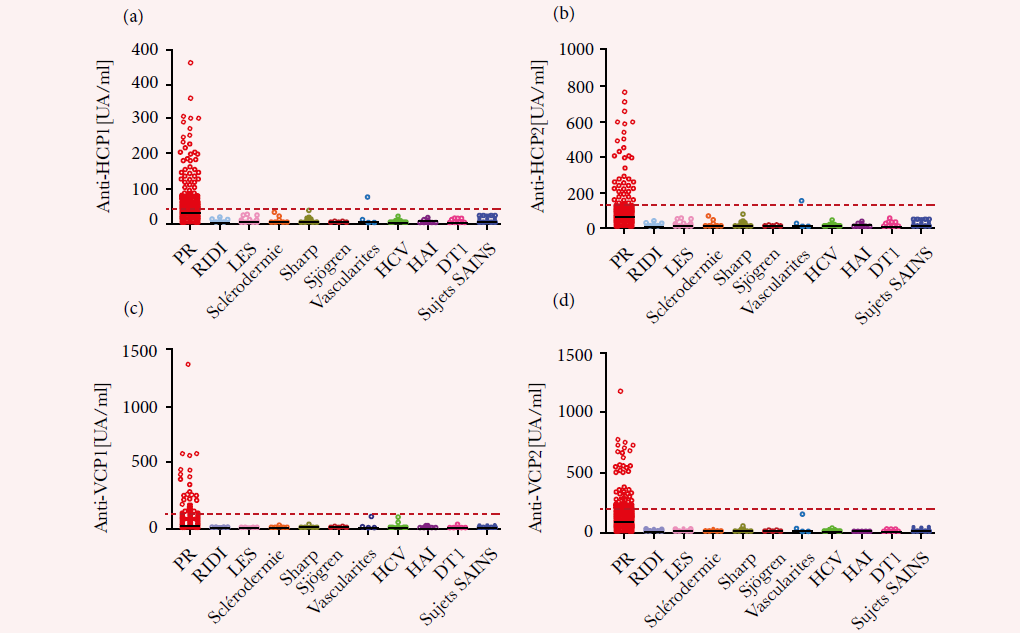
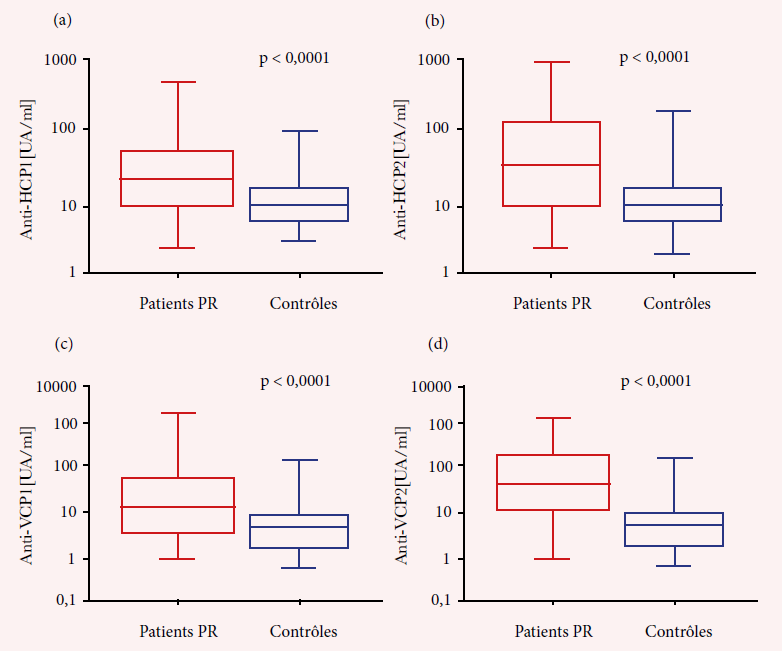
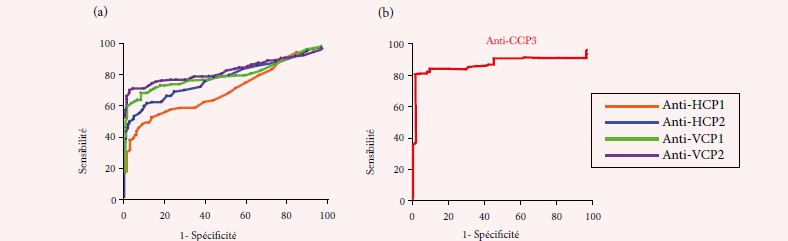
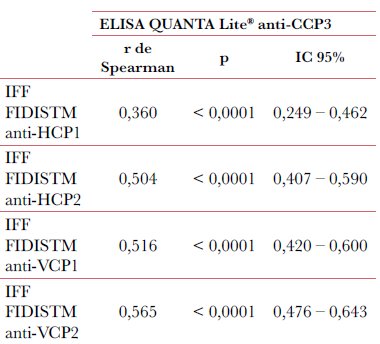
Material and Methods : ACPA measurement was performed in 273 sera of RA patients, 64 healthy subjects and 101 control patients (FIDISTM anti-CCP, Theradiag), immunofluorimetry assay and ELISA (QUANTA Lite® antibody -CCP3 IgG, Inova Diagnostics).
Results : 572 patients presenting with a debutante and eligible AR were analyzed. Characteristics of patients: mean age 45 years. Gender: more than three-quarters of patients were women. Delayed diagnosis: in more than half of the cases, 52.3% were diagnosed with a minimum of six months delay according to the first symptoms and 22.8% with a minimum of 3 months. Characteristics of AR: there are often very active AR in 61.7% (activity evaluated by DAS28), with structural impairment; average score of the modified SHARP of the order 10.8 +/-19.8 with functional disability between 0.5 and 1 in nearly half (40.6%), (disability assessed by the HAQ score). The DAS28 score was significantly related to the use of long-term treatment and to the duration of the disease. (84.1%) of cases, non-steroidal anti-inflammatory drugs (NSAIDs) in (79.9%) and analgesics in (81.6%) were the symptomatic drugs prescribed. The methotrexate is the most prescribed molecule (92.8%) at an average dose of 11.8 mg / week, which is not always related to the clinical picture. The combination Methotrexate + hydroxychloroquine + sulfasalazyne was prescribed only in three patients. Concerning biotherapy: it is inaccessible in a liberal sector, it was used only in 4 patients. National recommendations for the management of AR should be developed rapidly.
Key words : RA, ACPA, anti-HCP1, anti- HCP2, anti-VCP1, anti-VCP2, Immunofluorimetry assay, Multiplexing assay, ELISA
Résumé :
Introduction : La prise en charge thérapeutique de la polyarthrite rhumatoïde (PR) a beaucoup évolué au cours des dernières années. Cette évolution est due à l’apparition d’un nouvel arsenal thérapeutique plus performant, à une nouvelle stratégie de prise en charge ; la plus précoce possible, adaptée avec contrôle serré ; des objectifs précis et ambitieux. Les informations disponibles sont l’apanage d’études menées localement et sont très souvent limitées aux patients suivis dans un service de rhumatologie. L’objectif principal de cette étude est de décrire le traitement médicamenteux (traitement symptomatique et traitement de fond) utilisé dans la PR évoluant depuis moins de 2 ans.
Matériel et méthodes : Epi PR est une étude nationale, descriptive, transversale, multicentrique menée dans 36 centres de rhumatologie du secteur privé et public répartis sur le territoire algérien. Les données ont été récoltées sur des patients âgés de 18 ans et plus, ayant une PR évoluant depuis plus de 3 mois et moins de 2 ans, quel que soit le traitement symptomatique et le traitement de fond prescrit.
Résultats : 572 sujets présentant une PR débutante et éligibles ont été analysés. Caractéristiques des patients : âge moyen : 45 ans, sexe : plus des trois quarts (3/4) des patients sont des femmes, retard diagnostic dans plus de la moitié des cas (52,3%), le diagnostic est posé avec un minimum de 6 mois de retard par rapport aux premiers symptômes et dans près d’un quart des cas (22,3%) avec un minimum de 3 mois.
Caractéristiques de la PR : Il s’agit souvent de PR très active, 61,7% des cas, (activité évaluée par le DAS28) avec atteinte structurale ; score moyen du Sharp modifié évalué à 10,8 ± 19,8 avec un handicap fonctionnel compris entre 0,5 et 1 dans près de la moitié des cas (40,6%), handicap évalué par le score HAQ. La valeur du DAS 28 est significativement liée au retard diagnostic. Les scores de SHARP modifié et HAQ ne sont pas significativement liés à la durée d’évolution et à l’utilisation d’un traitement de fond.
Thérapeutique : médicaments symptomatiques : ce sont essentiellement les corticoïdes, les anti-inflammatoires non stéroïdiens (AINS) et les antalgiques, respectivement dans 81,6%, 79,9% et 84,1% des cas. Traitement de fond : le méthotrexate est la molécule la plus prescrite (92,8%), à une dose moyenne de 11,8mg/semaine, dose qui n’est pas toujours en rapport avec le tableau clinique. L’association méthotrexate + hydroxychloroquine + sulfasalazyne n’est prescrite que chez trois (3) patients, quant à la biothérapie, inaccessible en milieu libéral, elle n’est utilisée que chez quatre (4) patients.
Conclusion : Les médicaments de la polyarthrite rhumatoïde sont essentiellement représentés par les corticoïdes (85%) d’autant plus utilisés que la PR est sévère et/ou active, les AINS (70%), et le méthotrexate (92,8%) pour le traitement de fond.
Mots-clés : Atteinte structurale, capacité fonctionnelle, polyarthrite rhumatoïde, score d’activité, sévérité, traitement de fond.
Introduction :
a polyarthrite rhumatoïde (PR) est le rhumatisme in-lammatoire chronique le plus fréquent, avec une prévalence mondiale de 1%(1). Elle touche principalement la femme entre 40 et 60 ans avec un sex-ratio F/H de 3/1(2).
La PR est une maladie auto-immune qui se caractérise par une hyperplasie du tissu synovial, l’afflux articulaire de leucocytes vers la cavité articulaire, la destruction progressive du cartilage et des extrémités osseuses de voisinage, source à plus ou moins long terme d’altération de la capacité fonctionnelle cause de handicap. Elle s’associe à une inflammation systémique et à la production d’auto-anticorps dont le facteur rhumatoïde (FR) et les anticorps anti peptides citrullinés (ainti-CCP2)(2). Aussi, la recherche des anticorps dirigés contre les peptides citrullinés (anti-citrullinated protein auto-antibodies [Acpa]) est indispensable dans tous les cas de mono ou d’oligo-polyarthrite débutante, et est d’ailleurs recommandée par la Société Française de Rhumatologie sur la prise en charge de la PR en 2014(3). Leur positivité, isolée ou conjointe avec celle des FR, fait partie des nouveaux critères diagnostiques définis en 2010 dans le consensus transatlantique des Sociétés de Rhumatolo- gie Américaine et Européenne ACR et EULAR(4).
La PR se caractérise aussi par un tableau clinique polymorphe, elle évolue par poussées à tendance extensive polyarticulaire. En effet, après 10 ans de suivi, 92% des malades ont une diminution importante de leur capacité fonctionnelle(5,6,7), 50% des malades nécessitent une aide personnelle pour certaines activités de la vie quotidienne(8). La majorité des malades atteints sont obligés d’interrompre leur activité professionnelle moins de 10 ans après le début de leur maladie ou d’adapter leurs conditions de travail à leur handicap(9,10). En outre, elle nécessite des traitements agressifs dont les corticoïdes ; les traitements de fond, dont le méthotrexate ; et parfois une biothérapie(2). Malgré des associations de plusieurs traitements de fond, certains malades présentent des destructions articulaires et doivent subir de nombreuses interventions chirurgicales(7).
Du point de vue économique, les coûts directs engendrés par cette affection ont augmenté 3 à 6 fois par l’essor des biothérapies, dont les coûts excèdent ceux de l’hospitalisation dans les pays industrialisés (11,12). En 2014, une étude Suédoise a montré que les coûts des médicaments ont été partiellement contrebalancés par la diminution des visites ambulatoires, mais les coûts indirects sont restés inchangés et les coûts totaux ont augmenté dans les 6 ans après le diagnostic précoce de la PR. En effet, le coût total moyen de la PR a augmenté de 14.768 euros par patient durant la première année de diagnostic, jusqu’à 18.438 euros à la sixième année(13).
Quant au diagnostic, sa précocité est un élément clé dans la prise en charge des malades, bien que le diagnostic de la PR soit difficile dans les formes débutantes(3). Dans ce contexte, le clinicien doit évoquer la possibilité d’une PR en présence d’au moins une synovite clinique ou détectée par échographie et/ou IRM articulaire, et après exclusion d’un autre diagnostic, en excluant les localisations des premières articulations métatarso-phalangiennes (MTP) et inter-phalangiennes distales (IDP). Le diagnostic de PR est alors retenu si le patient a au moins une érosion radiographique ou plus de six points selon les critères ACR/EULAR(4). Par conséquent, la maladie doit être traitée dès la certitude du diagnostic, et agressivement en cas de mauvais pronostic(4).
Finalement, des consensus existent sur la prise en charge de la PR, basés sur des scores d’activité de la maladie (DAS 28, Disease Activity Score 28), des scores de capacité fonctionnelle (HAQ, Health Assessment Questionnaire ou modified HAQ , MHAQ) et sur l’atteinte structurale (score SHARP modifié)(14). En Algérie, les études menées sur la PR sont locales et limitées aux patients suivis dans un service de rhumatologie. On ne dispose que de peu ou pas d’informations sur les pratiques réelles des professionnels de santé en particulier des médecins rhumatologues des secteurs public et privé; ce qui a motivé l’étude dont l’objectif principal est de décrire le traitement médicamenteux (traitement symptomatique et traitement de fond) utilisé dans la PR évoluant depuis moins de 2 ans. Les objectifs secondaires assignés sont : estimer le score d’activité de la maladie par le score DAS 28, évaluer l’atteinte structurale par le score de « SHARP modifié » et estimer la capacité fonctionnelle par le score HAQ , les trois paramètres étudiés de manière globale, puis selon la durée d’évolution et selon le traitement médicamenteux utilisé.
Patients et méthodes :
Schéma et population d’étude :
Il s’agit d’une étude nationale, transversale et multicentrique menée de Septembre 2011 à Décembre 2012, sur des patients des deux sexes, âgés de 18 ans et plus, ayant une polyarthrite rhumatoïde ayant débuté depuis plus de 3 mois et ne dépassant pas deux ans d’évolution, quel que soit le traitement. Ne sont pas inclus les patients présentant une PR associée à une connectivite et ceux présentant des troubles neuropsychiques ou participant à une autre étude clinique.
Déroulement de l’étude :
Les patients répondant à l’ensemble des critères de sélection étaient inclus dans l’étude selon l’ordre chronologique de consultation, auprès des médecins investigateurs répartis sur le territoire national. Pour cela, 40 centres des secteurs privé et public ont été tirés au sort au niveau des wilayates suivantes : Alger, Blida, Tizi Ouzou, Oran, Tlemcen, Sidi Bel Abbès, Constantine, Sétif et Annaba avec un recrutement de 15 patients éligibles par centre. S’agissant d’une étude observationnelle, aucun traitement n’a été prévu ou exigé, seule la pratique courante des investigateurs a été observée et le choix thérapeutique était à la discrétion du médecin.
Collecte des données :
Les données recueillies portent essentiellement sur : la date d’obtention du consentement éclairé, la date d’inclusion du patient dans l’étude, la confirmation des critères de sélection du patient, ses caractéristiques sociodémographiques, les antécédents personnels et familiaux, les pathologies associées, les caractéristiques cliniques, biologiques et radiologiques de la maladie au moment de l’inclusion, le traitements en cours ; les scores DAS 28, SHARP modifié et HAQ ont aussi été notés sur le cahier d’observation en version tripliquée. Les évènements indésirables graves et non graves observés et les grossesses ont été rapportés.
Critères d’évaluation :
Le critère d’évaluation principal est la proportion de patients ayant une polyarthrite rhumatoïde par classe thérapeutique. Quant aux critères secondaires, l’activité de la maladie est évaluée par le score DAS 28, celle de la capacité fonctionnelle par le score HAQ et les lésions radiologiques par le score de SHARP modifié.
Analyse statistique :
Le calcul de la taille minimale de l’échantillon s’est basé sur la fréquence d’utilisation la plus basse ; selon les études locales, il s’agit de la thérapie ciblée utilisée chez 10 à 20 % des patients présentant une PR. En partant d’une fréquence p0 = 0,15 et un degré de précision i = 0,03, la taille minimale de l’échantillon est estimée à 600 patients.
L’analyse statistique est essentiellement descriptive. Les variables quantitatives continues sont décrites par le nombre de patients documentés, la moyenne, l’écart-type, les valeurs extrêmes, la médiane et les quartiles. Les variables discontinues et qualitatives sont déterminées par l’effectif et le pourcentage de chaque modalité. Le lien entre deux variables qualitatives a été recherché avec le test de Chi-2. La comparaison des moyennes a été faite par le test de Student ou le test ANOVA pour plus de deux groupes. En cas de non-respect des hypothèses, les tests non paramétriques étaient utilisés. Le lien entre les scores et la durée d’évolution de la maladie a été évalué avec le coefficient de corrélation de Pearson. Tous les tests ont été effectués en formulation bilatérale avec une limite de significativité fixée à 5%. Tous les calculs ont été effectués avec le logiciel SPSS (Edition 18).
Considérations éthiques :
En accord avec la réglementation locale concernant les études observationnelles (Article 14 de l’arrêté 388 du 31 juillet 2006), aucun comité d’éthique n’a été impliqué dans cette étude. Cette dernière a été soumise à l’autorité réglementaire locale (Ministère de la Santé, de la Population et de la Réforme Hospitalière) qui a accordé l’autorisation de conduire l’étude.
Résultats :
Caractéristiques des patients :
36 centres ont recruté de 2 à 46 patients répondant aux critères d’inclusion, totalisant ainsi 572 patients qui font l’objet de cette analyse.
Le délai d’évolution de la maladie (date séparant les premiers symptômes de la date de l’inclusion) varie de 93 à 729 jours, il est en moyenne de 375 jours ± 177.
Le diagnostic de PR, analysé chez 545 patients, est posé au cours des 6 premiers mois dans près de la moitié des cas (47,6 %) et dans la plupart des cas avant une année d’évolution (87,2%).
La mise en route du traitement de fond n’a été déterminée que 510 fois. Le traitement de fond a été instauré dans plus d’un tiers des cas (37,2%) avant 6 mois et dans plus des 3/4 des cas (78,2%) au cours de la première année d’évolution et dans près d’un tiers des cas (31,8%) après une année d’évolution. Le délai séparant la date des premiers symptômes de la date du diagnostic et la mise en route du traitement de fond sont rapportés dans le (Tableau 6).
| Variable | Effectif (%) |
| Délai de retard au diagnostic (n=545) | |
| ≤ 6 mois | 260 (47,7%) |
| ]6-12 mois] | 161 (29,5%) |
| ]12-18 mois] | 89 (16,4%) |
| ]18-24 mois] | 35 (6,4%) |
| Delai de retard à la mise en route du traitement de fond (n=510) | |
| < 3 | 71 (13,9%) |
| [3-6 mois[ | 119 (23,3%) |
| [6-9 mois[ | 96 (18,8%) |
| [9-12 mois[ | 62 (12,2%) |
| ≥ 12 mois | 162 (31,8%) |
L’âge des patients est en moyenne de 44,9 ans ± 13,7 avec des extrêmes variant de 18 à 83 ans. La majorité des patients sont des femmes (80%) : sexe ratio de 0,24. L’indice de masse corporelle était en moyenne de 25,5 ± 4,3 Kg/m2 sans différence significative entre les deux sexes. La majorité des patients (73,4%) sont mariés, et le niveau scolaire primaire est le plus fréquent (24,3%). Quant à la profession, 70% des patients n’exercent aucune activité avec différence significative selon le sexe (51 hommes inactifs (59,3%) versus 348 femmes inactives (80,7%), p <10-6. La majorité des patients bénéficient néanmoins d’une couverture médicale (79,1%, n=453) (Tableau 1).
Un tiers des patients (33,2%, n=190) avaient au moins un antécédent personnel à l’inclusion. Les antécédents familiaux de rhumatisme inflammatoire chronique étaient notés chez 67 patients (11,7%) ; 50 d’entre eux avaient un antécédent de polyarthrite rhumatoïde, le plus souvent chez la sœur, la mère ou la grand-mère, et plus rarement chez les parents du 2ème degré (Tableau 1).
| Variable | Effectif (%) | Valeurs extrêmes | Moyenne ± Ecart type | Médiane (intervalle interquartile) |
| Age (ans) | 571 | 18 à 83 | 44,9 ± 13,7 | 45 (35-54) |
| IMC(Kg/m2) | ||||
| Masculina | 86 | 16,6 à 35,3 | 24,8 ± 3,7 | 24,4 (22,5-26,6) |
| Féminina | 431 | 15,6 à 42,5 | 25,7 ± 4,4 | 25,7 (22,5-28,3) |
| Global | 517 | 15,6 à 42,5 | 25,5 ± 4,3 | 25,4 (22,5-28,0) |
| Sexe | ||||
| Masculin | 109 (19,0%) | |||
| Féminin | 460 (80,5%) | |||
| Non précisé | 3 (0,5%) | |||
| Statut marital | ||||
| Marié(e) | 420 (73,3%) | |||
| Célibataire | 120 (21,0%) | |||
| Divorcé(e) | 21 (3,7%) | |||
| Veuf(ve) | 10 (1,7%) | |||
| Non précisé | 1 (0,2%) | |||
| Niveau d’instruction | ||||
| Aucun | 113 (19,8%) | |||
| Primaire | 139 (24,3%) | |||
| Moyen | 109 (19,1%) | |||
| Secondaire | 119 (20,8%) | |||
| Supérieur | 88 (15,4%) | |||
| Non précisé | 4 (0,7%) | |||
| Situation professionnelle | ||||
| Non actif | 400 (69,9%) | |||
| Actif | 170 (29,7%) | |||
| Non précisé | 2 (0,4%) | |||
| Couverture médicale | ||||
| Oui | 453 (79,1%) | |||
| Non | 117 (20,5%) | |||
| Non précisé | 2 (0,4%) | |||
| Antécédent personnel | ||||
| Au moins 1 antécédent | 190 (33,2%) | |||
| Tabagisme actif | 29 (5,1%) | |||
| HTA | 83 (14,5%) | |||
| Hypercholestérolémie | 26 (4,6%) | |||
| Diabète | 48 (8,4%) | |||
| AAI | 3 (0,5%) | |||
| Hyperthyroïdie | 1/3 | |||
| Syndrome sec | 2/3 | |||
| Autre(s) pathologie(s) | 74 (12,9%) | |||
| Antécédent familial de RIC | ||||
| Oui | 67 (11,7%) | |||
| Polyarthrite rhumatoïde | 50/67 (74,6%) | |||
| Spondylarthrite ankylosante | 10/67 (14,9%) | |||
| Arthrite juvénile idiopathique | 1/67 (1,5%) | |||
| Connectivite | 5/67 (6,0%) | |||
| Autres (gouttes, syndrome du | ||||
| canal carpien, entérocolopa- | 3/67 (3,0%) | |||
| thie) | ||||
| Associations (PR + Scléro- | ||||
| dermie systémique ; SPA + | ||||
| entérocolopathie) | ||||
| Non | 505 (88,3%) | |||
Caractéristiques de la maladie à l’inclusion :
La durée moyenne de la raideur matinale est de 69,3 minutes ± 58,4, le nombre moyen d’articulations douloureuses de 11,2 ± 7,2 et le nombre d’articulations gonflées de 6,0 ± 5,4.
L’évaluation de la douleur par le patient (EVA patient) est en moyenne de 53,5 ± 21,3. (n=548). L’évaluation de la douleur par le médecin est de 46,3 ± 19,2 (n=549) (Tableau 2).
Les manifestations extra-articulaires ont été notées chez 221 patients soit dans 38,6% des cas (Tableau 2).
| Variable | Effectif (%) | Valeurs extrêmes | Moyenne± Ecart type | Médiane (intervalle interquartile) |
| Durée raideur matinale | 570 | 0 à 540 | 69,3 ± 8,4 | 60 (30-120) |
| Nombre articulations douloureuses | 572 | 0 à 28 | 11,2 ± 7,2 | 10 (6-16) |
| Nombre articulations gonflées | 572 | 0 à 28 | 6,0 ± 5,4 | 5 (2-9) |
| Evaluation globale de la douleur | 551 | 0 à 100 | 53,5 ± 21,3 | 50 (40-70) |
| Evaluation globale de la maladie par le malade | 548 | 0 à 100 | 53,6 ± 21,5 | 50 (40-70) |
| Evaluation globale de la maladie par le médecin | 549 | 0 à 90 | 46,3 ± 19,2 | 50 (30-60) |
| Manifestation extra articulaire | ||||
| Pleuropulmonaire | 11 (5,0%) | |||
| Cardiovasculaire | 4 (1,8%) | |||
| Oculaire | 22 (10,0%) | |||
| Ténosynovite | 63 (28,5%) | |||
| Fièvre | 64 (29,0%) | |||
| Fatigue | 180 (81,4%) | |||
| Autres manifestations (pleuro-pulmonaires, | 32 (14,5%) | |||
| cardiovasculaires, oculaires, sécheresse buccale | ||||
| ou oculaire et nodules rhumatoïdes) | ||||
| Bilan inflammatoire | ||||
| Vitesse de sédimentation | 562 | 2 à 142 | 47,1 ± 27,2 | 43,0 (26-64) |
| CRP | 410 | 1,46 à 192 | 29,0 ± 33,4 | 13 (6-38,4) |
| Formule numération sanguine | ||||
| Globules blancs (GB) (x 103) | 501 | 2 à 18,6 | 7,51 ± 2,56 | 7 (6-9) |
| GB < 4 000 éléments / mm3 | 16/501 (3,2%) | |||
| 4 000 ≤ GB < 10 000 éléments / mm3 | 389/501(77,6%) | |||
| GB ≥ 10 000 éléments / mm3 | 96/501 (19,2%) | |||
| Hémoglobine (g/dl) | 523 | 7,0 à 16,0 | 11,5 ± 1,5 | 11,4 (10,2-12) |
| < 10 | 56/523 (10,7%) | |||
| 10 ≤ Hémoglobine < 12 | 210/523 (40,2%) | |||
| 12 ≤ Hémoglobine < 14 | 204/523 (39,0%) | |||
| Hémoglobine ≥ 14 | 53/523 (10,1%) | |||
| Plaquettes (x 103) | 532 | 95 à 863 | 295,0 ± 99,6 | 280 (227-344) |
| Plaquettes < 150 000 | 9/523 (1,7%) | |||
| 150 000 ≤ Plaquettes < 450 000 | 486 (91,4%) | |||
| Plaquettes ≥ 450 000 | 37 (7,0%) | |||
| Bilan rénal | ||||
| Urée | 421 | 0,1 à 4,0 | 0,33 ± 0,27 | 0,29 (0,24-0,37) |
| Créatinémie | 466 | 4,9 à 66 | 8,62 ± 3,82 | 8,00 (7,00-9,56) |
| Bilan hépatique | ||||
| ALAT | 486 | 2 à 123 | 20,0 ± 12,0 | 17,0 (13-24) |
| ASAT | 486 | 2 à 100 | 20,0 ± 12,4 | 24,0 (12-24) |
| Bilan immunologique | ||||
| Facteur rhumatoïde | 528 | Positif dans 354 cas (67,0%) | ||
| Anti CCP2 | 360 | Positif dans 260 cas (72,2%) | ||
| Anti CCP3 | 95 | Positif dans 77 cas (81,1%) | ||
| Anti CCP (2 ou 3) | 443 | Positif dans 344 cas (77,6%) | ||
| Anticorps anti-nucléaires | 391 | Positif dans 64 cas (16,3%) | ||
| Autres examens (anticorps anti DNA, | 75 (13,1%) | |||
| anti SSA/SSB) | ||||
| DAS28 (n=572) | ||||
| En rémission (DAS28 < 2,6) | 16 (2,8%) | |||
| Faiblement active (2,6 ≤ DAS28 < 3,2) | 19 (3,3%) | |||
| Modérément active (3,2 ≤ DAS28 < 5,1) | 149 (26,0%) | |||
| Très active (DAS28 ≥ 5,1) | 353 (61,7%) | |||
| Non précisé | 35 (6,1%) | |||
| Radiologie des mains et poignets | ||||
| (n=498) | ||||
| Erosions | 152 (30,6%) | |||
| Pincement | 227 (45,7%) | |||
| Radiologie des pieds (n=335) | ||||
| Erosions | 60 (17,9%) | |||
| Pincement | 50 (14,9%) | |||
| Autres radiologies (n=153) | ||||
| Erosions | 6 (3,9%) | |||
| Pincement | 31 (20,4%) | |||
| Echographie articulaire (n=45) | ||||
| Erosions | 7 (30,5%) | |||
| Autre lésion (épanchement intra | 15 (45,6%) | |||
| articulaire, une ténosynovite ou une | ||||
| bursite) | ||||
| Autre examen (n=49) | ||||
| Anomalie(s) | 44 (91,7%) | |||
| Score SHARP global modifié | 245 | 0 à 140 | 10,8 ± 19,8 | 0 (0-15) |
| Score HAQ | 352 | 0 à 2,8 | 0,94 ± 0,74 | 1 (0-1,45) |
| HAQ ≤ 0,5 | 109/352 | |||
| (31,0%) | ||||
| 0,5 < HAQ ≤ 1 | 143/352 | |||
| (40,6%) | ||||
| HAQ >1 | 100/352 | |||
| (28,4%) | ||||
| Sévérité de la maladie | ||||
| Sévère | 173 (30,2%) | |||
| Pas sévère | 399 (69,8%) | |||
Au plan explorations biologiques, pour la vitesse de sédimentation à la première heure (VS), seuls les chiffres inférieurs à 150 mm ont été analysés, ceux supérieurs ont été considérés comme données aberrantes. L’analyse a été effectuée sur 562 patients, elle est évaluée en moyenne à 47,1mm ± 27,2. Idem pour la C réactive protéine (CRP), l’analyse n’a porté que sur les valeurs inférieures à 200. Le dosage n’a intéressé que 410 patients. La valeur moyenne est de 29,0g/l ± 33,4. Le taux moyen de globules blancs est de 7 510 éléments / mm3± 2 558, le taux moyen d’hémoglobine de 11,5 1,5 g/dl ± et le taux moyen de plaquettes de 29 4964 éléments / mm3± 99 595. Au plan rénal, l’urée sanguine est en moyenne de 0,33 g/l ± 0,27, la créatininémie à 8,62 ± 3,82 mg/l, les 2 dosages ont été déterminés chez 273 patients. Le cholestérol sanguin, noté chez 273 patients, est en moyenne de 1,77 g/l ± 0,40. L’hyper-cholestérolémie, définie par un taux de cholestérol supérieur à 2 g/l, a été notée chez 53 sujets soit dans 19,4% des cas, elle a concerné 11 hommes et 42 femmes. Le HDLc, dosé chez 154 patients, est en moyenne de 0,50 g/l ± 0,18, celui du LDLc dosé chez 153 patients, est en moyenne 1,07 g/l ± 0,33. Le taux moyen de triglycérides évalué chez 255 patients, est de 1,22 g/l ± 0,56. L’hypertriglycéridémie, définie par un taux supérieur à 1,75 g/l chez les hommes et supérieur à 1,40 g/l chez les femmes, a été notée chez 60 sujets soit 23,5% des cas. (10 hommes et 50 femmes). Au plan immunologique les facteurs rhumatoïdes sont considérés comme positifs chez 354 patients (67,1%) ; dans ce dernier cas, le taux a été noté chez 292 sujets avec une moyenne de 154 UI/ml ± 160. Les anti CCP2 ont été considérés positifs chez 261 patients (72,5%) avec un taux moyen de 169 UI/ml ± 128 calculé sur un effectif de 246 patients. Les anticorps antinucléaires, sur HEP200, ont été recherchés chez 391 patients soit dans 68,4% des cas. Ils sont considérés comme positifs chez 64 patients (16,4%) avec un taux moyen de 93,9 UI/ml ± 151,6 (extrêmes de 1 à 640). Le taux est supérieur à 80 UI/l dans 3,3% soit chez 13 patients. L’aspect en immunofluorescence indirecte est de type homogène dans 17 cas, moucheté dans 22 cas et nucléolaire dans 3 cas. Le type n’a pas été précisé pour les 21 autres patients (Tableau 2).
Le DAS28 VS calculé chez 520 patients est en moyenne de 5,52 ± 1,43, le DAS28 CRP chez 24 patients est en moyenne de 5,80 ± 1,13. Les deux scores DAS28 VS et DAS 28CRP ont été calculés chez 7 patients, aucun d’eux n’a été déterminé chez 35 patients soit dans 6,7% des cas.
Le Tableau 2 précise l’activité de la maladie en fonction de la valeur du DAS28.
Étude radiologique, seules les érosions ont été retenues comme critère de sévérité. Les radiographies des mains et des poignets (de face) ont été réalisées chez 497 patients (86,9%) alors que les radiographies des pieds (de face et ¾) chez 335 patients (58,6%). D’autres radiographies ont été réalisées chez 152 patients (26,6%), ce sont essentiellement des radiographies du bassin, du rachis dorsolombaire, des genoux, du coude et la radiographie du thorax (Tableau 2).
Le score de SHARP global modifié n’a pu être déterminé que chez 333 patients, ceux en possession de radiographies des mains et des pieds, il n’a été déterminé par le médecin investigateur que chez 245 patients. Il est en moyenne de 10,8 ± 19,8 (Tableau 3). Dans 139 cas (56,7%) le score est égal à 0.
Erosions | Pas d’érosions | Erosions | p-value* |
| Mains – Poignets | 3,63 ± 10,06 | 34,27 ± 35,85 | < 10-6 |
| Pieds | 8,00 ± 16,77 | 27,54 ± 27,40 | < 10-6 |
| Sévéritéa | 3,47 ± 10,38 | 27,50 ± 25,36 | < 10-6 |
* Niveau de significativité : p-value < 5%.
L’évaluation de la capacité fonctionnelle par le score HAQ a été réalisée chez 352 patients, il est en moyenne de 0,94 ± 0,74. La PR est jugée sévère chez 173 patients soit 30,2% des cas. La maladie a été notée avec un HAQ moyen de 1,19 ± 0,77 dans la PR sévère versus 0,85 ± 0,71 dans la PR non sévère (p<10-3).
Description du traitement médicamenteux :
Corticothérapie : elle est prescrite chez 423 patients soit 84,1% des cas. Trois molécules sont utilisées. Ce sont ; la prednisone, la méthyl prednisolone et la dexamethasone. La prednisone est prescrite chez 339 patients à une dose moyenne comprise entre 5 et 20 mg/jour ; elle est de 10 mg/jour dans 43,3% et de 5 mg dans 33,0% des cas. En deuxième position vient la méthylprednisone, elle est prescrite chez 225 patients à la dose de 4 mg/jour dans 51,6%, à la dose de 8 mg/jour dans 22% et à la dose de 16 mg/jour dans 7% des cas. La dexamethasone est prescrite chez 3 patients. Chez les patients restants le dosage n’est pas précisé.
Les anti-inflammatoires non stéroïdiens et les antalgiques sont respectivement utilisés par 400 (69,9%) et 467 patients (81,6%).
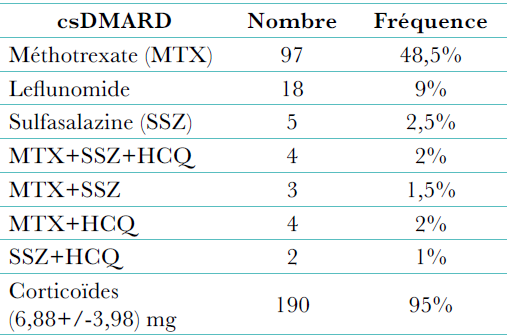
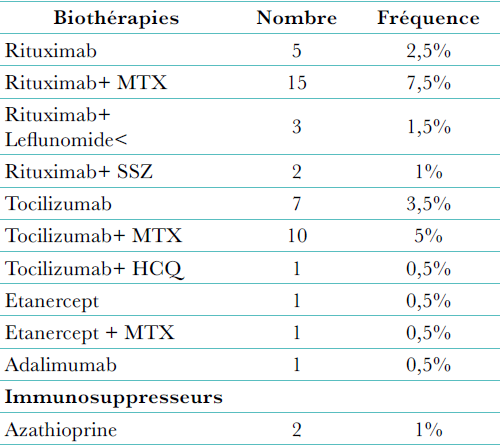
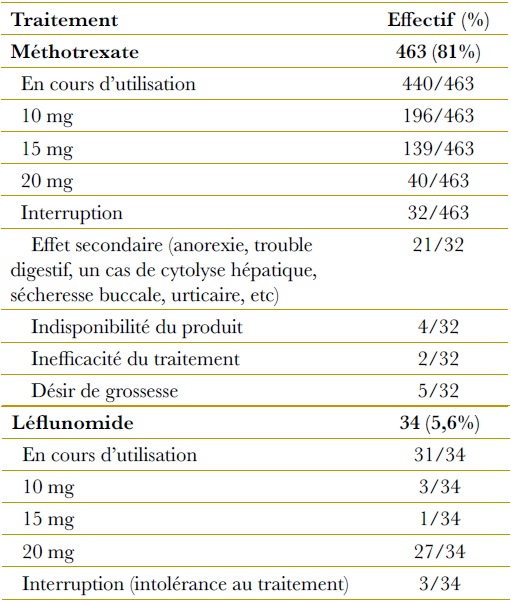
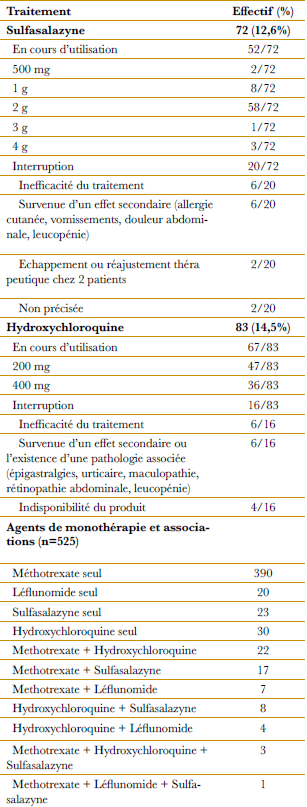
Traitement de fond conventionnel : méthotrexate, leflunomide, sulfasalazyne et hydroxychloroquine sont les quatre (4) molécules utilisées. Une molécule au moins a été prescrite chez 531 patients (92,8%). Le méthotrexate a été utilisé par 463 patients (81%), 441 d’entre eux en consomment encore. La dose la plus donnée est de 10 mg (196 patients). Le traitement a été interrompu chez 32 patients pour survenue d’un effet secondaire chez 21 patients, une indisponibilité du produit chez 4 patients, une inefficacité du traitement chez 2 patients et un désir de grossesse chez 5 patientes. Le leflunomide a été utilisé chez 34 sujets, soit dans 5,6% des cas, il a été interrompu chez 3 patients pour intolérance. La sulfasalazyne a été prescrite chez 72 patients (12,6%), 20 d’entre eux ont interrompu leur traitement. Quant à l’hydroxychloroquine, elle a été utilisée chez 83 patients avec interruption du traitement chez 16 patients. Quelques associations ont été utilisées, elles sont représentées dans le (Tableau 4).
Traitement biologique : parmi les molécules disponibles en Algérie, au moment de l’enquête ; infliximab, étanercept, adalimumab, tociluzimab, et anakinra, seul le rituximab a été prescrit en première intention chez 4 patients, 1 patient est en retraitement. Le rituximab a toujours été associé au méthotrexate. Il s’agissait de patients présentant une PR très active (DAS28 = 5,63), érosive (score SHARP global = 4). Il est à signaler que 41 patients (36 femmes et 5 hommes) de la série
(572) n’ont jamais reçu de traitement de fond. Les PR avaient une durée d’évolution moyenne de 325 ± 141 jours, elles étaient très actives dans 61,0% des cas qui représente 25 patients, le score HAQ , précisé chez 14 patients, est supérieur ou égal à 1 dans 12 cas et le score de SHARP global modifié est en moyenne de 20,7 ± 25,3. La PR est jugée sévère chez 13 patients (31,7%).
Traitement associé : L’acide folique a toujours été associé au méthotrexate. Le calcium est prescrit seul chez 239 patients (41,7%) ou associé à la Vit. D chez 163 patients. On relève des prescriptions en rapport avec des affections associées comme les antidiabétiques oraux, l’insuline ou les antihypertenseurs, ou en rapport avec un effet secondaire, protecteurs gastriques notamment ranitidine, oméprazole et même pansements gastriques.
Étude du traitement selon la sévérité de la maladie : Les corticoïdes sont plus souvent prescrits dans les formes sévères (90,8% dans les PR sévères versus 81,2% dans les PR non sévères p = 0,004) pour autant, la dose moyenne de prednisone n’est pas significativement différente entre les deux formes (p=468). Par contre, la dose moyenne de la méthylprednisolone a différé significativement selon la sévérité de la maladie ; 11,30mg ± 20,02 dans les formes sévères versus 8,49 mg ± 15,85 dans les formes non sévères (p=0,025). La fréquence d’utilisation du traitement de fond conventionnel n’est pas significativement différente entre les deux formes (p=0,468), elle est de 9,29 mg ± 4,04 dans les formes sévères versus 9,50 mg ± 6,45 dans les formes non sévères (p=0,832). Chez Les 41 patients qui n’ont pas reçu ou qui ne reçoivent pas de traitement de fond, 10 ont une PR sévère (21,3%). Le traitement biologique n’est prescrit que chez 4 patients, 3 d’entre eux n’ont reçu qu’une seule cure et une patiente est en retraitement au moment de l’inclusion. La fréquence d’utilisation du traitement n’a pas de relation significative avec la sévérité ou non de la PR ; il n’a pas été noté de lien significatif entre la sévérité de la maladie et le traitement de fond utilisé. En effet, la PR est sévère chez 10 (21,3%) des 47 patients qui n’avaient pas de traitment de fond conventionnel versus 163 (31,1%) des 525 patients qui avaient un traitement de fond conventionnel (p=0,160). Concernant la biothérapie, aucun lien significatif n’a été noté avec la sévérité de la PR entre ces deux variables (p=0,386).
Étude du traitement médicamenteux selon l’activité de la maladie : Les corticoïdes sont utilisés significativement plus fréquemment dans les formes sévères par rapport aux formes non sévères ; (89,8% chez ceux ayant une PR très active versus 78,3% dans les autres formes, p < 10-4), mais en ce qui concerne le traitement de fond conventionnel et la biothérapie, il n’y aucun lien significatif avec l’activité de la maladie, (p=0,754) et (p=0,105).
Scores moyens DAS28, SHARP global modifié et HAQ : Aucun des scores moyens DAS28, SHARP global modifié ou HAQ n’est lié significativement à l’utilisation ou non d’un traitement de fond au moment de l’étude (p=0,828, p=0,794 et p=0,763 respectivement). Ils ne sont aussi pas liés significativement à la présence d’érosions (p=0,165).
La valeur du score moyen DAS28 est liée significativement à la durée d’évolution (p=0,026) (Tableau 5). Le coefficient de corrélation entre délai et score DAS28 est estimé à r=0,09 ; le lien entre ces deux variables est à la limite de la significativité (p=0,070). Mais les scores moyens SHARP global modifié et HAQ ne sont pas liés significativement à la durée d’évolution (p=0,110 et p=0,691 respectivement).
| Délai (en mois) | Effectif | Score DAS28 moyen | p-value* |
| ≤ 6 | 81 | 5,58 ± 1,41 | 0,026 |
| ]6-12] | 163 | 5,53 ± 1,44 | |
| ]12-18] | 140 | 5,74 ± 1,36 | |
| ]18-24] | 93 | 5,13 ± 1,52 |
Retard au diagnostic et retard à la mise en route du traitement de fond :
Le délai séparant la date des premiers symptômes de la date du diagnostic et le retard à la mise en route du traitement de fond sont décrits dans le Tableau 6. Le lien entre le retard au diagnostic et l’activité de la maladie était à la limite de la significativité (p=0,094). Par contre, un lien significatif entre le retard au diagnostic et la sévérité de la maladie a été observé (p=0,032). En parallèle, le lien entre le retard à la mise en route du traitement de fond et l’activité de la maladie était significatif (p=0,038). Le lien entre le retard à la mise en route du traitement de fond et la sévérité de la maladie était à la limite de la significativité (p=0,058).
Évaluation de l’efficacité et des données de tolérance : Aucune évaluation de l’efficacité n’a été prévue par le protocole clinique de l’étude. Aussi, durant la conduite de l’étude, aucun événement indésirable ni autres données de tolérance n’ont été reportés par les investigateurs.
Discussion :
Notre étude est la première étude épidémiologique non-interventionnelle décrivant la prise en charge des patients ayant une polyarthrite rhumatoïde débutante dans la population algérienne consultant dans les secteurs privé et public.
Elle a porté sur 572 sujets présentant une PR débutante et répondant à tous les critères d’éligibilité ; le délai d’évolution était en moyenne de 375 jours. Une prédominance de femmes avec un sexe ratio égal à 0,24 a été conclue. Cette prédominance féminine concorde avec les données françaises où le sexe ratio (0.33) est supérieur à notre résultat(2). Certains facteurs environnementaux liés au genre ont vu le jour. Les femmes qui prennent des contraceptifs oraux ont activement une plus faible incidence de PR (~0,3/1000 années-femmes) par rapport aux femmes qui n’ont jamais pris des contraceptifs oraux (~0.65/1000 années-femmes) ou celles qui ont déjà pris des contraceptifs oraux (~0.55/1000 années-femmes). Aussi, l’hypofécondité des femmes et la période immédiate post-partum après une première grossesse (en particulier lors de l’allaitement) semblent augmenter le risque de PR(15). L’âge moyen est estimé à 45 ans, conformément à la population française où la PR apparaît le plus souvent entre 40 et 60 ans(2). Les caractéristiques de la population enquêtée (poids, taille, IMC, statut marital, niveau d’instruction, situation professionnelle ou couverture médicale) sont comparables à celles de la population générale ayant les mêmes tranches d’âge.
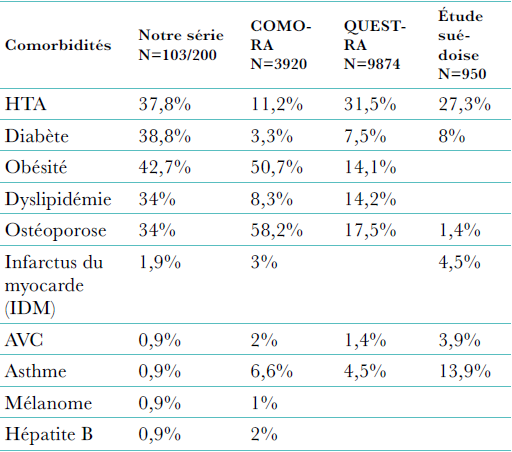
Quant à l’histoire médicale, notre étude a montré que le tiers des patients ont au moins un antécédent personnel ; il s’agit le plus souvent d’une hypertension artérielle ou d’un diabète, plus rarement d’une autre affection auto-immune associée notée chez trois patients. Les antécédents familiaux de rhumatisme inflammatoire chronique étaient également fréquents, notés dans 11,7% des cas, avec une prédominance pour la polyarthrite rhumatoïde ou la spondylarthrite ankylosante.
Les caractéristiques de la maladie à l’inclusion étaient la raideur matinale dont la durée dépasse 60 minutes dans 36 % des cas, les articulations douloureuses dont le nombre a dépassé 10 dans la moitié des cas et les articulations gonflées dont le nombre a dépassé 5 également dans la moitié des cas. L’évaluation globale de la douleur est en moyenne égale à 54, identique à l’évaluation globale de la maladie faite par le malade. Les chiffres sont plus bas lorsque l’évaluation a été faite par le médecin où elle était en moyenne égale à 46.
Les manifestations extra articulaires, notées chez 38 % de la population, sont dominées par la fatigue. Le bilan inflammatoire était le plus souvent perturbé, avec une VS allant jusqu’à 142 et une CRP allant jusqu’à 192. La formule numération sanguine était perturbée chez environ le quart de la population enquêtée (Hb < 10 g/dl, GB < 4000 éléments/mm3 ou GB > 10000 éléments/ mm3). Les transaminases ont dépassé 12 UI/ml dans la moitié des cas, et le bilan immunologique était essentiellement composé du facteur rhumatoïde, plus rarement des anti CCP2, qui étaient positifs dans plus des deux tiers des cas. À savoir que la PR peut par elle-même déterminer des perturbations hépatiques biologiques ou même histologiques dont il faut tenir compte pour interpréter les lésions hépatiques éventuellement constatées chez les patients traités par le méthotrexate(16).
L’évaluation de l’activité de la maladie par le DAS28 a montré que la PR est le plus souvent très active (dans 62% des cas), notons que si le DAS28 est > 5,1, la PR est active et il faudra donc changer le traitement de fond(17). L’évaluation de l’atteinte structurale par le score SHARP global modifié n’a été faite que pour les sujets disposant des radiographies des mains et des pieds ; ce score était en moyenne de 10,8 ± 19,8. L’évaluation de la capacité fonctionnelle par le score HAQ a révélé dans certains cas des données aberrantes, notées plus souvent au niveau de deux centres. La PR a été jugée sévère en présence d’érosions ; la sévérité a été retrouvée dans environ un tiers des cas et n’est pas liée à l’activité de la maladie.
Au niveau du traitement médicamenteux, il était composé de la corticothérapie (85%), des anti-inflammatoires non stéroïdiens (70%), des antalgiques, du traitement de fond (92,8%) dominé par le méthotrexate et la biothérapie. La corticothérapie est d’autant plus utilisée que la PR est sévère et/ou active. Aucun lien significatif n’est retrouvé entre l’utilisation d’un traitement de fond et l’activité ou la sévérité de la maladie.
Fait à signaler, la valeur du DAS28 n’est pas liée significativement à la présence d’érosions ou à l’utilisation ou non d’un traitement de fond. Par contre, il est lié significativement au délai d’évolution de la maladie. Quant aux scores SHARP global modifié et HAQ , ils ne semblent pas liés au traitement de fond ou au délai d’évolution de la maladie.
Le retard au diagnostic et le retard à la mise en route du traitement de fond sont liés significativement ou à la limite de la significativité avec l’activité ou la sévérité de la maladie. Cependant, la mise en place précoce d’un traitement efficace est une des meilleures garanties pour prévenir ou limiter une évolution défavorable dans la PR. La mise en place d’un traitement efficace rapidement nécessite donc un diagnostic précoce, avant la survenue de lésions articulaires irréversibles(18).
Références
- Gibofsky A. Overview of epidemiology, pathophysiology, and diagnosis of rheumatoid arthritis. Am j Manag Care. 2012;18(13 Suppl):S295-302.
- Inserm. Polyarthrite rhumatoïde. Février 2011. Disponible sur : http://www.inserm.fr/thematiques/physiopathologie-metabolisme- nutrition/dossiers-d-information/polyarthrite-rhumatoide. Dernier accès : 03 juin 2015.
- Gaujoux-Vialaa C, Gossec L, Cantagrel A, Dougados M, Fautrel B, Mariette X, Nataf H, Saraux A, Trope S, Combei B. Recommanda- tions de la Société française de rhumatologie pour la prise en charge de la polyarthrite rhumatoïde. Revue du Rhumatisme 2014 ; 81(4):303-12.
- Aletaha D, Neogi T, Silman Aj, Funovits j, Felson DT, Bingham CO 3rd, Birnbaum NS, Burmester GR, Bykerk VP, Cohen MD, Combe B, Costenbader KH,Dougados M, Emery P, Ferraccioli G, Hazes jM, Hobbs K, Huizinga TW, Kavanaugh A, Kay j, Kvien TK, Laing T, Mease P, Ménard HA, Moreland LW, Naden RL, Pincus T, Smolen jS, Stanislawska-Biernat E, Symmons D, Tak PP, Upchurch
- KS, Vencovsky j, Wolfe F, Hawker G. 2010 rheumatoid arthritis clas- sification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Ann Rheum Dis. 2010; 69(9):1580-8.
- Young A, Dixey j, Cox N, Davies P, Devlin j, Emery P, Gallivan S, Gough A, james D, Prouse P, Williams P, Winfield j. How does func- tional disability in early rheumatoid arthritis (RA) affect patients and their lives ? Results of 5 years of follow-up in 732 patients from the Early RA Study (ERAS). Rheumatology. 2000; 39:603-611.
- jantti j, Aho K, Kaarela K, Kautiainen H. Work disability in an inception cohort of patients with seropositive rheumatoid arthritis : a 20 year study. Rheumatology. 1999; 38:1138-1141.
- Cutolo M, Kitas GD, van Riel PL. Burden of disease in treated rheumatoid arthritis patients: going beyond the joint. Semin Arthritis Rheum. 2014; 43(4):479-88.
- Dellhag B, Bjelle A. A five-year follow-up of hand function and activities of daily living in rheumatoid arthritis patients. Arthritis Care Res. 1999;12:33-41.
- Wolfe F, Hawley Dj. The longterm outcomes of rheumatoid arth- ritis :Work disability : a prospective 18 year study of 823 patients. j Rheumatol. 1998; 25:2108-2117.
- Huscher D, Mittendorf T, von Hinüber U, Kötter I, Hoese G, Pfäfflin A, Bischoff S, Zink A; German Collaborative Arthritis Centres. Evolution of cost structures in rheumatoid arthritis over the past decade. Ann Rheum Dis. 2015; 74(4):738-45.
- Fautrel B, Gaujoux-Viala C. Aspects médico-économiques de la polyarthrite rhumatoïde. Bull Acad Natl Med. 2012 Oct;196(7):1295- 305; discussion 1305-6.
- Huscher D, Mittendorf T, von Hinüber U, Kötter I, Hoese G, Pfäfflin A, Bischoff S, Zink A; German Collaborative Arthritis Centres. Evolution of cost structures in rheumatoid arthritis over the past decade. Ann Rheum Dis. 2015;74(4):738-45.
- Hallert E, Husberg M, Kalkan A, Skogh T,Bernfort L. Early rheumatoid arthritis 6 years after diagnosis is still associated with high direct costs and increasing loss of productivity: the Swedish TIRA project. Scand j Rheumatol. 2014; 43(3):177-83.
- D.M. Van der Heijde, How to read radiographs according to the Sharp/van der Heijde Method, j Rheumatol 2000; 27:261-3.
- Silman Aj, Pearson jE. Epidemiology and genetics of rheumatoid arthritis. Arthritis Res. 2002;4(suppl 3):S265-S272.
- jacques Sany. La polyarthrite rhumatoïde de l’adulte : Conception actuelle Broché – 16 décembre 2003.
- Rhumato.info. Evaluation de la polyarthrite rhumatoïde. Dispo- nible sur : http://www.rhumato.info/cours-revues2/115-polyarth- rite-rhumatoide/1699-evaluation-de-la-polyarthrite-rhumatoide. Dernier accès : 03 juin 2015.
- Pr Bernard Combe, CHU de Montpellier. Diagnostic et pronostic de la polyarthrite rhumatoïde. journée nationale de l’ANDAR, Paris, 25 Septembre 2009. Disponible sur : http://www.rhumatologie.asso. fr/04-Rhumatismes/stop-rhumatismes/pdf-upload/GP_polyarthrite_