Mounira AMER YAHIA Pr Rachid DENINE CHU Beni Messous, Faculté de Pharmacie d’Alger
Introduction :
En matière de recherche, dans le cadre de l’amélioration des soins, on peut distinguer deux axes, deux intérêts :
- La découverte d’agents pharmacologiques nouveaux capables d’offrir une activité inexistante ou une activité plus intense : on peut parler alors d’innovation thérapeutique.
- La transformation, grâce à des artifices galéniques, de formes pharmaceutiques contenant la molécule active connue en vue d’en modifier la pharmacocinétique : on parle alors d’innovation galénique conduisant aux Systèmes de Délivrance des Médicaments (S.D.M.).
Les systèmes de délivrance des médicaments (S.D.M.)
D.D.S. est le sigle anglo-saxon utilisé pour Drug Delivery System. En français, ce terme se traduit par « système de délivrance des médicaments » (S.D.M.) alors que le terme exact devrait être « système de délivrance de substances actives ».
Doit être considéré comme S.D.M. toute forme ou tout dispositif médical visant à améliorer le ratio bénéfice/ risque d’un médicament grâce à la maitrise de la vitesse, du moment ou du site de libération, dans l’organisme, de la substance pharmacologiquement active. De plus, doit être ajouté à ce domaine tout système capable de favoriser l’observance des patients.
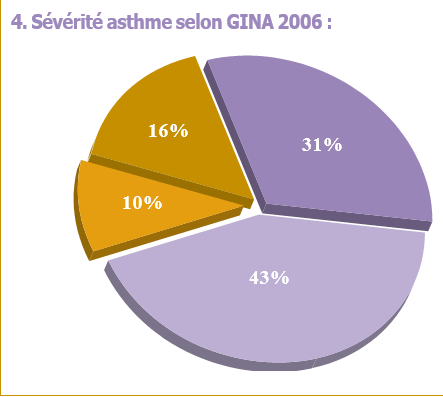
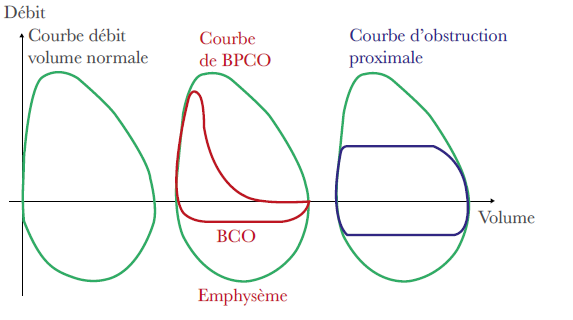
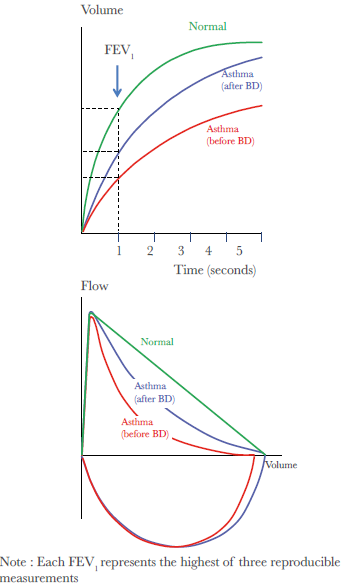
- Voie respiratoire (25 %). Ce sont des nébuliseurs et inhalateurs divers. Traitement de l’asthme,
- Voies muqueuses (10 %). Administration des peptides et des protéines (évite l’effet du premier passage hépatique) par des formes diverses pour voies buccales (intra orale), nasale, vaginale, etc.,
- Voie parentérale (6 %). Formes à libération prolongée, implants, etc. dans le traitement des cancers, administration des peptides et des protéines, etc.,
- Voie transdermique (6 %). Systèmes transdermiques dans le traitement de l’angor, du sevrage tabagique, la douleur, etc.
Il serait difficile de faire une liste exhaustive de toutes les innovations galéniques existantes ; les plus importantes seront cependant traitées.
La voie orale
La voie orale demeure la voie d’administration majeure des médicaments pour des raisons évidentes de simplicité et de coût. Néanmoins, afin d’améliorer l’observance des traitements, de nombreuses recherches ont eu pour but d’optimiser les formes d’administration orale, principalement de façon à réduire le nombre de prises journalières. C’est ainsi que sont nés les systèmes à libération modifiée, issus de différents concepts :
- Accélérer la libération : formes dites à « libération accélérée » (lyophilisats oraux, comprimés solubles, dispersibles et orodispersibles) ;
- Différer la libération : formes dites à libération différée (gastro-résistantes par exemple) ;
- Accroitre la durée d’action : formes dites à « libération prolongée » (ex : matrices) ;
- Maîtriser la vitesse de libération : formes dites à « libération contrôlée » (ex : systèmes osmotiques);
- Sélectionner le site de libération au niveau du tube digestif : formes dites à libération « ciblée » (colonique par exemple).
Les progrès réalisés dans la granulation et la gamme de polymères disponibles ayant différentes propriétés physicochimiques (comme la cellulose modifiée ou les dérivés de l’amidon) ont permis de concrétiser ces différentes approches.
Les formes à « libération accélérée »
Le problème de l’accélération de la libération de la substance active se pose surtout pour la voie orale et concerne notamment certains médicaments, tels les antalgiques, pour lesquels est souhaitable une action aussi rapide que possible.
L’une des premières solutions est venue des comprimés effervescents. Imaginée dès la fin du XIXe siècle, cette forme s’est surtout développée au cours des années 1960 et connaît encore aujourd’hui le succès : 80 spécialités commercialisées en France.
Beaucoup plus récente, la forme « lyophilisat oral » commercialisée sous le nom de « Lyoc® » est une innovation française (Laboratoires Lafon) des années 1980. Elle est utilisée, en France, pour administrer plusieurs substances actives : piroxicam, paracétamol, nicergoline, etc.
Aux deux formes précédentes est venue s’ajouter toute une série de systèmes caractérisés par une dissolution ou une dispersion très rapide au sein même de la bouche (en moins de trois minutes, selon la pharmacopée européenne). Appelés « formes orodispersibles », ces systèmes sont préparés selon une technologie qui leur est propre.
Parmi les substances actives commercialisées sous cette forme figurent le paracétamol, l’ibuprofène, la ranitidine, etc.
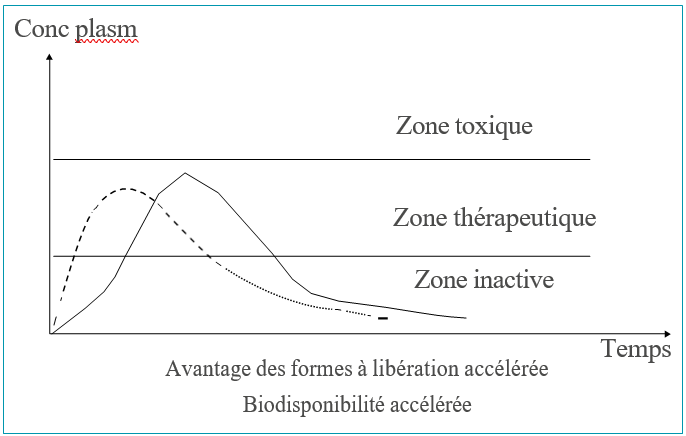
Les comprimés à libération accélérée, bien que d’aspect classique, doivent être dissous ou dispersés dans de l’eau avant administration ou en présence de salive. Ils présentent donc, en complément des avantages des comprimés conventionnels, une biodisponibilité accélérée comparable à celle des formes liquides.
Les lyophilisats oraux
Les lyophilisats oraux sont des formes galéniques originales qui ont tout à fait leur place dans l’arsenal thérapeutique actuel.
Ce sont des produits solides obtenus par sublimation de l’eau après congélation, selon un procédé dénommé lyophilisation ou cryodessiccation, de préparations aqueuses, liquides ou pâteuses, qui contiennent un ou plusieurs principes actifs.
Les lyophilisats sont caractérisés par une masse compacte ou granuleuse lyophile, de structure généralement poreuse. Par leur grande porosité et leur forte avidité pour l’eau (ils sont dits « lyophiles »), ils se dissolvent ou se dispersent très rapidement à son contact. De plus, ils peuvent être utilisés par voie sublinguale (contact immédiat avec la salive sans apport d’eau extérieur), ce qui accélère l’absorption de certains principes actifs, notamment s’ils sont solubles dans l’eau.
Grâce à ces caractéristiques, les lyophilisats possèdent des intérêts non négligeables du point de vue de la biodisponibilité qui pourra être accrue ou accélérée et de l’observance qui sera nettement facilitée chez de nombreux patients.
Toutefois, leur formulation, essentiellement liée au procédé de fabrication, est délicate, notamment en raison des conditions opératoires de lyophilisation, opération définie comme une cryodessiccation c’est-à-dire une dessiccation par sublimation d’un système préalablement congelé. Leur procédé de fabrication est donc délicat et nécessite une installation spécifique.
Domaines d’application en thérapeutique
- Les analgésiques (Paralyoc®) ;
- Les antispasmodiques (Spasfon Lyoc®) ;
- Les anti-inflammatoires (Feldène®, Piroxicam Béral®, Proxalyoc®) ;
- Les antidiarrhéiques (Lopéramide Lyoc®) ;
- Les antihistaminiques (Allergefon Lyoc®) ;
- Les antiémétiques (Motilium®, Vogalène Lyoc®, Zophren®) ;
- Les antimigraineux (Dihydroergotoxine RPG®, Séglor Lyoc®, Migrof®) ;
- Les antiulcéreux (Pepdine®, Ulfon Lyoc®) ;Les antihypertenseurs (Rénitec®) ;
- Les antivertigineux (Tanganil Lyoc®).
Les comprimés solubles, dispersibles et orodispersibles
Les comprimés solubles, dispersibles et orodispersibles sont apparus récemment et trouvent leur place à côté des lyophilisats oraux, formes plus contraignantes au niveau de leur fabrication.
Les comprimés solubles « Ce sont des comprimés non enrobés ou des comprimés pelliculés. Ils sont destinés à être dissous dans de l’eau avant administration. La solution obtenue peut être légèrement
opalescente en raison de la présence d’excipients ajoutés lors de la fabrication des comprimés ».
Les comprimés dispersibles « Ce sont des comprimés non enrobés ou des comprimés pelliculés destinés à être dispersés dans de l’eau avant administration, en donnant une dispersion homogène».
Les comprimés orodispersibles « Ce sont des comprimés non enrobés destinés à être placés dans la bouche où ils se dispersent rapidement avant d’être avalés ».
Leur formulation est basée sur l’introduction de « superdé-sintégrants » qui accélèrent la dissolution ou la dispersion du principe actif par éclatement du comprimé lors de son contact avec l’eau ou avec la salive.
Les principaux délitants rencontrés dans la formulation des comprimés dispersibles sont :
Carboxyméthylamidon sodique (Explotab® ou Primojel®)
- Cellulose microcristalline (Avicel PH101® ou Avicel PH102®)
- Carboxyméthylcellulose sodique réticulée (Ac-Di-Sol®)
- Crospovidone : Polyplasdone XL® ou Kollidon CL®
Domaines d’application en thérapeutique
- Les antibiotiques comme l’Amoxicilline en comprimés dispersibles (Agram®, Amoxicilline EG, RPG, RATIOPH®. Flemoxine®), le céfadroxil (Oracéfal® dispersible) et la josamycine (Josacine® dispersible) ;
- Les analgésiques comme le paracétamol (Febrectol® dispersible, Dolflash®. Dolitabs® et Efferalganodis® pour les comprimés orodispersibles) ;
- La prednisolone (Solupred® orodispersible), la bétaméthasone (Célestène® dispersible), la nabumétone (Nabucox® dispersible) et le piroxicam (Feldène® dispersible, Piroxicam® Merck dispersible) ;
- Les antimigraineux comme le zolmitriptan (Zomigoro® orodispersible);
- Les antiépileptiques comme la lamotrigine (Lamictal® dispersible);
- Les antiparkinsoniens comme la lévodopa (Modopar® dispersible);
- Les antidépresseurs comme la fluoxétine (Prozac® dispersible).
Les formes dites à libération différée : Les comprimés gastrorésistants
« Les comprimés gastro-résistants sont des comprimés destinés à résister à l’action du suc gastrique et à libérer le ou les principes actifs dans le suc intestinal ».
Cet effet est obtenu grâce à un revêtement gastrorésistant qui est insoluble dans le suc gastrique c’est-à-dire en milieu chlorhydrique mais se dissout en milieu neutre ou légèrement alcalin.
L’enrobage le plus classique est réalisé avec l’acétophtalate de cellulose. À côté de l’acétophtalate de cellulose on utilise actuellement de plus en plus le phtalate d’hypromellose et des dérivés méthacryliques, polymères comportant aussi des fonctions acides libres.
Les formes dites à « libération prolongée » : Les matrices « Les matrices sont des supports constitués d’excipients physiologiquement tolérés, plus ou moins inertes qui ne se désagrègent pas et forment un réseau piégeant le médicament ».
Elles sont caractérisées par la présence d’une dose unique de principe actif. La matrice comporte des canalicules où se trouve emprisonné le principe actif.
La libération du principe actif hors de la matrice se déroule en trois phases :
- Pénétration des liquides digestifs dans les canalicules de la matrice.
- Dissolution du principe actif par les liquides.
- Diffusion de la solution de principe actif de l’intérieur de la matrice vers la surface du compartiment médicamenteux.
Selon la nature du support et le mécanisme de libération, on distingue :
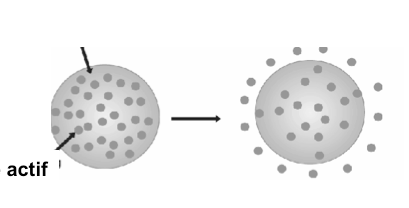
Les matrices inertes
Elles sont composées de supports indéformables qui après dissolution et diffusion du principe actif seront éliminées intactes dans les selles.
Polymère
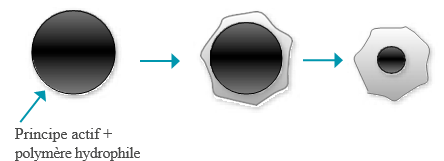
Les matrices hydrophiles
Elles ont la propriété de gonfler après hydratation par les liquides digestifs. Ceci est dû à l’excipient utilisé: c’est un polymère hydrophile qui au contact de l’eau gonfle et forme une barrière gélifiée qui s’oppose à la libération rapide du principe actif et régularise la pénétration du liquide à l’intérieur du comprimé.
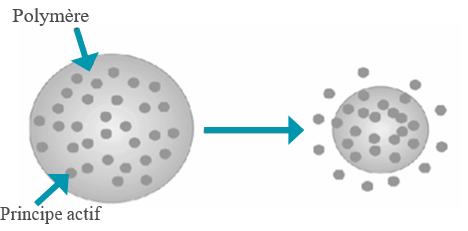
Les matrices érodables
Elles ont la particularité de s’éroder lors du transit gastro-intestinal sous l’action des enzymes ou du pH.
La libération résulte à la fois de l’érosion se produisant à la surface du comprimé et de la diffusion du principe actif à l’intérieur de la matrice.
Applications thérapeutiques
- Les antihypertenseurs de type bétabloquant (propranolol) ou de type antagoniste calcique (nifédipine) ;
- Les anti-inflammatoires (indométacine) ;
- Les antiasthmatiques (théophylline) ;
- Les analgésiques (morphine).
- Les formes à « libération contrôlée » : Les systèmes osmotiques
Dans le cas le plus simple, le dispositif est constitué d’un noyau solide contenant le principe actif souvent mélangé à un agent osmotique (NaCl ou KCl), et d’une membrane polymérique semi perméable entourant l’ensemble. Cette dernière présente un petit orifice percé au laser destiné au passage du produit dans le milieu extérieur. Ce système encore appelé pompe osmotique élémentaire est breveté par Alza Corp, sous le nom OROS®. L’eau pénètre donc à travers la membrane par simple appel osmotique. Cet apport de solvant augmente la pression et assure la libération d’un volume égal de solution saturée de principe actif à travers l’orifice.
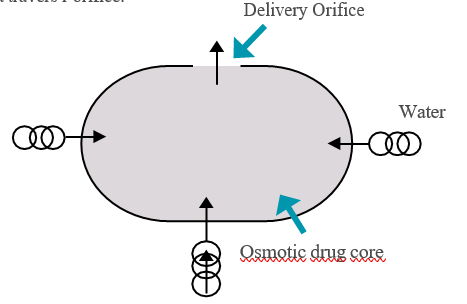
La vitesse de libération est contrôlée par les propriétés osmotiques du noyau, la surface de la membrane, son épaisseur et sa perméabilité à l’eau.
Un certain nombre de modifications de ce système sont disponibles aujourd’hui, comme la pompe osmotique push-pull®, qui est un comprimé bicouche approprié à la libération des principes actifs de grande taille ou faiblement solubles dans l’eau. La couche supérieure est composée du principe actif seul ou avec des agents osmotiques. La couche inférieure est composée d’agents osmotiques polymériques. Le comprimé est enrobé d’une membrane semi perméable présentant un petit orifice.
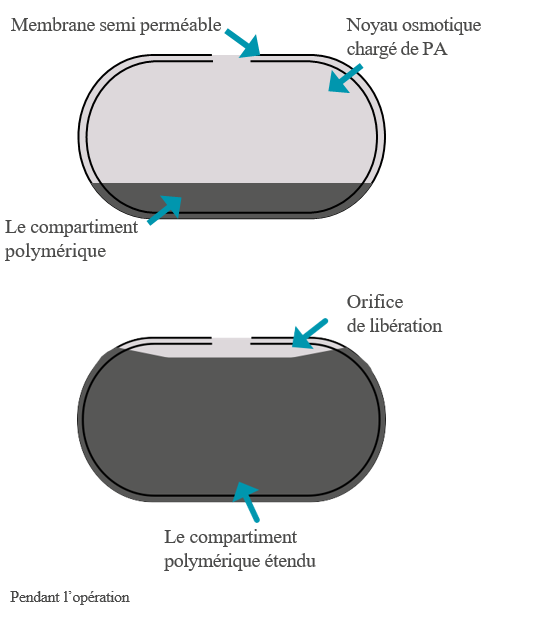
La pompe osmotique push pull®
Ces dispositifs présentent l’avantage de pouvoir assurer une libération constante et indépendante des conditions extérieures. Le problème majeur reste leur coût de fabrication élevé.
Applications thérapeutiques
| Nom commercial | DCI | Société pharmaceutique | Indication |
| Procardia XL® | Nifedipine | Alza/Pfizer | Hypertension/angine de poitrine |
| Tiamate® | Diltiazem | Merck/Aventis | Hypertension |
Les formes dites à « libération ciblée » : colonique
Bien que l’intestin grêle soit le site principal pour l’absorption du médicament et est par conséquent la zone préférée du tractus gastro-intestinal à cibler, un intérêt considérable s’est manifesté dans le ciblage du colon ces dernières années.
Les raisons principales sont :
- L’activité protéolytique réduite au niveau du colon ; ce qui peut être avantageux dans le ciblage de certains médicaments comme les protéines et les peptides dégradés par les enzymes de l’estomac ou de l’intestin grêle ;
- Le traitement topique des carcinomes et des maladies inflammatoires de l’intestin.
Afin d’atteindre la libération dans le colon, le début de libération du principe actif est contrôlé en augmentant l’épaisseur de l’enrobage, permettant une dissolution du polymère et une libération du principe actif dépendantes et du pH et du temps.
Domaines d’application en thérapeutique Oros CT® (Alza Corporation) est un système administré une ou deux fois par jour. C’est une forme galénique basée sur les principes de la pression osmotique.
Les avancées de la technologie de la libération modifiée sont attribuées au développement de nouveaux polymères biocompatibles et de machines qui permettent la fabrication de nouvelles formes galéniques de façon reproductible. Ils présentent de nombreux avantages :
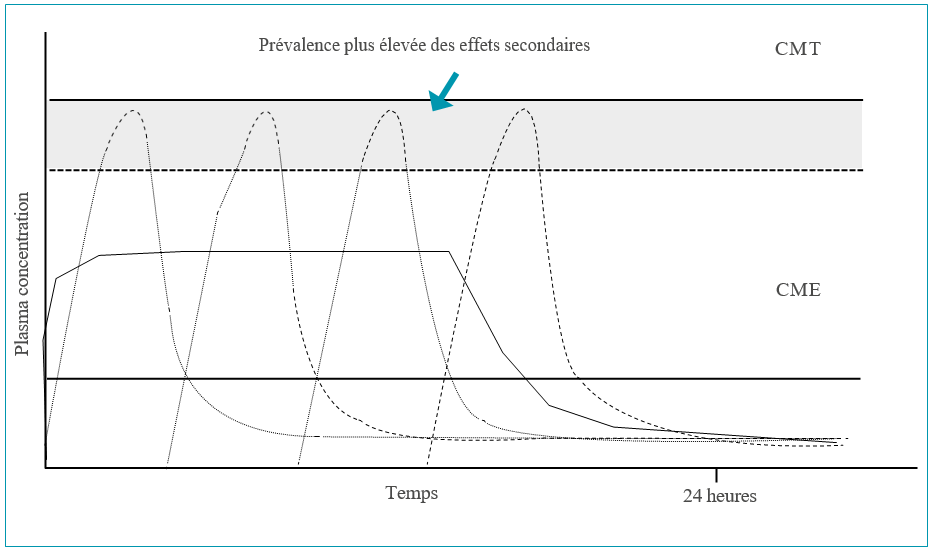
- Avantage thérapeutique : réduction des fluctuations au niveau plasmatique ; maintien d’un niveau plasmatique stable du principe actif sur une période prolongée.
- Réduction des effets secondaires et amélioration de la tolérance.
- Confort et compliance du patient.
- Réduction du coût des soins médicaux.
Néanmoins, aussi sophistiqués que soient ces systèmes, la durée totale de libération « utile » par voie orale est limitée à la durée du transit gastro-intestinal (moins de 12 heures en général). Par ailleurs, des variabilités interindividuelles importantes peuvent être rencontrées en termes de biodisponibilité des formes à libération modifiée, en raison de la variabilité du transit gastro-intestinal selon les individus
(âge, sexe, pathologie, …) ou l’alimentation. En conséquence, parvenir à concevoir des formes d’administration orale dont la durée d’action pourrait être plus indépendante du transit représente un réel enjeu. C’est ainsi qu’est né le concept d’augmentation du temps de résidence gastrique.
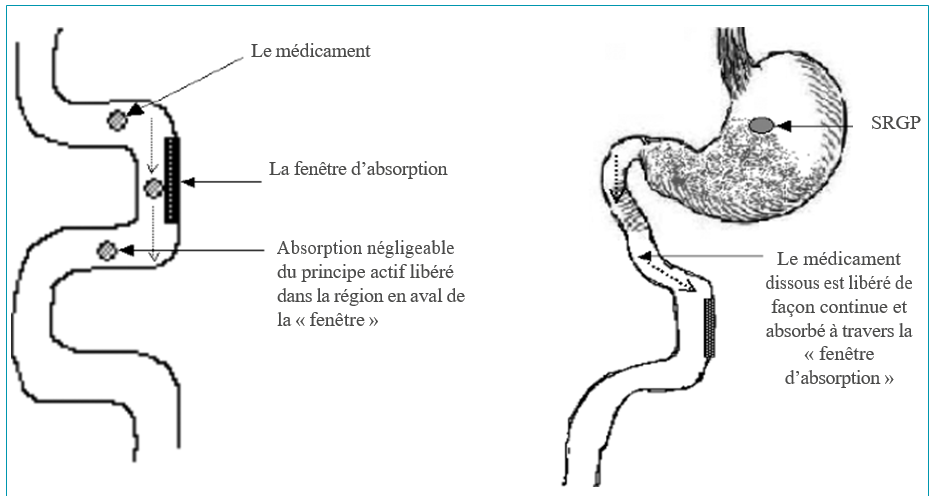
Les systèmes à libération gastrique prolongée
Diverses approches ont été développées pour répondre au besoin de rétention de certains principes actifs plus longtemps dans l’estomac.
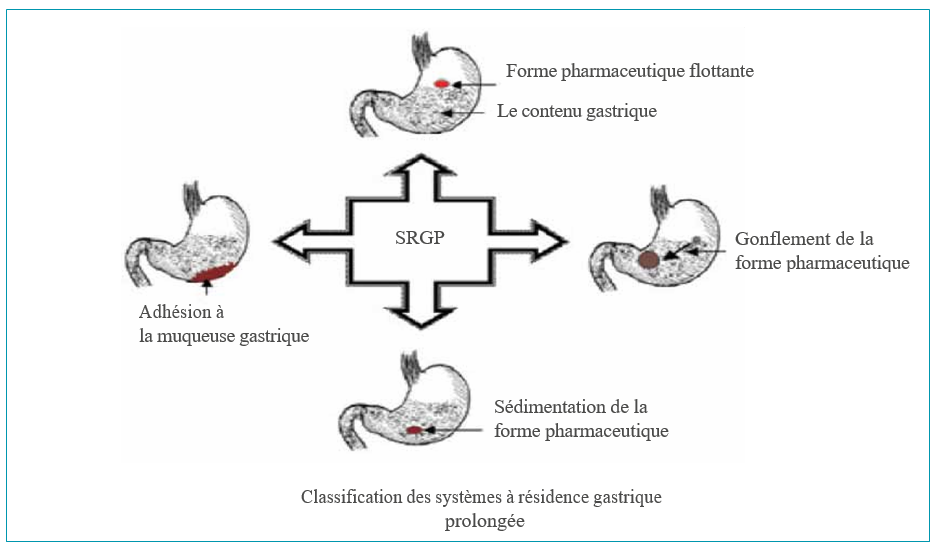
Les formes pharmaceutiques flottantes
Elles sont conçues de façon à présenter une densité nettement inférieure à 1 pour flotter à la surface du contenu gastrique. La majorité d’entre elles est à base d’un polymère hydrophile gonflant dans l’estomac. Elles diffèrent néanmoins par le moyen utilisé pour abaisser la densité de la forme finale :
Formulation du polymère hydrophile seul :
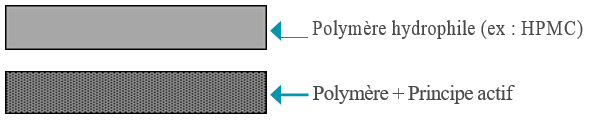
Modopar LP®: actuellement commercialisé par les laboratoires Roche, des gélules renfermant de la L-Dopa et du bensérazide.
– Formulation du polymère hydrophile additionné d’un mélange effervescent générant du gaz carbonique.
L’idée consiste à générer des bulles de gaz au sein des formes pharmaceutiques pour les faire flotter. Le principe le plus courant est d’incorporer à la formulation des substances effervescentes qui génèrent du gaz carbonique au contact de l’eau.
Un système a été proposé par Ishikawa et al. générant des « microballons ».
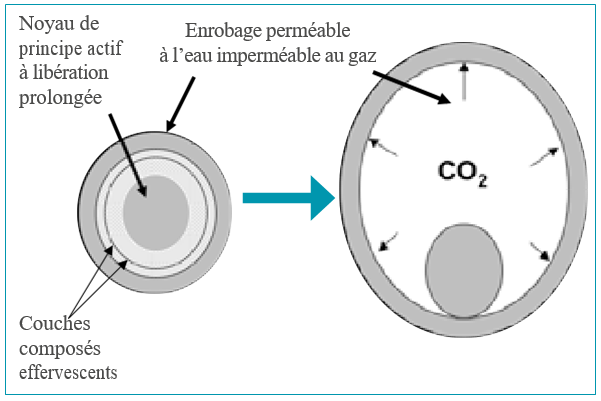
In vitro, la flottabilité des formes est obtenue plus rapidement qu’en l’absence d’effervescence et de façon plus prolongée.
In vivo, le temps moyen de résidence gastrique est aussi prolongé : jusqu’à 4 h chez le chien à jeun.
Les systèmes de densité élevée (d>1,4)
En réalité, les études in vivo réalisées jusqu’à ce jour sont peu concluantes, et il semblerait qu’il faille atteindre des densités de 2,4 à 2,8 g/ml, combinées à une taille suffisante pour observer une augmentation sensible du temps de résidence gastrique chez l’homme.
Les systèmes de grande taille (dépliables et gonflants)
Les systèmes dépliables : l’idée est de concevoir un système géométrique de grande taille (2 à 5 cm) qui puisse être replié de façon à pouvoir être transporté dans une gélule. Certains ont également imaginé une sorte de ressort dont les différentes lames sont maintenues collées par de la gélatine avant administration.
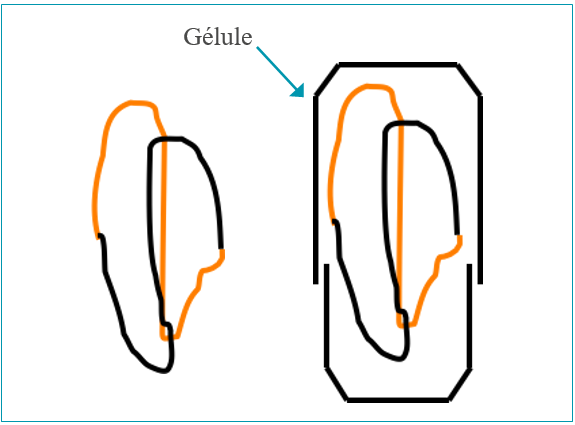
Ces systèmes présentent cependant un certain nombre d’inconvénients :
- Systèmes difficilement industrialisables.
- Ils n’ont pas une réelle supériorité en termes d’augmentation du temps de résidence gastrique par rapport aux autres systèmes existants.
- Il est indispensable de les formuler à base de polymères biodégradables assurant la désagrégation de la forme. Ces polymères sont très sensibles à l’hydrolyse, donc de conservation délicate.
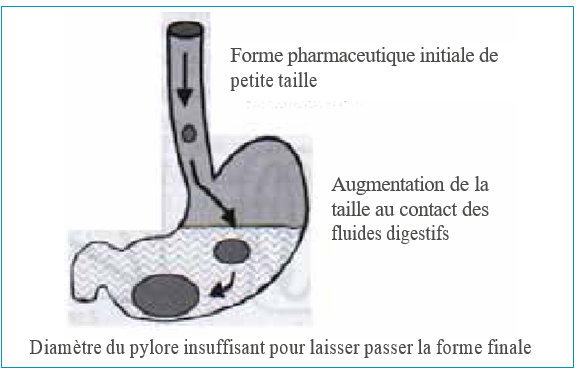
Les systèmes gonflants : l’idée est ici d’administrer une forme pharmaceutique solide qui pourra gonfler au contact des fluides digestifs de façon à atteindre une taille supérieure au diamètre d’ouverture du pylore.
L’augmentation de taille peut résulter de mécanismes différents :
- Gonflement d’hydrogels, formulés sous forme de matrices ;
- Gonflement d’agents osmotiques (sucres) ou hydrocolloïdes inclus dans un système réservoir enrobé par un polymère perméable et élastique.
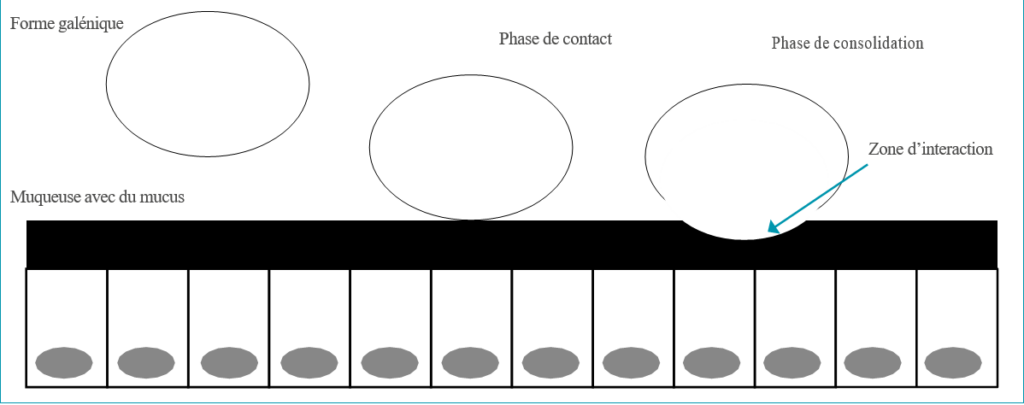
Les systèmes bioadhésifs
Le concept repose sur l’adhésion d’une forme pharmaceutique à la surface de la muqueuse digestive. Le principe consiste à utiliser des polymères capables de gonfler en milieu aqueux et d’interagir avec les macromolécules présentes dans le mucus recouvrant les muqueuses.
Les plus utilisées sont les polymères (acides acryliques) comme les Carbopols®, diversement réticulés.
Les résultats obtenus in vivo après administration orale sont décevants.
Les polymères utilisés ayant de très bonnes propriétés bioadhésives, il faut les transporter dans une gélule afin d’éviter une mucoadhésion prématurée dans la cavité buccale ou l’œsophage. Malheureusement, après dissolution, la gélatine est susceptible d’interférer avec les Carbopols®. Il en est de même pour la mucine libre dans les fluides biologiques, ce qui peut conduire à inhiber le processus de bioadhésion.
Conclusion
L’innovation galénique apporte de nombreux avantages tant sur le plan thérapeutique que sur le plan commercial. Son objectif est double :
- Proposer des formes originales et innovantes permettant d’améliorer la performance en termes d’observance du patient, sécurité et efficacité ;
- Remplacer la forme déclinante par une nouvelle forme afin d’avoir un avantage compétitif et d’augmenter la part de marché des produits.
Bibliographie
- FRANCOISE FALSON – RIEG, VINCENT FAIVRE, FABRICE PIROT; Nouvelles formes médicamenteuses (2004).
- PASCAL WEHRLE; Pharmacie galénique, formulation et technologie pharmaceutique (2007).
- Fan L.T. and S.K. Singh. 2008. Controlled release: a quantitative treatment. New York : Springer- Verlag.
- BURI P. et DOELKER E. Formulation des comprimés à libération prolongée – Pharm. Acta Helv. 55, 189-197, 2002.
- DESHPANDE A.A., RHODES C.T. SHAH N.H. MALICH A.W. (1996). Controlled release drug delivery systems for prolonged gastric residence: an overview. Drug. Dev. Ind. Pharm, 22 (6), 531 – 539.
- BAUMGARTNER S., KRISTL J., VRECER F., VODOPIVEC P.,ZORKO B. (2000). Optimisation of floating matrix tablets and evaluation of their gastric residence time. Int. J. Pharm., 195 (1-2) : 125 – 135. 7 – SAKR F.M. (1999). A programmable drug delivery system for oral administration. Int. J. Pharm., 184 (1) : 131 – 139.
- AULIN N. (1999). Optimisation de la fabrication des comprimés dispersibles. Th. Pharm., Paris V.
- LE HIR A. (2001). Comprimés. In : Pharmacie galénique. Bonnes pratiques de fabrication des médicaments. 8ème édition, Masson, Paris, 251 – 277.
- ROSSETTO Y. (1998). Excipients. In : Pharmacotechnie Industrielle φ 41, IMT Editions, Vendôme, 183 – 201.