Pr H. BENDAOUD, Dr H. BOUNEGHAR, Pr M. DERGUINI, Service de gynéco-obstétrique, EPH Kouba, Alger.
Abstract :
Menopause, a natural stage of life is perceived by women in more or less positive way by women and their families. Menopause means the cessation of menstruation, it can be either natural or surgical.
The median age of natural menopause in the population is between 50 and 51 years.
Menopause diagnosis is clinical, it is therefore based solely on clinical symptoms and signs.
The main difficulties encountered by women in menopause due to lower estrogen. Each sound on women’s quality of life in general from the beginning of menopause or early : hot flashes, sexual difficulties. Others alter the long-term health : arterial disease (myocardial infarction and stroke) and bone (osteoporosis) which are mainly related to age and certain predispositions. They can be worsened by estrogen deficiency.
The hormonal treatment (HRT) remains the cornerstone of the medical management of post-menopause.
Résumé :
La ménopause, étape naturelle de la vie est perçue par les femmes de manière plus ou moins positive.
La ménopause signifie la cessation des règles, elle peut être naturelle ou chirurgicale.
L’âge médian de la ménopause naturelle dans la population est compris entre 50 ans et 51 ans.
Le diagnostic de ménopause est clinique, il s’appuie donc uniquement sur les symptômes et signes cliniques.
Les principales difficultés rencontrées par les femmes à la ménopause sont dues à la diminution des estrogènes. Les unes retentissent sur la qualité de vie des femmes, en général dès le début de la ménopause ou précocement : les bouffées de chaleur, les difficultés sexuelles. Les autres altèrent la santé à long terme : les maladies artérielles (infarctus du myocarde et accident vasculaire cérébral), et osseuses (l’ostéoporose) qui sont principalement liées à l’âge et à certaines prédispositions. Elles peuvent être aggravées par la carence en estrogènes.
Le traitement hormonal de la ménopause (THM) reste la pierre angulaire de la prise en charge médicale de la post-ménopause.
Mots-clés : Ménopause, œstrogènes, troubles climatériques, conséquences à long terme, qualité de vie et de survie, THM.
Introduction :
Menopause, a natural stage of life is perceived by women in more or less positive way by women and their families. Menopause means the cessation of menstruation, it can be either natural or surgical.
The median age of natural menopause in the population is between 50 and 51 years.
Menopause diagnosis is clinical, it is therefore based solely on clinical symptoms and signs.
The main difficulties encountered by women in menopause due to lower estrogen. Each sound on women’s quality of life in general from the beginning of menopause or early : hot flashes, sexual difficulties. Others alter the long-term health : arterial disease (myocardial infarction and stroke) and bone (osteoporosis) which are mainly related to age and certain predispositions. They can be worsened by estrogen deficiency.
The hormonal treatment (HRT) remains the corner-stone of the medical management of post-menopause.
Introduction :
Les étapes de la vie hormonale de la femme commencent de la puberté à la ménopause selon un rythme physiologique très marqué. D’où l’intérêt de l’accompagner de la puberté à la ménopause.
La ménopause, étape naturelle de la vie est perçue par les femmes de manière plus ou moins positive.
L’espérance de vie des femmes en Algérie est actuellement en moyenne de 80 ans ; une femme vivra un tiers de sa vie pendant cette période. Il est donc important d’apprécier les manifestations présentes dans cette période afin de juger de l’opportunité d’un traitement préventif et/ou d’explorations particulières.
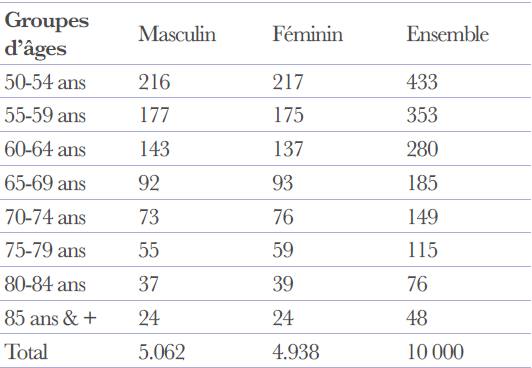
Tableau 1 : Structure de la population par âge et sexe (pour 10 000) au 01/07/2014
Qu’est-ce que la ménopause ?
(méno = la menstruation ou les règles ; pause = arrêt) (pré = avant ; péri = période avant et après ; post = après).
- La pré-ménopause désigne la période allant de la puberté jusqu’à la péri ménopause confirmée.
- La ménopause signifie la cessation des règles ; mais l’arrêt définitif des règles étant précédé de plusieurs mois à plusieurs années d’irrégularités dans les cycles.
- La péri ménopause (autrefois appelée en France pré-ménopause) comprend la période d’irrégularités des cycles menstruels précédant la ménopause et l’année qui suit l’arrêt apparent des règles.
- La post-ménopause ou la ménopause confirmée désignent la période de la vie féminine s’écoulant après la ménopause.
– La ménopause peut être naturelle ou chirurgicale.
Le diagnostic de ménopause est donc rétrospectif devant la constatation d’une aménorrhée d’une durée supérieure ou égale à 12 mois. (OMS)

ménopause
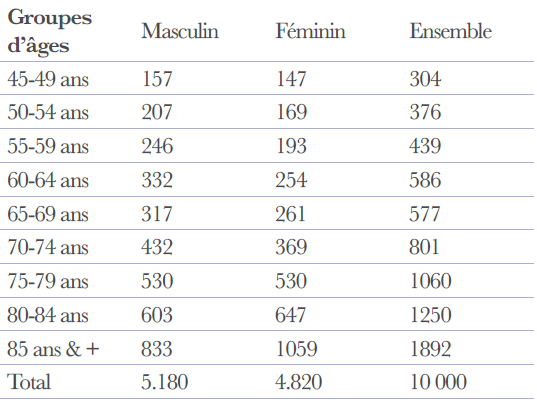
Tableau 2 : Structure des décès par âge et sexe
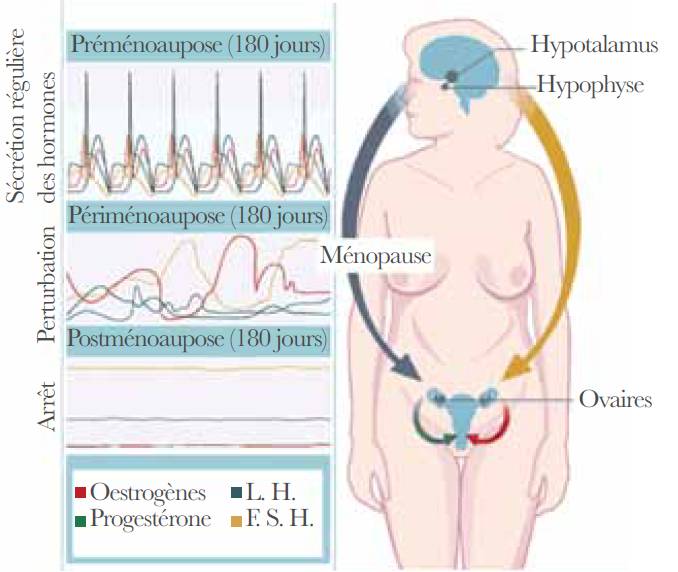
Physiologie de la ménopause :
Lors de la ménopause, la femme ne possède plus suffisamment de follicules car ceux-ci ont été soit utilisés pour le cycle ovarien soit les cellules folliculaires ont dégénéré par le phénomène d’atrésie folliculaire.
FSH et LH sont élevées, reflets de l’atrésie folliculaire et liées à la chute des stéroïdes sexuels et notamment de l’œstradiol.
Diagnostic de Menopause :
L’âge médian de la ménopause naturelle dans la population Algérienne est de 51,4 ans (Étude SAERM).
– Certains facteurs d’environnement peuvent influencer l’âge de la ménopause (tabac, hérédité, obésité…).
1. Ménopause précoce :
La ménopause précoce survient avant 40 ans, touchant 2 à 4% des femmes dans le monde,
En Algérie, elle est estimée entre 8 à 10 % (Pr DERGUINI, président de la SAERM) .
2. Ménopause tardive :
La ménopause tardive survient après 55 ans/60 ans.
- Autres causes de la ménopause :
- Une chimiothérapie lors de traitements du cancer.
- Ménopause artificielle provoquée par l’ablation des ovaires.
- Une maladie auto immune provoquant une réaction du système immunitaire entraînant la production d’auto anticorps qui peuvent altérer les ovaires.
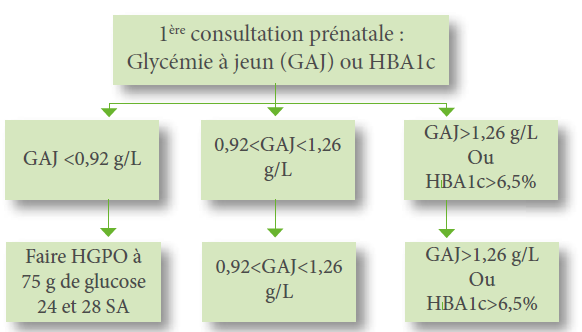
Le diagnostic de ménopause repose sur :
- Aménorrhée d’au moins 1 an liée à un épuisement du capital folliculaire ovarien.
- Le diagnostic de ménopause est clinique, il s’appuie donc uniquement sur les symptômes et signes cliniques.
- Le diagnostic positif est confirmé par le test au progestatif (négatif sur 3 mois de prise) qui signe l’arrêt de la sécrétion œstrogénique.
Classiquement les signes d’appel associent une aménorrhée vers l’âge de 50 ans associée à des signes climatériques : bouffées de chaleur, crises de sueur nocturne, sécheresse vaginale.
D’autres signes seront recherchés : troubles du sommeil, céphalées, douleurs articulaires, troubles de l’humeur et du caractère. Il n’y a aucune place pour une confirmation biologique du diagnostic.
Symptômes les plus courants de la ménopause
- Des examens complémentaires sont réalisés :
- Pour confirmer le diagnostic de ménopause :
- S’il existe des difficultés pour diagnostiquer l’aménorrhée (hystérectomie
- Si ce tableau est incomplet ou survient à un âge inhabituel (< 40 ans), dans ces cas, on pourra doser : FSH : > 30 UI/l et E2 < 30 pg/l.
Les conséquences de la ménopause :
1. Conséquences physiologiques de la ménopause :
Le syndrome climatérique Il correspond aux conséquences de l’hypo-œstrogène. Ces manifestations sont très variables d’une femme à l’autre, dans leur fréquence, intensité, moment d’apparition et durée.
Les bouffées de chaleur :
Elles sont constatées dans plus de 65 % des cas vers 50-55 ans. Leur intensité est variable depuis la simple rougeur de la face jusqu’à la grande bouffée de chaleur vasomotrice
(BVM) défigurant la femme : la rougeur monte du tronc vers la face et s’accompagne de sueurs profuses. Elles cèdent à une oestrogénothérapie modérée. Les bouffées de chaleur traduisent vraisemblablement un désordre au niveau des amines cérébrales, désordre spécifiquement induit par la carence œstrogénique ménopausique.
Elles durent en général quelques mois mais peuvent se poursuivre pendant des années :15 % des femmes de 75 ans peuvent encore se plaindre de BVM.
Autres troubles climatériques :
D’autres troubles sont parfois ressentis par les femmes en période ménopausique. Ces troubles ne sont pas toujours liés à la carence œstrogénique. Il s’agit de trouble de l’humeur (irritabilité, état dépressif, anxiété, tristesse) chez 40 % des femmes, d’une insomnie, de pertes de mémoire, de sécheresse vaginale pouvant être à l’origine de dyspareunie, de modifications de la libido, de modifications de la voix, etc.
Symptômes les plus courants de la ménopause

Symptômesrapportés enrelation avecla ménopause. Lessymptômes attribuablesà la carenceestrogénique dontsignalés engras
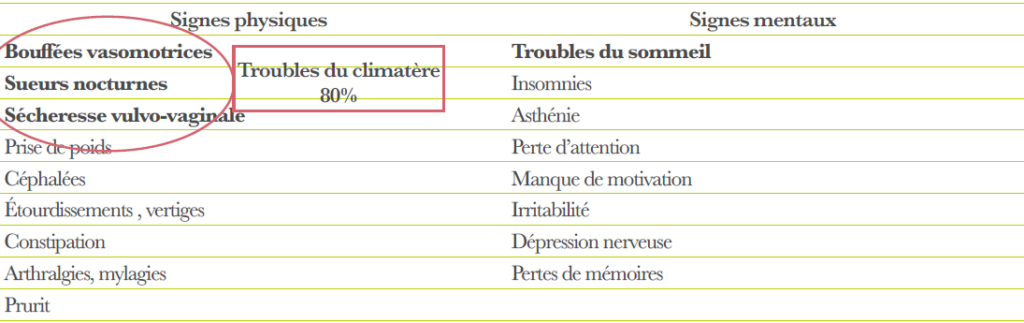
Autres conséquences :
- L’atrophie de la vulve et du vagin survient plus ou moins rapidement après la ménopause.
La sécheresse vaginale pouvant être à l’origine de dyspareunie La flore de protection vaginale diminue entraînant une sensibilité plus grande de l’épithélium (aminci) aux infections.
- Troubles urinaires : Sur le plan urinaire, l’atrophie peut favoriser les troubles urinaires, dysurie, incontinence urinaire, impériosité mictionnelle.
- Poils et cheveux : Ils tendent à se clairsemer dans les zones dépendantes des œstrogènes ; au contraire, peut apparaitre une pilosité de type androgénique (lèvre supérieure, joues).
- Peau : Au niveau de la peau, la carence œstrogénique est responsable d’un amincissement de la peau.
- Poids : L’index de masse corporel augmente après 50 ans ; ses causes sont multiples : diminution des dépenses énergétiques, augmentation de l’apport calorique, redistribution de la masse corporelle (augmentation de la masse grasse abdominale et diminution de la masse maigre).
– Métaboliques et cardio-vasculaires :
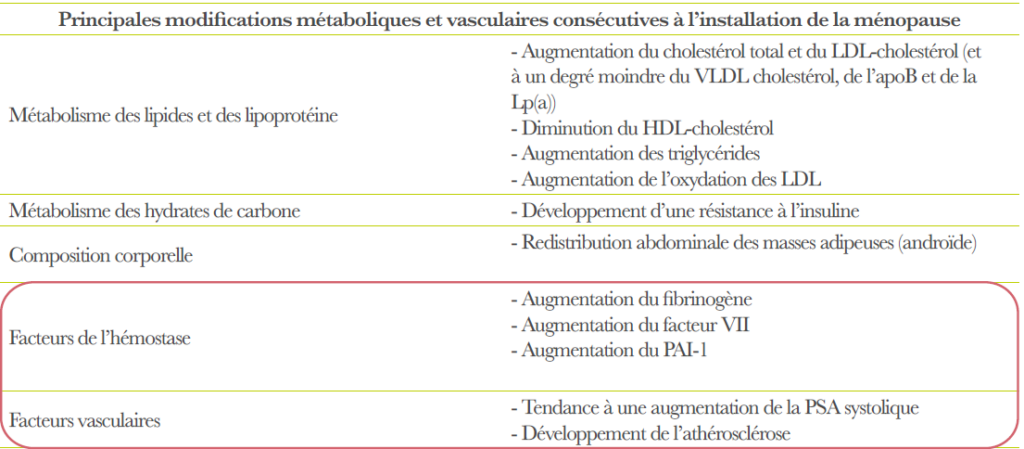
- Conséquences pathologiques de la ménopause Les principales conséquences potentielles de la carence œstrogénique à la ménopause (naturelle ou chirurgicale), au long cours et dont les effets se surajoutent à ceux du vieillissement sont représentées par :
- L’augmentation du risque d’ostéoporose
- Des maladies cardio-vasculaires, avec une progression de l’athérosclérose.
- La plus grande fréquence des démences d’Alzheimer chez les femmes.
Ostéoporose post-ménopausique
L’ostéoporose se définit par un état du squelette caractérisé par une diminution de la solidité osseuse exposant la femme à un risque accru de fracture.L’ostéoporose par déminéralisation est un phénomène physiologique lié au vieillissement mais dont le processus s’accélère à la ménopause. La perte osseuse est de 1 à 2 % par an à cette période contre 0,3 % à 30 ans.
Elle se manifeste 7 à 10 ans après l’arrêt des règles.
L’importance de l’ostéoporose dépend de deux éléments : la vitesse de résorption osseuse et la masse osseuse initiale atteinte à la puberté. Ces deux éléments sont dépendants de facteurs génétiques et de facteurs comportementaux (apport calcique, exercice physique).
L’ostéoporose favorise la survenue de fractures pour des traumatismes minimes.
Les fractures les plus fréquentes siègent au niveau des vertèbres et des poignets alors que les fractures liées à l’âge sont celles des os longs.
Ces fractures grèveront lourdement l’avenir des femmes concernées par ce problème avec 40 % de complications et une mortalité de 25 %.
Le risque fracturaire est apprécie par l’analyse de l’âge, des antécédents de fractures, ostéoporose dans la famille, des risques de chute, et par la densitomètre osseuse.
L’ostéoporose densitométrique se définit par :
– T-score densitométrique inferieur à moins 2,5. Toute diminution d’un écart-type de la densité minérale osseuse est associée à un doublement du risque de fracture ostéoporotique.
Athérosclérose coronarienne
Avant la ménopause, les maladies coronariennes sont beaucoup plus fréquentes chez l’homme que chez la femme. Après la ménopause, progressivement la fréquence des coronaropathies féminines va rejoindre celles des hommes. Le rôle respectif de l’âge et de la carence œstrogénique est controversé.
Les autres facteurs sont :
- Les modifications du métabolisme lipidique (cholestérol total, LDL-cholestérol) ;
- Les modifications de certains facteurs de coagulation (facteur VII, fibrinogène ;
Il existe un doublement de la fréquence des accidents coronariens après la ménopause.
Un certain nombre d’études semble confirmer l’effet favorable des traitements œstrogéniques chez la femme ménopausée sur le risque cardiovasculaire si ce traitement est donné précocement en prévention de l’athérosclérose.
Les démences d’Alzheimer :
La plus grande fréquence des démences d’Alzheimer chez les femmes ménopausées que chez les hommes a également conduit à l’hypothèse d’un effet favorisant de la carence œstrogénique dans la genèse de cette affection.
Prise en charge de la ménopause :
Le traitement hormonal de la ménopause (THM) reste la pierre angulaire de la prise en charge médicale de la post-ménopause.
Il permet :
- De corriger la symptomatologie fonctionnelle du climatère.
- De prévenir les conséquences à long terme de la carence ostrogénique (ostéoporose, développement de l’athérosclérose, dégradation des fonctions cognitives).
Comme tout traitement, il impose de connaître :
- Contre-indications.
- Inconvénients : réapparition possible des hémorragies de privation
- Risques potentiels : une augmentation du risque de cancer du sein ainsi que des maladies cardio-vasculaires.
En Algérie, cinq millions de femmes sont traitées. (SAERM).
1. Qui traiter ?
En fait la prise en charge se justifie si les signes climatériques gênent la qualité de vie.
Le THM doit être proposé après une information précise et adaptée sur les avantages, les inconvénients et les risques éventuels (balance bénéfices/risques). On aura au préalable vérifié l’absence de contre-indications de ce type de traitement substitutif.
Actuellement, moins de 25 % des femmes ménopausées sont traitées. Le traitement pour prévenir les conséquences à long terme fait l’objet de discussion.
Les femmes dont la ménopause spontanée ou iatrogène avant l’âge de 45 ans et particulièrement avant 40 ans sont les plus à risque pour les maladies cardiovasculaires et l’ostéoporose et peuvent être à un risque accru de troubles affectifs et de la démence.
Chez les femmes présentant une insuffisance ovarienne prématurée, THM orale est recommandé jusqu’à l’âge moyen de la ménopause naturelle.
2. Les armes thérapeutiques
Parmi les principaux traitements de la ménopause, on distingue :
- Le THM (Traitement Hormonal de la Ménopause)
- Les traitements non hormonaux.
- A-Traitement hormonal (THM)
Le THM repose sur l’administration d’œstrogènes (et de progestatifs chez la femme non hystérectomisée, en raison du risque de cancer de l’endomètre induit par le traitement œstrogènique seul). Ce traitement tend actuellement à être le plus «substitutif» possible, c’est-à-dire à se rapprocher des conditions de la physiologie ovarienne.
Œstrogènes :
Les différentes molécules pouvant être administrées sont le 17β estradiol, l’estradiol valérate, les estrogènes conjugués équins.
17ß-estradiol est l’estrogène de référence du THM, chimiquement et biologiquement identique à l’estradiol endogène (ce qui a permis de lever la plupart des contre-indications d’ordre métabolique) .
L’effet sur l’ostéoporose est prédominant au niveau du rachis, plus incertain au niveau du col fémoral. La prévention des fractures a été démontrée (WHI 2002).
La Progestérone et les Progestatifs :
- Ce sont la progestérone naturelle (Utrogestan®, Estima®, Menaelle®),
- Les progestatifs de synthèse ; la grande diversité des progestatifs, les dérivés nor-pregnanes (Promegestone®, acétate de nomégestrol) utilisés rend complexe l’analyse de leurs effets sur le métabolisme lipidique, leurs différences résident dans leur pouvoir androgénique qui s’oppose aux effets métaboliques favorables des œstrogènes.
- La dydrogestérone : est dépourvue d’effets secondaires androgéniques et bénéficie d’une très bonne tolérance métabolique, active par voie orale qui a une activité comparable à la progestérone administrée par voie parentérale.
Le progestatif est ajouté au traitement œstrogénique pour éviter le risque de cancer de l’endomètre (12 j/mois au minimum); Chez la femme hystérectomisée, il n’est pas nécessaire d’ajouter au traitement œstrogénique de la progestérone micronisée ou un progestatif.
Sous quelles formes le THM est-il disponible ?
Il existe sous quatre formes différentes : les comprimés, les patchs, les gels et les solutions nasales.
- Les comprimés sont administrés à raison d’un comprimé par jour sur des rythmes continus, séquentiels, discontinus
- Les patchs : Ces produits peuvent être posés de façon continue ou avec une pause d’une semaine tous les mois ;
- Les gels : Il n’existe pas de gel qui associe estrogènes et progestatifs ;
- La solution nasale, il s’agit d’un estrogène seul : l’Aerodiol® à la posologie d’une pulvérisation dans chaque narine par jour. Comprimés, patch, gel, spray…, le choix de l’association hormonale devra être adapté au mode de vie et aux symptômes de la patiente, en privilégiant les produits présentant le moins de risque.
La voie d’administration transdermique pourrait avoir un intérêt dans la mesure ou elle permet d’éviter le premier passage hépatique ; ceci entraine une augmentation plus modérée de la synthèse des Very Low Density Lipoprotein (lipoprotéine de très basse densité) et High Density Lipoprotein (lipoprotéine de haute densité) – Cholestérol, l’augmentation des Triglycéride, de l’angiotensinogène et des facteurs de coagulation, et surtout l’absence de modification de l’hémostase.
La dose d’œstrogènes efficace sur la prévention de l’ostéoporose est de 1 à 2 mg de 17-β-œstradiol ou de 25 a 50 μg par voie transdermique.
La forme orale reste principalement une question de confort et d’habitude, selon les recommandations de l’AFS- SAPS 2006, la prescription devra se faire « à la dose minimale efficace, pour une durée la plus courte possible ».
Les différents schémas thérapeutiques

Éléments de surveillance
La surveillance comporte la recherche d’un sur ou sous-dosage :
- En cas de sous-dosage, les bouffées de chaleur et la sécheresse vaginale peuvent réapparaitre. Dans cette situation, on augmentera la dose d’œstrogènes,
- En cas de surdosage en œstrogène, les seins sont tendus et les règles sont abondantes. Dans cette situation, on diminuera la dose d’œstrogènes. Les progestatifs peuvent être également responsable de mastodynies
- Un examen clinique est réalisé à 3 mois puis tous les 6 à 12 mois. La pratique des frottis, des dosages de cholestérol, TG, glycémie peuvent être réalisés tous les 3 ans en l’absence de risque particulier.
Le dépistage organisé recommande une mammographie tous les 2 ans.
La DMO ne doit pas être répétée avant 2 à 3 ans.
Contre-indications
Les principales contre-indications sont reparties en : Contre-indications absolues :
- Cancers gynécologiques hormono-dépendants
- Maladies thromboemboliques (antécédents de phlébite profonde, d’embolie pulmonaire
- Maladies plus rares (lupus, tumeur hypophysaire, porphyrie, affections hépatiques graves et évolutives, hyperlipidémies sévères, HTA grave) ;
Contre-indications relatives : elles nécessitent une discussion en fonction de leur sévérité et du contexte (désir de THM, possibilités de surveillance). Ce sont : fibrome, endométriose, mastopathies bénignes, HTA, diabète insulinodépendant, antécédents familiaux de cancer du sein, de l’endomètre, cholestase, etc.
Les principaux effets bénéfiques
- Prévention ou traitement des complications à court et moyen termes : bouffées de chaleur, atrophie vaginale, troubles de l’humeur, troubles de la trophicité vaginale.
– Prévention des complications à long terme :
- Ostéoporose : diminution de 50 % des fractures ostéoporotiques (rachis) ;
- Risques cardio-vasculaires : l’effet du THM est, depuis l’étude WHI, contesté en prévention des risques cardiovasculaires ;
- Troubles cognitifs : diminution probable de l’incidence de la maladie d’Alzheimer
- Cancer du colon : diminution probable de l’incidence.
Principales complications à rechercher
Les deux principales complications sont :
- Les maladies thromboemboliques : le risque est multiplie par 2 à 4 lorsque le THM comporte l’administration des œstrogènes par voie orale et en fonction de type de progestatif (progestérone micronisée et acétate de chlormadinone ont peu d’effets sur l’hémostase) ;
- Les cancers hormono-dépendants :
- Cancer du sein : La WHI a montré une augmentation de 8/10 000 AF du risque de cancer du sein. Ce risque se normalise 5 ans après l’arrêt du traitement.
De plus, une oestrogénothérapie pouvant aggraver l’évolution du cancer du sein lorsqu’il existe déjà, il importe donc d’examiner soigneusement les seins de toute candidate à un éventuel traitement et de discuter l’utilité de certaines investigations complémentaires.
Compte tenu du risque, l’AFSSAPS a demandé de « limiter le traitement à la posologie active la plus faible possible et de limiter la durée du THM avec une réévaluation annuelle de son intérêt »
B. Alternatives thérapeutiques
Dans tous les cas, il faut recommander une bonne hygiène de vie :
- Activités physiques (30 à 45 min de marche rapide par jour) pour la prévention des risques cardiovasculaires et osseux ;
- Hygiène alimentaire : calcium 1.200 à 1.500 mg/jour et vitamine D (correction de l’hypovitaminose.
- Les phyto-œstrogènes (ex. : isoflavone) sont des compléments alimentaires. Leur efficacité est discutée, tout est question de dose.
D’autres alternatives doivent être connues :
- Œstrogènes à action locale pour traiter la sécheresse vaginale : Trophigi®, Colpotrophine®, Trophicreme®;
- Traitements pour les bouffées de chaleur (Abufene®, Agreal®) ;
- Les SERM (modulateur sélectif des récepteurs aux œstrogènes (Evista®, Raloxifene®) : actifs sur l’ostéoporose, et ayant une action préventive sur la survenue d’un cancer du sein ; ils n’ont pas d’action sur les bouffées de chaleur ni la sécheresse vaginale, (dose : 60 mg/j) ;
- Bisphosphonates (Actonel® et Fosamax®) actifs sur la minéralisation.
_ Le Livial® (tibolone est un stéroïde actif sur l’ostéoporose, le vagin, les bouffées de chaleur et dont les actions sur les seins et l’endomètre sont en cours d’évaluation ;
Conclusion : take home
- La ménopause est un phénomène naturel. « Ce n’est pas une,maladie »
- La ménopause est vécue de façon très différente selon les femmes, les pays et les cultures. C’est une expérience propre à chaque femme.
- THM n’est pas un traitement standard administré à une femme standard.
- La forme orale reste principalement une question de confort et d’habitude. Elle permet de moduler le dosage pour un THM individualisé et répondre aux besoins des patientes.
- Les années à venir verront un vieillissement accéléré de la population de plus de 50 ans à travers l’ensemble du pays. la planification des actions de santé doit prendre en compte la prise en charge de cette population, vu l’augmentation du nombre des femmes ménopausées en Algérie dans les années à venir et les complications de la ménopause.
Points essentiels
¤ La ménopause est une période physiologique de la vie des femmes,
¤ La prescription d’œstrogènes corrige les troubles climatériques,
¤ Les conséquences à long terme sont les coronaropathies et l’ostéoporose,
¤ Les effets bénéfiques sont supérieurs aux effets secondaires en termes de qualité de vie et de survie,
¤ Le principal problème du traitement préventif est la mauvaise observance,
¤ Les contre-indications absolues sont réduites (cancer du sein et maladies thromboemboliques),
¤ L’information est essentielle dans ce domaine où doivent se mettre en balance les avantages et les risques du THS.
Bibliographie
- Pr Derguini, président de la Société algérienne d’étude et de la recherche sur la ménopause (SAERM) (10ème et 11ème Congrès
- Agence Française de Sécurité Sanitaire des Produits de Santé (AFSSAPS)
- Recommandations de l’AFSSAPS concernant la ménopause. Annales d’Endocrinolo- gie. 2004 Apr ; 65(2):179-183.
- Pr Soukhal : ménopause et tendance démographique, quelle évolution pour les pro- chaines décennies en Algérie, 2006 CHU Beni-Messous
- Les traitements hormonaux de la ménopause en 2002 (THS) ou la ménopause d’hier et d’aujourd’hui. Imagerie de la Femme. 2002 Jun ;12(1-2):175-183.
- Newton et al. J WomensHealth1997; *AFSSAPS 2006 – Climatériques 2013 ; 16:316-337
- Stevenson JC et al. Maturitas 2010 ;67:227–32
- International Menopause Society and Elsevier Inc.DOI : 2013.
- Rossouw JE et al. JAMA 2002 ; Mueck AO .Maturitas 2009
- E3N, Fournier. Breast Cancer ResTreat 2008
- The ESTHER Study” Circulation. 2007; 115:840-845.
- Sellahi Fatima Zohr née Boumaiza : thèse de doctorat : le vécu de la ménopause chez la femme algérienne
- Agence Nationale d’Accréditation et d’Evaluation en Sante (ANAES). : Médica- liser la ménopause ?
- Agrinier N, Cournot M, Ferrieres J. : Dyslipidémies de la femme après 50 ans : le rôle de l’âge et de la ménopause. Annales de cardiologie et d’angiologie. 2009 Jun ;58(3):159- 164.
- Aubard Y, Teissier MP, Grandjean MH, Le Meur Y, Baudet JH. : Les ménopauses précoces. Journal de Gynécologie Obstétrique et Biologie Jun ; 26(3):237.
- Bernard P. : T.H.S. de la ménopause : Quels avantages ? Quels risques ? Syndicat National des Gynécologues Obstétriciens de France (SYNGOF).
- Body JJ. : Traitement de l’ostéoporose post-ménopausique : actualités et perspectives. Revue Médicale de Bruxelles. 2008 ; 301-309.
- Collège des Enseignants d’Endocrinologie, Diabète et Maladies Métaboliques (CEEDMM). : Item 55 : Ménopause. Université Médicale Virtuelle Francophone (UMVF) ; 2010.
- Collège National des Gynécologues et Obstétriciens Français (CNGOF), Conférence nationale des PU-PH en Gynécologie-Obstétrique.; 2006. P. 67-76.
- Canonico M et al. “Hormone Therapy and Venous Thromboembolism Among Post- menopausal Women, Impact of the Route of Estrogen Administration and Progesto- gens.