L. BADAOUI,A. SEBA, Service de Néphrologie,Dialyse et Transplantation Rénale
Résumé : L’hypertension artérielle est la complication la plus fréquente chez la femme enceinte. Qu’elle soit chronique ou induite par la grossesse, elle touche 8 à 10 % des grossesses. Elle demeure la première cause de mortalité avec 15 % et s’accompagne d’une élévation du risque de retard de croissance intra-utérine et de prématurité. En Algérie, les résultats de l’étude STEP « WISE » réalisée en 2003 par le MSPRH en contribution avec l’OMS, ont montré une prévalence de l’HTA de 26 + 2.6 % dans la tranche d’âge comprise entre 25 et 64 ans (1). La prévalence de l’HTA gravidique est de 15 %. Les causes de mortalité maternelle sont similaires à celles recensés par l’OMS (1) ; l’HTA gravidique serait responsable de décès dans près de 26 % des cas (1).
Mots-clés : Pré éclampsie. HELLP Syndrome, éclampsie.
Abstract : Hypertension is the most common complication in pregnant women. Whether chronic or induced by pregnancy, it affects 8 to 10 % of pregnancies. It remains the leading cause of death with 15% and is accompanied by an elevation of the risk of intra-uterine growth retardation and prematurity. In Algeria, the results of the study STEP ‘WISE’ in 2003 by the MSPRH in contribution with WHO, has shown a prevalence of hypertension of 26 + 2.6% in the age group between 25 and 64 NASB (1). The prevalence of hypertension in pregnancy is 15%. Maternal causes of death are similar to those identified by WHO (1); pregnancy hypertension would be responsible for deaths in nearly 26% of cases.
Key-words : Pre-eclampsia. HELLP Syndrome, eclampsia.
Données épidémiologiques des grossesses en Algérie :
Le taux de fertilité/femme est passé de 7,52 en moyenne en 1960 à 2,8 naissances en moyenne en 2015. Le taux de natalité /1.000 habitants était de 50/1.000 habitants en 1960 et est passé à 24,9/1.000 en 2015 (1). Le taux de mortalité infantile est passé de 150 décès/1.000 naissances en 1960 à 25 décès/1.000 naissances en 2015. Le taux de mortalité est passé de 20/1.000 habitants à 5/1.000 habitants en 2015.
Les décès maternels constituent 10 % de l’ensemble des décès des femmes en âge de procréer (2,3).
Le taux de mortalité maternelle montre des disparités comme ailleurs dans le monde, et serait selon les régions d’Algérie, de 30 décès /100.000 naissances vivantes à Alger ; de 23 décès à Annaba et 130 décès à Adrar. Les décès surviennent dans 55 % des cas à l’hôpital et dans 57,3 % lors des évacuations. La cause immédiate de ces décès est en rapport avec la qualité de la prise en charge de la parturiente au lieu d’accouchement (4). Les causes sont similaires à celles recensés par l’OMS (5) ;
- L’HTA : 16,4 % pré partum et 10,4% post partum,
- Les hémorragies : 16,6 %,
- Les septicémies puerpérales : 14,1 %,
- Les cardiopathies : 13 %,
- Les dystocies 12,2 % (3).
Physiologie de la grossesse :
Le débit cardiaque augmente progressivement au cours du premier trimestre de la grossesse, tandis que les résistances vasculaires périphériques diminuent. La pression artérielle baisse du fait de la grande vasodilatation périphérique. Le système rénine angiotensine aldostérone est activé et cette activation limite la baisse de la pression artérielle.
La baisse des résistances vasculaires périphériques est due à l’ouverture de la circulation utéro placentaire et à une vasodilatation artériolaire, elle-même expliquée par une résistance aux hormones vasoconstrictrices et par la présence de substances vasodilatatrices dont la PGE2, PGI2, oxyde nitrique et VEGF.
L’augmentation du débit cardiaque s’accompagne d’une augmentation de la filtration glomérulaire, c’est ainsi que s’explique la baisse de l’urée, de la créatininémie. Une baisse de l’acide urique est observée. On note une glycosurie et une amino acidurie par augmentation de la charge filtrée.
Le bilan hydro sodé est positif avec une rétention progressive de 6-8 litres d’eau et de 500-900 mmol de sodium. L’hyper volémie est nécessaire en regard de la grande vasodilatation.
Au cours du dernier trimestre de la grossesse, la pression artérielle remonte progressivement vers les valeurs pré grossesse (5).
Comment mesurer la pression artérielle chez une femme enceinte ?
La pression artérielle doit être mesurée en position assise, en milieu médical, après au moins 5 minutes de repos, en utilisant un appareil électronique huméral.
En cas d’HTA légère à modérée dépistée en consultation, l’HTA doit être confirmée par des mesures en dehors du cabinet médical (auto mesure selon « la règle des 3 » ou moyenne diurne de la MAPA sur 24 heures) afin d’éliminer un effet blouse blanche.
Une PAS ≥ 135 mm Hg ou une PAD ≥ 85 mm Hg, en dehors du cabinet médical, est considérée comme pathologique.
Qu’implique la découverte d’une hypertension artérielle au cours de la grossesse ?
La découverte d’une HTA au cours de la grossesse constitue la première étape de la prise en charge. L’hypertension artérielle de la grossesse ou du post-partum immédiat (période couvrant les 6 semaines qui suivent l’accouchement) est définie par :
- Une PAS ≥ 140 mmHg ou PAD ≥ 90 mmHg
- Elle est légère à modérée si PAS = 140-159 mmHg ou PAD = 90-109 mmHg
- Elle est sévère si PAS ≥ 160 mmHg ou PAD ≥ 110 mmHg
Une fois confirmée, il est important de classer cette HTA selon la dernière classification de la Société Française de l’Hypertension Artérielle (SFHTA) (6). Une HTA de la grossesse peut être liée à :
- Une HTA chronique connue avant la conception ou avant 20 SA.
- Une HTA gestationnelle qui apparait après 20 SA sans protéinurie.
- Une pré éclampsie définie par l’apparition d’une HTA et d’une protéinurie après 20 SA.
Nous traiterons dans ce chapitre de la pré éclampsie qui est la première cause d’HTA chez la femme enceinte.
Ce qu’il faut connaitre de la pré éclampsie
La pré éclampsie est une pathologie de la grossesse qui complique, à l’échelle mondiale, 2 à 8 % des grossesses. Son incidence augmente avec l’augmentation des facteurs de risque au sein de la population. Surpoids et obésité pré gestationnels, HTA, diabète, multiparité et âge maternel de plus en plus tardif sont fortement incriminés de même qu’une grossesse gémellaire, des antécédents familiaux de pré éclampsie et la race noire. Elle représente l’une des trois principales causes de morbi mortalité maternelle au monde (6).
Il est actuellement admis qu’elle a un retentissement sur la santé ultérieure de la mère et de l’enfant, alors qu’elle était pendant longtemps considérée comme résolue après l’accouchement. Elle est actuellement considérée comme un important facteur de risque de maladies rénales, cardiovasculaires et neurologiques. Pour cela, un suivi doit être proposé à des fins préventives. Les modalités du suivi seront traitées plus loin.
Quels sont les facteurs de risque de la pré éclampsie ?
- Une HTA chronique,
- Un antécédent de pré éclampsie,
- Une nulliparité,
- Un âge maternel supérieur à 40 ans
- Une obésité,
- Un diabète préexistant,
- Une présence d’anticorps anti phospholipides
- Une maladie thromboembolique et
- Une néphropathie primitive ou secondaire sont autant de facteurs de risque connus pour l’apparition d’une pré éclampsie.
Physiopathologie
La pré éclampsie (PE) serait le résultat d’un défaut d’invasion des artères spiralées par le trophoblaste, responsable d’un défaut de perfusion placentaire. Cette insuffisance placentaire provoque la libération de cytokines et de radicaux libres, qui déclenchent un stress oxydatif systémique. La réponse maternelle est manifeste au deuxième trimestre et se traduit par un syndrome inflammatoire et une dysfonction endothéliale diffuse, responsable de l’hypertension artérielle et de la protéinurie, caractéristiques de la pré éclampsie.
L’hypo perfusion placentaire est responsable de la morbidité fœtale et néonatale associée à la pré éclampsie. Elle s’accompagne souvent d’une prématurité et/ou d’un retard de croissance intra utérine nécessitant le déclenchement parfois précoce de l’accouchement, qui est le seul traitement de cette maladie.
Des facteurs environnementaux, immunologiques et génétiques jouent également un rôle dans ce processus (6).
Quels sont les signes de cette pathologie ?
La pré éclampsie est une maladie multi systémique caractérisée par le développement d’une HTA nouvelle (≥ 140/90 mmHg) associée à une protéinurie (≥ 0,3 g/j) à partir de 20 semaines de gestation. On distingue la forme précoce et la forme tardive, qui se développent respectivement avant et après 34 semaines d’aménorrhée.
Une pré éclampsie peut également se développer de novo lors de la période du post-partum. Une PE est sévère en cas :
- HTA sévère (PAS > 160 mmHg et/ou PAD > 110 mmHg)
- Atteinte rénale avec : oligurie (< 500 ml/24h) ou créatinine > 135 µmol/L, ou protéinurie > 5 g/j
- HELLP Syndrome
- OAP
- Éclampsie
- Thrombopénie inférieure à 100000/mm3.
Le HELLP Syndrome est une complication sévère de la PE, apparait à la deuxième moitié de la grossesse (7).
Le diagnostic positif est posé devant une atteinte hépatique (50 % des cas), avec une douleur en barre de siège sus-épigastrique rarement associée à un ictère.
Des nausées et de vomissements, sont rapportés. Des céphalées et un flou visuel sont rapportés dans 17 à 20 % des cas.
Anémie hémolytique (LDH supérieurs à 600UI/L, bilirubinémie supérieure à 12 mg/l, haptoglobinémie basse, schizocytes), cytolyse hépatique (ASAT supérieures à 70 UI/L) et thrombopénie, définissent le HELLP (7,8).
L’éclampsie est une complication sévère de la pré éclampsie.
Elle est décrite comme une crise convulsive généralisée survenant chez une femme enceinte dans un contexte d’hypertension gravidique. Elle survient habituellement comme la complication majeure de la pré éclampsie et serait responsable de 12 % de décès.
Elle est souvent précédée de troubles neurologiques rebelles (troubles visuels, ROT poly cinétiques, céphalées). Il s’agit d’une urgence vitale pour la femme et l’enfant à naître.
Le traitement :
Il est recommandé de traiter sans délai toutes les hypertensions artérielles sévères : PAS ≥ 160 mmHg ou PAD ≥ 110 mmHg (7).
Si l’HTA est légère à modérée : PAS = 140-159 mmHg ou PAD = 90-109 mmHg, la présence de diabète pré-gestationnel, d’antécédent cardiovasculaire, de maladie rénale chronique nécessite le début d’un traitement anti-hypertenseur.
Si l’HTA est sévère, l’objectif est une PAD comprise entre 85 mmHg et 100 mmHg et une PAS inférieure à 160 mmHg (7,8).
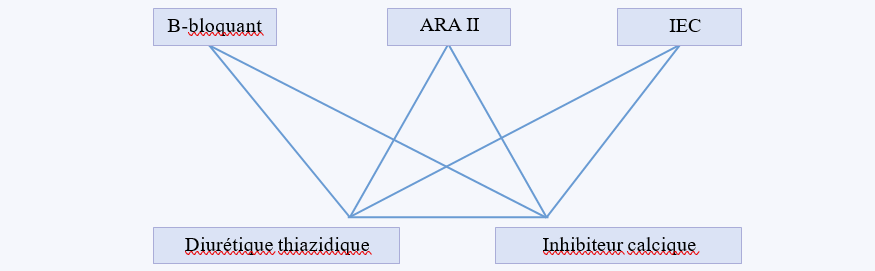
On utilisera en première intention, au choix, l’un des traitements suivants : l’alphaméthyldopa, le labétalol, la nicardipine, la nifédipine. Les inhibiteurs de l’enzyme de conversion, les antagonistes des récepteurs de l’angiotensine II et l’aliskiren sont contre-indiqués quel que soit le trimestre de la grossesse.
Un traitement par bétaméthasone injectable pour maturation fœtale est recommandé en cas de pré-éclampsie avant 34 SA et si une prise en charge néo-natale est envisagée.
En présence d’une pré éclampsie, il n’y a pas d’indication systématique à une restriction hydrosodée ni à un remplissage vasculaire. Une administration intraveineuse de sulfate de magnésium chez la femme pré-éclamptique, est recommandée en cas d’éclampsie, ou en cas de signes neurologiques faisant craindre la survenue d’une crise d’éclampsie (9).
En cas de pré-éclampsie, sévère ou non, entre 24 et 34 SA, la poursuite de la grossesse est justifiée, le plus souvent sous surveillance médicale rapprochée.
En cas de pré-éclampsie sévère, après 34 SA, il est recommandé de provoquer la naissance.
En cas de pré-éclampsie modérée, l’expectative est suggérée jusqu’à 37 SA, si l’état fœtal le permet.
Au-delà de 37 SA, il est recommandé d’envisager l’accouchement (10).
Pour prévenir la survenue d’une pré-éclampsie, il est recommandé de prescrire de l’aspirine à faible dose (75-160 mg) uniquement chez les patientes ayant un antécédent de pré-éclampsie. Ce traitement doit être débuté avant 20 SA, idéalement à la fin du premier trimestre. Il est suggéré de poursuivre l’aspirine jusqu’au 8ème mois (12).
La dialyse s’envisage en cas d’insuffisance rénale oligo anurique persistante ou de troubles hydro électrolytiques menaçant le pronostic vital (10).
Le Pronostic :
- Pronostic maternel : Les décès sont exceptionnels : 0-13 % (11),
- Pronostic rénal : la fonction rénale est récupérée dans son intégralité dans 97-100 %,
- Pronostic fœtal : 15 à 38 % des pré éclampsies associées à une IRA se compliquent de mort périnatale.
Devenir des femmes pré éclamptiques :
Sur le plan rénal :
Une grande étude rétrospective norvégienne a révélé un risque accru d’insuffisance rénale terminale ultérieure, après une pré éclampsie. Chez les primipares, ce risque est 4,7 fois supérieur à la population générale. Le risque augmente avec le nombre de grossesses compliquées et il est 15 fois supérieur en cas de deux ou trois grossesses avec pré éclampsie.
Sur le plan cardiovasculaire :
Les femmes développant une pré éclampsie présentent plus fréquemment les caractéristiques d’un syndrome métabolique, à savoir, une dyslipidémie, une hypertension, une obésité et une augmentation de la résistance à l’insuline que les femmes ayant eu une grossesse normale. Ces caractéristiques, lorsqu’elles sont présentes avant la conception, sont souvent méconnues des patientes ou de leur médecin et se manifestent initialement en cours de grossesse. La grossesse apparaissant comme un facteur révélateur. Les patientes avec un antécédent de pré éclampsie, présentent un risque relatif (RR) de 3,70 (IC 95% : 2,70-5,05) pour l’hypertension artérielle et de 2,16 (IC 95% : 1,86-2,52) pour une maladie ischémique cardiaque. De plus, une augmentation globale de la mortalité après une pré éclampsie a été démontrée, RR : 1,49 (IC 95% : 1,05-2,14).
Sur le plan neurologique :
Moins de 1% des grossesses seront compliquées par un AVC dans le péripartum. La pré éclampsie/éclampsie représente un facteur de risque important pour les événements vasculaires cérébraux dans le péripartum. L’AVC dans sa forme hémorragique est le plus souvent observé dans la pré éclampsie/éclampsie.
Les femmes ayant souffert d’une pré éclampsie ont un risque d’AVC à dix ans, quasi le double de celui de la population générale. En cas de pré éclampsie précoce, ce risque s’élève à 5 fois celui de la population générale.
Sur le plan métabolique :
Une étude de cohorte rétrospective canadienne publiée cette année, portant sur plus d’un million de femmes, a révélé que la pré éclampsie, en l’absence de diabète gestationnel concomitant, double le risque de développer ultérieurement un diabète de type 2.
Lorsqu’il existe un diabète gestationnel associé, ce risque s’élève considérablement jusqu’à atteindre seize fois celui de la population générale.
Devenir des enfants nés de mères pré éclamptiques : Les enfants nés d’une mère pré éclamptique avec un bas poids de naissance (< 2.500 g) ou un retard de croissance intra-utérine, sont aussi à risque de développer ultérieurement des maladies cardiovasculaires : une sensibilité au sel avec risque d’HTA x 1,5 ; un AVC ischémique x 2,5 ; un AVC hémorragique x 3,2 ; de même qu’un syndrome métabolique.
Prévention :
La nécessité d’un suivi médical à 06 semaines de l’accouchement chez une pré éclamptique s’impose
pour dépister et prévenir les complications rénales, cardiaques voire même neurologiques. Une évaluation des FDR rénal et cardio vasculaire doit être effectuée. On recherchera les antécédents de complications de l’HTA de la grossesse/petit poids de naissance, des signes persistants de la PE par la mesure de la PA et de la protéinurie. Un bilan lipidique, une glycémie à jeun et un indice de masse corporelle doivent être appréciés au moins une fois par an.
Un bilan de thrombophilie comportant la recherche d’un déficit en protéine C, en protéine S, un déficit en antithrombine III, la recherche d’un syndrome d’anti-corps anti phospholipides, sera réalisé en cas de PE précoce, de PE associée à un un retard de croissance intra utérin (RCIU), un décollement placentaire ou de mort fœtale in utéro (MFIU) (11,12).
Les femmes avec un antécédent de PE précoce, sévère, récidivant ou associé à une anomalie placentaire méritent donc un suivi au long cours.
Des conseils hygieno diététiques seraient également bénéfiques.
Résultats d’une expérience algérienne réalisée au service de Néphrologie du CHU de Tizi Ouzou :
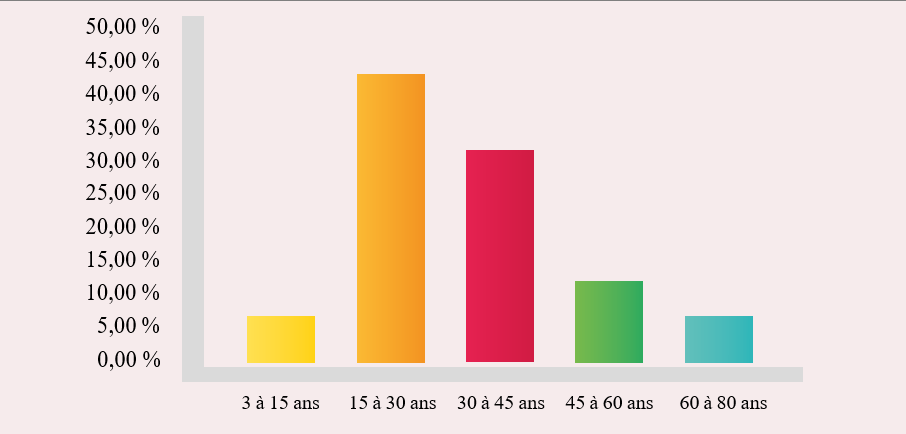
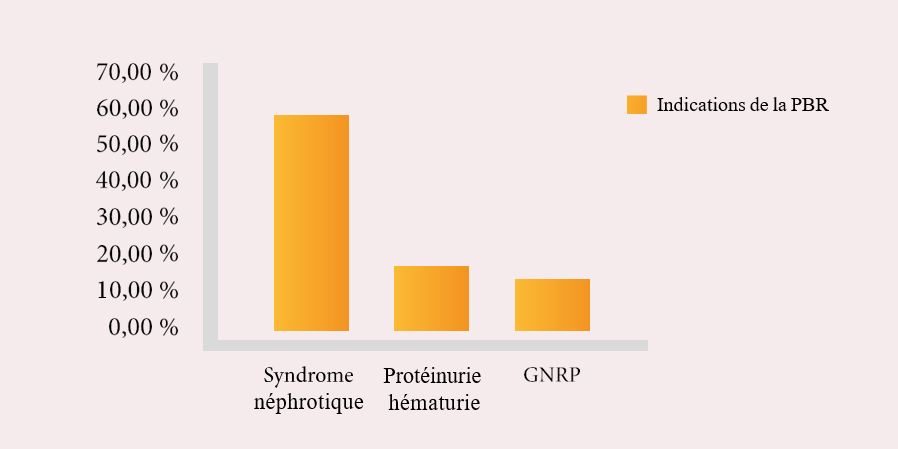
Une étude réalisée entre 2012 et 2015, sur 170 patientes présentant une insuffisance rénale aigue gravidique, a confirmé la fréquence de la pré éclampsie dans plus de 71,5 % des cas. La notion de multiparité, l’âge avancé, les récidives de pré éclampsie et la notion familiale de pré éclampsie était significatifs dans les proportions suivantes de 58 % ; 47 % ; 11 % ; 4,8 %.
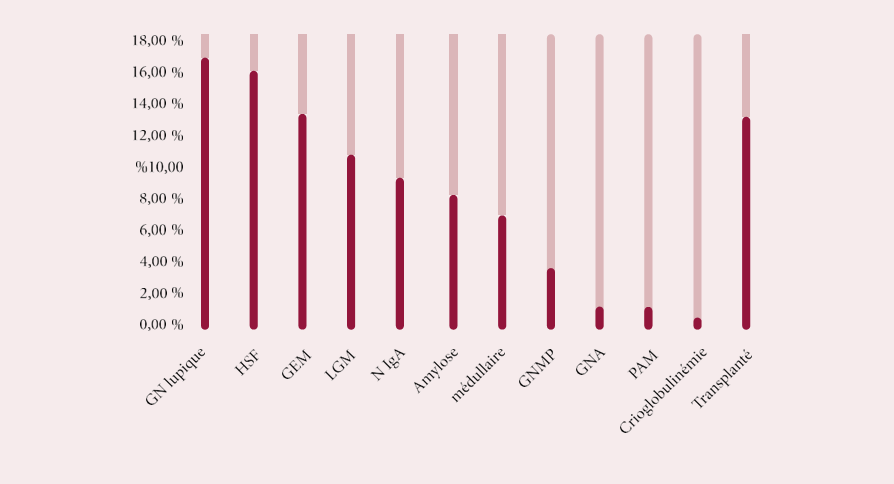
Une pathologie rénale préexistante à la pré éclampsie a été retrouvée chez ces patientes, dans 16,76% des cas (28 cas). Les néphropathies les plus fréquentes étaient :
- Soit primitive dans 11,4 % des cas en rapport avec :
- Une glomérulonéphrite chronique (GNC) de cause indéterminée,
- Une hyalinose segmentaire et focale (HSF),
- Une néphropathie à IgA,
- Une glomérulonéphrite extra membraneuse(GEM),
- Soit secondaire dans 5,4% des cas, en rapport avec un diabète, un lupus érythémateux disséminé (LED), un syndrome d’anticorps anti phospholipides (SAPL) et une polykystose rénale dominante (PKRD).
Une néphropathie sous-jacente a été diagnostiquée, en post partum, chez 9,58% des patientes (16 cas) ayant présenté une pré éclampsie ; et ce, après un suivi de 06 mois. Des cas de SAPL (08 cas), isolés dans 05 cas et associés à un LED dans 03 cas, ont été enregistrés.
Le diagnostic de LED a été porté dans 02 cas. Dans 06 cas, il s’agissait d’une HTA chronique.
Au total, 26,34% des femmes pré éclamptiques avaient une pathologie rénale sous-jacente.
Selon JAMES W. VAN HOO de l’université de Cincinnati, jusqu’à 20 % des patientes présentant une pré éclampsie, présentent une néphropathie chronique pré-existante ou découverte dans le post partum, dont la plus fréquente est représentée par la néphropathie diabétique, la glomérulonéphrite membrano proliférative (GNMP), la GNA post streptococcique et le LED.
Des formes graves de pré éclampsie, compliquées de HELLP Syndrome dans 25 cas, d’éclampsie dans 14 cas, d’insuffisance rénale aigue dans tous les cas, ont été enregistrés. Le recours à l’épuration extra rénale a été noté dans 20% avec une mortalité maternelle dans 2,4% : 04 patientes (13).
La mortalité fœtale a été notée chez les patientes présentant plusieurs facteurs de gravité dont, le délai de survenue précoce de la pré éclampsie (moins de 32 SA), l’HTA supérieure à 160/100 mm Hg, l’oligurie, la protéinurie supérieure à 3 g/j, l’insuffisance rénale aigue sévère, (HRP), le HELLP syndrome, l’éclampsie et l’hémorragie de la délivrance.
9% (15 patientes) ont présenté 04 facteurs de gravité ; 6% (10 patientes) 03 facteurs de gravité ; 2,4% (04 patientes) 05 facteurs de gravité ; 1,2% (02 patientes) 06 facteurs de gravité ; 1,2% (02 patientes) 07 facteurs de gravité ; 0,6% (01 patiente) 01 facteur de gravité.
La mortalité fœtale a atteint le taux de 20%.
Prakash J (Prakash, 2010) rapporte une mortalité fœtale de 38,8%. Une étude indienne réalisée par Godara et al (2014) rapporte une mortalité fœtale de 49,12% (14).
Dans notre étude, l’HTA a persisté chez 31 patientes ayant présenté une pré éclampsie sévère.
La protéinurie a persisté chez 21 patientes dont 17 cas étaient liés à la pré éclampsie.
L’insuffisance rénale a persisté chez 04 patientes ayant présenté une pré éclampsie : 01 PE/GNC, 01 PE + HELLP, 01 PE + HELLP + éclampsie et 01 PE + HELLP + éclampsie + hémorragie de la délivrance. L’insuffisance rénale a obligé à une hémodialyse définitive dans 01 cas : PE/GNMP.
Conclusion :
La pré éclampsie est une maladie unique de la grossesse qui complique, à l’échelle mondiale, 2 à 8% des grossesses. Longtemps considérée comme résolue après l’accouchement, il est maintenant admis que la pré éclampsie a un retentissement sur la santé future de la mère et de l’enfant. Un suivi doit être proposé à des fins de prévention et de dépistage car elle est considérée comme un facteur de risque de maladies cardiovasculaires, rénales et neurologiques
Références :
- Données de l’office national des statistiques
- Données de l’office national des statistiques
- Données de l’office national des statistiques
- Données de l’office national des statistiques
- Khan, Khalid S., et al., 2006 «WHO Analysis of Causes of Maternal Deaths: A Systematic Review», The Lancet, vol. 367, no. 9516, Avril 2006, pp. 1066-1074;
- Groupe d’Évaluation et de Mesure de la Société Française d’Hypertension Artérielle. « La prise de la tension artérielle chez la femme enceinte ». 2001; Ed. RanD, Meudon, France
- Sibai B.M., Barton J.R. Expectant management of severe preeclampsia remote from term: patient selection, treatment, and delivery indications Am J Obstet Gynecol 2007; 196: 514e19.
- Meher S., Duley L. Rest during pregnancy for preventing pre- eclampsia and its complications in women with normal blood pressure Cochrane Database Syst Rev 2006; 19: CD005939.
- Al Tranquilli G Dekker L Magee. The classification, diagnosis and management of the hypertensive disorders of pregnancy: A revised statement from the ISSHP. Preg Hypertens 2014 (4)
- BM. Sibai Diagnosis, controversies, and management of the syndrome of hemolysis, elevated liver enzymes, and low platelet count. Obstet Gynecol 2004 (103) [Medline]
- CA Bigelow GA Pereira a Warmsley Risk factors for new- onset late postpartum preeclampsia in women without a history of preeclampsia. Am J Obstet Gynecol 2014 (210) [Medline]
- WI Larsen JE Strong JH. Farley Risk factors for late postpar- tum preeclampsia. J Reprod Med 2012 (57) [Medline]
- James W Van hook, Acute kidney injury during pregnancy. Department of Obstetrics and Gynecology, University of Cin- cinnati College of Medicine, Cincinnati, Ohio. Vol 57. Numb 4 December 2014
- Godara SM, Kute VB, Trivedi HL, et al. Clinical profile and outcome of acute kidney injury related to pregnancy in deve- loping countries: A single-center study from India. Saudi J Kid- ney Dis Transpl 2014 ;25 :906-11.