Programmed cell Death 1 (PD1) et un de ses ligands, Programmed Death Ligand1 (PDL1), sont des protéines clefs dans le contrôle de la réponse immunitaire antitumorale. Des données suggèrent que PDL1 est un biomarqueur émergent pour l’immunothérapie par anticorps anti-PD1 et anti-PDL1 dans le cancer bronchique non à petites cellules (CBNPC).
S. Ketit, S. Hamdouche, L. Beddar. Service d’Anatomie et de Cytologie Pathologiques. CHU Abdesselam Benbadis, Constantine
Date de soumission : 11 Octobre 2020.
Résumé : Programmed cell Death 1 (PD1) et un de ses ligands, Programmed Death Ligand1 (PDL1), sont des protéines clefs dans le contrôle de la réponse immunitaire antitumorale. Des données suggèrent que PDL1 est un biomarqueur émergent pour l’immunothérapie par anticorps anti-PD1 et anti-PDL1 dans le cancer bronchique non à petites cellules (CBNPC). L’immunohistochimie (IHC) PD-L1 est le seul biomarqueur prédictif proposé en oncologie thoracique dans le cadre de l’immunothérapie PD-L1/PD1. Dans ce contexte, les études publiées relatives à ce biomarqueur sont nombreuses, mais elles soulèvent des interrogations sur la nature de l’anticorps à utiliser et dans quelle(s) condition(s) ; le seuil de positivité à appliquer et l’intégration de cette activité dans le fonctionnement quotidien d’un laboratoire d’anatomo cytopathologie (ACP), ce qui implique de rendre un examen fiable, devant éviter impérativement, compte tenu des conséquences thérapeutiques, un résultat faussement positif ou faussement négatif. Ainsi l’interprétation de l’IHC PD-L1 demande une expertise et une formation spécifique des pathologistes.
Mots clés : PD-L1, immunohistochimie, interprétation, poumon, cancer non à petites cellules.
Abstract: Programmed cell death 1(PD1) and one of its ligands, Programmed Death Ligand1(PDL1), are key immune checkpoint proteins. Data suggest that PDL1 is an emerging biomarker for immunotherapy by anti-PD1 antibodies and anti-PDL1 in lung cancer non-small cell (NSCLC). PD-L1 detection by immunohistochemistry (IHC) is the only predictive biomarker available to date for PD-L1/PD1 immunotherapy in thoracic oncology. While many studies have been published in the domain of this biomarker, they raise a number of questions mainly concerning the type of antibody for use and its condition of utilization, the threshold to be used; and the adoption of this methodology as part of the daily practice of a pathology laboratory; which implies providing an extremely reliable result that, taken the therapeutic consequences, avoids any false positive and negative results. In this context, assessment of PD-L1 IHC requires considerable expertise and specific training of pathologists.
Keywords: PD-L1, immunohistochemistry, interpretation, lung, non-small cell carcinoma.
Introduction
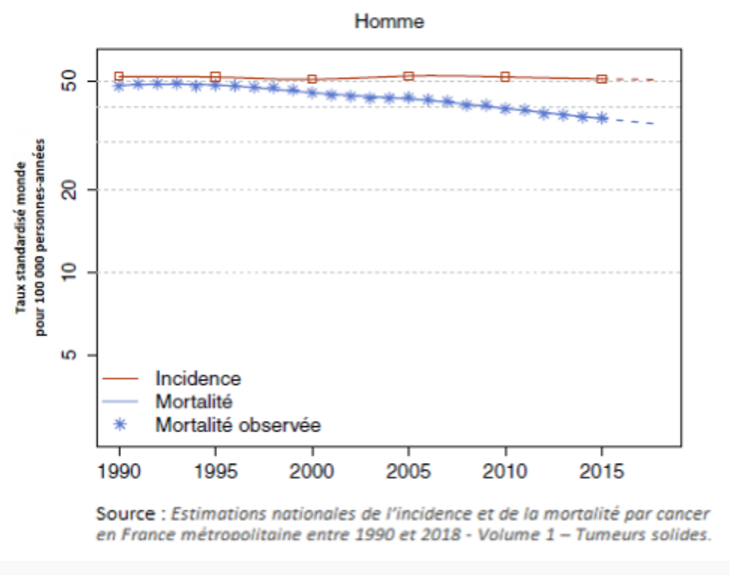
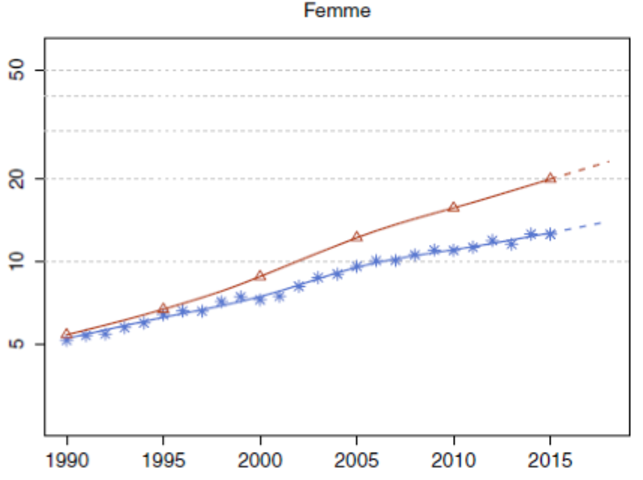
Le cancer bronchique non à petites cellules (CBNPC) représente la forme histologique la plus fréquente des cancers bronchiques. Il constitue la première cause de décès par cancer dans la population masculine de par le monde et en Algérie, avec de faibles taux de réponse à la chimiothérapie conventionnelle. Ces dix dernières années, la prise en charge du cancer du poumon a bien évolué. De nombreuses altérations moléculaires des voies de signalisation des tumeurs ont été découvertes, conduisant au développement de thérapies dites ciblées, et à la notion de médecine personnalisée [1]. Cependant, près de la moitié des patients atteints d’un CBNPC ne présentent pas ces mutations et ne peuvent pas bénéficier de ces thérapies ciblées [2].
La recherche contre le cancer du poumon a exploré alors d’autres pistes thérapeutiques. L’une de ces pistes concerne le rapport paradoxal qui existe entre le système immunitaire et les cellules tumorales.
Problématique
De nouvelles stratégies thérapeutiques ont émergé et transformé le pronostic de sous-groupes spécifiques de CBNPC métastatiques : ce sont les thérapies ciblées, représentées essentiellement par les inhibiteurs de tyrosine kinase en présence de mutation ou de réarrangement des oncogènes EGFR, ALK et ROS1, observés principalement dans les adénocarcinomes des sujets peu ou non-fumeurs et l’immunothérapie par ciblage du point de contrôle de la réponse immunitaire PD1/PD-L1 par des anticorps appelés inhibiteurs des checkpoints de l’immunité (ICI).
PD-1 est une molécule de costimulation exprimée par les lymphocytes T activés ; son engagement avec son ligand, PD-L1 (PD1-ligand également désigné CD274 ou B7-H1), déclenche un signal inhibant transitoirement ou définitivement les capacités cytotoxiques des lymphocytes T CD8+. L’interaction PD1/PD-L1 est d’abord un mécanisme physiologique visant à réduire l’auto-immunité, mais lorsque PD-L1 est exprimé par les cellules tumorales, cette interaction leur permet d’échapper à la surveillance immunitaire en inhibant l’activation des lymphocytes T cytotoxiques. C’est dans ce contexte que sont actuellement développés les ICI PD1/PD-L1 dans les cancers thoraciques. Le ciblage de PD1/PD-L1 repose sur l’utilisation de molécules levant l’interaction entre PD1/PD-L1 et réactivant la supposée réponse immunitaire anti tumorale préexistante. Ces anticorps sont soit dirigés contre PD1, comme le nivolumab (Opdivo®, Bristol-Myers Squibb) et le pembrolizumab (Keytruda®, Merck et Co) ou contre PD-L1, comme l’atezolizumab (Tecentriq®, Genentech), le durvalumab (Imfinzi®, Astra-Zeneca) et l’avelumab (Bavencio®, EMD Serono). La prescription de certains de ces ICI repose sur l’expression de PD-L1 en IHC par les cellules tumorales [3-4].
Indications du test PD-L1 dans le CBNPC
Quel patient tester et quand ?
Le test PD-L1 doit être réalisé de manière systématique dès le diagnostic de CBNPC métastatique. Il peut être réalisé a posteriori en cas de progression de la maladie à la demande du clinicien.
Le pembrolizumab (Keytruda®, Merck et Co), est le seul inhibiteur de PD1/PD-L1 pour lequel une restriction d’utilisation est basée sur l’expression de PD-L1. Un seuil minimal d’expression par les cellules tumorales de 50% est requis pour la prescription en première ligne, il est de 1% pour la prescription en seconde ligne et au-delà.
L’expression de PD-L1 étant souvent hétérogène ou modulée par certains traitements, un nouveau prélèvement tumoral peut être demandé par le clinicien, pour une nouvelle évaluation de l’expression de PD-L1, en particulier si le premier prélèvement était négatif.
En dehors de ces indications, le clinicien peut être amené à demander une recherche d’expression de PD-L1, pour évaluer la probabilité de réponse du patient à un anti-PD1/PD-L1
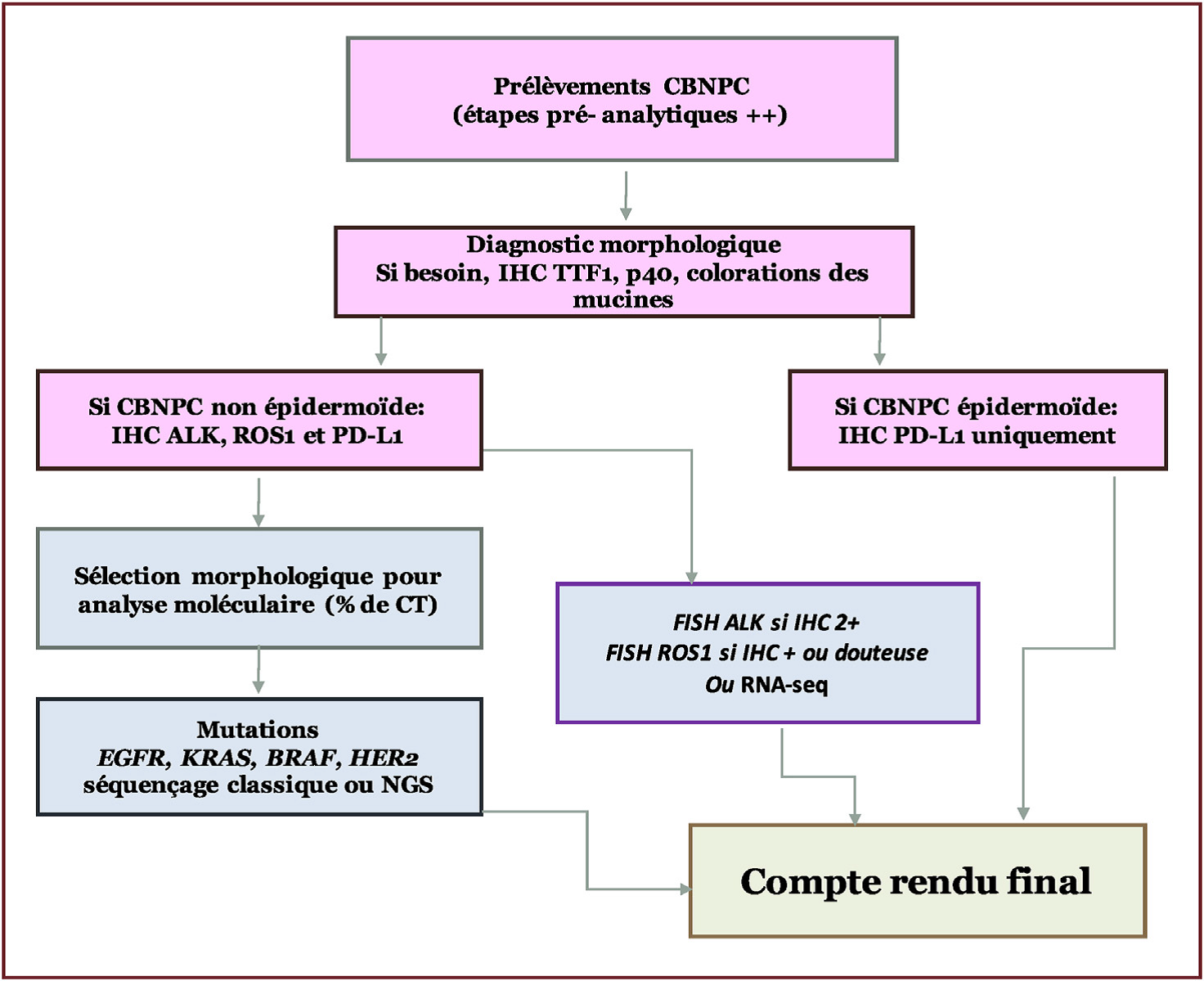
Schéma 1. Algorithme de tests diagnostiques et théranostiques pour tout carcinome broncho- pulmonaire non à petites cellules à un stade avancé. (Algorithm for diagnostic and theranostic tests for advanced stage NSCLC. www.sciencedirect.com
Quel type d’échantillon tumoral utiliser ?
L’expression de PD-L1 peut être testée sur biopsie ou prélèvement chirurgical, sur la tumeur principale, la récidive, ou le site métastatique.
Sur biopsie, il existe un risque de faux négatif du test immunohistochimique lié à l’hétérogénéité intratumorale de l’expression de PD-L1.
Il existe également une hétérogénéité d’expression entre site tumoral primitif et métastases avec en moyenne 75% de concordance entre les différents prélèvements [5] avec des seuils de 1%, 5%, 10% et 50%. Ainsi dans environ 20% des cas, la métastase ganglionnaire devient PD-L1 positive à la différence de la tumeur primitive négative ; à l’inverse, 10% de ces métastases peuvent être négatives avec une tumeur initiale PD-L1 positive. Les prélèvements discordants correspondent le plus souvent à des échantillons tumoraux prélevés à plus de 6 mois d’intervalle [6].
L’utilisation rationnelle des prélèvements de petite taille est souhaitable en favorisant l’inclusion des fragments dans plusieurs cassettes.
Un minimum de 100 cellules tumorales analysables est recommandé. Lorsque le nombre de cellules tumorales est inférieur à 100 et surtout inférieur à 50, il est possible de rendre un résultat en émettant des réserves sur la représentativité du prélèvement.
Sur pièce opératoire, l’expression est le plus souvent homogène entre différents blocs tumoraux en termes d’expression de PD-L1 par les cellules tumorales (TC) [7].
95% des biopsies sont adéquates pour le test PD-L1 avec des résultats comparables entre biopsies et pièces opératoires si elles comportent plus de 100 cellules tumorales [8].
Les prélèvements cytologiques fixés et inclus en paraffine (cytoblocs) peuvent être utilisés pour l’évaluation de l’expression de PD-L1, dès lors que ces prélèvements comportent plus de 100 cellules tumorales analysables. L’utilisation des échantillons cytologiques n’a pas été validée dans les essais cliniques et n’est pas recommandée actuellement pour l’utilisation des tests (ou kits) PD-L1 [8].
L’étape pre-analytique. La phase pré-analytique conditionne la qualité des techniques ultérieures (IHC, ISH et biologie moléculaire), et donc la détection de PD-L1 par IHC [9-10].
Ischémie froide. Il est recommandé de réduire le plus possible la durée d’ischémie froide des prélèvements. L’ischémie froide est définie comme le temps écoulé entre le moment où le prélèvement tissulaire est extrait du corps humain et sa mise au contact du fixateur. Un retard de fixation supérieur à 1 heure diminue de manière significative la détection de marqueurs immunohistochimiques et le signal en ISH.
Pour les biopsies, il est recommandé de fixer le prélèvement dans le fixateur immédiatement (délai de quelques minutes). Pour les pièces opératoires, le délai de fixation doit être inférieur à 1 heure.
Fixation. Les prélèvements doivent être fixés dans le formol neutre tamponné à 10% durant 6 à 48 heures, en utilisant un volume de fixateur suffisant. Le seul fixateur recommandé est le formol neutre tamponné à 10%, car les protocoles des tests compagnons ont été validés cliniquement uniquement avec ce fixateur de référence.
Le temps de fixation doit être d’au moins 6 heures pour les biopsies afin d’éviter une sous fixation dommageable de façon irrémédiable et au maximum de 72 h (24-48 h recommandé) pour les pièces opératoires (une fixation plus longue doit être rapportée dans le compte rendu) [11-12].
Inclusion. L’utilisation d’une paraffine à point de fusion bas (inférieur à 60°C idéalement 55-58°C) est recommandée [12].
Décalcification. La décalcification des échantillons tissulaires est à éviter, du fait de l’altération des acides nucléiques et des protéines qu’elle induit. Si une décalcification s’avère nécessaire, il est préférable d’utiliser l’EDTA à 10% (chélateur de calcium), afin de limiter l’impact sur les techniques d’IHC [12-13].
Confection des coupes. Il est recommandé d’effectuer le marquage PD-L1 sur des coupes fraichement coupées et ne datant pas de plus de 6 mois. Dans les guides d’interprétation des différents tests, un délai maximum de conservation de 2 mois pour le test SP142 (Ventana PD-L1 SP142 Assay, Ventana Medical Systems Inc.), de 4 mois pour le test 28-8 PharmDx (Agilent Technologies/Dako) et de 6 mois pour le test 22C3 PharmDx (Agilent Technologies/Dako) est recommandé [14-15].
Si des lames blanches doivent être conservées pour des études ultérieures, ou comme témoins externes, il faut privilégier soit une conservation des lames à 4°C soit à température ambiante, à l’abri de la lumière, après couverture des lames par une fine couche de paraffine, qui n’empêche cependant pas une légère perte de signal [9-11-12-16].
Témoins externes et internes. Les échantillons qui serviront de témoins externes doivent avoir été pris en charge selon les mêmes conditions pré-analytiques que les échantillons à tester. Afin de s’assurer de la reproductibilité de la technique d’IHC, des fragments de témoins externes positif et négatif doivent être inclus sur chaque lame dans la mesure du possible, sinon il faut prévoir une lame de témoins externes au cours de chaque cycle de marquage. Les témoins externes permettent de contrôler l’intensité du marquage et de détecter des variations éventuelles de la sensibilité du test. Ce point est particulièrement critique pour le test PD-L1 qui prend en compte le pourcentage de cellules marquées quelle que soit l’intensité.
Des blocs témoins externes peuvent être faits avec de l’amygdale normale ou avec des tumeurs du laboratoire montrant une expression variable de PD-L1. Afin de préserver le matériel, un bloc peut être constitué en réalisant des punchs biopsiques de 3 mm.
Idéalement, les témoins doivent être coupés en même temps que le prélèvement à tester. Des lames blanches du bloc témoin peuvent toutefois être faites à l’avance en respectant le délai et les conditions de conservation. La date de coupe devra être indiquée sur la lame [11-12].
Le tissu placentaire (cellules trophoblastiques) n’est pas adapté comme témoin positif externe en raison d’un très haut niveau d’expression de PD-L1, qui ne permet pas de détecter les faibles niveaux d’expression et donc un manque de spécificité du test IHC.
Les témoins internes exprimant PD-L1 sont les cellules dendritiques et macrophages ainsi que certains sous-types de lymphocytes T et B. Si ces cellules ne sont pas présentes sur le prélèvement, il est nécessaire de se référer au témoin externe.
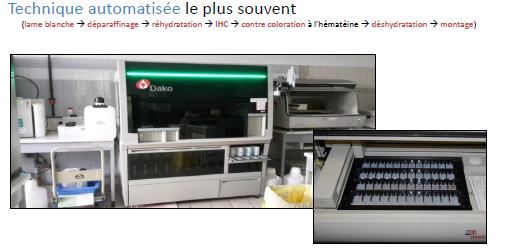
Fig 1. Technique d’immuno-histochimie. www.sciencedirect.com
L’étape analytique
Technique immunohistochimique
L’utilisation de tests standardisés (kits prêts à l’emploi) doit être favorisée dans la mesure du possible. Le test SP142 (Ventana PD-L1 SP263 Assay, Ventana Medical Systems Inc), le test 28-8 PharmDx (Agilent Technologies/Dako) et le test 22C3 PharmDx (Agilent Technologies/Dako) paraissent interchangeables en raison de leur très bonne concordance pour le marquage PD-L1 des cellules tumorales dans les CBNPC [17-18].
Les tests développés dans les laboratoires (Laboratory Developed Tests ou LDT dans la littérature anglo-saxonne) appelés encore « tests maison » peuvent être utilisés pour évaluer l’expression de PD-L1. Leur concordance doit être validée en comparaison à un test (ou kit) de référence et leur calibration doit faire l’objet d’une attention particulière.
Il est par ailleurs particulièrement recommandé de participer régulièrement à un test de contrôle qualité externe, surtout en cas d’utilisation d’un test développé localement.
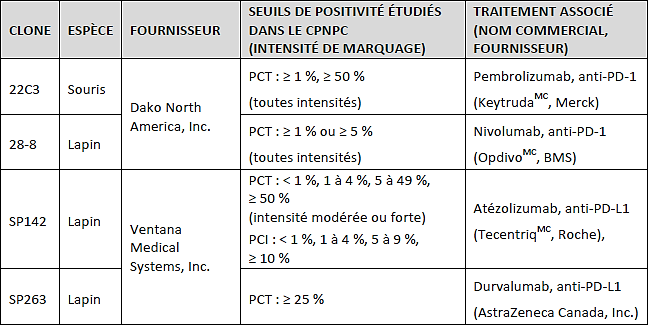
Tableau1 : Principaux anticorps utilisés en IHC pour la détection de la protéine PD-L1 dans le CPNPC, seuils de positivité et traitement associé (adapté de celui publié par Adam et ses collaborateurs (2016) [19]).
Interprétation du marquage PD-L1
Avant toute interprétation du marquage PDL1, il est indispensable d’évaluer la qualité de la préservation du tissu et sa fixation, la représentativité du matériel et la quantité de cellules tumorales sur la coloration standard HES.
Ainsi, une quantité de cellules tumorales inférieure à 100 cellules doit être mentionnée et doit faire émettre des réserves sur la représentativité du prélèvement, voire conduire à considérer le prélèvement comme non adéquat pour la détermination du statut PD-L1.
Également une nécrose abondante qui peut générer un bruit de fond, des artéfacts d’écrasement ou des effets de bordures liés au séchage, une fixation défectueuse ou une décalcification, doivent être mentionnés et pris en compte pour l’interprétation.
L’interprétation du marquage PD-L1 des témoins internes et externes est requise avant toute analyse.
Le témoin positif externe permet de contrôler que le protocole d’IHC offre la sensibilité requise. Si le témoin externe positif n’est pas ou insuffisamment marqué, la lame ne doit pas être interprétée. L’intérêt d’avoir un témoin négatif est de s’assurer qu’il n’a pas de marquage non spécifique de type bruit de fond ou marquage cytoplasmique.
L’examen immunohistochimique est interprété en appliquant un système d’évaluation spécifique au poumon, Tumor Proportion Score (TPS). Il s’agit du pourcentage total des cellules tumorales viables, exprimant PD-L1 sur la lame examinée. Un marquage membranaire uniquement, linéaire, complet ou non donc n’a pas besoin d’être circonférentiel et quelle qu’en soit l’intensité. L’intensité du marquage n’est pas prise en compte, toute intensité étant considérée de la même manière. L’analyse au faible grandissement (G×2 ou G×4) permet d’apprécier un marquage intense, et d’évaluer sa distribution homogène ou hétérogène sur la coupe. Les zones peu ou pas marquées à faible grandissement doivent être examinées à fort grandissement (G×10 à G×40) pour ne pas méconnaître un marquage membranaire incomplet et/ou de faible intensité. Il est recommandé d’évaluer le pourcentage de cellules tumorales positives, en ne prenant en compte que, pour l’administration de pembrolizumab, le seuil de 1% en deuxième ligne et de 50% en première ligne.
Différentes techniques sont proposées pour aider à résoudre le problème de l’hétérogénéité tumorale, surtout sur des pièces opératoires. Il est possible :
- Soit d’évaluer le pourcentage de zones fortement marquées (3+) d’intensité, visibles dès le faible grandissement, de zones moyennement marquées (2+) et de zones faiblement marquées (1+) visibles seulement à fort grandissement et les additionner pour obtenir un pourcentage total de cellules marquées ;
- Soit d’évaluer les zones de pourcentage de positivité identique et les additionner (par ex, 30% de la tumeur comporte 80% de cellules positives, 20% comporte 30% de cellules positives et le reste est négatif = 30% × 80 + 20% × 30 = 24 + 6 = 30% au total).
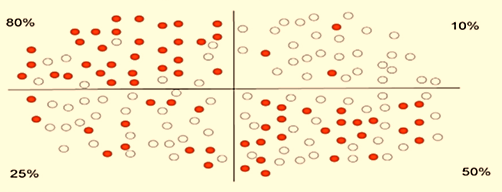
Schéma 2. Exemple de méthode permettant de quantifier l’expression de PD-L1 quand elle est hétérogène : le % de cellules tumorales marquées est (80 + 10 + 25 + 50): 4 ∼ 40%. (Suggestion of a scoring method for PD-L1 expression: A systematic approach could be to divide the section into equal areas evaluated for percentage of tumor cell positivity, and then to average this percentage. As an example: (80 + 10 + 25 + 50): 4 ∼40%). www.sciencedirect.com
 |
 |
|
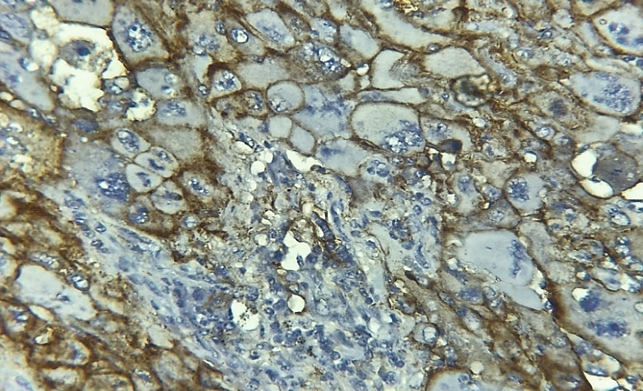
Fig 2. IHC PDL1+ diffus forte intensité. Diffuse and strong membranous staining. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
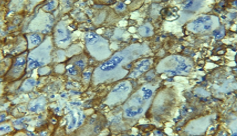
Fig 3. IHC PD-L1+ diffus intensité modérée. Diffuse and moderate membranous staining. Laboratoire d’anatomie pathologique CHU Benbadis Constantine. |
 |
 |
|
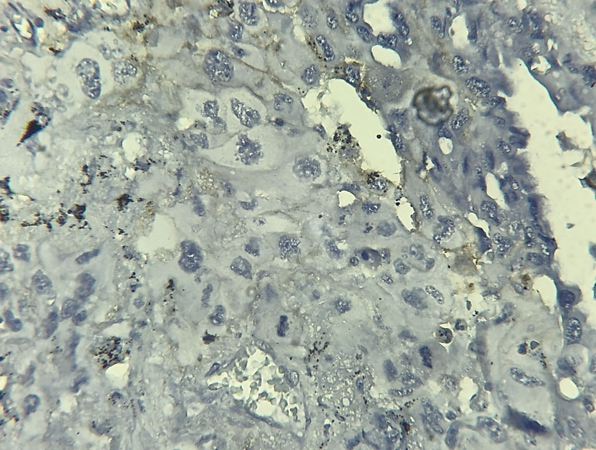
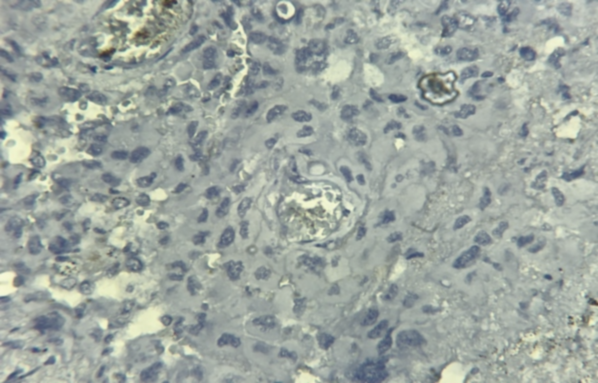
Fig 4. IHC PD-L1+ faible intensité. Focal and low membranous staining. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
Fig 5. IHC PD-L1– absence de marquage. Lack of staining. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
 |
 |
|
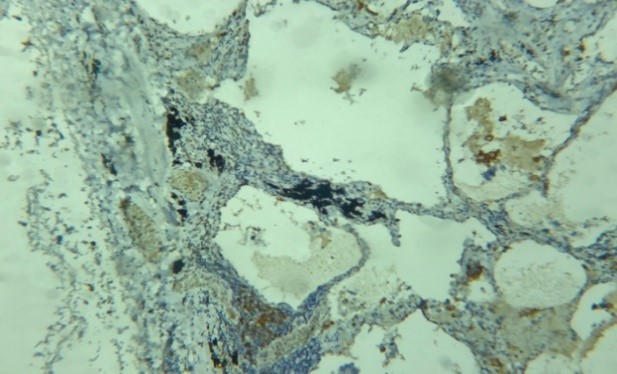
Fig 6. Bruit de fond non spécifique. Non-specific background noise. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
Fig 7. Pigments anthracosiques. Anthracosic pigments. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
 |
 |
|
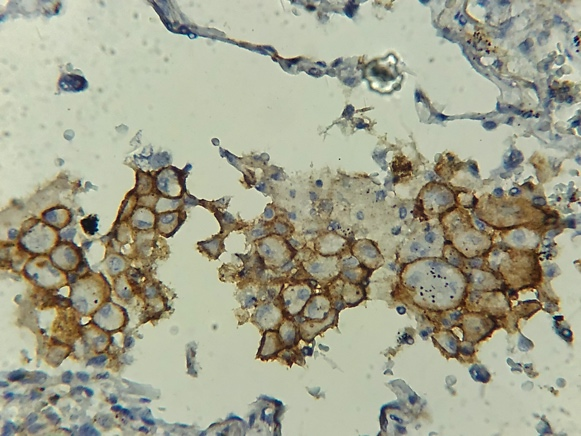
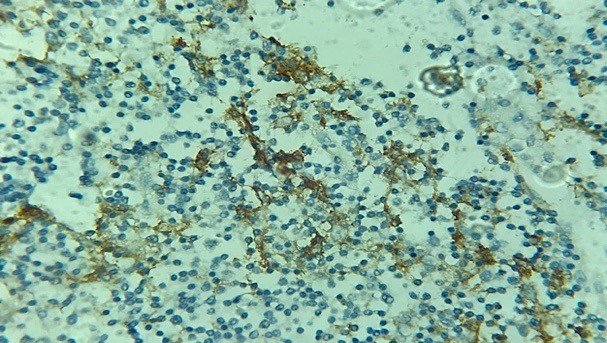
Fig 8. Marquage des macrophages alvéolaires. Staining of alveolar macrophages. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
Fig 9. Marquage de cellules immunitaires. Staining of numerous immune cells. Laboratoire d’anatomie pathologique CHU Benbadis Constantine |
 |
 |
|
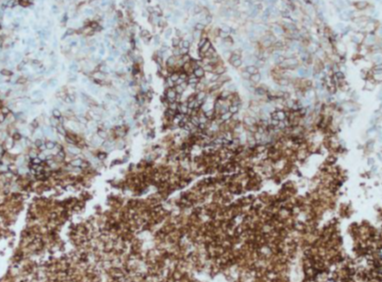
Fig 10. Necrose. Necrosis. PD-L1 IHC 22C3 PharmDx Interpretation Manual, DAKO. |
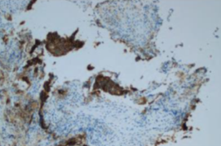
Fig 11. Artéfact d’écrasement Crush artifact. PD-PD-L1 IHC 22C3 PharmDx Interpretation Manual, DAKO |
Pièges et artéfacts
Il s’agit des mêmes artéfacts que ceux observés au cours de toute analyse immunohistochimique : bruit de fond lié aux séchage, déparaffinage ou rinçage insuffisants des lames, effets de bordure liés au séchage du tissu avant fixation ou pendant la coloration, artéfacts d’écrasement ou d’électrocoagulation liés à la procédure de prélèvement, nécrose, pigments d’anthracose, mauvaise conservation de la morphologie et des épitopes liée à une fixation insuffisante.
Certaines cellules tumorales peuvent présenter un marquage granulaire cytoplasmique gênant la visualisation du marquage membranaire (notamment avec le test SP263) ou présenter des contours cytoplasmiques indistincts.
La présence de très nombreuses cellules immunitaires positives situées à l’interface avec les cellules tumorales peut gêner considérablement l’analyse de ces dernières.
Enfin les macrophages sont parfois très marqués et constituent un piège surtout lorsqu’ils se mêlent aux cellules tumorales. Ils se distinguent néanmoins par leurs caractéristiques cytologiques (petit noyau régulier, faible ratio N/C) et leur topographie (souvent endo-alvéolaire ou en bordure de nécrose).
L’étape post-analytique
Le compte-rendu de l’évaluation de l’expression de PD-L1 doit mentionner la date, le siège, le type de prélèvement (cytologie, biopsie, pièce opératoire), la fixation, une éventuelle étape de décalcification, ainsi que certains paramètres pouvant influencer l’expression de PD-L1 tels que le stade de la maladie, la notion de tumeur primitive, de récidive, de métastase et les traitements antérieurs. Il peut éventuellement intégrer les altérations génomiques associées qui influencent l’expression de PD-L1 [20-21].
Pour la partie analytique, il est nécessaire d’indiquer l’anticorps (clone), et l’automate utilisé ainsi que de préciser s’il s’agit d’un test prêt à l’emploi ou d’un LDT.
Seul le pourcentage de cellules tumorales marquées, quel que soit le niveau d’intensité, est à rapporter. La connaissance des seuils permettant l’indication thérapeutique est importante (actuellement 1% et 50%).
Il faut confirmer le marquage des témoins positifs externes et/ou internes (cellules immunitaires) et pour les échantillons de petite taille, il faut préciser combien de cellules tumorales sont analysables, avec des réserves si leur nombre est inférieur à 100. Il est également possible d’émettre des réserves si les étapes pré-analytiques posent problème (fixation non connue ou hors délais, décalcification, trop grand délai de stockage des lames blanches, etc.)
En ce qui concerne la conclusion du compte-rendu, il n’est pas recommandé de conclure par un résultat positif ou négatif pour l’expression de PD-L1. Il est préférable de la simplifier en indiquant le pourcentage de cellules tumorales exprimant PD-L1.
Assurance qualité
Les récentes recommandations publiées au niveau international [22-23-24] préconisent de mettre en place un programme de contrôle de la qualité des techniques d’analyse au sein des laboratoires effectuant des tests PD-L1, en prônant en particulier l’utilisation de témoins calibrés à chaque série de tests. Un nombre minimal de tests doit être réalisé et interprété par an, dans chaque structure ACP pour asseoir l’expertise technique et médicale et optimiser la qualité et les coûts des analyses. La réalisation du test PD-L1, doit être conditionnée à la participation à une évaluation externe de la qualité, avec des résultats satisfaisants, selon les critères définis par l’organisme d’Assurance Qualité (AQ).
Conclusion
Le statut PD-L1 en immunohistochimie fait partie des biomarqueurs potentiels les plus étudiés. L’évaluation immunohistochimique de l’expression de PD-L1 par les cellules tumorales est maintenant requise pour la prescription du pembrolizumab en première et en deuxième ligne dans les CBNPC avancés ou métastatiques. L’IHC PD-L1 est considérée comme un test théranostique, ce qui place les pathologistes au centre des décisions thérapeutiques. Ce test doit donc être mis en place dans tous les laboratoires ayant un recrutement en pathologie pulmonaire et réalisé dans le même temps que les autres marqueurs théranostiques. Des programmes de formation nationaux ont déjà permis à plusieurs pathologistes de se former pour l’interprétation du test PD L1 et de l’implémenter dans leurs laboratoires. Mais comme toute interprétation quantitative ou semi-quantitative d’une analyse immunohistochimique est sujette à une certaine variabilité entre les lecteurs, d’autres programmes de formations pour les pathologistes seront souhaitables afin d’harmoniser nos pratiques et renforcer la qualité de ce test théranostique, pour améliorer encore la prise en charge de nos patients.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Eberlé F. Characterization of principal predictive biomarkers of targeted therapies in thoracic cancer]. Ann Pharm Fr. Nov 2013; 71(6):369‑
- Gibault L, Cazes A, Narjoz C, Blons H. [Molecular profiling of non-small cell lung cancer]. Rev Pneumol Clin. Avr 2014; 70 (1-2):47‑
- Du ruisseaux M, Rouquette I, Adam J, et al. [Efficacy of PD-1/PD-L1 immune checkpoint inhibitors and PD-L1 testing in thoracic cancers]. Ann Pathol 2017; 37:61-78.
- Roussel H, Gibault L, Verkarre V, et al.Quiz: Ready, study, score! Ann Pathol 2017; 37:7-10.
- Kim S, Koh J, Kwon D, et al. Comparative analysis of PD-L1 expression between primary and metastatic pulmonary adenocarcinomas. Eur J Cancer Oxf Engl 1990 2017; 75:141-9.
- Mansfield AS, Aubry MC, Moser JC, et al. Temporal and spatial discordance of programmed cell death-ligand 1 expression and lymphocyte tumor infiltration between paired primary lesions and brain metastases in lung cancer. Ann Oncol2016; 27:1953-8.
- Rehman JA, Han G, Carvajal-Hausdorf DE, et al. Quantitative and pathologist-read comparison of the heterogeneity of programmed death-ligand 1 (PD-L1) expression in non-small cell lung cancer. Mod Pathol 2017; 30:340-9.
- Heymann JJ, Bulman WA, Swinarski D, et al. Programmed death-ligand 1 expression in non-small cell lung carcinoma: comparison among cytology, small biopsy, and surgical resection specimens Cancer 2017 undefined
- Engel KB, Moore HM. Effects of pre analytical variable son the detection of proteins by immunohistochemistry in formalin-fixed, paraffin-embedded tissue. Arch Pathol Lab Med2011; 135:537-43.
- Bass BP, Engel KB, Greytak SR, et al. A review of pre analytical factors affecting molecular, protein, and morphological analysis of formalin-fixed, paraffin-embedded (FFPE) tissue: how well do you know your FFPE specimen? Arch Pathol Lab Med2014; 138:1520-30.
- Bussolati G, Annaratone L, Maletta F. The pre-analytical phase in surgical pathology. Recent Results Cancer Res2015;199:1-13.
- Mac Grogan G, Mathieu M-C, Poulet B, et al. [Pre-analytical stage for biomarker assessment in breast cancer: 2014 update of the GEFPICS’ guidelines in France]. Ann Pathol2014; 34:366-72.
- Aisner DL, Rumery MD, Merrick DT, et al. Do more with less: tips and techniques for maximizing small biopsy and cytology specimens for molecular and ancillary testing: the University of Colorado experience. Arch Pathol Lab Med 2016,undefined
- undefined pd-l1-ihc-22C3-pharmdx-nsclc-interpretaion-manual.pdf manual 22C3.
- undefined interpretation-manual.pdf
- undefined
- Hirsch FR, Mc Elhinny A, Stanforth D, et al. PD-L1 Immunohistochemistry assays for lung cancer: results from Phase 1 of the Blueprint PD-L1 IHC Assay Comparison Project. J Thorac Oncol2017; 12:208-22.
- Adam J, Le Stang N, Rouquette I, et al. Multicenter French harmonization study for PD-L1 IHC testing in non-small cell lung cancer. Ann Oncol 2018, undefined
- Adam J, Planchard D, Marabelle A, Soria JC, Scoazec JY, Lantuejoul S. Évaluation de l’expression de PD-L1 en immunohistochimie : un biomarqueur émergent dans les carcinomes pulmonaires non à petites cellules. Ann Pathol 2016;36(1):94-102.
- Yang C-Y, Lin M-W, Chang Y-L, et al. Programmed cell death-ligand 1 expression in surgically resected stage I pulmonary adenocarcinoma and its correlation with driver mutations and clinical outcomes. Eur J Cancer Oxf Engl 1990 2014; 50:1361-9.
- Ota K, Azuma K, Kawahara A, et al. Induction of PD-L1 Expression by the EML4-ALK Onco protein and Downstream Signaling Pathways in Non-Small Cell Lung Cancer. Clin Cancer Res2015; 21:4014Q-21.
- Torlakovic EE, Cheung CC, D’Arrigo C, et al. Evolution of quality assurance for clinical immunohistochemistry in the era of precision medicine -Part 2: immunohistochemistry test performance characteristics. Appl Immunohistochem Mol Morphol AIMM 2017; 25:79-85.
- Cheung CC, D’Arrigo C, Dietel M, et al. Evolution of quality assurance for clinical immunohistochemistry in the era of precision medicine: Part 4: Tissue Tools for Quality Assurance in Immunohistochemistry. Appl Immunohistochem Mol Morphol AIMM 2016, undefined
- Lantuejoul S, et al. Tests immunohistochimiques PD-L1 dans les cancers du poumon non-à petites cellules: recommandations par le groupe PATTERN de pathologistes thoraciques. Annales de pathologie (2018), undefined