L’arthrose lombaire est une pathologie à constatation radiographique avec expressions cliniques variables. Elle se définit par trois lésions élémentaires : le pincement discal, les ostéophytes et l’ostéocondensation des plateaux vertébraux
Rachida Allat, Amina Mameche, Chafika Haouichat
Service de rhumatologie CHU Douéra, maitre assistante rhumatologie
Service de rhumatologie CHU Douéra, assistante pharmacologie
Service de rhumatologie CHU Douéra, professeur et chef de service rhumatologie
Date de soumission : 27/06/2020
Résumé
L’arthrose lombaire est une pathologie à constatation radiographique avec expressions cliniques variables. Elle se définit par trois lésions élémentaires : le pincement discal, les ostéophytes et l’ostéocondensation des plateaux vertébraux. La compréhension des processus physiopathologiques de la dégénérescence discale a permis le développement de stratégies de médecine régénératrice : thérapie cellulaire et ingénierie tissulaire.
Abstract
Lumbar osteoarthritis is a pathology with radiographic findings with variable clinical expressions. It is defined by three elementary lesions: disk space narrowing, osteophytes endplates osteocondensation. Understanding the pathophysiological processes of disc degeneration has enabled the development of regenerative medicine strategies: cell therapy and tissue engineering.
Mots clés : Arthrose lombaire, Disque intervertébral, Médecine régénératrice, Thérapie cellulaire.
Keywords : Lumbarosteoarthritis, Intervertebral disc, Regenerative medicine, Cell therapy
Introduction
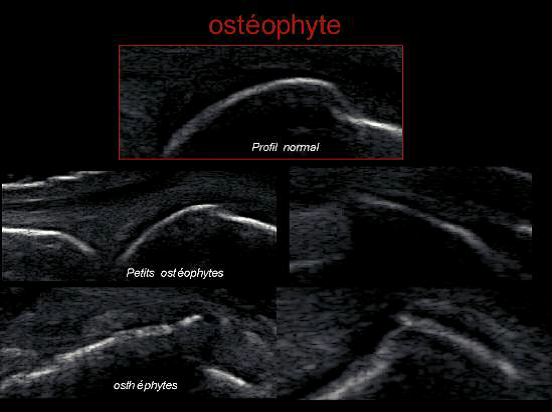
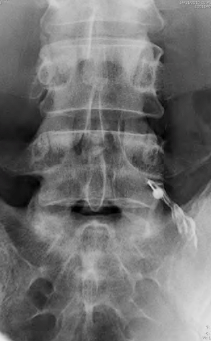
L’arthrose lombaire se définit par trois lésions élémentaires : le pincement discal, les ostéophytes et l’ostéocondensation des plateaux vertébraux.
Le rachis lombaire est constitué de cinq vertèbres mobiles. L’articulation intervertébrale comporte à chaque étage trois systèmes articulaires :
- L’articulation inter-corporéale que constitue le disque intervertébral (DIV)
- Les deux articulations inter apophysaires postérieures qui sont d’authentiques articulations synoviales
- Un riche environnement ligamento-musculaire assure le maintien du rachis.
Le rachis lombaire est soumis tout au long de la vie à des contraintes liées à sa mobilisation quasi permanente, et aux contraintes de poids qu’il subit. C’est pour cela cette structure autant sollicitée se détériore et soit exposée précocement à l’arthrose. Chez la majorité des sujets cette détérioration se manifeste très tôt, dès le début de l’âge adulte. Elle commence par la détérioration des disques intervertébraux, en particulier de ceux soumis aux plus fortes contraintes. Avec le temps, le noyau gélatineux a tendance à se dessécher, et donc à moins bien répartir les forces qui s’exercent sur lui, à diminuer de hauteur (radiologiquement, l’espace intervertébral se pince). Dès lors, les fibres concentriques de l’anneau, moins bien maintenues par la tension du noyau et soumises à des contraintes en compression, ont tendance à se fissurer, à se déchirer latéralement. Dans certaines circonstances, lors de mouvements ou d’efforts violents, des fragments du noyau peuvent s’introduire dans ces fissures, éventuellement venir faire saillie en dehors de l’anneau : c’est la classique hernie discale. Plus tard, le noyau, continuant à se dessécher, se fragmente et même disparaît, ce qui explique que les hernies discales s’observent surtout entre 30 et 50 ans, et sont beaucoup plus rares plus tard.
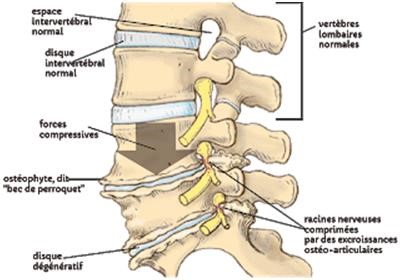
La détérioration du disque diminue son rôle d’amortisseur vertical. Les vertèbres sont soumises à des contraintes plus importantes et sont obligées de réagir pour y faire face : les plateaux vertébraux se densifient, au pourtour des vertèbres se développent des ostéophytes (fig.1). Ce processus arthrosique intéresse aussi les articulations inter apophysaires postérieures, fonctionnellement très liées à l’articulation disco vertébrale dans le même segment mobile (1).
La lombarthrose est une pathologie à constatation radiographique avec expressions cliniques variables. Elle peut être soit asymptomatique soit d’expression locale (lombalgie chronique, lombalgie aigue ou lumbago) soit d’expression compressive radiculaire (lombosciatalgie, cruralgie) soit responsable d’un tableau de syndrome de la queue de cheval qui s’explique par un canal lombaire rétréci secondaire à une lombarthrose.
Cette pathologie invalidante est l’une des principales causes de handicap dans le monde.
Les traitements actuels des douleurs lombaires sont basés sur des traitements conservateurs ou chirurgicaux. Les découvertes récentes relatives à la physiopathologie ont permis de constituer de nouvelles perspectives thérapeutiques à visée curative telle que la médecine régénératrice : thérapie cellulaire et ingénierie tissulaire (2).
Figure 1 : Arthrose lombaire d’après Lefebvre ostéopathe
Thérapie cellulaire discale
Les différents types cellulaires
- Les cellules du nucleus pulposus (NP) et les chondrocytes articulaires
Le principe est donc la mise en culture de chondrocytes matures prélevés chez le receveur pour être réinjectés au niveau de la perte de substance cartilagineuse l’injection de ces cellules a permis de restaurer l’intensité du signal en T2 à l’IRM reflétant une amélioration de l’état d’hydratation discal Aujourd’hui la pertinence de l’utilisation de chondrocytes est remise en question pour la médecine régénératrice du DIV. Dans ce contexte, l’utilisation d’autres types cellulaires a été envisagée (3).
- Les cellules souches
- Les cellules induced pluripotent stem (iPS): c’est des cellules adultes « reprogrammables, Cette reprogrammation passe par des modifications génétiques ayant pour objectif de réactiver les signaux d’immaturité et de prolifération. Elles possèdent les propriétés des cellules souches embryonnaires (CSE). Les cellules iPS pourraient constituer un tournant dans la stratégie de prise en charge de la dégénérescence discale. Ces cellules se sont révélées capables de synthétiser les composants de la matrice extracellulaire d’un NP natif (protéoglycanes et collagène de type II) (4).
- Lescellules souches mésenchymateuses (CSM): La multi potence des cellules souches mésenchymateuses (CSM) en fait des candidates prometteuses pour la médecine. C’est les plus utilisées dans le développement d’applications thérapeutiques en rhumatologie. Elles produisent de nombreux facteurs solubles directement ou par le biais de vésicules extracellulaires qui ont des propriétés (prolifération cellulaire, immunosuppression, angiogenèse…) exploitables en médecine régénérative.
Dans ce contexte, les CSM, principalement issues du tissu adipeux ou de la moelle osseuse, constituent une perspective intéressante. Différents modèles animaux de discarthrose ont été développés avec des résultats prometteurs sur le ralentissement du processus dégénératif.
Les premiers essais cliniques ont également montré l’intérêt des CSM, autologues ou allogéniques, avec une diminution de la douleur, mais la durée du suivi était généralement limitée et la hauteur du disque n’était pas modifiée (5).
L’essai clinique européen RESPINE, en cours, évaluera l’efficacité à 2 ans des CSM de moelle osseuse allogénique versus une procédure factice. Le projet européen RESPINE, commencé en 2019 devrait apporter la réponse. Il est fondé sur une injection unique, au sein même du disque intravertébral du patient, de cellules souches mésenchymateuses (CSM) provenant de dons de moelle osseuse. Ces CSM sont à même de produire des cellules appartenant au tissu squelettique comme les os et le cartilage, avec l’espoir de restructurer ainsi le disque intervertébral.
112 patients dont plus de 40 Français ont fait l’objet d’un suivi dans neuf centres européens (quatre en France, trois en Espagne, un en Italie et un en Allemagne) en réalisant des imageries par résonance magnétique (IRM) et en répondant à des questionnaires réguliers(Fig. 2). Seules des personnes âgées de moins de 60 ans et présentant une atteinte modérée d’un seul disque sont incluses dans l’essai. Les résultats sont attendus fin 2020.
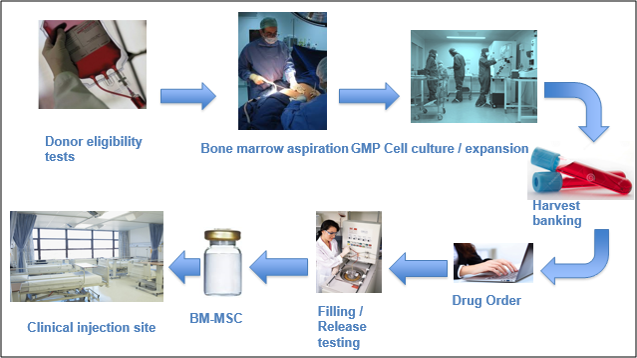
Figure 2 : Le projet RESPINE porte sur le développement d’une thérapie régénérative par injection de cellules souches
- Ingénierie tissulaire discale
L’ingénierie tissulaire peut se définir comme l’ensemble des techniques et des méthodes s’inspirant des principes de l’ingénierie et des sciences de la vie pour développer des substituts biologiques pouvant restaurer, maintenir ou améliorer les fonctions des tissus.
Une des approches actuelles est de préférer utiliser des structures issues de l’ingénierie tissulaire pour cultiver des CSM et les différencier en chondrocytes et les injecter au niveau d’un site lésionnel pour aboutir à une régénération du cartilage. Il ne s’agit pas simplement d’un milieu de culture où se différencie la cellule souche à l’aide de facteurs de croissance mais d’un véritable ensemble contenant la structure en trois dimensions, les cellules, les facteurs de croissance et le milieu de culture.
Plusieurs biomatériaux peuvent être utilisés pour construire l’échafaudage au sein duquel les CSM vont croître et se différencier.Dans l’étude de Sheykhhasan et coll., il s’avère que c’est dans l’échafaudage à base de fibrine que les CSM ont proliféré et se sont différenciées le plus en chondrocytes (6).
Contrairement aux études de thérapie cellulaire, aucun essai clinique chez l’homme n’a actuellement été effectué en ingénierie, néanmoins, une méta analyse récente a permis de comparer l’ensemble de ces études animales. Elle montre une amélioration au cours du temps des signaux IRM, reflétant l’hydratation des DIV traités (7). L’absence de données biomécaniques ne permet cependant pas de conclure quant à l’efficacité de cette stratégie d’ingénierie tissulaire sur l’amélioration de la résistance aux contraintes mécaniques des DIV traités.
Conclusion
L’arthrose lombaire est une maladie de plus en plus présente dans la société. La réduction de la qualité de vie et les douleurs associées à cette pathologie sont des facteurs qui nécessitent une prise en charge adaptée.
La connaissance physiopathologique couplée aux progrès de la biologie des cellules souches offrent des stratégies thérapeutiques pertinentes dans la prise en charge des lombalgiques.
Conflit d’intérêt
Les auteurs ne déclarent aucun conflit d’intérêt
Références bibliographiques
- Anne-Sophie OTTENIN : Thèse : Les lombalgies, rôle du pharmacien d’officine Septembre 2007, Diplôme d’Etat de Docteur en Pharmacie
- Nina Henry, Pauline Colombier, Laurent Lescaudron, Olivier Hamel, Jean Le Bideau, Jérôme Guicheux, Johann Clouet : Médecine régénératrice du disque intervertébral. De la physiopathologie à l’application clinique : médecine/sciences : 2014 ; 30 : 1091-100
- Hohaus C, Ganey TM, Minkus Y, Meisel HJ. Cell transplantation in lumbar spine disc degeneration disease. Eur Spine J 2008 ; 17 Suppl 4 : 492-503
- Chen J, Lee EJ, Jing L, et al. Differentiation of mouse induced pluripotent stem cells (iPSCs) into nucleus pulposus-like cells in vitro. PLoS One 2013 ; 8 : e75548
- Navani A et al. Responsible, Safe, and Effective Use of Biologics in the Management of Low Back Pain: American Society of Interventional Pain Physicians (ASIPP) Guidelines. Pain Physician. 2019 Jan;22(1S):S1-S74.
- Sheykhhasan M, Qomi RT, Kalhor N et al. Evaluation of the ability of natural and synthetic scaffolds in providing an appropriate environment for growth and chondrogenic differentiation of adipose-derived mesenchymal stem cells. Indian J Orthop. 2015;49(5):561-8.
- Mehrkens A, Muller AM, Valderrabano V, et al. Tissue engineering approaches to degenerative disc disease-a meta-analysis of controlled animal trials. Osteoarthritis Cartilage 2012 ; 20 : 1316-25.
.