E. Kerboua, K. Hannachi, Service d’Oncologie médicale, Centre Pierre & Marie Curie, Alger.
Résumé : Le cancer du cavum ou nasopharynx ou encore appelé rhinopharynx représente le premier cancer ORL en Algérie, son incidence chez l’homme selon le Réseau National des Registres du Cancer (RNRC) en 2017 est de 3,4 /100.000 habitants soit 756 nouveaux cas /an, ce qui le place au 7e rang. C’est un cancer chimiosensible et radiocurable mais son traitement reste délicat de par les effets secondaires et les séquelles qu’il engendre. Dans cette question, nous aborderons les actualités dans la classification et dans la prise en charge thérapeutique aussi bien en première ligne qu’en récidive.
Mots-clés : Nasopharynx, actualités, classification, prise en charge thérapeutique.
Abstract: Cavum or nasopharygeal cancer or also called Rhinopharygeal cancer represents the first ORL cancer in Algeria, its incidence in men according to the National Network of Cancer Registries (RNRC) in 2017 is 3.4 / 100,000 in habitants or 756 new cases / year, which places it in 7th place.
It is a chemosensitive and radiation-curable cancer, but its treatment remains difficult due to the side effects and sequelae it causes. In this question, we will address the news in the classification and in the therapeutic management both in the first line and in recurrence.
Key-words: Nasopharygeal cancer, news, classification, therapeutic management.
Introduction
Le cavum constitue la partie supérieure du pharynx. Il mesure chez l’homme adulte : 40 mm de large, 30 à 40 mm de hauteur et 20 mm de grand axe antéropostérieur.
Il est situé sous la base du crâne et il est compris entre les choanes en avant et le rachis cervical haut en arrière. Il est caché à l’observateur par le rideau vélo-palatin. Sa taille et sa forme évoluent avec l’âge. Il est de forme parallélépipèdique.
Sa limite inférieure est constituée par un plan horizontal passant par le palais dur. Il s’ouvre en bas directement dans l’oropharynx. Sa paroi latérale est musculo-aponévrotique. Sa paroi antérieure est constituée par les choanes et la face postérieure du voile du palais. Sa paroi postéro-supérieure présente une formation lymphoïde (végétations adénoïdes).
La muqueuse du cavum est un épithélium de type respiratoire riche en éléments lymphoïdes Il est vascularisé par des branches collatérales de l’artère carotide externe.
Les voies de drainage lymphatiques du cavum sont communes à celles des cavités nasales. Le réseau lymphatique est très riche au niveau du toit et des parois latérales du cavum. En cas de cancer du cavum, le drainage lymphatique se fait vers trois relais principaux (avec possibilité de saut de relais). Le caractère croisé des voies lymphatiques explique la fréquence des adénopathies bilatérales en cas de cancer du cavum.
Épidémiologie
L’épidémiologie est variable selon les pays.
Dans les zones à haut risque, l’incidence annuelle pour 100 000 personnes varie de 30 à 80. Elles concernent l’Asie du Sud-Est : sud de la Chine, population cantonaise, Hong-Kong. Dans ces régions, il s’agit de l’affection maligne la plus fréquente.
Dans les zones à risque intermédiaire, l’incidence annuelle est de 10 pour 100 000 personnes. Elle concerne l’Afrique du Nord et le Moyen Orient, le pourtour méditerranéen, Taiwan, Vietnam, Philippines, Indonésie, Malaisie, Thaïlande / Inuits du Groenland / Eskimos d’Alaska.
Les zones à risque faible ont une incidence annuelle pour 100 000 personnes variant de 0,5 à 2 cas dans les zones à faible endémie, 30 à 80 cas dans les zones à forte endémie. La France appartient à cette classe avec, annuellement, moins d’un cas pour 100 000 habitants
Qui est affecté ?
Le pic se situe vers 40–50 ans, avec une distribution souvent bimodale : 20 – 30 ans et après 50 ans.
L’homme est plus fréquemment touché que la femme (sexe ratio : 2,5 – 3).
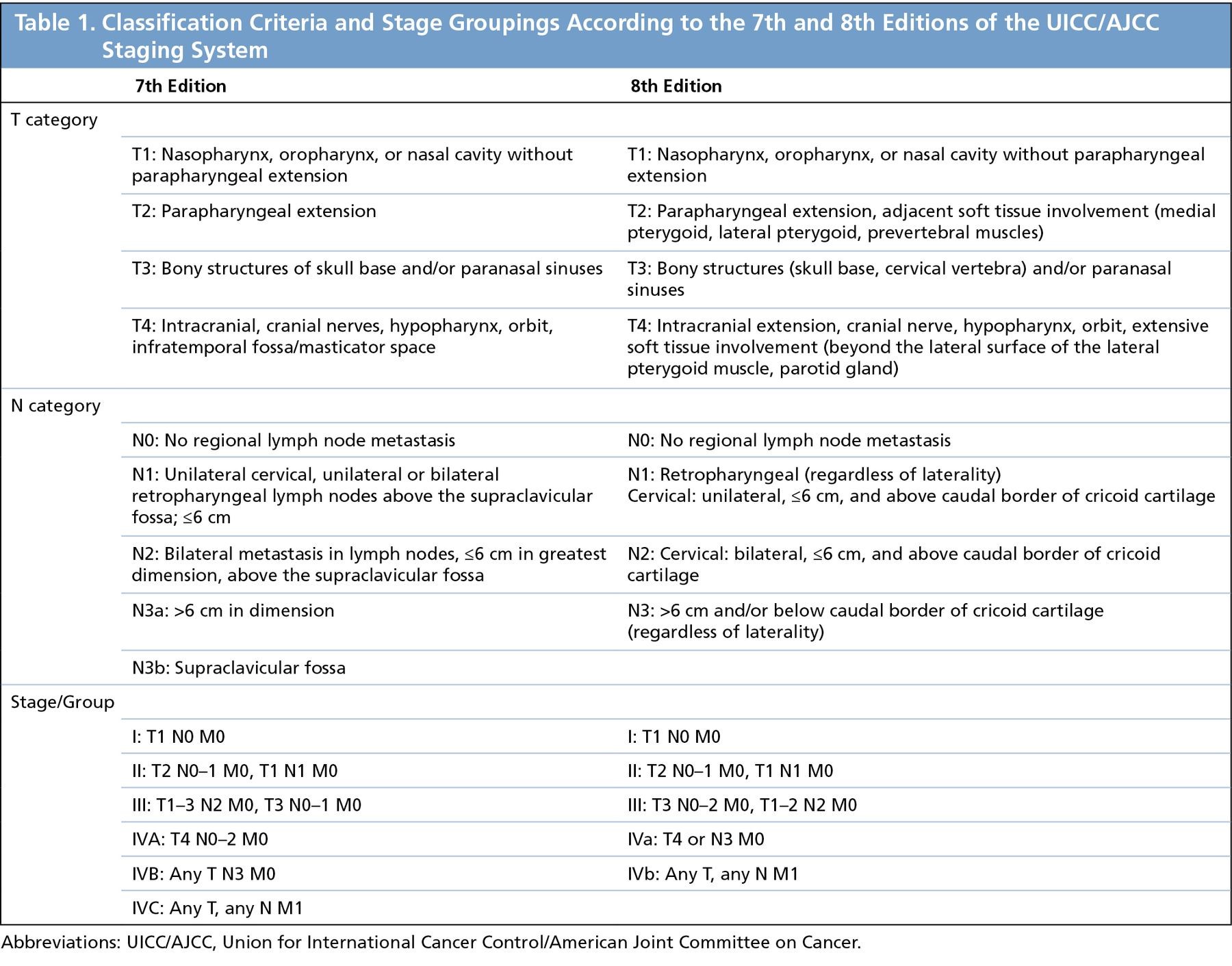
Nouvelle Classification 8e édition :
Le cancer du cavum ou nasopharynx (NPC) est cliniquement stadifié selon la 8e édition de la classification de the American Joint Committee on Cancer (AJCC).
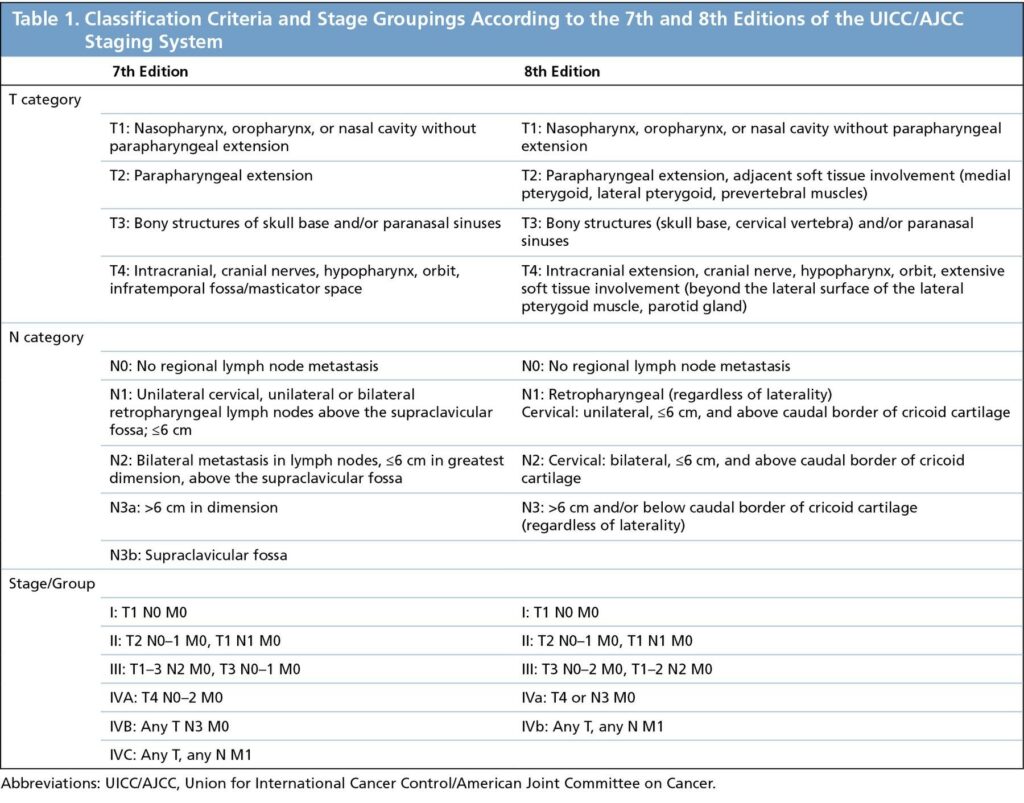
Par rapport à l’édition précédente, la nouvelle classification délimite mieux le stade T2 pour inclure également le muscle prévertébral et l’atteinte ptérygoïdienne médiale ou latérale et le stade T4 inclut désormais la glande parotide et/ou l’infiltration au-delà de la surface latérale du muscle ptérygoïdien latéral, éliminant ainsi une autre terminologie ambiguë. L’extension nodale à la fosse supraclaviculaire a été remplacée par la limite du bord caudal du cartilage cricoïde et délimite ainsi mieux l’extension «bas du cou»; la définition N3 inclut à la fois les groupes N3a et N3b précédents. De plus, les ganglions cervicaux EBV-positifs dans le cancer primitif inconnu sont classés selon la classification NPC.
Tableau 1: Classification Criteria and Stage Groupings According to the 7th and 8th Editions of the UICC/AJCC Staging System
Immunothérapie dans le cancer du nasopharynx :
L’IPILIMUMAB en association avec le NIVOLUMAB est actif dans le carcinome nasopharyngé réccurent et/ou métastatique
Le double blocage de CTLA-4/PD-1 avec l’ipilimumab plus le nivolumab a fourni des réponses durables chez les patients atteints d’un carcinome du nasopharynx récurrent ou métastatique, selon les résultats actualisés d’efficacité et de sécurité d’une étude de phase II présentée au congrès virtuel ESMO Asia 2020, qui s’est tenu du 20 au 22 novembre 2020.
Selon le Dr Hsiang-Fong Kao du Département d’oncologie, National Taiwan University Hospital et National Taiwan University Cancer Center à Taipei, Taiwan, le carcinome nasopharyngé montre une infiltration de cellules T-régulatrices et une expression élevée de PD-L1, mais une monothérapie ciblant PD-1 /PD-L1 a montré une activité limitée. Cette observation a conduit à rechercher si le blocage de CTLA-4 supprimerait la fonction de régulation T et compléterait le blocage de PD-1 dans une étude de phase II sur l’ipilimumab en association avec le nivolumab (NCT03097939).
L’étude dirigée par le Dr Darren Wan-Teck Lim du National Cancer Center de Singapour, a recruté 40 patients, de juillet 2017 à septembre 2019, de Singapour et de Taïwan, atteints d’un carcinome nasopharyngé récurrent/métastatique et d’ADN plasmatique mesurable du virus Epstein Barr. Les patients devaient en outre avoir un indice de performance ECOG de 0 à 1, une fonction organique adéquate et ne pas avoir reçu plus d’une ligne de chimiothérapie antérieure.
Lors du congrès virtuel ESMO Asia 2020, le Dr Kao a présenté les résultats d’une analyse actualisée de l’efficacité et de l’innocuité de cette étude de phase II à un seul bras, Simon en 2 étapes, qui intégrait une expansion pré-planifiée pour l’innocuité et l’efficacité.
Tous les participants à l’étude ont été traités par nivolumab à 3 mg/kg toutes les deux semaines plus ipilimumab à 1 mg/kg toutes les six semaines. Tous les patients recevant au moins une dose de l’association ont été inclus dans l’analyse de l’innocuité et de l’efficacité. La majorité (90,0%) des patients étaient des Chinois avec un âge médian de 53 ans (extrêmes : 23 à 73) et 82,5% des patients étaient des hommes. Une chimiothérapie antérieure avait été administrée à 39 (97,5%) patients.
Le critère principal d’évaluation de l’efficacité était la meilleure réponse globale (BOR) selon RECIST v1.1. La toxicité a été évaluée à l’aide des critères CTCAE.
L’association ipilimumab/nivolumab était sûre chez les patients atteints d’un carcinome du nasopharynx.
À la date limite des données en février 2020, les patients avaient reçu une médiane de 4 cycles de traitement et 6 (15%) patients restaient à l’étude.
Le BOR était une réponse partielle, qui a été obtenue par 14 (35 %) patients (intervalle de confiance à 95% [IC] 20,6 – 51,7%). Les patients répondeurs ont montré une durée médiane de réponse de 5,9 mois (IC à 95 % 3,95 – 8,97).
Avec un suivi médian de 17,3 mois, la survie sans progression (SSP) médiane était de 5,3 mois (IC à 95% 3,0 – 6,4 mois) et la survie globale médiane était de 17,6 mois (IC à 95 % 13,1 – 30,0).
Des événements indésirables liés au traitement (EITR) sont survenus chez 34 (85 %) patients, dont une éruption maculopapuleuse chez 40 % et une hypothyroïdie chez 28 % des patients. Quatre patients (10 %) avaient des EITR graves de grade 3/4, notamment un hypocortisolisme, une pneumonie, une myasthénie grave et une augmentation de la lipase.
Aucune relation n’a été observée entre la réponse et le fardeau des mutations tumorales ou l’expression de PD-1.
Conclusion
Les auteurs précisent qu’il s’agit de la première étude de phase II de cette association dans le carcinome du nasopharynx. Ils ont en outre conclu que le traitement combiné avec nivolumab et ipilimumab était actif sur la base de la démonstration de réponses durables et des données de SSP chez les patients atteints d’un carcinome du nasopharynx.
Les auteurs suggèrent que la combinaison peut fournir une alternative possible à la chimiothérapie de sauvetage et mérite une étude plus approfondie à intégrer dans les futurs essais cliniques et les paradigmes de traitement du carcinome du nasopharynx.
Cette étude a été financée en partie par Bristol-Myers Squibb et ONO Pharmaceuticals.
Le Toripalimab en première ligne dans le carcinome du Nasopharynx avancé
L’ajout du toripalimab à la chimiothérapie standard de première intention gemcitabine plus cisplatine (GP), améliore considérablement les résultats des patients atteints d’un carcinome du nasopharynx récurrent ou métastatique après un traitement à visée curative, suggère une recherche présentée lors de la réunion annuelle 2021 de l’ASCO.
L’inhibiteur de PD-1 a déjà été approuvé en Chine comme traitement de troisième ligne pour cette indication sur la base des résultats de POLARIS-02, a expliqué l’auteur présentateur Rui-hua Xu, du Sun Yat-Sen University Cancer Center à Guangzhou, en Chine.
Il estime que les derniers résultats de phase III de l’essai JUPITER-02, mené en Chine, à Taïwan et à Singapour, indiquent que «le toripalimab en association avec la gemcitabine et le cisplatine pourrait représenter un nouveau standard de soins pour le traitement de première ligne des maladies récurrentes ou métastatiques [carcinome du nasopharynx]».
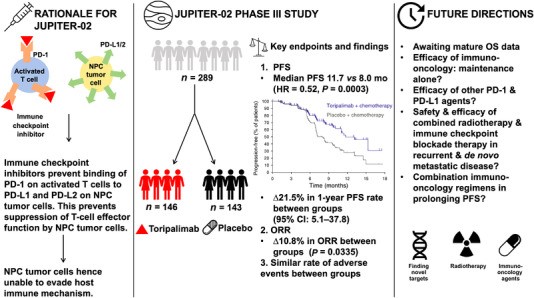
Le critère d’évaluation principal de la survie sans progression (SSP) évaluée en aveugle par un comité d’examen indépendant, était une médiane de 11,7 mois pour les 146 patients randomisés pour recevoir jusqu’à six cycles de toripalimab 240 mg toutes les 3 semaines plus gemcitabine 1000 mg/m2 les jours 1 et 8 et cisplatine 80 mg/m2 le jour 1 de chaque cycle, le toripalimab étant maintenu à la même posologie jusqu’à 2 ans.
Cela se compare à une médiane de 8,0 mois pour les 143 patients ayant reçu un placebo avec une chimiothérapie, ce qui donne un rapport de risque (HR) stratifié significatif de 0,52 pour la progression de la maladie ou le décès en faveur de l’utilisation de l’inhibiteur de PD-1.
Les taux de SSP à 1 an dans les bras combinés et MG uniquement étaient de 49,4 % et 27,9 %, respectivement. L’analyse des sous-groupes a favorisé de manière significative l’utilisation du toripalimab indépendamment du sexe, de l’état de performance ECOG, de l’état de la maladie récurrente ou métastatique, du nombre de copies EBV et de l’expression de PD-L1. Cependant, le bénéfice de la SSP n’a atteint une signification statistique que chez les patients âgés de moins de 50 ans et non chez les participants plus âgés.
Neuf mois après la réalisation de l’analyse intermédiaire de la SSP, la survie globale (SG) médiane n’a pas été atteinte dans les deux bras de traitement, mais le RR stratifié pour le décès était significatif de 0,60 en faveur du toripalimab plus GP par rapport au GP seul.
Les taux de SG à 1 an correspondants étaient de 91,6 % et 87,1 %, avec des taux à 2 ans de 77,8 % et 63,3 %.
Le taux de réponse objective était de 77,4 % avec toripalimab plus GP, avec 19,2 % de patients obtenant une réponse complète et 58,2 % une réponse partielle et 10,3 % de maladie stable, avec une durée médiane de réponse de 10,0 mois. Les valeurs correspondantes pour le médecin généraliste uniquement étaient de 66,4 %, 11,2 %, 55,2 %, 13,3 % et 5,7 mois, respectivement.
Le présentateur a déclaré qu’il n’y avait “aucun nouveau signal de sécurité” identifié pour le traitement combiné. Des événements indésirables (EI) liés au traitement de grade 3 et plus graves sont survenus chez 80,8 % des patients ayant reçu toripalimab plus GP contre 83,2 % de ceux ayant reçu un placebo plus GP, avec des EI liés au système immunitaire de cette gravité signalés chez 7,5 % et 0,7 %, respectivement.
Les EI les plus fréquents de grade 3 et plus graves apparus sous traitement avec l’association toripalimab étaient hématologiques et principalement attribués au schéma thérapeutique du médecin généraliste, a fait remarquer le présentateur, le plus souvent la leucopénie (61,6 contre 58,0 % avec le médecin généraliste uniquement), la neutropénie (57,5 contre 63,6 %), l’anémie (47,3 vs 39,9 %) et la thrombocytopénie (32,9 vs 28,7 %).
Rui-hua Xu a conclu qu’une deuxième analyse intermédiaire de la SG est maintenant prévue et celle-ci sera suivie par les analyses finales pré-spécifiées de la SSP et de la SG pour l’essai JUPITER-02.
Le commentateur de la session Anthony Chan, du Hong Kong Cancer Institute, a noté que les courbes de SSP dans l’étude JUPITER-02 semblent se séparer au moment où la thérapie systémique se termine et où le toripalimab d’entretien ou le placebo est lancé, avec un schéma similaire se produisant dans le système d’exploitation immature courbes.
“La question de savoir si cette amélioration du toripalimab par rapport au placebo peut être obtenue en utilisant une chimiothérapie systémique d’entretien est évidemment une question ouverte”, a-t-il fait remarquer.
Le présentateur a conclu que le cisplatine de première intention plus la gemcitabine “restent la norme de soins” pour cette population de patients jusqu’à ce que les avantages de la SG puissent être démontrés comme “changeant la pratique” par une analyse suffisamment puissante.
Il a ajouté, que le “rôle de la thérapie systémique d’entretien reste à définir” mais qu’il existe un “potentiel énorme” pour les stratégies d’immunothérapie combinées et le séquençage du traitement dirigé par des biomarqueurs dans le carcinome du nasopharynx, avec des études en cours évaluant les inhibiteurs de PD-1 en combinaison avec l’immunothérapie, inhibiteurs de signalisation et conjugués bispécifiques ou anticorps-médicament.
Le PEMBROLIZUMAB ne prolonge pas la SG par rapport à la chimiothérapie dans l’UCNT récurrent et/ou métastatique prétraité au platine.
Selon les résultats de l’étude de phase III multicentrique, ouverte et randomisée KEYNOTE-122 qui a évalué l’efficacité et l’innocuité du pembrolizumab par rapport à la chimiothérapie chez les patients atteints d’un carcinome du nasopharynx prétraité au platine, récidivant ou métastatique, le pembrolizumab n’a pas prolongé la survie globale (OS) sur la chimiothérapie dans cette population. Les résultats ont été présentés par le professeur Anthony TC Chan du département d’oncologie clinique de l’Université chinoise de Hong Kong, Hong Kong PRC lors de la session d’articles sur le cancer de la tête et du cou au congrès ESMO 2021 (16 – 21 septembre).
Le professeur Chan a expliqué que les options de traitement pour le carcinome nasopharyngé récurrent ou métastatique sont limitées. Auparavant, dans l’étude de phase Ib KEYNOTE-028, le pembrolizumab avait montré une activité antitumorale et une sécurité gérable dans une cohorte de 27 patients atteints d’un carcinome nasopharyngé récurrent ou métastatique.
Dans le KEYNOTE-122, les patients atteints d’un carcinome du nasopharynx non kératinisant différencié (classe II de l’OMS) ou indifférencié (classe III de l’OMS), prétraité au platine, positif au virus d’Epstein-Barr, récurrent ou métastatique, histologiquement confirmé, avec un score de performance ECOG de 0-1, et maladie mesurable selon RECIST v1.1 ont été randomisés 1:1 pour recevoir du pembrolizumab toutes les 3 semaines pendant un maximum de 35 cycles ou le choix de l’investigateur de doses standard de chimiothérapie.
Le critère d’évaluation principal de l’étude était la SG. Les critères d’évaluation secondaires comprenaient la survie sans progression (PFS), le taux de réponse objective (ORR) et la durée de la réponse (DoR), tous mesurés selon RECIST v1.1 par un examen central indépendant en aveugle.
Entre le 5 mai 2016 et le 28 mai 2018, 233 patients ont été randomisés dans cette étude, dont 117 au pembrolizumab et 116 à la chimiothérapie. Dans le bras chimiothérapie, 39 patients ont reçu de la capécitabine, 46 patients ont reçu de la gemcitabine et 31 patients ont reçu du docétaxel. Dans le bras pembrolizumab, 74,4 % des patients et 62,9 % des patients du bras chimiothérapie avaient un score positif combiné (CPS) PD-L1 ≥ 1. Le délai médian entre la première dose et la date limite des données (effectuée le 30 novembre 2020) était de 45,1 mois (intervalle, 30,2-54,8).
Dans la population en intention de traiter (ITT), la SG médiane était de 17,2 mois (intervalle de confiance [IC] à 95 % 11,7–22,9) avec le pembrolizumab et de 15,3 mois (IC à 95 % 10,9–18,1) avec la chimiothérapie (risque relatif 0,90 ; 95 % IC 0,67 – 1,19 ; p = 0,2262 ; seuil de signification pour l’analyse finale : 0,0187). Chez les patients avec PD-L1 CPS ≥ 1, la SG était de 17,2 mois dans le groupe pembrolizumab contre 18,0 mois dans le groupe chimiothérapie. Le taux de SG à 24 mois était de 40,2 % avec le pembrolizumab contre 32,2 % avec la chimiothérapie.
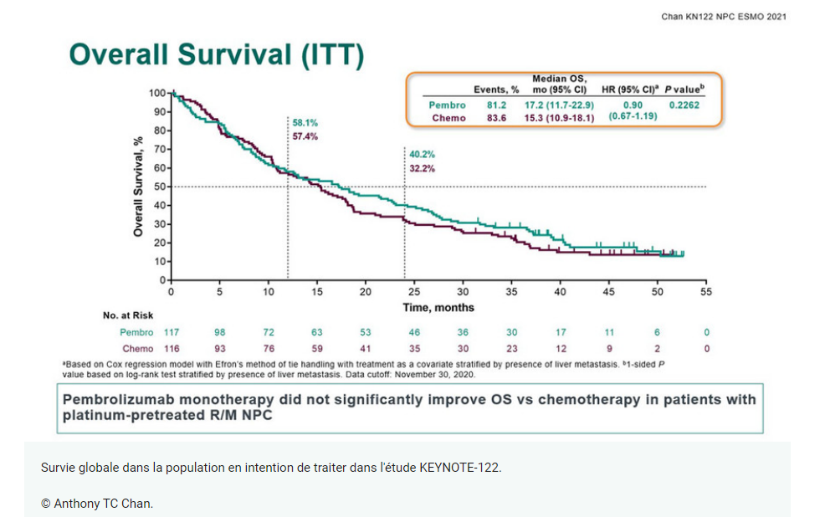
La SSP médiane n’était pas différente entre les deux bras, 4,1 mois avec le pembrolizumab et 5,5. mois avec la chimiothérapie.
Le TRG dans la population ITT était de 21,4 % avec le pembrolizumab et de 23,3 % avec la chimiothérapie et de 23,0 % contre 26,0 % chez les patients avec PD-L1 CPS ≥ 1. Dans la population ITT, le taux de contrôle de la maladie comprenant les patients avec des réponses complètes et partielles, ainsi qu’avec une maladie stable était de 50,4 % chez les patients ayant reçu du pembrolizumab contre 63,8 % chez ceux ayant reçu une chimiothérapie.
La DoR était de 12,0 mois chez les patients traités par pembrolizumab contre 13,1 mois chez ceux traités par chimiothérapie.
Au moment de la rédaction du rapport, les analyses de biomarqueurs étaient en cours.
Le taux d’événements indésirables liés au traitement était de 61,2 % chez les patients traités par pembrolizumab contre 87,5 % chez ceux qui ont reçu une chimiothérapie avec une incidence de grade 3 à 5 de 10,3 % chez ceux traités par pembrolizumab contre 43,8 % chez les patients qui ont reçu une chimiothérapie.
Bien que dans cette étude, le pembrolizumab n’ait pas amélioré la SG par rapport à la chimiothérapie, ni en ITT ni chez les patients avec PD-L1 CPS ≥ 1, il a montré une innocuité gérable et une incidence plus faible d’événements indésirables liés au traitement.
L’étude a été financée par Merck Sharp & Dohme Corp., une filiale de Merck & Co., Inc., Kenilworth, NJ, USA.
Références
- Ferlay J.Ervik M.Lam F.et al. Global Cancer Observatory: Cancer Today. International Agency for Research on Cancer, Lyon, France2018 (Available at:) https://gco.iarc.fr/today
- Amin M.B. Edge S. Greene F.et al. AJCC Cancer Staging Manual. 8th ed. Springer International Publishing, New York2017
- Xu Rh, Mai HQ, Chen QY et al. JUPITER-02 : Étude randomisée, en double aveugle, de phase III sur le toripalimab ou un placebo associé à la gemcitabine et au cisplatine en tant que traitement de première intention du carcinome du nasopharynx (NPC) récidivant ou métastatique . J Clin Oncol 2021 ; 39 (suppl 15; résumé LBA2). DOI : 10.1200/JCO.2021.39.15_suppl.LBA2
- 858O – Chan ATC, Lee VHF, Hong R-L et al. Results of KEYNOTE-122: A phase III study of pembrolizumab (pembro) monotherapy vs chemotherapy (chemo) for platinum-pretreated, recurrent or metastatic (R/M) nasopharyngeal carcinoma (NPC). ESMO Congress 2021 (16 – 21 September).
- 266O – Kao HF, Ang MK, Ng QS, et al. Combinaison Ipilimumab et Nivolumab dans le carcinome nasopharyngé récurrent/métastatique (R/M NPC) – Analyse mise à jour de l’efficacité et de l’innocuité du NCT03097939. Congrès virtuel ESMO Asia 2020 (20 – 22 novembre)
- American Society of Clinical Oncology 2021 Annual Meeting: Abstract LBA2. Présenté le 6 juin 2021.