Initialement développés dans le domaine des maladies chroniques, les soins de supports méritent d’être soigneusement étudiés dans leur concept et leurs principes afin d’en envisager la pertinence pour les patientes atteintes d’un cancer du sein, dans le but de maintenir, voire d’améliorer la qualité de vie
Ould Hadj, E. Kerboua, K. Bouzid, Service d’Oncologie Médicale, Centre Pierre et Marie Curie, Alger.
Date de soumission : 27 Août 2019.
Résumé : L’augmentation de la durée de vie des patientes atteintes de cancer du sein contribue progressivement à donner à cette pathologie les caractéristiques d’une maladie chronique comme le diabète et l’asthme et autres qui bénéficient déjà d’une éducation thérapeutique bien codifiée pour le patient, qui lui permettent d’acquérir et de conserver les capacités et compétences pour la prise en charge active de sa maladie. Dans le cadre du cancer du sein, les équipes soignantes qui accompagnent ces patientes assurent déjà une éducation thérapeutique partielle et non formalisée en particulier dans le dispositif autour de l’annonce mais en raison de la spécificité du cancer du sein qui atteint la femme au plus profond de sa féminité, le terme soins de support nous paraît plus adapté dans cette situation que celui d’éducation thérapeutique. Les soins de support sont donc l’ensemble de soins et soutiens nécessaires tout au long de la maladie conjointement aux traitements anti cancéreux spécifiques qui ont pour principal but l’amélioration de la qualité de vie.
Mots clés : Cancer du sein, éducation thérapeutique, soins de supports, chimiothérapie, effets secondaires, qualité de vie.
Abstract: The increase of life expectancy in breast cancer patients has progressively led us to see this pathology as a chronic disorder. We have studied the usefulness of therapeutic patient education with respect to this pathology in the light of what is already an established practice in the case of diabetes and asthma. In breast cancer, from diagnosis through to post-treatment follow-up visits, we offer several approaches to therapeutic education. The physicians and the support team who accompany these patients already supply partial and informal therapeutic education particularly at the moment of diagnosis disclosure. A greater awareness of this situation and specific training would enable healthcare providers to improve their approach and efficacy. Given the specificity of breast cancer, affecting as it does a woman at the very core of her femininity, we would prefer to use the expression “therapeutic accompaniment” rather than “therapeutic education.
Keywords: Therapeutic education, breast cancer, supportive care, chemotherapy, side effects, therapeutic accompaniment, quality of life.
Introduction
Initialement développés dans le domaine des maladies chroniques, les soins de supports méritent d’être soigneusement étudiés dans leur concept et leurs principes afin d’en envisager la pertinence pour les patientes atteintes d’un cancer du sein, dans le but de maintenir, voire d’améliorer la qualité de vie. L’augmentation de la durée de vie des patientes atteintes d’un cancer du sein contribue progressivement à donner à cette pathologie les caractéristiques d’une maladie chronique qui pourrait de ce fait être concernée par ce type de soins. Beaucoup d’enquêtes d’opinion réalisées partout dans le monde, s’intéressant au vécu des femmes souffrant de cancer du sein ont mis en évidence l’importance et l’utilité pour ces patientes des informations données à l’annonce du diagnostic et au moment des traitements ; et l’intérêts de la bonne gestion des effets secondaires du traitement spécifique tel que la chimiothérapie tant sur les plans physique que moral et psychique .
Le cancer du sein est le cancer le plus fréquent chez la femme. Le taux de survie se situe à environ 87%, cela permet de classer le cancer du sein comme un cancer de bon pronostic. Cependant, le cancer du sein reste la première cause de décès par cancer chez la femme et il demeure un enjeu majeur de santé publique. La prise de conscience de cet enjeu majeur a été à l’origine de la mise en place de nouvelle vision de l’organisation des soins en cancérologie avec le développement des soins de support. Ils doivent permettre d’apporter un accompagnement global des patientes et d’améliorer leur qualité de vie. De plus, ils vont permettre de mieux appréhender certains aspects de la maladie dès l’annonce de celle-ci. Le traitement du cancer provoque différents effets indésirables, variables selon les thérapeutiques utilisées et selon les individus. Les soins de support sont également un moyen important de réduire ces effets indésirables.
Définitions des soins de support
Les soins de support ont été définis comme « l’ensemble des soins et soutiens nécessaires aux personnes malades tout au long de la maladie conjointement aux traitements onco-hématologiques spécifiques, lorsqu’il y en a ». Cette notion de soins de support est inspirée du terme anglo-saxon « supportive care » donnée en 1990 par la MASCC (Multinational Association for Supportive Care in Cancer) et définie comme « l’ensemble des aides médicales, soins infirmiers et psychosociaux dont le patient a besoin, en plus du traitement spécifique contre le cancer ».
Les soins de support correspondent donc à une approche globale du patient, afin d’améliorer sa qualité de vie physique, psychologique et sociale tout au long de la maladie ainsi qu’à l’aider à mieux supporter les effets indésirables des traitements et les conséquences de la maladie.
Ces soins s’adressent aux patients malades ainsi qu’à leur entourage dès le diagnostic de la maladie, pendant et après le traitement. Les soins de supports s’inscrivent dans une continuité et une globalité des soins.
Cancer et féminité, apport des soins de supports
Le cancer du sein touche à l’image de la femme ainsi qu’à sa féminité. Il bouleverse à la fois le corps et l’esprit. Les étapes de la maladie ont un impact sur la féminité de chaque patiente de façons différentes. Le sein est un organe riche symboliquement dans notre société, il représente la féminité de par son image érotique et la maternité de par son image du sein nourricier de la mère. En effet, depuis des siècles le sein est représenté de diverses manières dans l’art, lui donnant une représentation et une symbolique propre à chaque pays et à chaque culture. Dans la mythologie grecque la déesse Artémis d’Ephèse est une des déesses de la fertilité, pour cela elle a été représentée avec une multitude de seins. Ces seins seraient engorgés de lait divin pouvant ainsi nourrir l’humanité entière. Par la présence de ces nombreux seins apparents, la déesse apparait comme la mère nourricière, elle représente la fertilité et la maternité.
Lors d’un cancer du sein, la féminité peut être malmenée de différentes façons selon les traitements qui entrainent une modification anatomique, physiologique ou fonctionnelle. Ces modifications du corps sont des conséquences principalement de la chirurgie notamment la mastectomie, de la chimiothérapie induisant une alopécie, et des traitements hormonaux pouvant provoquer une prise de poids. La féminité est définie par l’encyclopédie du Larousse comme « un caractère particulier, distinctif de la femme ». Le cancer du sein peut affecter l’estime de soi et l’image corporelle. La notion d’image corporelle a été introduite et définie en 1935 comme « la représentation à la fois consciente et inconsciente du corps, désignant non seulement une connaissance physiologique mais renvoyant également à la notion de libido et à la signification sociale du corps ». De plus, « l’image du corps humain, c’est l’image de notre propre corps que nous formons dans notre esprit, autrement dit, la façon dont notre corps nous apparaît à nous-mêmes ». L’image de soi correspond à la façon dont on se voit, ce que l’on ressent face à soi-même tandis que l’image corporelle correspond à la façon dont le corps est perçu. Ces deux notions sont intriquées.
Dans la société actuelle, le paraître occupe une place importante, plus importante que l’être, induisant des troubles psychologiques lorsque la maladie peut toucher l’apparence corporelle. La perte d’intégrité corporelle est donc redoutée par le patient.
En oncologie, l’incidence des traitements sur l’image du corps constitue de plus en plus un enjeu dans la prise en charge globale. En effet, il a été admis que l’image corporelle participe à des facteurs associés à l’ajustement de la qualité de vie et de l’équilibre psychologique.
Il a été estimé qu’un syndrome dépressif post mastectomie se déclarait dans 14 à 25% des cas. L’effondrement des repères d’identification explique ce syndrome dépressif post mastectomie. Des études ont essayé de mettre en évidence un lien entre l’image du corps et la survie et bien que le lien entre l’image du corps et la survie n’ait pu être démontré, les soins de support en oncologie afin d’améliorer l’image de soi, l’estime de soi et la qualité de vie des patients se sont développés.
Atteinte des phanères
Les phanères correspondent à un organe de protection caractérisé par une kératinisation intense, cela inclut donc les cheveux, les poils et les ongles. Les différents traitements vont entraîner des effets secondaires au niveau des phanères.
- Alopécie
La perte des cheveux, ou alopécie, est l’un des effets secondaires les plus redoutés. En effet, elle a un impact important sur l’image de soi, cela renvoie à une image négative avec une dégradation de l’image corporelle. L’alopécie expose au regard des autres, la maladie est un rappel constant de celle-ci. De plus, cela touche la femme dans sa féminité. Toutes les chimiothérapies n’induisent pas le même risque alopéciant, on distingue trois catégories :
- Peu ou pas alopéciants : le 5-fluoro uracile, le cisplatine, la gemcitabine et la bléomycine.
- Fortement alopéciants : le méthotrexate, la vincristine, la vinblastine, la mitomycine et la mitoxantrone.
- Très fortement alopéciants : le cyclophosphamide, la doxorubicine, le paclitaxel et le docetaxel.
L’alopécie peut apparaître entre dix à vingt jours après le début de la chimiothérapie. Elle est très souvent réversible à l’arrêt du traitement ; une alopécie irréversible reste exceptionnelle. La repousse débute environ entre quatre et six semaines après l’arrêt de la chimiothérapie, dans certains cas la repousse des cheveux peut commencer avant la fin de la chimiothérapie. Elle est progressive et est estimée à un centimètre par mois environ. Lors de la repousse des cheveux, il peut y avoir une modification de la couleur et de la texture par rapport aux cheveux d’origine. Il a été montré que l’alopécie chimio-induite serait due à l’activation des mécanismes de l’apoptose au niveau du follicule pileux. De plus, on note une régression des glandes sébacées. L’alopécie n’étant pas un effet indésirable grave sur le plan médical, sa prise en charge a longtemps été délaissée. Or, il est bien reconnu de nos jours que l’impact de l’alopécie peut avoir un fort retentissement psychologique chez les patients entrainant une diminution de l’adhésion aux traitements. Néanmoins, il n’existe pas de traitement médicamenteux afin de prévenir cette alopécie. Afin de mieux affronter l’étape de la chute des cheveux, il est conseillé aux patientes de couper de façon courte les cheveux avant la chute. Cela permet aux patientes d’être dans une stratégie active plutôt que passive et il est plus facile de perdre des cheveux courts que des cheveux longs.
Quelques conseils peuvent être donnés à la patiente. Par exemple, avant la chute des cheveux il est conseillé d’éviter de se brosser les cheveux le jour de la cure. Pendant les huit jours qui la suivent, il est préférable de laver les cheveux avec une faible quantité de shampooing doux à l’eau tiède, de laisser les cheveux sécher à l’air libre, ainsi qu’utiliser une brosse à poils souples ou un peigne à larges dents. Il est préconisé également d’éviter les teintures, les brushings mais aussi les permanentes entre les cures. Lorsque la chute des cheveux s’est produite, il est important que la patiente hydrate son cuir chevelu afin d’éviter la desquamation.
- Ongles
Les molécules utilisées en chimiothérapie touchent tous les phanères cela inclut donc les ongles. Différentes pathologies peuvent être induites, la toxicité unguéale est transitoire, elle peut persister jusqu’à six mois après les traitements pour les doigts de la main et jusqu’à dix-huit mois pour les orteils. Elle peut également toucher les ongles des pieds et des mains de façons isolées ou globales. Tous les agents cytotoxiques ne provoquent pas de toxicités unguéales. Les anthracyclines et les taxanes peuvent provoquer de forts désordres unguéaux. Il n’existe pas de traitement préventif. Des gants ou des chaussettes réfrigérées peuvent être utilisés, cela permettrait de diminuer le nombre de pathologies unguéales. L’utilisation de vernis peut être conseillée afin d’apporter une protection au niveau des ongles. Il est conseillé de poser deux couches de vernis au silicium, puis deux couches de vernis foncés non nacré afin d’éviter la photosensibilisation et de fortifier l’ongle. Cependant, il n’a pas été prouvé que l’utilisation de ces vernis puisse avoir un effet préventif dans l’apparition de toxicité unguéale. Dans certains cas, il peut être utile de masser la racine de l’ongle avec des crèmes émollientes ou des pommades à la vitamine A. Il est conseillé aux patientes de ne pas retirer les cuticules, de ne pas curer les ongles afin d’éviter de les soulever et de les faire tomber. De plus, il est également recommandé de couper à ras les ongles décollés pour soulager la douleur. Enfin, il est plus prudent d’utiliser des gants doublés de coton pour les travaux ménagers ou de jardinage.
Le syndrome main-pied
Le syndrome main pied correspond à une réaction inflammatoire due à certains traitements de chimiothérapie. Il est caractérisé par l’apparition de rougeurs pouvant aller jusqu’à une hyperpigmentation, pouvant être accompagnées de fourmillements et de gonflements. En général, cela apparait deux à douze jours après l’administration des cytotoxiques. Son mécanisme physiopathologique reste méconnu. On note des formes hyperkératosiques avec les thérapies ciblées anti-angiogéniques. La gravité de ce syndrome varie selon les doses prescrites, les produits administrés, les associations faites, ainsi que la durée du traitement. Le syndrome main-pied est réversible et les symptômes diminuent progressivement à l’arrêt du traitement.
Il n’existe pas d’étude actuellement sur l’efficacité de traitements dans la prise en charge du syndrome main-pied. Le port de gants réfrigérants peut être recommandé, notamment s’il s’agit de perfusions courtes. Des packs réfrigérants peuvent être positionnés au niveau du poignet ou des chevilles. Le froid va induire une vasoconstriction locale permettant de diminuer la diffusion des drogues cytotoxiques localement. Il est important d’hydrater la peau dès le début du traitement et cela plusieurs fois par jour, des crèmes émollientes pourront être utilisées. Des crèmes à base d’urée pourront être utilisées mais à une concentration ne dépassant pas 10% afin de produire simplement un effet hydratant. En effet, l’urée est un facteur naturel d’hydratation, elle est hygroscopique, absorbe l’humidité et la conserve dans la couche cornée afin de réguler l’hydratation cutanée.
En cas de présence de corne avant le traitement, il est conseillé de faire une pédicure.
Certaines mesures préventives peuvent être préconisées :
- Porter des chaussures larges, souples et bien ajustées,
- Éviter les sources de chaleur,
- Privilégier les douches courtes et pas trop chaudes.
Modification du poids
- Prise de poids
La prise de poids est un effet indésirable des traitements adjuvants. Les mécanismes ne sont pas encore totalement élucidés, plusieurs facteurs en seraient à l’origine : l’hormonothérapie, la chimiothérapie, la corticothérapie associée, ainsi que l’aménorrhée induite par la chimiothérapie chez les femmes non ménopausées.
La moitié des patientes sont affectées par une prise de poids, elle est en général de l’ordre de 3 kg, mais dans certains cas la prise de poids peut être plus importante et être de l’ordre de 10 kg. Dans un rapport établi par des experts du World Cancer Research Fund, il a été mentionné que l’activité physique et les mesures pouvant être prises pour lutter contre le surpoids amélioreraient l’état de santé et de bien-être des patients et réduiraient le risque de récidive dans le cas du cancer du sein. Ces variations de poids doivent être suivies de près par l’équipe médicale. En effet, elles sont un facteur de mauvais pronostic. Une étude a mis en évidence que 30 à 40% des femmes subissant une variation de poids supérieure à 5% du poids initial, ont présenté des rechutes ou sont décédées. Les causes et les mécanismes de ces variations de poids ne sont pas élucidés actuellement. Une étude a suggéré que la chimiothérapie induit une dérégulation des peptides alimentaires comme le peptide Y. Le peptide Y est sécrété en postprandial à partir des cellules endocrines L du tube digestif afin d’exercer un rôle anorexigène. Au cours de la chimiothérapie, les patients ayant un poids stable ou ayant perdu du poids ont eu une augmentation de 30% de ce peptide tandis que chez les patients ayant pris du poids une légère diminution de 7% de ce peptide a été notée.
D’autres hypothèses ont été émises afin d’identifier les facteurs agissant sur la variation de poids. Lors de la prise de poids sous chimiothérapie, on note une augmentation de la masse grasse avec une stabilité voire une diminution de la masse maigre. La masse grasse aurait une localisation préférentielle au niveau abdominal. De plus, il pourrait y avoir une diminution de la masse musculaire. Les différents mécanismes susceptibles d’expliquer la relation entre l’augmentation de la masse grasse et le risque de rechute et de mortalité seraient une augmentation de la production d’œstrogènes, des cytokines et de la leptine, avec parallèlement une diminution de la production d’adiponectine et l’apparition d’une insulinorésistance.
En ce qui concerne l’augmentation de la synthèse des œstrogènes, elle serait due à l’augmentation de la masse adipeuse qui provoquerait l’aromatisation des androgènes surrénaliens, et ainsi augmenterait le taux d’œstrogènes libres circulant, provoquant la stimulation de la croissance tumorale. L’insulinorésistance est due notamment à la masse adipeuse, à l’augmentation des cytokines (IL-6 et TNF-α). Cette insulinorésistance provoque une augmentation du taux d’insuline qui entraîne la stimulation de la synthèse d’IGF-1. Ce facteur de croissance a un effet positif sur la croissance de la tumeur. De plus, les cytokines jouent également un rôle dans la stimulation de la production d’œstrogènes et dans la croissance tumorale par une action mitogénique et anti-apoptique. La leptine qui est une hormone du tissu adipeux est davantage sécrétée lors de l’augmentation du tissu adipeux. Cette hormone est impliquée dans la croissance tumorale par la surexpression de ses récepteurs au niveau du tissu cancéreux mammaire.
- Perte de poids :
La chimiothérapie peut entrainer une modification du goût et de l’odorat, une sécheresse buccale, des nausées et des troubles du transit conduisant à une perte d’appétit. Cela peut causer une diminution du poids. Un suivi par un diététicien peut être indiqué. Ce dernier, veille à adapter l’alimentation du patient en fonction de ses difficultés et de ses besoins. Des compléments nutritionnels oraux peuvent être proposés et prescrits par le médecin. Il s’agit de produits riches en calories et/ou protéines. Ils se présentent sous la forme de boissons lactées, de crèmes, de jus de fruits, de potages ou de plats mixés.
En oncologie, la perte de poids est un facteur de mauvais pronostic en ce qui concerne la survie globale, la survie sans récidive ainsi que la qualité de vie. De plus, elle est un marqueur de complications. En chirurgie, lorsque la diminution de poids est de plus de 10%, le risque de complications postopératoires est augmenté. En oncologie médicale, une perte de poids de 5% augmente le risque de toxicité de la chimiothérapie et de la radiothérapie. [94]
L’évaluation nutritionnelle du patient ne doit pas tenir compte que de l’IMC, qui n’est pas assez spécifique. La réduction des ingesta et une hypoalbuminémie sont des facteurs de mauvais pronostic.
Les troubles digestifs :
- Les nausées et vomissements :
Les nausées et les vomissements font partie des effets indésirables les plus redoutés par les patients qui débutent un traitement par chimiothérapie anticancéreuse. On estime que jusqu’à 80% des patients cancéreux traités souffriront de nausées pendant leur chimiothérapie. Les nausées et vomissements chimio-induits ont un impact majeur sur la qualité de vie des patients, sur leurs activités quotidiennes, professionnelles et sur leur vie sociale.
Le réflexe de vomissement est un mécanisme complexe de protection de l’organisme. Le centre du vomissement peut être stimulé de deux façons : soit de manière périphérique par des neurones vagaux abdominaux, soit de manière centrale au niveau de la zone du déclencheur du chimiorécepteur. Dans le cas de la chimiothérapie, les agents anti-tumoraux vont stimuler la libération de médiateurs notamment la sérotonine au niveau des cellules entérochromaffines de l’intestin grêle supérieur. Ces médiateurs vont se lier à leurs récepteurs respectifs au niveau des terminaisons digestives du nerf vagal pour stimuler et activer le CPG. De plus, d’autres neuromédiateurs interviennent également. La dopamine va ainsi avoir un rôle majeur dans ce phénomène. Récemment, l’implication de la neurokinine de type 1 a été identifiée, elle semble également jouer un rôle majeur au contraire de l’histamine et de l’acétylcholine dont l’importance est finalement moindre. Cependant, on ne connaît pas encore tous les mécanismes précis par lesquels la chimiothérapie induit des nausées et des vomissements.
L’arsenal thérapeutique permet d’agir au niveau des différents récepteurs des neurotransmetteurs mis en évidence dans le mécanisme. Ces quinze dernières années, le traitement des nausées et vomissements chimio-induits a beaucoup évolué. On retrouve les antagonistes dopaminergiques, les antagonistes des récepteurs à la sérotonine de type 3 ou sétrons, les antagonistes des récepteurs aux neurokinines de type 1 et les corticoïdes.
On distingue les vomissements dits aigus lorsqu’ils surviennent dans les vingt-quatre heures et les vomissements dits retardés qui apparaissent jusqu’à sept jours après la fin de la chimiothérapie. De plus, il existe des vomissements dits anticipatoires qui surviennent deux à trois jours avant la chimiothérapie ; ils sont d’origine psychologique et sont dus à une mauvaise expérience ou à un souvenir d’une chimiothérapie précédente. Cependant, le risque émétique dépend aussi de la dose administrée, du mode d’administration ainsi que des associations faites entre les différents agents anti-tumoraux. Des facteurs intrinsèques au patient doivent être pris en compte tels que l’âge, le sexe, l’alcoolisme chronique, les antécédents de vomissements (grossesse, mal des transports, etc.), sujet anxieux. En plus de l’arsenal thérapeutique, les thérapies complémentaires peuvent être utilisées.
- Les mucites :
La mucite est un effet secondaire aigu fréquent des thérapies anticancéreuses (radiothérapie, chimiothérapie). Elle peut apparaître jusqu’à quatorze jours après la cure de chimiothérapie et peut durer quelques semaines. La mucite correspond à une inflammation de la muqueuse qui recouvre l’intérieur des cavités et des viscères. Cela peut atteindre tout type de muqueuses, qu’elles soient buccales, digestives, vaginales ou oculaires. Lorsque c’est la muqueuse buccale qui est touchée, on parle de stomatite. Ces mucites buccales peuvent être classées selon différents grades.
Syndrome climatérique
Les bouffées de chaleur peuvent être dues à la ménopause soit naturelle soit induite par la chimiothérapie mais elles peuvent aussi être induites par les traitements hormonaux adjuvants (anti-aromatases et tamoxifène).
Les bouffées de chaleur chez les femmes ayant un cancer du sein posent un problème particulier du fait de leur fréquence, de leur sévérité et de la difficulté de leur prise en charge. Une étude a rapporté que chez les patientes atteintes de cancer du sein 65% d’entre-elles manifestent des bouffées de chaleur pendant ou après le traitement et que 64 à 82% d’entre elles les qualifient de modérées à sévères. De plus, leur prise en charge est difficile étant donné que le traitement hormonal substitutif est contre-indiqué dans le cas d’un cancer du sein ou d’antécédent de celui-ci. Certains médicaments sont utilisés hors AMM pour traiter ces bouffées de chaleurs telles que la venlafaxine, la clonidine ou bien la gabapentine. Les bouffées de chaleur ont un retentissement sur la qualité de vie des patientes. Il est important qu’elles soient prises en charge afin d’obtenir une meilleure qualité de vie, et donc une meilleure chance de guérison. Cette prise en charge permet également de favoriser une bonne observance du traitement notamment des traitements hormonaux adjuvants. En effet, les effets indésirables des anti-aromatases et des anti-œstrogènes aboutissent à une mauvaise observance du traitement voire un abandon de celui-ci.
Asthénie
L’asthénie est un symptôme fréquent chez les personnes atteintes d’un cancer, elle peut apparaitre à différents stades de la maladie, même après la guérison. De plus, tout le monde n’est pas touché de la même façon. L’asthénie concerne environ 80% des patients en cancérologie. Elle est souvent multifactorielle, en effet, elle peut être due à de nombreux facteurs physiques, émotionnels, cognitifs et comportementaux tels que la maladie elle-même, les différents traitements et leurs effets secondaires, le stress et la douleur. Le médecin devra d’abord rechercher les causes corrigeables telles que l’anémie et la douleur afin d’adapter le traitement. Les conséquences de l’asthénie sont considérables puisqu’elle engendre une diminution générale de la qualité de vie.
Une fois ces causes corrigeables éliminées, l’asthénie peut être prise en charge via des techniques complémentaires.
Cancer du sein et sexualité
Il a été estimé qu’environ la moitié des patientes ayant un cancer du sein souffre de difficultés sexuelles. Les causes sont multiples. Elles peuvent être physiques ; on retrouve la fatigue, la douleur, ou liées à d’autres effets indésirables du traitement. Elles peuvent être psychologiques avec une modification de l’image corporelle et de l’estime de soi, un syndrome anxio-dépressif ou une peur de l’éloignement du partenaire. Certains traitements de chimiothérapie et d’hormonothérapie perturbent l’équilibre hormonal et ont un impact sur la libido. La chirurgie, elle aussi, exerce une influence sur les troubles sexuels. Même si le couple est très largement préservé durant cette épreuve, il n’en est pas de même concernant la sexualité.
La sexualité après une mastectomie
La chirurgie a un impact sur la sexualité. La nouvelle image du corps peut entraîner un sentiment de dévalorisation et ainsi perturber l’intimité de la patiente. Différents travaux ont mis en évidence que la chirurgie reconstructrice ou la mastectomie partielle entraîne moins de troubles sexuels que la mastectomie totale sans reconstruction. Cependant, lorsque le traitement conservateur est de mauvaise qualité esthétique cela peut conduire à des réactions dépressives plus importantes. La mastectomie a des répercussions à différents niveaux. On observe une réaction dépressive et/ou anxieuse ainsi qu’une diminution de l’estime de soi. La chirurgie a un impact sur l’image corporelle, elle peut donner à la patiente le sentiment d’être moins désirable, de déformation de son corps et une diminution de son intégrité. Ces répercussions sont d’autant plus fortes que la patiente est jeune, cela dépend également du statut socio familial et des difficultés sexuelles préexistantes.
Les difficultés au niveau de la vie sexuelle ne sont pas toujours évoquées avec le médecin, en effet ; beaucoup de femmes n’osent pas aborder le sujet et les médecins et l’équipe soignante ont également des difficultés à l’évoquer. La psycho-oncologie peut aider les patientes à surmonter cette difficulté.
Conclusion
La prise en charge du cancer du sein a évolué aux cours de ces dernières années, les soins de support sont intégrés au parcours de soins des patients atteints de cancer en général et des femmes atteintes de cancer du sein en particulier.
Les différents traitements, la chirurgie, la radiothérapie et la chimiothérapie perturbent l’image corporelle de la femme, impliquant un bouleversement dans la féminité de la patiente et résultant en un impact psychologique négatif. C’est dans ce contexte que les soins de support vont pouvoir améliorer le quotidien des patientes et permettre une meilleure adhésion au traitement. Ceci s’inscrit dans une volonté d’améliorer la qualité de vie des patientes et d’humaniser les soins. Le renforcement des soins de support permet de limiter l’impact personnel et social.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts en relation avec cet article.
Références
- Trétarre B., Guizard A.V., Fontaine D. et al. Cancer du sein chez la femme : incidence et mortalité, France 2000. BEH 2004 ; 44 ; 209-210.
- Inserm, expertise collective. Cancer et environnement. Inserm 2008 ; 889 pages
- Espié M. Prise en charge du cancer. Journal de radiologie diagnostique et interventionnelle 2014 ; 95 ; 740-744.
- De Angelis R., Sant M., Coleman M. et al. Cancer survival in Europe 1999–2007 by country and age: results of EUROCARE-5—a population-based study. Lancet Oncol 2013 ; 15 (1) ; 23-34
- Mignotte H. Maladies du sein (3ème édition) 2011. Ed Elsevier Masson.198 pages
- Roché H. Cancers du sein : évolution des grands concepts thérapeutiques. Bull Cancer. 2013 ; 100 ; 857-63.
- Frénel J.S., Campone M. Chimiothérapie des cancers du sein non métastatiques : état des lieux en 2010. Journal de gynécologie obstétrique et biologie de la reproduction 2010 ; 39S ; F79-F84.
- Molnar-Stanciu D., Guimas V., Bensalem A. et al. Thérapie ciblée et cancer du sein : état de l’art. Pathologie biologique. 2012 ; 60 ; 254-263.
- Beuzeboc B. Indications de l’Herceptin dans le traitement du cancer du sein. Gynécologie obstétrique et fertilité. 2004 ; 32 ; 164-172.
- Debled M., Dalenc F., Mauriac L. et al. Traitements médicaux des cancers du sein RH+ Her2 -. Bulletin du Cancer. 2011 ; 98 (6) ; 655-670. 110
- Krakowski I., Boureau F., Bugat R. et al. Pour une coordination des soins de support pour les personnes atteintes de maladies graves : proposition d’organisation dans les établissements de soins publics et privés. 2004 ; 6 ; 7-15.
- Agence Française des soins oncologiques de support; http://www.afsos.org/IMG/pdf/THERAPIES_COMP_J2R_2012_12_07.pdf consulté en février 2015
- Tagliaferri M., Cohen I., Tripathy D. et al. Complementary and alternative medicine in early stage breast cancer. Semin Oncol. 2001 ; 28 ; 121-134
- Guiraud G.G., Le recours aux médecines parallèles. Presse Méd. 2003 ; 32 ; 1638-1641
- Trager-Maury S., Tournigand C., Maindrault-Goebel F. et al. Use of complementary medicine by cancer patients in a French oncology department. Bull Cancer. 2007; 94(5); 1017-1025
- George B., Delfieu D. Les principaux syndromes douloureux liés au cancer. Oncologie. 2008; 10; 591-597
- Lakdja F., Dixmerias F., Labreze L. et al. ATS7-1 Douleurs et cancers : Actualités 2007. Douleurs
- Boiron M., Roux F., Wagner J.P. Accompagnement en oncologie. Newsmed, Courbevoie 2014. 165 pages.
- Ezzo J., Vickers A., Richardson M.A. et al. Acupuncture-point stimulation for chemotherapy-induced nausea and vomiting; J ClinOncol.2005; 23(28); 7188–7199 112
- Ryan J.L., Heckler C.E., Roscoe J.A. et al. Ginger (Zingiberofficinale) reduces acute chemotherapy-induced nausea: A URCC CCOP study of 576 patients. Support Care Cancer. 2012; 20(7); 1479-89
- Pérol D., Provençal J., Hardy-Bessard A.C. et al. Can treatment with Cocculine improve the control of chemotherapy-induced emesis in early breast cancer patients? A randomized, multi-cantered, double-blind, placebo-controlled Phase III trial. BMC Cancer. 2012; 12(1) ; 603.
- Mustian K.M., Palesh O., Sprod L. et al. Effect of YOCAS yoga on sleep, fatigue, and quality of life: a URCC CCOP randomized controlled clinical trial among 410 cancer survivors. J ClinOncol. 2010 ;28(15); supplement 9013.
- Boehm K., Cramer H., Staroszynski T. et al. Arts therapies for anxiety, depression, and quality of life in breast cancer patients: a systematic review and meta-analysis. Evid Based Complement Alternat Med 2014.
- Puetz T.W., Morley C.A., Herring M.P. Effects of creative arts therapies on psychological symptoms and quality of life in patients with cancer. JAMA Intern Med. 2013 ; 173(11); 960-969.
- Bradt J., Dileo C., Grocke D. et al. Music interventions for improving psychological and physical outcomes in cancer patients. Cochrane Database of systematic reviews 2011. Issue 8.
- Lang E.V., Berbaum K.S., Faintuch S. et al. Adjunctive self-hypnotic relaxation for outpatient medical procedures: a prospective randomized trial with women undergoing large core breast biopsy. Pain. 2006; 126(1-3); 155–164 113
- Jacobs J., Herman P., Heron K. et al. Homeopathy for menopausal symptoms in breast cancer survivors: a preliminary randomized controlled trial. J Altern Complement Med. 2005; 11; 21–27
- Christensen S., Zachariae R., Jensen A.B. et al. Prevalence and risk of depressive symptoms 3-4 months post-surgery in a nationwide cohort study of Danish women treated for early stage breast-cancer. Breast Cancer Res Treat 2008.
- Cousson-Gelie F., Bruchon-Schweitzer M., Dilhuydy J.M. et al. Do anxiety, body image, social support and coping strategies predict survival in breast cancer? A ten-year follow-up study. Psychosomatics. 2007 ; 48 : 211-216
- Humbert P. Prévenir L’alopécie chimio-induite. Annales de dermatologie et vénéréologie. 2009 ; 136(2) ; S29-S32
- Brochure « traitement du cancer et chute des cheveux », institut national du cancer édité en 2009 disponible : http://www.e-cancer.fr/Expertises-et-publications/Catalogue-des-publications/Traitements-du-cancer-et-chute-des-cheveux consulté le 09/02/2016
- Guide de soins et maquillage, belle et bien pour les femmes face au cancer disponible : http://www.bellebien.fr/uploads/pdf2/f05eb70fe5101b1d672ee23aba913fee2b17f47e.pdf consulté le 09/02/2016
- Merial-Kieny C., Nocera T., Mery S. Maquillage correcteur médical en post chimiothérapie. Annales de dermatologie. 2008. Hors-série 1. 25-28.
- Francequin G. Cancer du sein une féminité à reconstruire. Toulouse, ERES « Sociologie clinique », 2012, 268 pages.
- Zelek L. Aider à vivre après un cancer. Edition Springer Paris, 2010, p.275
- Parent A. La parole aux amazones. La lettre du sénologue. 2013 ; 62; 30-34
- Rapport 2014 de l’observatoire sociétal des cancers – Cancer du sein, se reconstruire après une mastectomie. http://www.ligue115cancer.net/sites/default/files/docs/observatoire_societal_des_cancers_rapport_2014.pdf
- Senesse P., Vasson M.P. Nutrition chez le patient adulte atteint de cancer : quand et comment évaluer l’état nutritionnel d’un malade atteint de cancer ? Comment faire le diagnostic de dénutrition et le diagnostic de dénutrition sévère chez un malade atteint de cancer ? Quelles sont les situations les plus à risque de dénutrition ? Nutrition clinique et métabolique. 2012 ; 26 (4) ; 165-188.
- Hannoun-Levi J.M. Traitement du cancer du sein et de l’utérus : impact physiologique et psychologique sur la fonction sexuelle. Cancer/ Radiothérapie. 2005 ; 9 (3) ; 175-182.
- Arnal-Morvan B., Laganier M. Anticancer du sein : prévenir et accompagner. Edition Eyrolles 2015. 184 pages.
- Jamin C. Utilisation des phyto-estrogènes après cancer du sein. Gynécologie Obstétrique & fertilité. 2003 ; 31 ; 667-675.


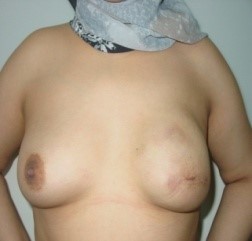


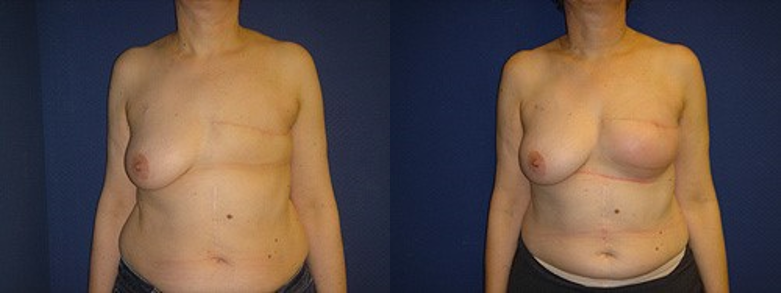
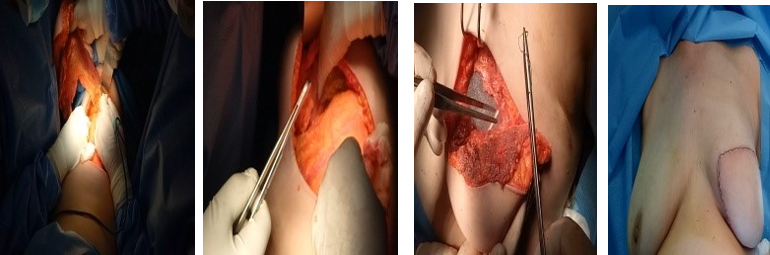
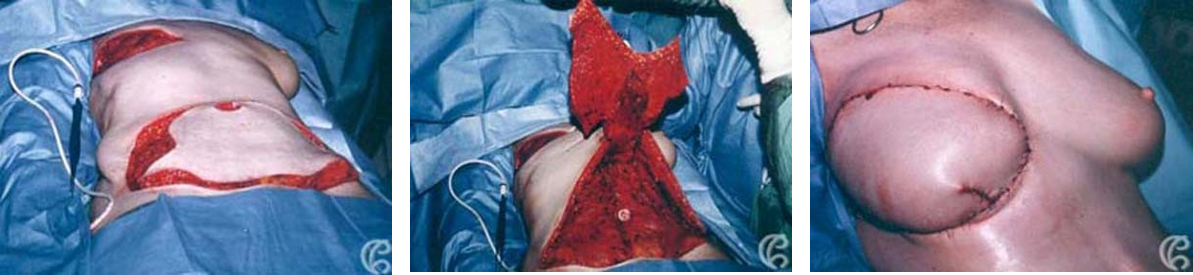
 (Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC
(Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC