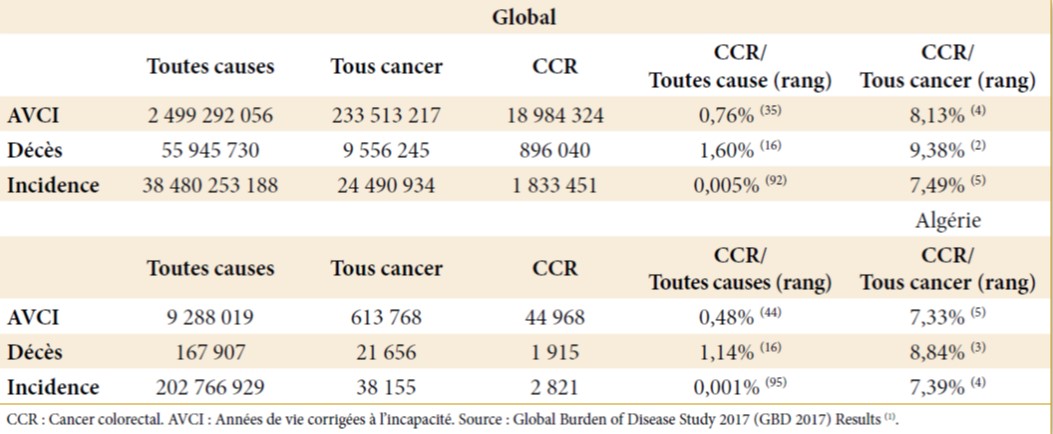
Plusieurs études randomisées et contrôlées ont déterminé l’efficacité de la colectomie par voie laparoscopique dans le traitement curatif du cancer du côlon. Actuellement, une colectomie par voie laparoscopique pour cancer peut être réalisée selon les règles carcinologiques.
Mahfouf, Service de Chirurgie Viscérale et Oncologique, Hôpital Ibn Ziri, Bologhine, Alger.
Date de soumission : 05 Février 2020.
Résumé : Plusieurs études randomisées et contrôlées ont déterminé l’efficacité de la colectomie par voie laparoscopique dans le traitement curatif du cancer du côlon. Actuellement, une colectomie par voie laparoscopique pour cancer peut être réalisée selon les règles carcinologiques. La morbidité est moindre que pour l’abord classique et la mortalité faible. Les résultats de survie semblent comparables à la chirurgie ouverte. Depuis la première description d’une résection laparoscopique d’un cancer du côlon en 1991, l’approche laparoscopique a été vivement discutée et était même controversée. De nos jours, celle-ci est associée à une diminution des pertes sanguines, un meilleur résultat esthétique, une réduction des douleurs post-opératoires, une durée plus courte de l’iléus post-opératoire et par conséquent à un retour au domicile plus rapide. La technique laparoscopique qui est standardisée et validée depuis 2005, garantit une résection adéquate, néanmoins un apprentissage spécifique est nécessaire. Le traitement curatif du cancer du côlon repose sur la résection chirurgicale de la tumeur. Tous ces avantages sont clairement secondaires dans le cadre du traitement curatif d’une maladie maligne, la guérison et la survie devant être les objectifs principaux.
Mots clés : Chirurgie, côlon, cœlioscopie, traitement curatif
Abstract: Several randomized and controlled studies have determined the efficacy of laparoscopic colectomy in the curative treatment of colon cancer. Currently, a laparoscopic colectomy for cancer can be performed according to the carcinological rules. Morbidity is lower than for the classical approach and low mortality. Survival results appear to be comparable to open surgery. Since the first description of a laparoscopic resection of colon cancer in 1991, the laparoscopic approach has been hotly debated and even controversial. Nowadays, this is associated with a decrease in blood loss, a better aesthetic result, a reduction in postoperative pain, a shorter duration of the postoperative ileus and therefore a faster return home. The laparoscopic technique which has been standardized and validated since 2005, guarantees adequate resection, however specific training is necessary. The curative treatment of colon cancer is based on surgical resection of the tumor. All these advantages are clearly secondary in the curative treatment of a malignant disease, healing and survival must be the main objectives.
Keywords : Surgery, Colon, Laparoscopy, curative treatment
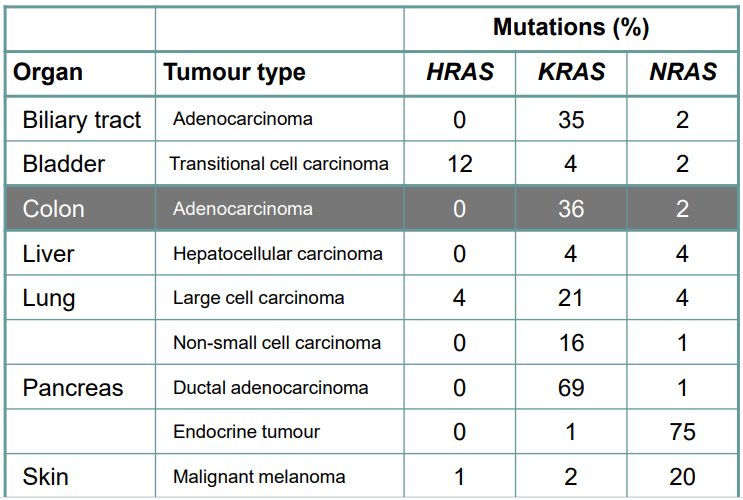
Le cancer colorectal est un problème de santé publique mondial (1) avec une incidence annuelle d’environ 1 million de cas et une mortalité annuelle de plus de 500.000 cas (1,2).
Le nombre absolu de cas augmentera pendant les décennies à venir du fait de l’expansion et du vieillissement de la population dans les pays développés ou en voie de développement (2,3).
Les premières résections colorectales laparoscopiques dans le monde étaient rapportées par Jacobs aux États-Unis en 1991 (4) ; ceci a procuré au début un grand enthousiasme, mais rapidement des études rapportaient des récidives néoplasiques pariétales sur orifices de trocarts consécutives aux résections colorectales pour cancer transformant l’optimisme en scepticisme, et plusieurs chirurgiens ont abandonné la technique laparoscopique (4,5).
En 1994, aux USA, la société américaine des chirurgiens du colon et du rectum prônait que les résections colorectales par cœlioscopie soient réservées aux seuls essais randomisés contrôlés et c’est seulement en 2005 que la technique fût validée (5,6,7).
L’abord classique représente un traumatisme pour la paroi abdominale, il est responsable en post opératoire de douleurs abdominales, d’une diminution de la fonction respiratoire par rapport à sa valeur pré-opératoire, une augmentation du séjour hospitalier, une augmentation du coût ; et, en post opératoire tardif, il y a le risque de survenue d’éventrations et d’occlusions intestinales (7,8).
L’abord laparoscopique permet une épargne pariétale, un confort post opératoire et un séjour hospitalier plus court compensant le coût initial plus élevé de la cœlioscopie (7,8).
La crainte d’une diminution de la qualité de l’exérèse a longtemps pesé sur le bénéfice de la laparoscopie pour cancer ; dans cette indication, bien plus que les suites post-opératoires plus simples, l’impératif est d’obtenir un résultat carcinologique satisfaisant, assurant une survie globale et un taux de récidives locales ou métastatiques au moins équivalent à ceux obtenus par laparotomie (5,6,7,8).
Plusieurs essais randomisés ont rapidement permis de démontrer que ces résultats oncologiques étaient exactement superposables entre les deux voies d’abord pour le cancer du côlon (5,6,7,8,9).
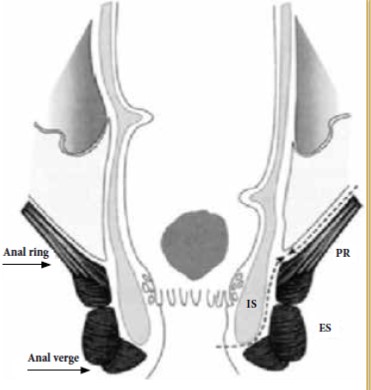
- Anatomie
Le colon s’interpose entre l’intestin grêle et le rectum ; pour le chirurgien, il comporte principalement deux portions : le colon droit, vascularisé par les branches de l’artère mésentérique supérieure et le colon gauche vascularisé par l’artère mésentérique inférieure.
Nous devons distinguer les segments coliques fixes (colon ascendant et colon descendant) des segments mobiles (colon transverse et colon sigmoïde) amarrés par un long méso libre
La vascularisation colique est décrite en tenant compte de l’importance pratique des arcades artérielles et du drainage lymphatique (9,10).
- Principes généraux
Ligature première des vaisseaux avec technique du « no touch » consistant en un clippage premier des vaisseaux avant toute manipulation de la tumeur (10,11).
Clippage à l’origine des vaisseaux autorisant une exérèse large du mésocolon et des ganglions lymphatiques de drainage et permet l’ablation des ganglions pédiculaires (10,11).
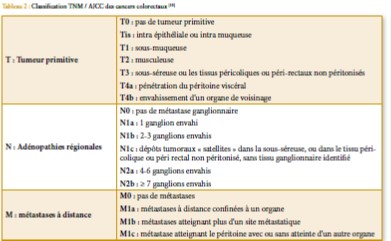
Pour permettre une stadification correcte, il faut retrouver et examiner un nombre minimum de ganglions sur la pièce opératoire, la classification de l’UICC propose le chiffre de 12 ganglions (10,11,12).
Les marges longitudinales de section colique d’au moins 05 cm est recommandé, pour les tumeurs infiltrantes, une marge longitudinale de 10 cm est préconisée chaque fois que cela est possible sans risque chirurgical supplémentaire (10,11,12,13).
Protection de la paroi lors de l’extraction de la pièce opératoire avec utilisation systématique d’un sac (12,13,14).
Les anastomoses doivent se faire sans aucune tension.
- Technique de la colectomie gauche laparoscopique pour cancer (12,13,14,15) :
- Installation du patient à l’intervention
Le patient est installé en décubitus dorsal, jambes écartées légèrement fléchies, les deux bras le long du corps, en position dite de double équipe.
La voie d’abord laparoscopique nécessite de basculer le patient en position de Trendelenburg maximale avec roulis droit ; des appuis sont mis en place à la partie supérieure des deux épaules, des sangles sont mises en place afin d’éviter que le patient ne glisse de la table opératoire.
Le chirurgien s’installe à droite du patient, le premier aide à sa gauche, l’instrumentiste à droite du chirurgien et le second aide à gauche du patient ; la colonne de cœlioscopie est placée à gauche du patient.
- Mise en place des trocarts
Le premier trocart de 10 mm est mis en place en para-ombilical droit, un trocart de 05 mm dans l’hypochondre gauche, un trocart de 05 mm dans l’hypochondre droit, un trocart de 12 mm dans la fosse iliaque droite permettant de passer l’endo-GIA et un trocart de 05 mm en sus-pubien.
Figure 1 : installation du patient. (Photo : collection personnelle de l’auteur).
- Exploration de la cavité abdominale
Après avoir repéré la tumeur, il faut explorer l’ensemble de la cavité abdominale : le péritoine, le mésentère et le foie à la recherche de métastases.
Pendant toute la durée de l’intervention, il convient de manipuler avec précaution le colon et son méso pour ne pas réaliser de plaies ou d’effractions tumorales, l’abord médial a l’avantage de permettre le minimum de mobilisation colique.
- Principes généraux
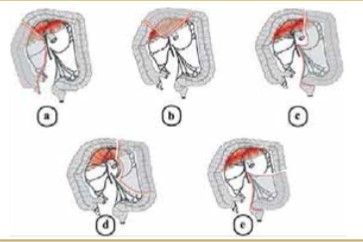
L’approche dite médiale consiste en la dissection du mésocolon gauche, de dedans en dehors, ses différents temps opératoires sont :
- Incision du feuillet péritonéal du mésocolon gauche en avant de l’aorte :
Une pince fenêtrée atraumatique tirant le colon vers le haut et la gauche fait saillir dans le mésocolon l’artère et la veine mésentériques inférieures.
Le feuillet péritonéal du mésocolon est incisé sur la face antérieure de l’aorte.
Dissection le long de la veine mésentérique inférieure facilitant le repérage et la dissection de l’artère mésentérique inférieure.
- Clippage et section de la veine et de l’artère mésentériques inférieures et dissection du mésocolon gauche de dedans en dehors :
Dans le cas du cancer, dans la perspective de réaliser un curage ganglionnaire satisfaisant, la veine mésentérique inférieure est sectionnée entre clips ;
Le clippage de l’artère doit se faire à environ 01 cm de son origine sur l’aorte.
La dissection de dedans en dehors se poursuit en avant du fascia de Toldt qui protège l’uretère et les vaisseaux génitaux ; cette dissection passe donc en avant de l’uretère puis des vaisseaux génitaux jusqu’à la gouttière pariéto-colique gauche.
- Décollement colo-épiploïque et mobilisation de l’angle colique gauche :
La libération de l’angle colique gauche est réalisée après un décollement colo épiploïque premier, puis par une mobilisation de l’angle de dehors en dedans.
- Dissection de la charnière recto-sigmoïdienne et section du haut rectum :
Pour un cancer de la charnière recto-sigmoïdienne, le plan de dissection du haut rectum doit prendre en considération l’exérèse de 05 cm de rectum et de méso-rectum en dessous du pôle inférieur de la tumeur.
Le recto sigmoïde est verticalisé, le plan rétro-rectal s’ouvre au niveau du promontoire, la dissection se fait dans le plan du méso-rectum mousse qui est un plan avasculaire.
Une fois la zone de section rectale choisie, nous incisons le fascia recti et nous procédons à la section coagulation progressive jusqu’à la paroi rectale.
La section rectale est réalisée à l’aide d’une agrafeuse linéaire coupante endo-GIA ; lors de l’agrafage, le rectum est tracté vers le haut et latéralisé vers la gauche pour que la pince endo-GIA soit la plus perpendiculaire possible par rapport à l’axe du rectum.
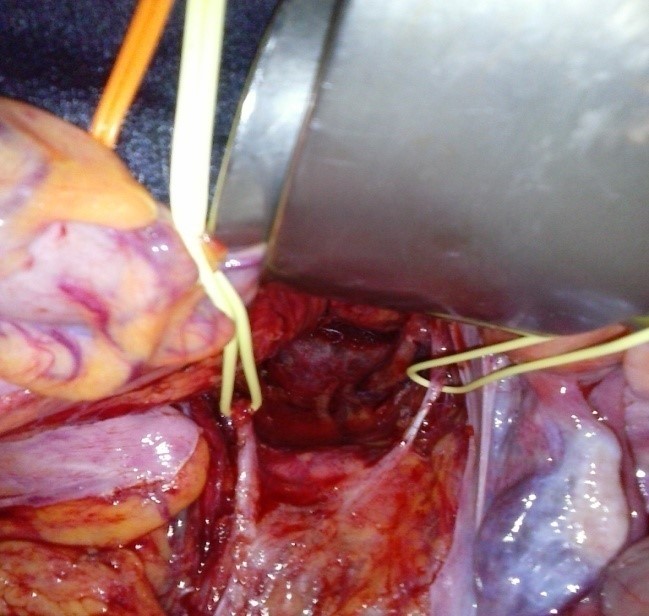
- Extraction et résection sigmoïdienne par une incision de Pfanenstiel :
Après incision type Pfanenstiel et mise en place d’une jupe de protection de la paroi, le colon est extériorisé prudemment en évitant tout essorage contre la paroi, celui-ci est sectionné.
Mise en place de l’enclume d’une agrafeuse circulaire est introduite dans l’extrémité colique proximale dont les berges sont fermées par une bourse.
Le colon est réintroduit dans l’abdomen et l’incision est refermée.
Figure 2 : Extraction de la pièce opératoire. (Photo : collection personnelle de l’auteur).
- Anastomose colorectale mécanique :
Le pneumopéritoine est recréé et le patient est repositionné en position de Trendelenburg et latérale droite.
Avant l’agrafage, il faudrait s’assurer de l’absence du Twist du colon gauche descendu.
L’agrafeuse circulaire est introduite par l’anus, le moignon rectal est perforé par la pointe de la pince mécanique ; une pince saisit l’enclume et l’emboite avec la pointe de la pince EEA, un cliquetis est alors perçu.
L’anastomose est alors réalisée en prenant soin de ne pas interposer d’anses grêles ou d’épiploon.
Aspiration du liquide de lavage et mise en place d’un drain tubulé.
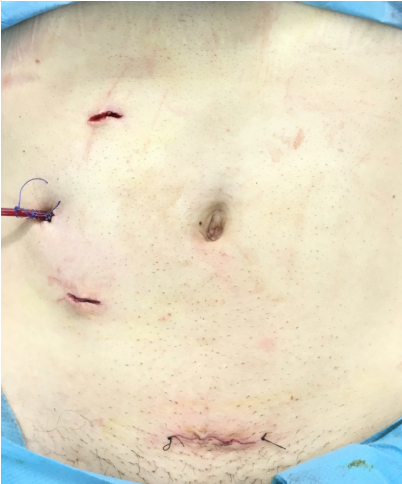
Figure 3 : cicatrices en post opératoire immédiat. (Photo : collection personnelle de l’auteur).
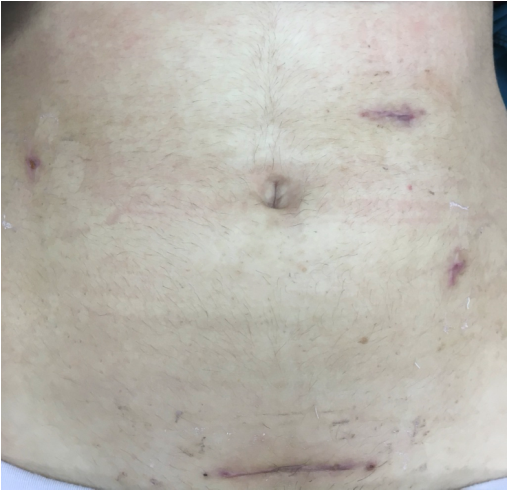
Figure 4 : Cicatrices après 15 jours. (Photo : collection personnelle de l’auteur)
- Technique de la colectomie droite laparoscopique pour cancer (13,14,15)
- Variantes de la colectomie droite sous cœlioscopie
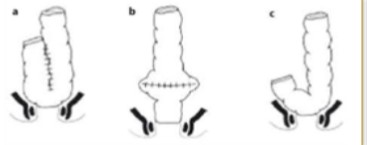
Sur le plan technique, à la différence de la colectomie gauche dont les temps opératoires sont standardisés et globalement réalisés de la même manière, la colectomie droite par cœlioscopie peut avoir trois variantes :
- Colectomie droite avec libération coelioscopique
Dans cette variante, seule la libération colique est faite par cœlioscopie. Les ligatures vasculaires, la colectomie et l’anastomose sont faites ex situ à la faveur d’une mini laparotomie.
- Colectomie droite coelio-assistée
Dans cette variante, la libération colique et les clippages et sections vasculaires sont réalisés in situ par cœlioscopie. La colectomie et l’anastomose sont faites ex situ.
La résection colique et l’anastomose sont dans ce cas extracorporelles à la faveur d’une mini laparotomie.
- Colectomie droite entièrement coelioscopique
Dans cette variante, tous les temps opératoires se font sous cœlioscopie. Une mini laparotomie est faite uniquement pour l’extraction de la pièce opératoire.
Les clippages et sections vasculaires, le curage ganglionnaire, la colectomie ainsi que l’anastomose iléo-colique sont donc réalisés sous cœlioscopie. L’anastomose dite intra-corporelle est faite sous contrôle coelioscopique.
- Installation du patient
Le patient est installé le membre supérieur gauche le long du corps, le membre supérieur droit en abduction, les membres inférieurs en abduction.
Une position de Trendelenburg modérée et un roulis important vers la gauche facilitent l’exposition. L’opérateur est à gauche du malade, l’aide à la droite de l’opérateur, l’instrumentiste entre les jambes du malade.
Le pneumopéritoine est réalisé dans l’hypochondre gauche. On positionne à cet endroit le trocart optique. Un trocart de 10/12 mm est ensuite mis en sous et latéro-ombilical gauche pour la main droite de l’opérateur et un trocart de 5 mm sus pubien pour la main gauche de l’opérateur.
Un dernier trocart de 5 mm est placé dans l’hypochondre droit. Il permet de présenter le côlon ou son méso. C’est à cet endroit que va être faite l’incision d’extraction de la pièce opératoire.
La colectomie droite sous cœlioscopie avec abord premier des vaisseaux est décrite de bas en haut par son auteur Goasguen. Elle comporte successivement la dissection et la section du pédicule iléocolique, le décollement de bas en haut et de dedans en dehors du mésocôlon droit, puis la dissection et la section des autres vaisseaux, principalement des vaisseaux coliques supérieurs droits.
L’abord des vaisseaux de bas en haut peut être rendu mal aisé par le caractère sessile de la partie droite du mésocôlon qui le rend large et court et peut rendre difficile l’identification des vaisseaux pouvant être l’objet de nombreuses variations. L’abord des vaisseaux de haut en bas peut donc rendre l’identification et la dissection des vaisseaux plus faciles.
- Colectomie droite sous cœlioscopie de bas en haut :
- Exposition du pédicule iléo-cæco-colique
Le grêle est basculé du côté gauche, le grand épiploon placé dans l’hypochondre gauche. La jonction iléocæcale est saisie par une pince fenêtrée, introduite par l’orifice de l’hypochondre droit. Elle permet de mettre en tension le pédicule iléo-cæco-colique dont le relief devient ainsi très visible.
- Section du pédicule iléo-cæco-colique
Le péritoine est incisé au bord inférieur du relief du pédicule iléo-cæco-colique. Ce geste permet de trouver le repère postérieur que constitue la face antérieure du troisième duodénum. Sa mise en évidence permet de localiser, à son bord inférieur puis à droite, le fascia de Toldt droit. L’artère se présente en premier. Artère et veine sont clippées puis sectionnées séparément. Il est utile dans ce temps de pousser la dissection du fascia de Toldt en dehors et de débuter la section du mésentère.
- Libération de la face antérieure du deuxième duodénum
La dissection est poursuivie en suivant la face antérieure du deuxième duodénum, en soulevant le méso-côlon à l’aide de la pince introduite par l’hypochondre droit. On voit alors, sur la gauche de la brèche péritonéale, la branche droite du pédicule colique supérieur droit ou, plus rarement, le tronc lui-même. Il faut souvent pour individualiser le tronc, poursuivre la dissection jusqu’à atteindre la tête du pancréas. Il faut faire attention dans ce temps de ne pas être brutal et d’arracher les vaisseaux. La veine gastro-épiploïque droite est habituellement plus en arrière, à proximité du parenchyme pancréatique. Le pédicule colique supérieur droit est alors sectionné.
- Libération de la face antérieure du premier duodénum
La section du pédicule colique supérieur droit permet de continuer la dissection vers le haut. On ouvre ainsi le péritoine en avant du duodénum. Le repère de fin de dissection est la face inférieure du foie ou de la vésicule biliaire. Cela permet d’ouvrir la partie postérieure du méso-côlon transverse.
- Exposition de la tête du pancréas
On abaisse ensuite le grand épiploon et le côlon transverse. Puis on réalise la section du grand épiploon pour l’amener au niveau souhaité sur le côlon transverse. Dès lors, le simple abaissement du côlon transverse permet de voir toute la face antérieure de la tête du pancréas qui a déjà été́ disséqué.
- Mobilisation du côlon droit
La mobilisation du côlon droit est ensuite effectuée de haut en bas, en libérant la face antérieure du rein droit et en ouvrant la gouttière pariéto-colique.
On rejoint alors le début de la dissection du fascia de Toldt droit, initialisée lors de la section du pédicule iléocæco-colique. Il ne reste plus qu’à mobiliser la dernière anse grêle et terminer de sectionner le mésentère.
- Extériorisation du côlon mobilisé
L’incision d’extraction se fait habituellement dans celle du trocart de l’hypochondre droit. Elle est horizontale. Il est souvent possible de dissocier les muscles sans les sectionner, ce qui est moins douloureux dans les suites. Le côlon est extériorisé. Il reste à sectionner l’arcade paracolique et à dépouiller le tube digestif au niveau de la future zone d’anastomose.
- Confection de l’anastomose
Toutes les techniques d’anastomose sont possibles, intracorporelle ou extracorporelle. En extracorporel, avec une incision étroite de l’hypochondre droit, il est souvent simple de réaliser une anastomose latéro-latérale. Il est nécessaire dans cette variante de bien refouler les deux mésos des mords de la pince. On referme ensuite l’extrémité digestive par une application transversale de pince à suture automatique.
- Contrôle coelioscopique
Après réintroduction du côlon et fermeture de l’incision de l’hypochondre droit, il est nécessaire de repasser en laparoscopie pour vérifier l’abdomen, aspirer d’éventuels épanchements dans la gouttière pariétocolique et au fond du cul de sac de Douglas, et replacer le tube digestif, habituellement en refermant la brèche mésentérico-mésocolique. Enfin, les orifices de trocart sont systématiquement refermés.
- Colectomie droite sous cœlioscopie de haut en bas
- L’abaissement de l’angle colique droit
Le grand épiploon est fendu verticalement sur la ligne médiane, depuis le côlon transverse vers le bas, puis vers le haut en ouvrant l’arrière-cavité des épiploons, en suivant ensuite le bord inférieur de l’arcade vasculaire de la grande courbure gastrique qui est conservée, puis le bord inférieur du premier duodénum. Le péritoine pré-rénal droit est incisé de dedans en dehors et l’angle colique droit abaissé. Le pédicule colique supérieur droit apparait alors dans le mésocôlon transverse. Chez les malades qui s’y prêtent, on peut poursuivre le décollement du mésocôlon assez bas pour exposer tout le deuxième duodénum et la partie droite du troisième duodénum, ce qui facilite grandement la fin de l’intervention. En refoulant le grand épiploon vers le haut, on met en tension la veine gastro-épiploïque droite qui, lorsqu’elle se jette dans la veine colique supérieure droite, doit être sectionnée pour bien exposer la terminaison du tronc gastro-colique.
- La section du pédicule colique supérieur droit
Le mésocôlon est alors ouvert sur la ligne médiane, au contact du côlon, puis sectionné d’avant en arrière jusqu’à sa racine, au besoin en sectionnant une branche droite d’une artère colique transverse ou même un pédicule colique transverse lui-même si l’on veut faire porter la section colique vers la gauche. La section du mésocôlon est poursuivie vers la droite jusqu’au pédicule colique supérieur droit. Celui-ci est disséqué en mettant à nu la face antérieure du pancréas, du duodénum et de la veine mésentérique supérieure. L’artère et la veine sont séparées, contrôlées par des clips et sectionnées en emportant le tissu cellulo-ganglionnaire qui les accompagne. Le décollement de la racine du mésocôlon est poursuivi en dehors jusqu’à la gouttière pariétocolique et en bas jusqu’au genu inferius si cela n’a pas été́ fait lors du temps précèdent.
- La section du pédicule iléocolique
Le grand épiploon et le côlon transverse sont refoulés vers le haut. Le pédicule iléocolique est mis en tension par traction sur le carrefour iléocæcal. Le péritoine est incisé au bord inférieur de ce pédicule, puis devant la veine mésentérique supérieure. Lorsque la dissection par le haut a exposé le troisième duodénum, on retrouve immédiatement le bon plan ; sinon le décollement du mésocôlon droit est amorcé avec identification de la face antérieure du duodénum. Le pédicule iléocolique est disséqué au bord droit la veine mésentérique supérieure. L’artère et la veine sont dissociées, contrôlées par des clips, puis sectionnés en emportant les ganglions de voisinage. La dissection est poursuivie vers le haut, le long de la veine mésentérique supérieure en emportant le tissu cellulo-ganglionnaire qui s’y trouve et en rejoignant la zone de section de la veine gastrocolique. Le pédicule colique droit moyen est sectionné de la même façon, sans qu’on puisse le confondre avec le pédicule colique supérieur droit.
- Fin de l’intervention
La mobilisation du côlon et du grêle distal est achevée. L’exérèse de la pièce est faite par une petite incision et la continuité digestive est rétablie par une anastomose manuelle ou mécanique.

Figure 5 : Cicatrices après 15 jours. (Photo : collection personnelle de l’auteur)
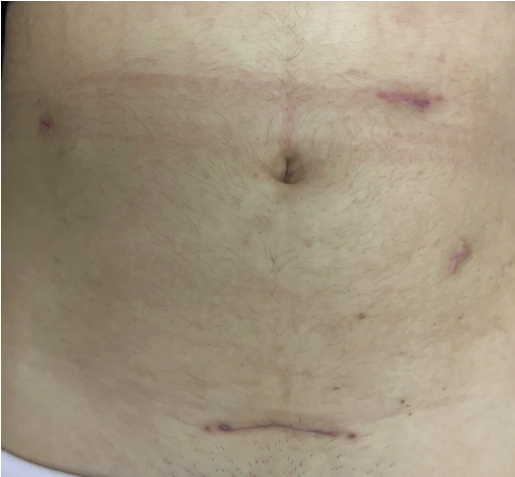
Figure 6 : Cicatrices après 01 mois. (Photo : collection personnelle de l’auteur)
Conclusion
La chirurgie associée au traitement adjuvant constitue la thérapeutique de choix dans le cancer du côlon (16).
L’amélioration de la prise en charge commence nécessairement par un dépistage précoce, des moyens d’investigation modernes et une collaboration entre les différentes spécialités.
La chirurgie laparoscopique, grâce aux évolutions technologiques, a été adaptée aux colectomies. Cette technique constitue une évolution réelle, assurant une meilleure ergonomie pour le chirurgien et un confort post-opératoire pour le malade. La sécurité carcinologique étant prouvée, l’autre bénéfice substantiel de cette chirurgie mini invasive est l’aspect cosmétique agissant sur l’aspect psychologique des patients.
La colectomie laparoscopique est actuellement une technique bien codifiée, et dont les résultats sont excellents (7,8,16). Cependant, cette méthode est matériel-dépendante, la réalisation de colectomies laparoscopique doit se faire lorsque toutes les conditions sont réunies. La formation à cette technique est impérative pour la généraliser et la vulgariser.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références :
- Haute Autorité de santé. Cœlioscopie en chirurgie du cancer colorectal. Évaluation en santé publique. Saint Denis La Plaine: HAS ; 2005.
- Colorectal: multidisciplinary management : European consensus conferences colon & rectum, Eur J Cancer (2013) .06.048.
- National Institute for Health Clinical Excellence. Laparoscopic surgery for colorectal cancer. London: Nice; 2006.
- Jacob BP, Salky B. Laparoscopic colectomy for colon adenocacinoma: an 11-year retrospective review with 5-year survival rates. Surg Endoc 2005, published online March 28,2005
- Janson M, Bjorholt I, Carlsson P, Haglind E, HenrikssonM, Lindholm E, Anderberg A. Randomized clinical trial of the costs of open and laparoscopic surgery for colonic cancer. Br J Surg 2004 ;91 :409-417.
- Society of American Gastrointestinal and Endoscopic Surgeons. Guidelines for laparoscopic resection of curable colon and rectal cancer. Los Angeles: Sages; 2006.
- Mariette, A. Alves, S. Benoist, F. Bretagnol, J.Y. Mabrut, K. SIim. Soins péri-opératoires en chirurgie digestive. Recommandation de la Société Française de Chirurgie Digestive (SFCD) Annales de chirurgie 130 (2005)108- 124.
- Kehlet H, Wilmore W. Evidence based surgical care and evolution of fast track surgery. Ann Surg 2008.248:189-198.
- Clinical Outcomes of Surgical Therapy Study Group. A comparison of laparoscopically assisted and open coIectomy for colon cancer. Heidi Nelson, M.D., Daniel J. Sargent, Ph.D., H. Sam Wieand, Ph.D., James Fleshman -N Engl J Med 2004 ;350:2050-9.
- Panis Yves. Principes Techniques à Respecter lors des Colectomies pour Cancer. Séminaire National du DESC, Paris 2013.
- Leung KL, Kwok SP, Lam SC, Lee JF, Yiu RY, Ng SS, et al. Laparoscopic resection of rectosigmoid carcinoma: prospective randomised trial. Lancet 2004;363 (9416) 1187- 92
- Prise en charge du cancer colique gauche (en dehors de l’occlusion) cancer du côlon gauche: principes chirurgicaux et voie d’abord. F Bretagnol. Session Développement professionnel Continu. SFCD-2013.
- Veldkamp R, Gholghesael M, Bonjer HJ, Meijer DW, Buunen M, et al. European Association of Endoscopic Surgery, Laparoscopic resection of colon cancer. Surg Endosc 2004;18(8) : 1163- 85.
- Lacy AM, Garcia-Valdecasas JC, Delgado S, et al. Laparoscopy-assisted coIectomy versus open colectomy for treatment of non-metastatic colon cancer: a randomized trial. Lancet 2002 ;359 :2224-9.
- Simons AJ, Anthone GJ, Ortega AE, et al. Laparoscopic-assisted colectomy learning cuve. Dis Colon Rectum 1995;38:600˗̶ 03.
- Laparoscopy in colon cancer: The new standard? F. Fumo, M. D’Ambra, S. Franzese. U.O.C. Chirurgie générale, Aorn A. Cardarelli, Napoli, Italy. EJC – Supplement S6 (2008) 100-101