L’arthrose de la main constitue la deuxième localisation après celle du genou en termes de fréquence, elle affecte principalement les femmes et représente un élément clé de la définition de l’arthrose généralisée.
M. M. Mebarek1, A. Moussa Mebarek2, A. Mammeche1, Z.F. Lakhal1, N. Benyerbah1, H. Rahmouni1, M. Elrakaoui1, C. Haouichat1.
1 Service de Rhumatologie, 2 Laboratoire Central de Biologie,
CHU Djilali Bounaâma, Douéra, Alger.
Date de soumission : 27 Juin 2020.
Résumé : L’arthrose de la main constitue la deuxième localisation après celle du genou en termes de fréquence, elle affecte principalement les femmes et représente un élément clé de la définition de l’arthrose généralisée. L’étiologie semble être multifactorielle et hétérogène, comprenant plusieurs sous-ensembles cliniques et radiologiques. Elle inclut les arthroses touchant la base du pouce (articulation trapézo-métarcarpienne), les articulations métacarpo-phalangiennes, les articulations interphalangiennes distales et proximales et l’arthrose érosive. Le diagnostic est facile et repose sur la clinique et les radiographies standards. L’impact important sur la qualité de vie et le préjudice esthétique occasionné par cette maladie, ont justifié l’énorme progrès réalisé ces dernières années en termes de connaissances des mécanismes physiopathologiques et de sa prise en charge. Ainsi, plusieurs facteurs génétiques et biologiques sont impliqués, notamment les adipokines et les cytokines pro-inflammatoires, et différents traitements ont été essayés, tel que le méthotrexate et les thérapies anti-cytokines dites ciblées. L’objectif de ce travail est d’effectuer un état des lieux sur les connaissances physiopathologiques actuelles, ainsi que les essais cliniques réalisés dans l’arthrose digitale.
Mots clés : arthrose, mains, arthrose érosive, biologie, traitements.
Abstract: Hand osteoarthritis is the second location after that of the knee in terms of frequency, it affects mainly women and it is a key element in the definition of generalized osteoarthritis. The aetiology appears to be multifactorial and heterogeneous, comprising several clinical and radiological subsets. It includes arthritis affecting the base of the thumb (trapezo-metarcarpal joint), metacarpophalangeal joints, distal and proximal interphalangeal joints and erosive arthritis. The diagnostic is easy and is based on the clinic and standard radiographs. Due to its significant impact on quality of life, and its aesthetic damage, hand osteoarthritis has benefited from progress in the knowledge of its pathophysiology and treatment. Several genetic and biological factors are involved, specially adipokines and proinflammatory cytokines, and diverse treatments have been tried, such as methotrexate and anti-cytokine therapies. The purpose of this work is to give an over review concerning pathophysiology and clinical trials made in this disease.
Key words: osteoarthritis, hands, erosive osteoarthritis, biology, treatments.
Introduction
L’arthrose de la main est un groupe hétérogène de lésions, incluant l’arthrose nodale interphalangienne, l’arthrose de la base du pouce et l’arthrose érosive.
C’est la deuxième localisation de l’arthrose par ordre de fréquence, cette dernière considérée comme la maladie articulaire la plus fréquente.
La prévalence de l’arthrose symptomatique est significativement plus importante chez la femme que chez l’homme et augmente avec l’âge.
L’arthrose digitale radiographique touche 67% des femmes et 55% des hommes après 55 ans, ce qui représente 100 millions d’Européens (1) dont 20% vont avoir une arthrose symptomatique (2). Sa prévalence radiographique ou symptomatique vient statistiquement en premier, avant les arthroses du genou et de la hanche, touchant deux femmes pour un homme (3.4).
Elle touche par ordre de fréquence les articulations interphalangiennes distales, puis celles de la base du pouce et enfin les interphalangiennes proximales (5).
L’histoire de la maladie et les symptômes varient selon les patients.
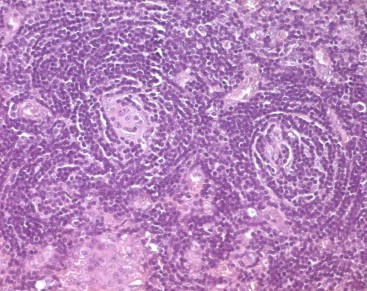
L’examen clinique d’une arthrose de la main montre une hypertrophie osseuse des articulations des doigts et des déformations.
Des nodosités au niveau des articulations interphalangiennes distales (IPD) et articulations interphalangiennes proximales (IPP) des doigts, appelés nodosités d’Heberden et de Bouchard, peuvent être observées. Ces déformations qui sont typiques de l’arthrose de la main, surviennent avec ou sans symptômes, douleur, raideur ou handicap.
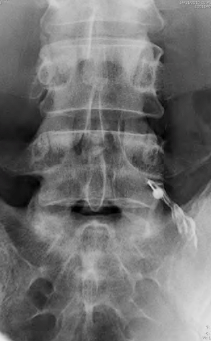
Les caractéristiques radiographiques de l’arthrose de la main incluent érosions, amincissement de l’espace articulaire, ostéophytes et sclérose osseuse sous-chondrale.
Des critères de classification ont été développés par l’American College of Rheumatology (ACR)(6), et sont sensibles à 92% et spécifiques à 98% (tableau 1).
Les scores radiographiques ne sont pas nécessairement liés à l’évaluation clinique. Pour une étude italienne, il n’y avait pas d’association entre les signes cliniques, les symptômes et les scores radiographiques (7).
En revanche, une étude anglaise montrait une association positive entre nodules et amincissement de l’espace articulaire en radiographie (8).
La radiographie reste la technique de référence pour l’évaluation morphologique de l’arthrose de la main. Cependant, l’imagerie par résonance magnétique (IRM) utilisée pour le diagnostic de l’arthrose de la main, fait apparaître plus d’informations, comme des synovites modérées à sévères, des lésions médullaires, des érosions, et des ostéophytes.
L’échographie peut mettre en évidence des érosions infra-radiographiques, et des signes d’inflammation dans l’arthrose digitale sous forme de synovite avec hyper-vascularisation.
L’arthrose érosive des mains est un sous-groupe de l’arthrose de la main ciblant les articulations interphalangiennes notamment les IPD, et caractérisée par une apparition brusque avec douleur intense et associée à un handicap fonctionnel, des symptômes et signes inflammatoires (rigidité, gonflement des tissus mous, érythème, paresthésies, légère augmentation de la protéine C-réactive ; et une évolution plus défavorable que celle de l’arthrose non érosive de la main. Elle est définie radiographiquement par l’érosion sous chondrale, caractéristique quand elle est centrale, la destruction corticale et la réaction réparatrice secondaire, qui peut inclure l’ankylose osseuse.
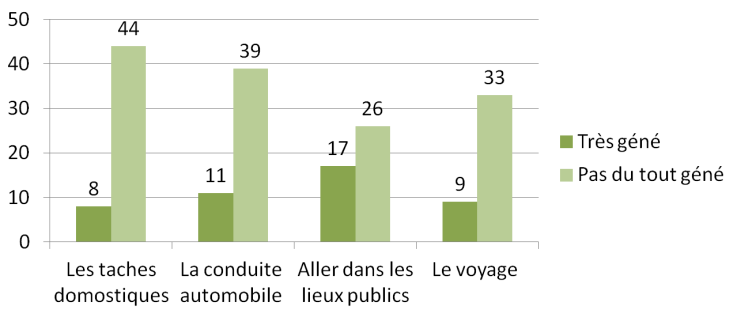
La qualité de vie des patients souffrant d’arthrose de la main peut être fortement altérée dans les activités quotidiennes du fait de limitations fonctionnelles, comme cela a été rapporté dans l’analyse de Kwok et al.,(9). Pour les femmes, l’importance des altérations esthétiques des mains ne doit pas être sous-estimée.
Tableau 1 : Critères de classification diagnostique de l’arthrose digitale. Les 10 articulations sélectionnées sont : la trapézo-métacarpienne, les interphalangiennes proximales et distales des 2e et 3e doigts des deux mains. Le diagnostic est positif si les critères 1, 2 et 3 sont présents + le critère 4 ou le critère 5. Sensibilité de ces critères : 92 % ; spécificité : 98 %.
Etiopathogénie de l’arthrose digitale
De multiples facteurs sont impliqués dans la pathogénie de l’arthrose des mains, et pourraient donc constituer autant de cibles thérapeutiques.
Une étude de Denisov at al., a montré que l’obésité peut être considérée comme un facteur de risque pour la progression de l’arthrose du genou et de la main (10).
Dans une autre étude, l’obésité était associée à l’arthrose, avec une augmentation du risque pour les arthroses du genou et de la main (11).
Chez l’homme, l’obésité est corrélée avec la progression de l’arthrose de la main, mais ce n’est pas le poids tout seul (12). Cela suggère que l’obésité est un facteur de risque de progression des arthroses du fait de ses conséquences pro-inflammatoires plutôt que simplement par son effet mécanique sur la charge articulaire.
En effet, le tissu adipeux en excès produit des facteurs humoraux appelés adipokines qui peuvent contribuer aux lésions du cartilage articulaire, tel que la leptine, l’adiponectine, la visfatine et la résistine.
Les taux de leptine sont étroitement corrélés à l’IMC, ils sont plus élevés dans le cartilage arthrosique comparé au cartilage normal, et sont corrélés avec le degré de destruction et la quantité d’ostéophytes, le rôle de ce facteur reste controversé. Les études chez l’animal ont montré également que la leptine stimulait fortement les fonctions anaboliques des chondrocytes (13).
La leptine semble être un facteur local et systémique important, influençant l’homéostasie de l’os et du cartilage, même si son rôle n’est pas encore clairement établi et les mécanismes non encore déchiffrés (14).
L’adiponectine est l’adipokine circulante la plus abondante avec différents isoformes ayant des fonctions opposées (propriétés pro ou anti-inflammatoires).
Les taux d’adiponectine sérique sont augmentés chez les patientes ayant une arthrose érosive des mains. L’adiponectine pourrait donc jouer un rôle dans la physiopathologie des arthroses érosives des mains ( 15,16).
Dans une étude de cohorte transversale, les taux sériques de résistine ont été corrélés avec des changements radiographiques dans l’arthrose de la main, en particulier avec des érosions dans l’os sous-chondral (17).
En plus d’être une source d’adipokines, les tissus adipeux locaux et systémiques pourraient aussi jouer un rôle pathogène important dans l’arthrose comme sources d’autres cytokines pro-inflammatoires et de chémokines (18).
L’arthrose digitale possède une composante génétique, avec une héritabilité estimée entre 48% et 65%. Les nodules d’Heberden sont transmis selon un mode mendélien dominant chez les femmes, et récessif chez les hommes ; les autres formes d’arthrose digitale sont multifactorielles avec un gène majeur et un composant résiduel multifactoriel en interaction avec de probables facteurs environnementaux.
Des antécédents familiaux sont un facteur de risque reconnu pour l’arthrose de la main. Une étude sur les jumeaux a montré que les facteurs génétiques contribuaient jusqu’à 59% du risque de développer une arthrose de la main (19).
Une étude d’association familiale a testé l’hypothèse que la variation génétique au locus ectonucléotide pyrophosphatase phosphodiés-terase 1 (ENPP1), était impliquée dans l’étiologie de l’arthrose de la main et avait souligné qu’il pourrait représenter un facteur génétique important dans la pathogénie de l’arthrose de la main idiopathique (20,21).
Spector et al., ont étudié l’association entre quatre variantes génétiques présumées fonctionnelles du gène Klotho, un gène fortement lié au vieillissement, et l’arthrose de la main dans une population féminine caucasienne. Les résultats suggèrent qu’un variant du gène Klotho est associé avec une susceptibilité pour l’arthrose de la main, en particulier avec la formation d’ostéophytes plutôt que des lésions du cartilage (22).
Growth/differentiation factor 5 (GDF5) et frizzled-related protein (FRZB) ont été proposés comme étant des loci génétiques conférant une susceptibilité à l’arthrose.
Au cours des recherches de gènes de prédisposition à l’arthrose, des études d’association pangénomiques ont permis d’identifier un locus sur le chromosome 2q. Certains chercheurs ont ciblé la région 2q11.2, où la preuve de liaison était la plus forte avec l’arthrose sévère de l’articulation IPD.
L’association de gènes codant pour des cytokines a été rapportée, notamment le cluster de l’IL1, des recherches ont démontré une association entre l’arthrose sévère de la main et le gène de l’IL-1R1, codant le récepteur 1 de l’IL-1. Quatre SNP dans le gène de l’IL-1R1 ont apporté les preuves d’une association entre le gène de l’IL-1R1 et l’arthrose de la main. Cette découverte est pertinente, puisque l’IL-1R1 est le récepteur fonctionnel de l’IL-1, une cytokine connue pour ses propriétés pro-inflammatoires et ses activités cataboliques sur le cartilage articulaire (23).
Actualités thérapeutiques
Le traitement de l’arthrose digitale doit être adapté à chaque cas, puisqu’elle présente un groupe hétérogène sur le plan clinique et radiologique. Selon la localisation, le caractère érosif, le degré de douleur et d’invalidité, différentes approches thérapeutiques peuvent être proposées (24-26).
La prise en charge de l’arthrose digitale est bien codifiée selon les recommandations EULAR actualisées en 2018 (27) :
|
Recommandation n° 1 :
|
L’éducation et information sur les principes ergonomiques, l’entrainement aux activités manuelles et le recours aux aides techniques devraient être proposés à chaque patient.
|
|
Recommandation n° 2 :
|
Le recours aux exercices destinés à améliorer la fonction et la force musculaire, aussi bien qu’à visée antalgique, devrait être envisagé pour tous patients.
|
|
Recommandation n° 3 :
|
Le recours aux orthèses à visée symptomatique devrait être envisagé pour les patients avec rhizarthrose du pouce. Leur utilisation sur le long terme doit être préconisée.
|
|
Recommandation n° 4 :
|
Le recours aux traitements topiques doit être privilégié comparativement aux traitements par voie systémique et ce pour des raisons de tolérance. Les AINS par voie topique sont les traitements locaux pharmacologiques de choix.
|
|
Recommandation n° 5 :
|
Les thérapeutiques orales contre la douleur et notamment les AINS ne devraient être envisagées que sur des périodes de courte durée.
|
|
Recommandation n° 6 :
|
La chondroïtine sulfate peut être proposée aux patients avec arthrose digitale à visée antalgique et amélioration fonctionnelle.
|
|
Recommandation n° 7 :
|
En règle générale, on ne devrait pas recourir aux infiltrations intra-articulaires dans l’arthrose digitale ; mais ceci peut être toutefois envisagé en cas d’arthrose interphalangienne douloureuse.
|
|
Recommandation n° 8 :
|
Les patients avec arthrose digitale ne devraient pas faire l’objet d’un traitement de fond de type conventionnel ou biologique.
|
|
Recommandation n° 9 :
|
Le recours à la chirurgie pourrait être envisagé chez les patients avec atteinte structurale et en situation d’échec aux différentes thérapeutiques symptomatiques antalgiques. La trapézectomie devrait être envisagée chez les patients avec rhizarthrose du pouce et l’arthrodèse ou arthroplastie chez les patients avec arthrose inter phalangienne.
|
|
Recommandation n° 10 :
|
Le suivi à long terme des patients avec arthrose digitale devrait être adapté selon les besoins de chaque patient.
|
Études Cliniques : De nombreux essais cliniques ont été réalisés dans la prise en charge de l’arthrose digitale et de nombreuses molécules ont été étudié, nous rapportons quelques résultats.
Chondroïtine sulfate : une étude clinique randomisée et contrôlée visant à étudier l’efficacité de la chondroïtine sulfate versus placebo a montré que cet AASAL, présente un effet positif significatif sur la perception par le patient de la douleur, de la gêne fonctionnelle et de la réduction de la durée de la raideur matinale(28).
Hydroxychloroquine et méthotrexate : L’arthrose digitale est parfois très douloureuse et invalidante, des traitements de fond de la PR ont été essayés, tel que l’hydroxychloroquine (HCQ) et le méthotrexate. Un essai contrôlé, randomisé, a conclu à l’inefficacité de l’HCQ dans le traitement symptomatique de l’arthrose digitale (29).
Une autre étude a examiné l’effet du méthotrexate sur la douleur ainsi que l’efficacité fonctionnelle et structurale chez les patients atteints d’arthrose digitale érosive, cet essai randomisé contrôlé par placébo, n’a pas montré d’efficacité supérieure du méthotrexate à 10mg/semaine pris pendant 12 mois sur la douleur et la fonctionnalité des doigts mais un effet structural possible (30).
Les résultats de cette étude ne présentent pas le méthotrexate comme une solution thérapeutique intéressante pour améliorer la douleur et la fonctionnalité des doigts dans l’arthrose digitale érosive, toutefois, ils montrent l’intérêt du traiter précocement la maladie pour renforcer le remodelage osseux et ainsi limiter la progression de l’érosion articulaire.
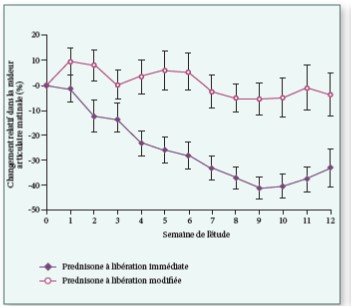
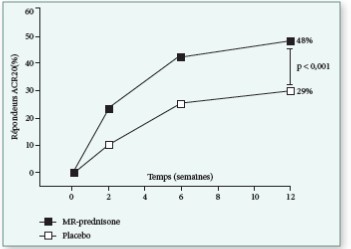
Prednisolone : Un essai randomisé à double insu et contrôlé par placebo (Essai HOPE) a étudié l’efficacité et la tolérance de la prednisolone à faible dose à court terme dans l’arthrose digitale érosive, et a conclu qu’un traitement de six semaines par de la prednisolone orale à 10 mg/j a entraîné une amélioration substantielle mais transitoire des symptômes chez les patients présentant une arthrose douloureuse des mains. Cet essai tend à montrer que l’inflammation locale reste une cible appropriée pour le traitement médicamenteux de l’arthrose digitale érosive (31).
Anti-cytokines : Compte tenu du caractère inflammatoire parfois sévère dans l’arthrose érosive des mains, plusieurs traitements biologiques ont été essayés tels que les anti-TNF alpha, l’anti-IL1, et l’anti-IL6.
L’anti-IL1 alpha/Beta a été étudié dans l’arthrose digitale érosive et n’a pas montré d’efficacité en termes de douleur ou d’évolution structurale, mais une diminution de la CRPus (32).
Les anti-TNF alpha qui ont été essayés dans l’arthrose digitale érosive et inflammatoire sont l’Etanercept et l’Adalimumab.
L’essai EHOA a étudié l’efficacité de l’Etanercept (Embrel®, à 50 mg/semaine pendant 6 mois puis 25mg/semaine sur une durée totale de 1 an) sur l’arthrose digitale érosive, et a montré des résultats négatifs en termes de douleur et d’évolution structurale (33).
Plusieurs essais cliniques ont été publiés avec l’Adalimumab (Humira®), les plus récents ont conclu sur son inefficacité sur la douleur dans l’arthrose digitale réfractaire aux traitements symptomatiques (34), et son inefficacité sur l’évolution structurale dans l’arthrose érosive (35).
L’efficacité du Tocilizumab (Actemra®) a été étudiée sur l’arthrose digitale sévère dans l’essai français TIDOA (2 perfusions de Tocilizumab à 2 mois d’intervalle), et a montré qu’il ne permet pas de soulager significativement les plaintes des patients (36).
La recherche clinique a bien évolué ces dernières années, de nombreuses molécules, s’inspirant du modèle inflammatoire de la polyarthrite rhumatoïde, ont été essayées dans le traitement de l’arthrose digitale et notamment dans sa forme érosive, néanmoins aucune thérapie anti-cytokine n’a montré son efficacité sur l’arthrose digitale.
Conclusion
L’arthrose digitale est une maladie fréquente, douloureuse et invalidante, aux conséquences fonctionnelles souvent sous-estimées.
Nous manquons encore cruellement de solutions thérapeutiques pour l’arthrose digitale, nous devons cependant nous baser essentiellement sur la pratique quotidienne et proposer une véritable prise en charge multimodale aux patients.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Tableau 1 : Critères de classification diagnostique de l’arthrose digitale. Les 10 articulations sélectionnées sont : la trapézo-métacarpienne, les interphalangiennes proximales et distales des 2e et 3e doigts des deux mains. Le diagnostic est positif si les critères 1, 2 et 3 sont présents + le critère 4 ou le critère 5. Sensibilité de ces critères : 92 % ; spécificité : 98 %.
Références
1. Dahaghin S, Bierma-Zeinstra SMA, Ginai AZ, Pols HAP, Hazes JMW, Koes BW. Prevalence and pattern of radiographic hand osteoarthritis and association with pain and disability (the Rotterdam study). Ann Rheum Dis. 2005 May;64(5):682–7.
2. Dahaghin S, Bierma-Zeinstra SMA, Reijman M, Pols HAP, Hazes JMW, Koes BW. Prevalence and determinants of one-month hand pain and hand related disability in the elderly (Rotterdam study). Ann Rheum Dis. 2005 Jan;64(1):99–104.
3. Pereira D, Peleteiro B, Araújo J, Branco J, Santos RA, Ramos E. The effect of osteoarthritis definition on prevalence and incidence estimates: A systematic review. Vol. 19, Osteoarthritis and Cartilage. 2011. p. 1270–85.
4. Kalichman L, Cohen Z, Kobyliansky E, Livshits G. Patterns of joint distribution in hand osteoarthritis: Contribution of age, sex, and handedness. Am J Hum Biol. 2004 Mar;16(2):125–34.
5. Wilder F V., Barrett JP, Farina EJ. Joint-specific prevalence of osteoarthritis of the hand. Osteoarthr Cartil. 2006 Sep;14(9):953–7.
6. Altman R, Alarcon G, Appelrouth D, Bloch D, Borenstein D, Brandt K, et al. The American College of Rheumatology criteria for the classification and reporting of osteoarthritis of the hand. Arthritis Rheum. 1990;
7. Addimanda O, Mancarella L, Dolzani P, Ramonda R, Fioravanti A, Brusi V, et al. Clinical associations in patients with hand osteoarthritis. Scand J Rheumatol. 2012;41(4):310–3.
8. Rees F, Doherty S, Hui M, MacIewicz R, Muir K, Zhang W, et al. Distribution of finger nodes and their association with underlying radiographic features of osteoarthritis. Arthritis Care Res. 2012 Apr;64(4):533–8.
9. Kwok WY, Vliet Vlieland TPM, Rosendaal FR, Huizinga TWJ, Kloppenburg M. Limitations in daily activities are the major determinant of reduced health-related quality of life in patients with hand osteoarthritis. Ann Rheum Dis. 2011 Feb;70(2):334–6.
10. [Role of Obesity in the Development of Osteoarthrosis and Concomitant Diseases] – PubMed [Internet]. Available from: undefined
11. The Association of Obesity with Osteoarthritis of the Hand and Knee in Women: A Twin Study – PubMed [Internet]. Available from: undefined
12. Killock D. Osteoarthritis: The influence of obesity on OA-does size matter or is metabolic dysfunction more important? Vol. 8, Nature Reviews Rheumatology. 2012. p. 61.
13. Dumond H, Presle N, Terlain B, Mainard D, Loeuille D, Netter P, et al. Evidence for a Key Role of Leptin in Osteoarthritis. Arthritis Rheum. 2003 Nov;48(11):3118–29.
14. Teichtahl AJ, Wluka AE, Proietto J, Cicuttini FM. Obesity and the female sex, risk factors for knee osteoarthritis that may be attributable to systemic or local leptin biosynthesis and its cellular effects. Med Hypotheses. 2005;65(2):312–5.
15. Yammani RR, Loeser RF. Extracellular nicotinamide phosphoribosyl-transferase (NAMPT/visfatin) inhibits insulin-like growth factor-1 signaling and proteoglycan synthesis in human articular chondrocytes [Internet]. 2012. Available from: undefined
16. Filková M, Šenolt L, Braun M, Hulejová H, Pavelková A, Šléglová O, et al. Serum hyaluronic acid as a potential marker with a predictive value for further radiographic progression of hand osteoarthritis. Osteoarthr Cartil. 2009 Dec;17(12):1615–9.
17. Choe JY, Bae J, Jung HY, Park SH, Lee HJ, Kim SK. Serum resistin level is associated with radiographic changes in hand osteoarthritis: Cross-sectional study. Jt Bone Spine. 2012 Mar;79(2):160–5.
18. Farooq Rai M, Sandell LJ. Inflammatory Mediators: Tracing Links Between Obesity and Osteoarthritis [Internet]. Vol. 21, Critical Reviews TM in Eukaryotic Gene Expression. 2011. Available from: www.begellhouse.com
19. Spector TD, Cicuttini F, Baker J, Loughlin J, Hart D. Genetic influences on osteoarthritis in women: a twin study.
20. Jakowlev K, Livshits G, Kalichman L, Ben-Asher E, Malkin I, Lancet D, et al. Search for hand osteoarthritis susceptibility locus on chromosome 6p12.3-p12.1. Hum Biol. 2007 Feb;79(1):1–14.
21. E.K. S, I. M, S. D, L. K, N. R, E. K, et al. Association of ENPP1 gene polymorphisms with hand osteoarthritis in a Chuvasha population. Arthritis Res Ther. 2005;
22. Zhang F, Zhai G, Kato BS, Hart DJ, Hunter D, Spector TD, et al. Association between KLOTHO gene and hand osteoarthritis in a female Caucasian population. Osteoarthr Cartil. 2007;
23. Näkki A, Kouhia ST, Saarela J, Harilainen A, Tallroth K, Videman T, et al. Allelic variants of IL1R1 gene associate with severe hand osteoarthritis [Internet]. 2010. Available from: undefined
24. Bliddal H, Leeds AR, Stigsgaard L, Astrup A, Christensen R. Weight loss as treatment for knee osteoarthritis symptoms in obese patients: 1-Year results from a randomized controlled trial. Ann Rheum Dis. 2011 Oct;70(10):1798–803.
25. Richette P, Poitou C, Garnero P, Vicaut E, Bouillot JL, Lacorte JM, et al. Benefits of massive weight loss on symptoms, systemic inflammation and cartilage turnover in obese patients with knee osteoarthritis. Ann Rheum Dis. 2011 Jan;70(1):139–44.
26. Baraf HSB, Gold MS, Petruschke RA, Wieman MS. Tolerability of topical diclofenac sodium 1% gel for osteoarthritis in seniors and patients with comorbidities. Am J Geriatr Pharmacother. 2011 Feb;10(1):47–60.
27. Kloppenburg M, Kroon FPB, Blanco FJ, Doherty M, Dziedzic KS, Greibrokk E, et al. 2018 update of the EULAR recommendations for the management of hand osteoarthritis. Ann Rheum Dis. 2019 Jan 1;78(1):16–24.
28. Gabay C, Medinger-Sadowski C, Gascon D, Kolo F, Finckh A. Symptomatic effects of chondroitin 4 and chondroitin 6 sulfate on hand osteoarthritis: A randomized, double-blind, placebo-controlled clinical trial at a single center. Arthritis Rheum. 2011 Nov;63(11):3383–91.
29. Lee W, Ruijgrok L, Boxma-de Klerk B, Kok MR, Kloppenburg M, Gerards A, et al. Efficacy of Hydroxychloroquine in Hand Osteoarthritis: A Randomized, Double-Blind, Placebo-Controlled Trial. Arthritis Care Res. 2018 Sep 1;70(9):1320–5.
30. Ferrero S, Wittoek R, Allado E, Cruzel C, Fontas E, Breuil V, et al. Methotrexate in Patients with Hand Erosive Osteoarthritis Refractory to Usual Treatments: A Randomized, Double-Blind, Placebo-Controlled Trial. SSRN Electron J. 2020;
31. Kroon F, Kortekaas M, Boonen A, Böhringer S, Reijnierse M, Rosendaal F, et al. OP0180 low-dose prednisolone in patients with hand osteoarthritis (hope): results from a randomized double-blind placebo-controlled trial. In: Oral Presentations [Internet]. BMJ Publishing Group Ltd and European League Against Rheumatism; 2019 [cited 2020 May 29]. p. 165.2-166. Available from: undefined
32. Kloppenburg M, Peterfy C, Haugen I, Kroon F, Chen S, Wang L, et al. OP0168 A phase 2a, placebo-controlled, randomized study of ABT-981, an anti-interleukin-1ALPHA and -1BETA dual variable domain immunoglobulin, to treat erosive hand osteoarthritis (EHOA). In BMJ; 2017. p. 122.1-122.
33. Kloppenburg M, Ramonda R, Bobacz K, Kwok WY, Elewaut D, Huizinga TWJ, et al. Etanercept in patients with inflammatory hand osteoarthritis (EHOA): A multicenter, randomized, double-blind, placebo-controlled trial. Ann Rheum Dis. 2018 Dec 1;77(12):1757–64.
34. Chevalier X, Ravaud P, Maheu E, Baron G, Rialland A, Vergnaud P, et al. Adalimumab in patients with hand osteoarthritis refractory to analgesics and NSAIDs: A randomized, multicenter, double-blind, placebo-controlled trial. Ann Rheum Dis. 2015;
35. Verbruggen G, Wittoek R, Vander Cruyssen B, Elewaut D. Tumor necrosis factor blockade for the treatment of erosive osteoarthritis of the interphalangeal finger joints: A double blind, randomized trial on structure modification. Ann Rheum Dis. 2012;
36. Runhaar J, Rozendaal R, Middelkoop M van, Bijlsma J, Doherty M, Dziedzic K, et al. SAT0523 No treatment effects of oral glucosamine for subgroups of knee and hip osteoarthritis patients; an individual patient data meta-analysis from the oa trial bank. In BMJ; 2017. p. 973.3-974.
Télécharger le PDF de cet article