La BPCO, maladie respiratoire chronique dont le principal facteur de risque est environnemental, constitue une cause importante de morbidité et de mortalité dans le monde (1) et particulièrement dans les pays à revenu faible et intermédiaire (PRFI)
H.H. Cherkaski, R. Benali, Faculté de Médecine – Université Badji Mokhtar Annaba
Date de soumission : 16 Février 2021
RESUMÉ
INTRODUCTION : La broncho-pneumopathie chronique obstructive (BPCO) constitue une préoccupation de santé, particulièrement dans les pays en développement.
OBJECTIF : L’objectif de notre travail est de déterminer la prévalence de la maladie à Elhadjar et de décrire ses facteurs de risque.
METHODE : Une enquête transversale est menée sur un échantillon représentatif de la population âgée de quarante ans et plus, utilisant le protocole Burden Obstructive Lung Disease (BOLD). Le diagnostic et le degré d’obstruction bronchique sont basés sur les critères du Global Initiative for Chronic Obstructive Lung Disease (GOLD). Les taux de prévalence sont estimés selon les poids de sondage.
RESULTATS : La prévalence de la BPCO à Elhadjar est 8.8%, soit 11.9% et 5.7% respectivement chez les hommes et les femmes. Elle augmente significativement avec l’âge (22.5% chez les 70 ans et plus). Seulement 6.8% des patients dépistés sont déjà connus.
Outre l’âge de plus de soixante ans, les facteurs indépendamment associés à l’obstruction bronchique chronique symptomatique sont l’exposition à la biomasse et aux poussières professionnelles, l’insuffisance pondérale, l’asthme, la tuberculose ancienne, les antécédents familiaux de maladies respiratoires chroniques.
CONCLUSION : Les données recueillies constituent un vrai besoin de santé et contribuent à l’élaboration d’un plan d’action local adapté dont les axes centraux sont la prévention et le diagnostic précoce de la BPCO.
Mots clés : BPCO, prévalence, enquête BOLD, facteurs de risque, plan d’action
ABSTRACT
INTRODUCTION: Chronic obstructive pulmonary disease (COPD) is a health concern, particularly in developing countries.
OBJECTIVE: The aim of our study was to determine the prevalence of the disease in El Hadjar and to describe its risk factors.
METHODS: A cross-sectional survey was conducted on a representative sample of the population aged forty and over, using the protocol of Burden of Obstructive Lung Disease (BOLD). The diagnosis and the degree of airway obstruction are based on the criteria of the Global Initiative for Chronic Obstructive Lung Disease (GOLD). Prevalence rates are estimated using the survey weights.
RESULTS: The prevalence of COPD in El Hadjar is 8.8%, or 11.9% and 5.7% respectively in men and women. It significantly increases with age (22.5% in 70 years). Only 6.8% of screened patients are already known.
Besides age of sixty years, the factors independently associated with symptomatic chronic airway obstruction are exposure to biomass and occupational dust, the state of thinness, asthma, old tuberculosis, family history of chronic respiratory diseases.
CONCLUSION: The data collected is a true need for health and contribute to the development of a suitable local action plan whose central axes are prevention and early diagnosis of COPD.
Key words: COPD, prevalence, BOLD survey, health action plan
La BPCO, maladie respiratoire chronique dont le principal facteur de risque est environnemental, constitue une cause importante de morbidité et de mortalité dans le monde (1) et particulièrement dans les pays à revenu faible et intermédiaire (PRFI) (2,3).
En effet, elle est source de handicap médico-social et de demande en soins de santé. C’est aussi une maladie potentiellement mortelle qui occupe, selon l’Organisation Mondiale de la Santé (OMS), le troisième rang des causes de décès annuels (4).
De plus, les coûts financiers qu’elle suscite, notamment dans ses formes évoluées, sont considérables particulièrement dans les PRFI (5).
La mesure de l’ampleur du problème de santé posé par une maladie chronique constitue un des principes fondamentaux de santé publique. C’est ainsi que toute stratégie de prise en charge à l’échelle collective repose sur un préalable indispensable à savoir le calcul du taux de prévalence de la maladie.
Les données de prévalence de la BPCO dans le monde connaissent une grande variabilité en partie en raison des différences méthodologiques des études et des critères diagnostiques utilisés.
Dans l’optique de rationnaliser la méthode d’estimation de la prévalence, un groupe d’experts a élaboré en 2005 un protocole standardisé, valide et faisable, basé sur des critères diagnostiques objectifs de la BPCO. Ainsi, une enquête populationnelle internationale a pu être menée à travers le monde : « Burden Obtructive Lung Disease Inititative » (BOLD) à laquelle participe le service de pneumo-phtisiologie de la Faculté de Annaba (6).
Dans le monde, la prévalence est estimée entre 4 et 15% (7-10) et plusieurs facteurs laissent envisager une augmentation sans cesse croissante : allongement de l’espérance de vie, pyramide des âges, de la consommation de tabac fumé, pollution (11,12).
Peu de données épidémiologiques fiables sont disponibles en Algérie où les enquêtes de prévalence de la BPCO ont utilisé des méthodologies diverses rendant difficile toute comparaison ou extrapolation (13-15).
Qu’en est-il de la BPCO dans notre région, caractérisée par un axe routier développé, une industrialisation importante, un tissu social diversifié (urbain, semi-urbain, rural) ?
Aussi, nous nous sommes proposé de réaliser une étude dont le but est de déterminer la prévalence et les principaux déterminants de la BPCO dans la commune d’El-Hadjar. La perspective étant de mettre en place un plan d’action sanitaire local efficient.
Les objectifs de la présente étude sont doubles :
- Estimer la prévalence de la BPCO dans la population de la commune d’El-Hadjar (Annaba) selon le protocole de l’enquête internationale BOLD,
- Identifier ses facteurs de risque.
Le protocole de l’enquête BOLD a été adapté aux conditions socio-culturelles locales notamment pour la visite des ménages et le contenu des questionnaires (6).
Il s’agit d’une enquête auprès des ménages, réalisée sur un échantillon randomisé de la population de la commune d’El-Hadjar.
La commune d’El-Hadjar, distante de 12 Km du chef-lieu de wilaya avec 37.364 habitants (16) et une superficie de 63 km², est un véritable pôle industriel. Y sont implantés un complexe sidérurgique, un complexe d’engrais phosphatés et une zone d’activité industrielle.
L’étude s’est déroulée du 01 Mars au 30 Juin 2012, soit sur une durée de quatre mois.
- Échantillonnage de la population
Nous avons opté pour un échantillonnage aléatoire en grappes à trois degrés.
- Recrutement des participants
Au niveau de chaque ménage randomisé, tous les individus âgés de 40 ans et plus ont été invités à participer à l’étude.
- Critères de non inclusion
L’individu sélectionné ne pouvait prendre part à l’étude lorsqu’il :
- Refusait d’y participer,
- Présentait une contre-indication médicale à la spirométrie : chirurgie récente, cardiopathie aiguë, problème ophtalmologique (décollement rétinien par exemple), dernier trimestre de grossesse, tuberculose évolutive sous traitement,
- N’était pas en mesure de réaliser des manœuvres spirométriques correctes.
Pour le diagnostic de BPCO, nous avons utilisé la définition spirométrique du GOLD (17).
Ainsi, tout participant présentant à la spirométrie un rapport un Déficit Ventilatoire Obstructif (DVO) non ou peu réversible (ou persistant) après bronchodilatation aux Bêta2-mimétiques inhalés à courte durée d’action était considéré comme porteur de BPCO. Le DVO étant défini par un rapport VEMS/CVF < 0,7.
Selon le GOLD, le degré de sévérité du DVO était évalué par la valeur du VEMS post-bronchodilatation par rapport à sa valeur théorique (17). Quatre stades ont été individualisés (Tableau 1).
Tableau 1 :Classification de la sévérité du Déficit ventilatoire obstructif selon le GOLD(17)
|
STADE
|
VEMS1 / CVF2
post-bronchodilatation
|
VEMS post-bronchodilatation
% VP3
|
|
Stade 1
|
≤ 0.70
|
VEMS ≥ 80
|
|
Stade 2
|
50 ≤ VEMS < 80
|
|
Stade 3
|
30 ≤ VEMS < 50
|
|
Stade 4
|
< 30
|
1. Volume Expiratoire maximal en une Seconde ; 2. Capacité Vitale Forcée ; 3. En pourcentage de la valeur théorique (ou prédite).
- Facteurs de risque de BPCO
Nous avons relevé par questionnaires les principaux facteurs de risque auxquels le participant était exposé : Tabagisme actif et passif, expositions domestique et professionnelle aux toxiques inhalés, niveau d’instruction, antécédents d’asthme ou de tuberculose pulmonaire.
Les questionnaires, au nombre de quatre, étaient inspirés des questionnaires validés et standardisés BOLD (6), traduits et adaptés à notre contexte socio-culturel. Ils étaient administrés en arabe dialectal par un enquêteur.
- Questionnaire de spirométrie : contre-indication éventuelle, prise de médicaments, données anthropométriques et cliniques, qualité des manœuvres spirométriques, éventuels effets indésirables.
- Questionnaire principal : données sociodémographiques, symptômes respiratoires, exposition aux facteurs de risque, antécédents respiratoires et comorbidités.
- Questionnaire professionnel : profession actuelle et antécédents professionnels, exposition professionnelle, impact des problèmes respiratoires éventuels.
- Questionnaire d’exposition aux biocombustibles solides domestiques.
Nous avons utilisé un spiromètre portable électronique type EasyOne ndd, quotidiennement étalonné. Les mesures étaient effectuées selon les standards de l’ATS/ERS (18). Pour que nos résultats soient comparables à ceux des autres études internationales, nous avons utilisé les valeurs de référence de la troisième enquête du National Health and Nutrition Examination, NHANES III (19). Le contrôle de qualité des mesures spirométriques était assuré par le Centre de Coordination BOLD à Londres selon les critères d’acceptabilité et de reproductibilité de l’ATS/ERS (18).
Des sessions de formation des enquêteurs (techniciens) d’une durée de cinq jours ont été assurées par l’enquêteur principal, avec le concours d’un épidémiologiste et d’un fonctionnaliste respiratoire. La collecte standardisée des données des questionnaires et surtout la réalisation des mesures spirométriques constituaient l’objectif principal de cette formation.
Notre protocole a été soumis au Comité d’Éthique de la Faculté de Médecine d’Annaba qui a accordé son approbation écrite. Nous avons assuré la confidentialité des données et des mesures. Enfin, chaque participant devait accorder son consentement éclairé.
- Déroulement de l’enquête proprement-dite
Le recueil des données du participant s’est effectué selon les étapes suivantes :
- Réponse au questionnaire de spirométrie et mesures anthropométriques
- Si pas de contre-indication, mesures spirométriques pré-bronchodilatation
- Administration de Salbutamol inhalé
- Réponse au questionnaire principal
- Mesures spirométriques post-bronchodilatation
- Réponse au questionnaire biomasse
- Réponse au questionnaire professionnel, si le participant avait ou avait eu un emploi
La durée moyenne de la collecte de données était de 50 à 90 minutes par participant. Elle dépendait en grande partie de son âge et de son niveau d’instruction.
Les fiches de recueil des données ont été saisies sur le logiciel EPI-INFO 6.04d. La phase d’analyse a été effectuée avec le logiciel Stata 9.2 selon la procédure “svy” qui permet de prendre en compte les échantillonnages complexes. Les données de prévalence ont été pondérées selon l’âge et le sexe.
Les analyses multivariées pour déterminer les facteurs de risque potentiels associés au diagnostic de BPCO chez les participants à l’étude, ont été effectuées à l’aide de modèles de régression logistique.
Huit cent quatre-vingt dix individus, soit 448 femmes et 442 hommes, ayant répondu aux quatre questionnaires et réalisé des mesures spirométriques considérées comme exploitables, ont constitué l’échantillon représentatif de la population d’El-Hadjar.
- Description de la population étudiée (Tableau 1)
L’âge moyen était de 54,0 (11) ans et ne différait pas significativement entre les deux sexes. Le participant le plus âgé avait 87 ans.
Tableau 1 : Caractéristiques sociodémographiques de la population
|
|
Total
n=890
|
Hommes
n=442
|
Femmes
n=448
|
p
|
|
Age (ans)1
– 40-49
– 50-59
– 60-69
– 70+
|
42.0 (1.5)
31.4 (1.6)
15.6 (1.1)
10.9 (1.5)
|
41.4 (2.4)
32.2 (2.4)
15.5 (1.5)
10.9 (2.6)
|
42.6 (2.5)
30.7 (2.2)
15.8 (1.7)
10.9 (2.6)
|
–
|
|
Scolarité1
Années d’études2
– Primaire
– Moyen
– Secondaire
– Form. prof.
– Université
– Aucune
|
8.1 (5.3)
23.3 (1.5)
23.8 (1.4)
12.2 (1.1)
13.3 (1.2)
7.1 (0.8)
20.3 (1.6)
|
9.2 (5.3)
21.1 (2.0)
26.7 (2.1)
9.6 (1.4)
20.0 (1.9)
10.3 (1.4)
12.3 (1.7)
|
7.0 (5.0)
25.5 (2.2)
21.0 (1.9)
14.9 (1.7)
6.6 (1.1)
3.9 (0.9)
28.2 (2.6)
|
<10-4
|
|
Profession1
– Oui
– Non
|
65.6 (1.7)
34.4 (1.7)
|
99.5 (0.4)
0.5 (0.4)
|
31.8 (2.3)
68.2 (2.6)
|
<10-4*
|
|
Nombre de personnes sous le même toit2
|
5.2 (0.07)
|
5.3 (0.1)
|
5.2 (0.1)
|
0.87
|
|
Nombre de pièces2
|
3.1 (0.03)
|
3.1 (0.04)
|
3.1 (0.04)
|
0.69
|
|
Confort domestique1
– Électricité
– Eau courante
– Réfrigérateur
– Télévision
|
100
96.1 (0.6)
98.8 (0.4)
99.6 (0.2)
|
100
95.9 (0.9)
98.9 (0.5)
99.5 (0.3)
|
100
96.4 (0.8)
98.8 (0.5)
99.6 (0.3)
|
1
0.70
0.77
0.90
|
1. Estimation pondérée, en% et (erreur-type) 2. Moyenne et (écart-type)
La prévalence estimée des fumeurs et ex-fumeurs chez la population d’El-Hadjar de 40 ans et plus étaient respectivement de 16,7% et 21,9% (Tableau 2). Ainsi, 38,6% étaient ou avaient été tabagiques. En termes de quantité cumulée de tabac fumé ; 44,1% fumaient ou avaient fumé plus de 19 paquets-année (PA). Par ailleurs, presque tous les tabagiques étaient des hommes (76,8% vs 0,6%) et fumaient exclusivement des cigarettes à raison de 26,9 PA en moyenne.
Tableau 2 : Statut tabagique selon l’âge1
|
|
Total
|
40-49
|
50-59
|
60-69
|
70+
|
p
|
|
Fumeurs
|
16.7 (1.3)
|
17.6 (2.0)
|
17.1 (2.4)
|
16.7 (2.7)
|
12.6 (4.1)
|
0.35
|
|
Ex-fumeurs
|
21.9 (1.4)
|
19.1 (2.0)
|
22.9 (2.7)
|
21.6 (3.0)
|
30.0 (6.2)
|
1
|
|
Non-fumeurs
|
61.4 (1.7)
|
63.3 (2.4)
|
60.1 (3.0)
|
61.7 (3.7)
|
57.3 (7.3)
|
0.17
|
1. Estimation pondérée, en% et (erreur-type)
- Selon l’âge et le sexe (Tableau 3)
La prévalence de la BPCO selon les critères diagnostiques du GOLD était de 8.8% pour les stades 1 et plus. Elle était significativement plus élevée chez les hommes que chez les femmes avec respectivement avec respectivement 11,9% vs 5,7% et avait tendance à augmenter avec l’âge notamment chez les hommes.
Tableau 3 : Prévalence de la BPCO selon l’âge et le sexe
|
|
Total
|
40-49
|
50-59
|
60-69
|
70+
|
p*
|
|
Hommes
|
11.9 (1.6)
|
4.6 (1.5)
|
6.6 (2.3)
|
28.4 (4.6)
|
31.7 (7.9)
|
<10-4
|
|
Femmes
|
5.7 (1.3)
|
3.9 (1.3)
|
6.4 (2.0)
|
4.0 (2.3)
|
13.5 (8.9)
|
0,266
|
|
Total
|
8.8 (1.0)
|
4.2 (1.0)
|
6.5 (1.5)
|
16.1 (2.7)
|
22.5 (6.1)
|
<10-4
|
Estimation pondérée, en% et (erreur-type) *p for trend
- Selon le statut tabagique
Chez les fumeurs et ex-fumeurs, la prévalence de la BPCO selon les critères GOLD était respectivement de 16,9% et 10,8%. Elle était de 5,9% chez les non tabagiques, soit 6,4% chez les hommes et 5,7% chez les femmes.
Autrement dit 59,0% des individus ayant les critères spirométriques de BPCO étaient ou avaient été tabagiques ; soit 32,2% de fumeurs et 26,8% d’ex-fumeurs.
La prévalence de la BPCO stade 1+ chez les non-fumeurs était de 5,9%, pratiquement identiques dans les deux sexes (Tableau 4).
Tableau 4 : Prévalence de la BPCO selon le statut tabagique et le sexe
| |
Total
|
Non-fumeurs
|
Fumeurs
|
Ex-fumeurs
|
p
|
|
Hommes
|
11.9 (1.6)
|
6.4 (2.4)
|
17.1 (3.1)
|
10.8 (2.3)
|
0,011
|
|
Femmes
|
5.7 (1.3)
|
5.7 (1.4)
|
–
|
–
|
|
Total
|
8.8 (1.0)
|
5.9 (1.2)
|
16.9 (3.0)
|
10.8 (2.3)
|
<10-4
|
Estimation pondérée, en% et (erreur-type)
La prévalence de la BPCO augmentait avec le nombre cumulé de PA fumé (Tableau 5).
Tableau 5. Prévalence de la BPCO stade 1 et plus selon le sexe et le nombre de PA
|
Sexe
|
PA
|
p*
|
|
0-9
|
10-19
|
20+**
|
|
Hommes
|
6.1 (3.5)
|
6.7 (2.8)
|
18.8 (2.8)
|
<10-4
|
|
Femmes
|
–
|
–
|
–
|
|
Total
|
6.1 (3.4)
|
6.6 (2.7)
|
18.7 (2.8)
|
<10-4
|
PA : Nombre de paquets-année – Pas de cas observés. * p for trend ; ** 20 PA et plus
- Stades de sévérité de l’obstruction bronchique persistante
La prévalence du stade 2 GOLD était la plus élevée avec un taux de 4,8%. Le faible effectif du stade 4 GOLD a justifié son regroupement avec le stade 3. La prévalence de ce stade de sévérité 3 et plus est restée toutefois basse, de l’ordre de 1,5%, (Tableau 6).
Pour chaque stade de sévérité, il n’a pas été constaté de différence selon l’âge.
Tableau 6: Prévalence de la BPCO selon le stade de sévérité GOLD par âge
| |
Total
|
40-49
|
50-59
|
60-69
|
70+
|
p
|
|
Stade 1
|
2.5 (0.1)
|
0.8 (0.5)
|
2.3 (0.9)
|
3.6 (1.3)
|
7.9 (4.1)
|
0,11*
|
|
Stade 2
|
4.8 (0.8)
|
2.7 (0.8)
|
3.0 (1.1)
|
9.6 (2.2)
|
11.7 (4.6)
|
0,13*
|
|
Stade 3+
|
1.5 (0.4)
|
0.8 (0.5)
|
1.1 (0.7)
|
2.9 (1.2)
|
2.9 (2.0)
|
0,12*
|
* Test de Fisher exact
- Antécédents de maladie respiratoire chronique
La notion de maladie respiratoire chronique connue était nettement plus fréquente chez les individus ayant présenté les critères spirométriques de BPCO stade 1+. Parmi eux ; 25,5% étaient étiquetés asthmatiques, alors que seuls 6,8% étaient déjà connu porteur de BPCO avant l’enquête (Tableau 7).
Tableau 7 : Fréquence des antécédents de maladies respiratoires chroniques chez les patients BPCO stade 1+ GOLD
| |
Total
|
Non BPCO
|
BPCO stade 1+
|
p
|
|
Asthme
|
8.0 (0.9)
|
6.3 (0.8)
|
25.5 (5.7)
|
<10-3
|
|
Emphysème
|
0.2 (0.1)
|
0.1 (0.1)
|
2.0 (1.4)
|
0,02**
|
|
BC*
|
1.1 (0.4)
|
0.2 (0.2)
|
10.8 (3.6)
|
<10-3
|
|
BPCO
|
0.9 (0.3)
|
0.3 (0.2)
|
6.8 (3.0)
|
<10-3
|
* Bronchite chronique ** Test de Fischer exact
- Symptômes respiratoires chroniques (Tableau 8)
Chez les individus étiquetés BPCO, la prévalence des symptômes respiratoires chroniques et des symptômes évocateurs de BC augmentait avec le stade de sévérité GOLD.
Ainsi, 43,8% des individus BPCO étaient tout à fait asymptomatiques, ils étaient 76,8% (9.7) au stade 1 et 40,2% (8.3) au stade 2 ; alors que la totalité des patients au stade 3 et plus étaient symptomatiques.
Parmi les symptômes les plus fréquemment signalés, quel que soit le stade de sévérité DVO, deux d’entre eux prédominaient : la dyspnée d’effort et les sifflements thoraciques expiratoires.
D’une manière générale, un tiers des individus dépistés porteurs d’une obstruction bronchique non réversible, avait bénéficié de test spirométrique auparavant (32,8%).
Tableau 8 : Fréquence des symptômes respiratoires chroniques chez les patients BPCO selon le stade de sévérité GOLD
| |
BPCO
|
Selon la classification GOLD
|
p value
|
|
Stade 1
|
Stade 2
|
St. 3+
|
|
Toux chronique
|
12.3 (3.8)
|
5.6 (5.4)
|
13.7 (5.4)
|
19.1 (10.3)
|
<10-3
|
|
Expectoration
|
12.7 (3.9)
|
5.6 (5.4)
|
14.5 (5.6)
|
19.1 (10.3)
|
<10-3
|
|
Toux + Expectoration Chroniques, BC
|
15.8 (4.3)
|
5.6 (5.4)
|
17.3 (6.1)
|
26.8 (12.5)
|
<10-3
|
|
Sifflements
|
43.4 (6.0)
|
13.7 (7.6)
|
46.1 (8.1)
|
85.1 (8.3)
|
<10-3
|
|
Dyspnée
|
38.1 (5.8)
|
9.6 (6.8)
|
36.2 (7.7)
|
93.8 (6.7)
|
<10-3
|
|
Asymptomatiques respiratoires
|
43.8 (6.3)
|
76.8 (9.7)
|
40.2 (8.3)
|
–
|
|
|
Spirométrie Ant.
|
32.8 (6.0)
|
4.0 (4.0)
|
37.9 (8.3)
|
65.4 (12.5)
|
<10-3
|
- Comorbidités (Tableau 9).
L’hypertension artérielle constituait la première comorbidité chez les patients BPCO avec 34,4%, loin devant le diabète type II.
La proportion de la tuberculose pulmonaire était de 9.1% parmi les individus BPCO stade 1+ et de 12.7% des stades 2+. Tous les cas avaient été déclarés guéris avant notre enquête.
Tableau 9. Fréquence des comorbidités chez les patients BPCO stade 1+ et stade 2+ GOLD
| |
GOLD 1+
n=79
|
GOLD 2+
n=58
|
p
|
|
Cardiopathie
|
7.3 (2.6)
|
6.6 (2.9)
|
0,85
|
|
HTA1
|
34.4 (6.0)
|
35.4 (6.7)
|
0,80
|
|
Diabète
|
14.0 (5.0)
|
12.3 (4.6)
|
0,75
|
|
AVC2
|
0.8 (0.8)
|
1.1 (1.1)
|
|
|
Antécédents de tuberculose3
|
9.1 (3.4)
|
12.7 (4.7)
|
0,74
|
- Facteurs de risque (Tableau 10)
Les analyses de régression logistique multivariable ont montré qu’un âge de 60 ans et plus, une IMC inférieure à 18 kg/m2, des antécédents d’asthme ou de tuberculose pulmonaire étaient significativement associés au diagnostic de BPCO stade 2+ GOLD.
Tableau 10 : Analyse de régression brute et ajustée des facteurs de risque (variables catégorielles) de BPCO stade 2+ GOLD
|
Variables
|
OR ajusté
|
IC 95%
|
p-value
|
|
Sexe
Hommes
Femmes
|
2.53
1.0 Réf.
|
0.77-8.25
|
0.124
|
|
Age, années
40-49
50-59
60-69
70+
|
1.0 Réf.
1.29
6.28
6.74
|
0.49-3.42
2.38-16.60
1.92-23.62
|
0.604
<10-4
0.003
|
|
Niveau d’instruction
– Secondaire et plus
– Aucun et primaire
|
1.0 Réf.
1.26
|
0.61-2.59
|
0.529
|
|
Statut tabagique (2)
– Non-fumeurs
– Fum. et ex-Fum.
|
1.0 Réf.
1.91
|
0.52-7.02
|
0.327
|
|
Nombre de PA
– Non-fumeurs
– 0-9
– 10-20
– 20+
|
1.0 Réf.
0.32
–
1.37
|
0.05-1.88
–
0.49-3.85
|
0.205
–
0.549
|
|
IMC, Kg/m2
– <18
– 18-24.9
– 25-29.9
– ≥30
|
6.58
1.0 Réf.
0.98
0.60
|
1.88-23.00
0.47-2.02
0.23-1.54
|
0.003
0.953
0.286
|
|
Exposition professionnelle,
– Oui
– Non
|
0.86
1.0 Réf.
|
0.37-1.99
|
0.726
|
|
Exposition régulière à la Biomasse (cuisine et/ou chauffage)
– Oui
– Non
|
0.83
1.0 Réf.
|
0.37-1.85
|
0.653
|
|
Notion d’asthme
– oui
– non
|
20.19
1.0 Réf.
|
8.27-49.24
|
<10-4
|
|
Antécédents de tuberculose
– oui
– non
|
5.04
1.0 Réf.
|
1.47-17.28
|
0.001
|
|
Antécédents familiaux de maladie respiratoire chronique
– Oui
– Non
|
3.23
1.0 Réf.
|
1.21-8.58
|
0.019
|
Le taux de prévalence de la BPCO chez la population d’El-Hadjar (Annaba) âgés de 40 ans et plus (≥40 ans) est de 8,8% pour le stade 1 et plus (1+) et de 6,3% pour le stade 2 et plus (2+) de la classification GOLD 2006.
Les hommes sont plus fréquemment touchés avec un sex-ratio à 2,4, ainsi que les personnes âgées de 60 ans et plus (≥60 ans).
Nous pouvons considérer la BPCO comme une affection prévalente à El-Hadjar. Les résultats illustrent l’ampleur de la charge que cette pathologie posera dans un avenir proche au vu du vieillissement de la population. En effet, l’augmentation de l’espérance de vie expose les personnes les plus âgées aux maladies chroniques dont la BPCO (20).
De plus, la multiplication des facteurs environnementaux, générés par l’urbanisation accélérée et incontrôlée et l’implantation des industries de transformation dans la région d’Annaba et particulièrement à la commune d’El-Hadjar, a probablement favorisé le développement de maladies non spécifiques des voies aériennes (21).
En Algérie, seule une enquête de prévalence basée sur des critères spirométriques a été publiée en 2011. Elle a été réalisée auprès des ménages de la wilaya d’Alger sur la base d’un questionnaire et des tests fonctionnels respiratoires. Elle porte sur un échantillon de 1.800 individus de 21 ans et plus. Le diagnostic de BPCO, utilisant la valeur seuil de 0.70 du rapport VEMS/CVF mesuré en post-bronchodilatation, est posé en milieu hospitalier. La prévalence de la BPCO chez les 40 ans et plus est de l’ordre de 9,2% (14). Cette enquête, qui présente des différences méthodologiques avec notre travail, a permis toutefois de rapporter un chiffre de prévalence pour la wilaya d’Alger.
Au Maghreb, deux enquêtes transversales BOLD ont été menées à Sousse (Tunisie) (23) et à Fès (Maroc) (24). Les taux de prévalence enregistrés dans ces deux villes, ainsi que leurs tendances selon le sexe et l’âge, sont assez proches de ceux d’El-Hadjar avec :
- 7,8% et 12,6% respectivement à Sousse et Fès (vs 8,8% El-Hadjar) pour le stade 1+;
- 4,2% et 7,9% respectivement à Sousse et Fès (vs 6,3% El-Hadjar) pour le stade 2+.
Ces résultats pourraient être expliqués non seulement par la méthodologie et des critères de contrôle de qualité des mesures spirométriques standardisés au niveau des trois sites, mais aussi par les similitudes socio-culturelles et environnementales des populations étudiées.
Sur le plan mondial, il existe une grande variabilité de la prévalence de la maladie, quel que soit la situation géographique et le statut économique des pays (25-27), allant à titre d’exemple de 0,2% au Japon à 37% aux États-Unis selon une méta-analyse des données épidémiologiques publiées (28).
De plus, l’étude PLATINO, dont la méthodologie est pratiquement similaire à celle de la présente enquête, rapporte des estimations variant de 7,8% à 19,7% dans cinq pays d’Amérique Latine (29).
Dans une autre étude publiée en 2015, les auteurs rassemblent les données de quatre études internationales (BOLD, PATINO, EPI-SCAN, PREPOCOL) au niveau de 44 sites (27 pays) chez une population de 30.874 adultes ≥ 40 ans. La prévalence globale de la BPCO définie par le rapport VEMS/CVF < LIN en post-bronchodilatation est de 9,7%, variant de 3,6% (Barranquilla, Colombie) à 19,0% (Le Cap, Afrique du Sud) (30). Cette hétérogénéité des résultats est due en partie aux différentes méthodologies utilisées.
Toutefois, l’étude BOLD (7) démontre qu’en dépit d’une conduite méthodologique standardisée et une définition spirométrique de la BPCO standardisée, les taux de prévalence de la BPCO dans 12 pays demeurent très variables. D’autres études internationales confirment cette disparité géographique des taux de prévalence de la BPCO (29,31). Les facteurs environnementaux, le niveau du tabagisme des populations locales, la prédisposition génétique, la situation épidémiologique (cas de l’Afrique du Sud où tuberculose et pneumoconioses sont prévalentes) seraient autant de facteurs de risque différents (7,8,10) (Tableau 56).
A El-Hadjar, la prévalence de la BPCO augmente avec l’âge, dans les deux sexes, passant de 4,2% pour les 40-49 ans à 22,5% pour les 70 ans et plus.
De nombreuses enquêtes épidémiologiques ont retrouvés des résultats identiques (7,32,33). Selon les données épidémiologiques prédictives, l’augmentation de la prévalence de la BPCO dans le monde serait bien plus le fait du vieillissement de la population (allongement de l’espérance de vie) que de l’augmentation de la prévalence du tabagisme (33).
Cette transition démographique s’accompagne d’une transition épidémiologique et incite les professionnels et les décideurs politiques chargés de la santé à un changement dans le mode de pensée afin d’identifier les besoins et de s’adapter aux nouvelles exigences de santé publique (21).
Notre étude montre que la BPCO est deux fois plus prévalente chez les hommes que chez les femmes (11,9% vs 5,7%). Cette prédominance masculine est probablement le fait du tabagisme exclusivement masculin et d’une consommation importante.
Des constatations similaires sont relevées aussi bien dans les études multicentriques internationales (7,34) qu’au niveau local (Alger) (14) et régional (Sousse, Fès) (23,24).
En revanche, il est noté à El-Hadjar une prévalence de la BPCO chez la femme nettement plus élevée qu’à Alger et Sousse (El-Hadjar 5,7% vs Alger 2,5%, Sousse 1,9%) malgré la quasi-absence de tabagisme féminin (proportion de femmes tabagiques : El-Hadjar 0,4% vs Alger 5,8%, Sousse 5,2%).
Cette observation laisse supposer l’existence dans notre région d’autres facteurs exposants notamment environnementaux. En effet, jusqu’aux années 1970, la région d’El-Hadjar était totalement rurale et agricole. La plupart des femmes aujourd’hui âgées de 40 ans et plus ont été exposées dans leur jeunesse à la fumée de la biomasse utilisée pour la cuisson et/ou le chauffage.
Le fait qu’à exposition égale au tabagisme et autres aérocontaminants, les femmes seraient plus susceptibles de développer une BPCO que les hommes est toujours controversé (35).
- Sévérité du DVO persistant
La prévalence du stade GOLD 1 à El-Hadjar est plus faible que celle retrouvée dans les douze sites de l’étude BOLD (7). Ceci est probablement dû au fait que notre population soit relativement plus jeune avec une moyenne d’âge à 54 ans. En effet, le seuil fixe du rapport VEMS/CVF, utilisé dans notre étude comme critère diagnostique de BPCO, diminue physiologiquement avec l’âge. Il pourrait en résulter une surestimation du diagnostic chez les personnes d’âge avancé (36,37). Dans une perspective de santé publique, la charge sociale et économique de la BPCO est modeste au stade 1 et augmente progressivement avec la sévérité de la maladie (38).
Les stades GOLD 2 et 3+ sont plus fréquents que dans l’enquête menée à Alger (El-Hadjar 4,8% et 1,5% vs 2,7% et 0,5% Alger) (14), qui a utilisé les mêmes équations de références européennes (39). Par ailleurs, dans l’étude tunisienne, où la spirométrie a été réalisée dans les mêmes conditions qu’à El-Hadjar et soumise au même contrôle de qualité rigoureux, la prévalence du stade 2 est identique à celle de notre enquête (El-Hadjar 4,8% vs Sousse 4,2%) et légèrement différents pour le stade 3+ (El-Hadjar 1,5% vs Sousse 0%) (23).
Notre travail met en exergue le sous-diagnostic dont souffre la BPCO à El-Hadjar. En effet, seuls 6,8% des cas dépistés étaient déjà connus et 32,8% avaient bénéficié d’une spirométrie auparavant (Tableaux 7 et 8). Nous évoquons ci-dessous les raisons qui nous semblent l’expliquer :
- Une expression clinique pauvre : seuls 56,1% des patients au stade 1+ GOLD ont au moins un symptôme pendant au moins trois mois par an en dehors de toute atteinte virale saisonnière, alors que 100% des stades 3+ GOLD sont symptomatiques. Aussi, compte tenu de la prévalence relativement faible et de la valeur prédictive négligeable des symptômes, l’approche diagnostique la plus efficiente serait de rechercher un DVO persistant chez les personnes considérées comme « à risque ».
- Une sous-utilisation de la spirométrie : La prescription de cet examen ne parait pas fréquente même pour les patients symptomatiques respiratoires (100% des stades 3+ sont symptomatiques et parmi eux 93,8% souffrent d’une dyspnée d’effort). De nombreuses études à travers le monde mettent en évidence le recours insuffisant à la spirométrie dans le diagnostic des maladies respiratoires chroniques dont la BPCO (30,40). Ceci est d’autant plus vrai que les principales recommandations admettent que l’examen spirométrique reste un élément diagnostique indispensable.
- Un sous-diagnostic : Nos résultats confirment ceux de la quasi-totalité des études concernant le sous-diagnostic de la BPCO (14,23,24,41). Les raisons en sont variées et souvent liées. Les plus communes semblent être: la pauvreté et la banalisation des signes cliniques, la méconnaissance de la maladie, la sous-prescription de la spirométrie en pratique courante.
Deux points d’ordre méritent d’être soulevés quant au diagnostic de la BPCO :
Celui-ci est mis en évidence lorsque le rapport VEMS/CVF, mesuré en post-bronchodilatation, est diminué. La problématique réside dans la définition de cette « diminution ». Il n’y a pas à ce jour d’unanimité sur le seuil limite d’anormalité à considérer : seuil fixe de 0,70 (GOLD) (4), limite inférieure de la normale (ATS/ERS) (42) ou Z-score (ERS/GLI) (43).
Nous pouvons dire qu’actuellement deux types de définitions caractérisent le DVO:
- Une définition opérationnelle, représentée par un rapport VEMS/CVF < 0,70 ; dont le but principal est le dépistage et la détection précoce du syndrome fonctionnel obstructif. Cette définition, même si elle manque de fiabilité chez les personnes âgées, a le mérite d’être simple, facilement applicable par les professionnels de santé, et indépendante des valeurs de références.
- Une définition physiologique, représentée par un rapport VEMS/CVF < LIN, plus fiable sur le plan épidémiologique car elle réduit le risque d’erreur diagnostique chez certains groupes de la population (personnes âgées). Toutefois, dans les pays à revenu bas ou intermédiaire, la disponibilité plus qu’insuffisante des spiromètres électroniques dotés d’un logiciel adéquat, leur coût relativement élevé et le manque de personnel qualifié constituent un véritable obstacle à leur utilisation large.
Par ailleurs, nous avons appliqué le protocole BOLD (rapport < 0,7) pour avoir des résultats comparables à ceux des autres sites participants. Toutefois, nous adhérons en partie aux arguments des partisans de la LIN, notamment en ce qui concerne la précision du diagnostic.
Il nous semble que l’approche pratique de privilégier et d’implanter les tests spirométriques et la formation des personnels de santé constituent des priorités plus importantes que les subtilités épidémiologiques (44).
Lors de l’élaboration et de l’implantation du protocole BOLD en 2005, le diagnostic et le degré de sévérité de la BPCO, selon le GOLD, était exclusivement basés sur des critères spirométriques avec respectivement le rapport VEMS/CVF et le VEMS mesurés en post-bronchodilatation. L’approche diagnostique des principales bronchopathies chroniques (BPCO, asthme) était alors très bien individualisée.
Depuis 2011 (45), le GOLD associe de plus en plus, dans ses recommandations, des éléments cliniques (dyspnée, fréquence d’exacerbation), au critère fonctionnel rendant le diagnostic et surtout l’évaluation de la BPCO plus « humanisé ». Le DVO persistant pris seul définit maintenant le concept d’obstruction bronchique chronique (Chronic Airflow Obstruction pour les anglo-saxons) dont l’approche est intégrative.
- Facteurs de risque identifiés
- Antécédents d’asthme bronchique
20,3% des participants avec DVO persistant rapportent la notion d’asthme connu. Ces deux pathologies peuvent partager le même tableau clinique et le même profil fonctionnel respiratoire. Les patients pourraient alors être étiquetés asthmatiques d’autant plus que, comme mentionné plus haut, le recours à la spirométrie n’est pas tout à fait intégré dans la pratique courante (30,40).
D’un autre côté, étant largement inconnue du public et méconnue d’une grande partie des professionnels de santé, la dénomination « asthme » est parfois attribuée à tort à la BPCO, car elle désigne une maladie plus connue et plus redoutée dans l’esprit collectif. Ainsi, toute dyspnée, intermittente ou permanente, est assimilée à de l’asthme surtout si elle s’accompagne de sifflements. Cet état de fait pourrait expliquer le taux d’individus rapportant, à tort ou à raison, le diagnostic d’asthme dans notre enquête.
Toutefois, il a été montré dans de nombreuses études menées à travers le monde, que l’asthme constituait un facteur de risque significatif de BPCO (47,48).
Aussi, en l’absence de plus d’informations cliniques, thérapeutiques et évolutives nous ne sommes pas en mesure d’interpréter avec précision nos résultats.
Dans notre étude, la proportion des personnes avec obstruction bronchique chronique est d’autant plus élevée que l’IMC est plus bas. De nombreuses études transversales, dont les études BOLD et PLATINO, rapportent également cette tendance, avec une prévalence de la BPCO plus élevée dans le groupe classé en état d’insuffisance pondérale (49). Il constitue d’ailleurs un facteur prédictif de mortalité (50).
- Antécédents de tuberculose pulmonaire
L’analyse des Odds Ratio ajustés de la population d’El-Hadjar montre une association statistiquement significative entre les antécédents de tuberculose pulmonaire et l’obstruction chronique des voies aériennes (BPCO) au stade 2+ GOLD (OR=5,04, IC 1,47-17,28, p=0.001), indépendamment des autres facteurs de risque.
Nos résultats rejoignent ceux de nombreuses études précédentes réalisées en milieu hospitalier ou en population générale (51), dont les études PLATINO (52) et PREPOCOL (53). Dans l’étude PLATINO il est également souligné que la notion de tuberculose pulmonaire antérieure est associée aux stades spirométriques obstructifs les plus sévères (29).
Si les séquelles anatomiques de la tuberculose pulmonaire, ainsi que leurs conséquences fonctionnelles respiratoires restrictives, sont bien connues, il n’en est pas de même pour les mécanismes menant à l’obstruction des petites et moyennes bronches.
- Antécédents familiaux de maladie respiratoire chronique
Comme pour la tuberculose, la notion d’antécédents de maladie respiratoire chronique dans la famille proche (BPCO, bronchite chronique, emphysème) est indépendamment corrélée au DVO persistant stade 2+ GOLD (OR= 3,23 ; IC 1,21-8,58 ; p=0.019). Là aussi, le lien de causalité ne peut être établi de façon formelle en raison du faible effectif enregistré.
Ces résultats sont toutefois relativement proches de l’étude multicentrique américaine « COPD Gene » réalisée sur une population adultes de quarante ans et plus comptant 821 patients BPCO et 776 cas-contrôle fumeurs. Il est démontré que les antécédents familiaux de BPCO sont un facteur de risque d’obstruction bronchique chronique caractéristique (OR=1,73 ; IC 1,36-2,20 ; p<0.0001) sans rapport avec le tabagisme familial ou personnel. Ils auraient également un impact sur la sévérité de la maladie (54).
L’implication de facteurs génétiques dans la genèse et la sévérité de la BPCO est de plus en plus plausible comme en témoignent les conclusions de nombreuses études génomiques de cohortes (55, 56).
Le présent travail a permis de conforter notre idée que cette maladie est un problème local à court et probablement à long terme.
Chez la population âgée de 40 ans et plus d’El-Hadjar soit 10.940 individus, la prévalence des fumeurs et ex-fumeurs à raison de 10 PA et plus est de 31.1% soit 3.402 personnes. Si l’on considère que 20% d’entre eux feront une BPCO post-tabagique, le nombre prédit de malades porteurs de cette maladie dans les années à venir à El-Hadjar sera de 680. Ce calcul simplifié laisse présager de la charge médico-sociale de la maladie dans notre région.
Aussi, il y a nécessité d’élaborer et de mettre en place un plan d’action de santé pertinent pour faire face au problème que pose la BPCO en termes de prévention et de prise en charge.
Ce plan d’action doit être centré sur le patient, focalisé sur ses besoins et animé par le médecin généraliste. Ses objectifs généraux se résument en quatre points :
- Recueillir les données sanitaires de la BPCO : indicateurs d’activité et de gestion de la maladie ;
- Assurer un diagnostic précoce de la maladie pour une l’efficience de notre action : mise en place d’un parcours de soins (médecin généraliste, pneumologue, consultation anti-tabac, laboratoire de spirométrie) ;
- Améliorer la qualité de vie des patients en évitant ou en réduisant les incapacités fonctionnelles : programme d’éducation thérapeutique, initiation de plan de formation ;
- Instaurer une évaluation périodique des actions menées.
Les principaux intervenants de ce plan de santé seraient :
- Les décideurs chargés de la santé pour la mise à disposition des moyens matériels et humains et la participation à l’implantation d’un réseau de santé adapté;
- le médecin généraliste, véritable cheville ouvrière, pour le sevrage tabagique (conseil minimal), le diagnostic précoce de la BPCO chez les groupes à risque, le traitement approprié, le suivi régulier et les principes de base de l’éducation thérapeutique.
Il constitue ainsi le point d’attache, toujours disponible, nécessaire à tout malade chronique.
Toutefois, ces attentes ne resteront qu’un vœu pieux sans une formation adaptée, opérationnelle, utile et réaliste, ainsi que la participation effective des partenaires de santé (faculté de médecine, assurance maladie).
La prévalence de la BPCO chez les résidents d’El-Hadjar (Annaba) âgés de quarante ans et plus est de l’ordre de 8,8% tous stades confondus et de 6,3% pour le stade 2 et plus.
La maladie reste sous-diagnostiquée même chez les patients aux stades avancés de sévérité, pourtant symptomatiques et potentiellement demandeurs de soins. Par ailleurs, l’obstruction bronchique chronique chez les non-fumeurs, étiquetés BPCO, pourrait contribuer au retard diagnostique et laisse supposer l’implication possible de facteurs de risque autre que le tabac dans la genèse de la maladie.
Notre étude montre qu’à El-Hadjar, outre les personnes de plus de 60 ans et les tabagiques à plus de 20 PA, les individus avec des antécédents d’asthme ou de tuberculose pulmonaires constituent aussi un groupe à risque de développer une obstruction irréversible des voies aériennes.
Nous restons convaincus que les meilleurs moyens de lutte contre cette maladie restent les mesures préventives, notamment la lutte anti-tabac et le sevrage tabagique à tous les niveaux d’intervention.
Afin de réduire la morbi-mortalité et les dépenses de santé liées à cette grave maladie émergente, il nous parait urgent de mettre en place un plan d’action sanitaire local.
La mesure de la prévalence de la BPCO est un prérequis à l’évaluation de la charge médico-sociale et financière de la maladie, tant au niveau local que national et dont la finalité serait la conception et l’implantation d’un programme de santé spécifique.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Collaborators GBDCoD. Global, regional, and national age-sex-specific mortality for 282 causes of death in 195 countries and territories, 1980–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2018;392(10159):1736–1788. doi:10.1016/S0140- 6736(18)32203-7
- Adeloye D, Chua S, Lee C, Basquill C, Papana A, Theodoratou E, et al. Global and regional estimates of COPD prevalence: systematic review and meta-analysis. J Glob Health. 2015;5:020415.
- World Health Organization. Global surveillance, prevention and control of chronic respiratory diseases: a comprehensive approach. undefined Accessed 4 Mar 2018.
- Global Strategy for the Diagnosis, Management and Prevention of COPD, Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2018. undefined Accessed June 25, 2019. 2019.
- European Respiratory Society. European Lung White Book: Huddersfield, European Respiratory Society Journals, Ltd; 2003.
- Buist AS, Vollmer WM, Sullivan SD, Weiss KB, Lee TA, Menezes AM et al. The burden of obstructive lung disease Initiative (BOLD): rationale and design. COPD 2005; 2:277-83.
- Buist AS, McBurnie MA, Vollmer WM, Gillespie S, Burney P, Mannino DM, et al. International variation in the prevalence of COPD (the BOLD Study): a population-based prevalence study. Lancet 2007 ; 370 : 741-50.
- Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM. Global burden of COPD: systematic review and meta-analysis. Eur Respir J 2006; 28: 523-32.
- Rycroft CE, Heyes A, Lanza L, Becker K. Epidemiology of chronic obstructive pulmonary disease: a literature review. Int J Chron Obstruct Pulmon Dis 2012;7:457-94.
- Halbert RJ, Isonaka S, George D, Iqbal A. Interpreting COPD prevalence estimates: what is the true burden of disease? Chest. 2003; 123(5):1684-92.
- Mascarenhas J, Bettencourt P, Azevedo A. Clinical epidemiology of chronic obstructive pulmonary disease. Arquivos de Medicina. 2011;25(4):146–52.5. GOLD. Global Strategy for the Diagnosis, Management and Prevention of COPD, Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2018. undefined Accessed June 25, 2019. 2019.
- Beran D, Zar HJ, Perrin C, Menezes AM, Burney P, for the Forum of International Respiratory Societies working group collaboration. Burden of asthma and chronic obstructive pulmonary disease and access to essential medicines in low-income and middle-income countries. Lancet Respir Med 2015;3: 159-70.
- Aït-Khaled N, Hamadache M, Benhabyles K. Analysis of demand for pulmonary function testing for obstructive airway disease in an Algerian laboratory. Bull Union Int Tuberc 1990; 65: 39-41.
- Khelafi R, Aissanou A, Tarsift T, Skander F. Épidémiologie de la bronchopneumopathie chronique obstructive dans la wilaya d’Alger. Rev Mal Respir2011 ; 28, 32-40.
- Tageldin MA, Nafti S, Ahmed Khan J, Nejjari C, Beji M, Mahboub B and al. Distribution of COPD-related symptoms in the Middle East and North Africa: Results of the BREATHE study. Respir Med 2012 ; 106(S2), S25-S32.
- Office National des Statistiques. Résultats du Recensement Général de la Population et de l’Habitat 2008.
- Rabe KF, Hurd S, Anzueto A, Barnes PJ, Buist AS, Calverley P et al. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary. Am J Respir Crit Care Med 2007; 176: 532-55.
- Albert P, Agusti A, Edwards L, Tal-Singer R, Yates J, Bakke P, et al. Bronchodilator responsiveness as a phenotypic characteristic of established chronic obstructive pulmonary disease. Thorax 2012;67(8):701-8.
- National Health and Nutrition Examination Survey III: Hankinson JL, Odencrantz JR, Fedan KB. Spirometric Reference Values from a Sample of the General U.S. Population. Am J Respir Crit Care Med 1999;159(1):179-87.
- Lopez AD, Shibuya K, Rao C, Mathers CD, Hansell AL, Held LS et al. Chronic obstructive pulmonary disease: current burden and future projections. Eur Respir J 2006;27:397-412.
- Chaulet P. After health sector reform, whither lung health. International Journal of Tuberculosis Lung Disease, 1998, 2(S) : 349-59.
- Mannino DM, Buist AS. Global burden of COPD: risk factors, prevalence, and future trends. Lancet. 2007;370:765.
- Daldoul H, Denguezli M, Jithoo A, Gnatiuc L, Buist S, Burney P. Prevalence of COPD and Tobacco Smoking in Tunisia-Results from the BOLD Study. Int. J. Environ. Res. Public Health 2013, 10, 7257-71.
- El Rhazi K, Nejjari C, BenJelloun MC, El Biaze M, Attassi M, Garcia-Larsen V. Prevalence of chronic obstructive pulmonary disease in Fez, Morocco: results from the BOLD study. Int J Tuber Lung Dis 2016; 20: 136-41.
- Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM. Global burden of COPD: systematic review and meta-analysis. Eur Respir J 2006; 28: 523-32.
- Salvi S. The silent epidemic of COPD in Africa. Lancet 2015;3:e6-e7.
- Chermiti Ben Abdallah F, Taktak S, Chtourou A, Mahouachi R, Ben Kheder A. Burden of Chronic Respiratory Diseases (CRD) in Middle East and North Africa (MENA). World Allergy Organization Journal 2011; Jan. Suppl: 6-8.
- Rycroft CE, Heyes A, Lanza L, Becker K. Epidemiology of chronic obstructive pulmonary disease: a literature review. Int J Chron Obstruct Pulmon Dis 2012;7:457-94.
- Menezes AM, Perez-Padilla R, Jardim JR, Muiño A, Lopez MV, Valdivia G and al. Chronic obstructive pulmonary disease in five Latin American cities (the PLATINO study): a prevalence study. Lancet 2005; 366:1875-81.
- Lamprecht B, Soriano JB, Studnicka M, Kaiser K, Vanfleteren L, Gnatiuc L and al. Detreminants of underdiagnosis of COPD in National and International surveys. Chest 2015;148(4): 971-85.
- De Marco R, Accordini S, Cerveri I, Corsico A, Sunyer J, Neukirch F, et al. An international survey of chronic obstructive pulmonary disease in young adults according to GOLD stages. Thorax 2004: 59(2): 120-5.
- Tilert T, Dillon C, Paulose-Ram R, Hnizd E, Doney B. Estimating the U.S. prevalence of chronic obstructive pulmonary disease using pre- and post-bronchodilator spirometry: the National Health and Nutrition Examination Survey (NHANES) 2007–2010. Respir Res 2013, 14:103-13.
- Feenstra TL, van Gunugten ML, Hoogenveen RT, Wouters EF, Rutten-van Molken MP. The impact of aging and smoking on the future burden of chronic obstructive pulmonary disease: A model analysis in the Netherlands. Am J Respir Crit Care Med 2001; 164: 590-596.
- Tageldin MA, Nafti S, Ahmed Khan J, Nejjari C, Beji M, Mahboub B and al. Distribution of COPD-related symptoms in the Middle East and North Africa: Results of the BREATHE study. Respir Med2012 ; 106(S2), S25-S32.
- Sørheim IC, Johannessen A, Gulsvik A, Bakke BS, Silverman EK, DeMeo DL. Gender differences in COPD: are women more susceptible to smoking effects than men? Thorax 2010; 65:480-85.
- Stanojevic S, Wade A, Stocks J. Reference values for lung function: past, present and future. Eur Respir J 2010; 36: 12-9.
- Miller MR, Quanjer PH, Swanney MP, et al. Interpreting lung function data using 80% predicted and fixed thresholds misclassifies more than 20% of patients. Chest 2011;139:52-9.
- Garrido PC, Diez J, Gutierrez JR, et al. Negative impact of chronic obstructive pulmonary disease on the health-related quality of life of patients. Results of the EPIDEPOC study. Health Qual Life Outcomes 2006; 4:31-40.
- Quanjer PH, Tammeling GJ, Cotes JE, Pedersen OF, Peslin R, Yernault JC. Lung volumes and forced ventilatory flow. Report working party standardization of lung function tests, European community for steel and coal. Official statement of the European respiratory society. Eur Respir J 1993;6(suppl. 16):5-40.
- Lamprecht B, Mahringer A, Soriano JB, Kaiser B, Buist AS, Studnicka M et al. Is spirometry properly used to diagnose COPD? Results from the BOLD study in Salzburg, Austria: a population-based analytical study. Prim Care Respir J 2013; 22:195-200.
- Casas Herrera A, Montes de Oca M, López Varela MV, Aguirre C, Schiavi E, Jardim JR, PUMA Team. COPD Underdiagnosis and misdiagnosis in a highrisk primary care population in four Latin American countries. A key to enhance disease diagnosis: the PUMA study. PLoS One. 2016;11(4) doi: 10. 1371/journal.pcbi.1004820.
- Pellegrino R, Viegi G, Brusasco V, et al. Interpretative strategies for lung function tests. Eur Respir J. 2005;26(5):948–968. PubMed PMID: 16264058; eng.
- Quanjer PH, Stanojevic S, Cole TJ, et al. Multi-ethnic reference values for spirometry for the 3–95-yr age range: the global lung function 2012 equations. Eur Respir J. 2012;40(6):1324–1343. PubMed PMID:22743675.
- Rennard I, Vestbo J, Agusti A. What is chronic obstructive lung disease anyway? Continua, categories, cut points, and moving beyong spirometry. Am J Respir Crit Care Med 2013;187:1036-7.
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management and prevention of chronic pulmonary disease, 2011. undefined
- Lamprecht B, Schirnhofer L, Kaiser B, Buist S, Studnicka M. Non-reversible airway obstruction in never smokers: results from the Austrian BOLD study. Respir Med 2008; 102:1833-38.
- Shirtcliffe P, Marsh S, Travers J, Weatherall M, Beasley R. Childhood asthma and GOLD-defined chronic obstructive pulmonary disease. Intern Med J 2012; 42(1):83-8.
- Hooper R, Burney P, Vollmer MW, McBurnie M, Gislason T, Tan WC, Jithoo A et al. Risk factors for COPD spirometrically defined from the lower limit of normal in the BOLD project. Eur Respir J. 2012; 39(6): 1343-53.
- Celli BR, Cote CG, Marin J, Casanova C, Montes de Oca M, Mendez R, et al. The body mass-index, airflow obstruction, dyspnea and exercise capacity index in COPD.N Engl J 2004;350:1005-12.
- Baig IM, Saeed W, Khalil KF. Post-tuberculous chronic obstructive pulmonary disease. J Coll Physicians Surg Pak. 2010;20:542-4.
- Laniado de la Mora I, Martınez-Oceguera D, Laniado-Laborın R. Chronic airway obstruction after successful treatment of tuberculosis and its impact on quality of life. Int J Tuberc Lung Dis 2015; 19(7):808-10.
- Lam KB, Jiang CQ, Jordan RE, Miller MR, Zhang WS, Cheng KK, et al: Prior TB, smoking, and airflow obstruction : a cross-sectional analysis of the Guangzhou Biobank cohort study. Chest 2010; 137: 593-600.
- Shirtcliffe P, Weatherall M, Marsh S, et al. COPD prevalence in a random population survey: a matter of definition. Eur Respir J 2007; 30:232-39.
- Tan WC, Sin DD, Bourbeau J, Hernandez P, Chapman KR, Cowie R, and al. Characteristics of COPD in never-smokers and ever-smokers in the general population: results from the Can COLD study. Thorax 2015;70:822-29
- Kurmi, O.P.; Semple, S.; Simkhada, P.; Smith, W.C.S.; Ayres, J.G. COPD and chronic bronchitis risk of indoor air pollution from solid fuel: A systematic review and meta-analysis. Thorax 2010, 65, 221–228
Télécharger le PDF de cet article

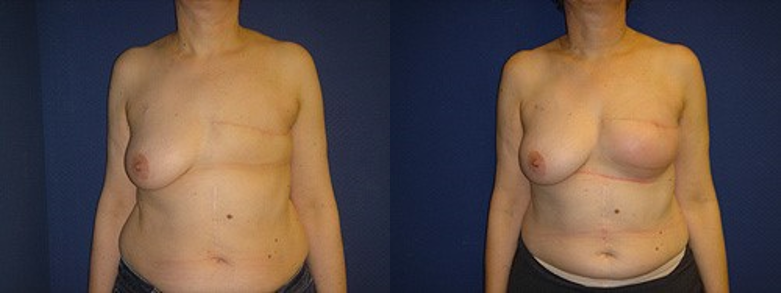
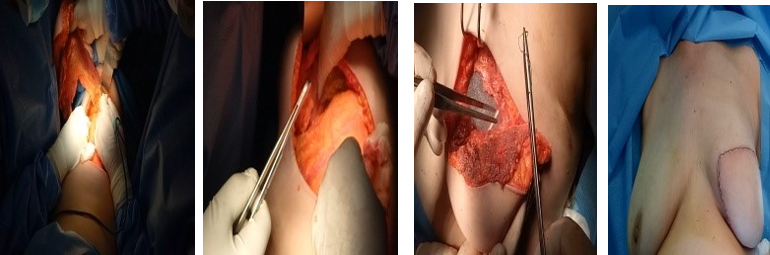
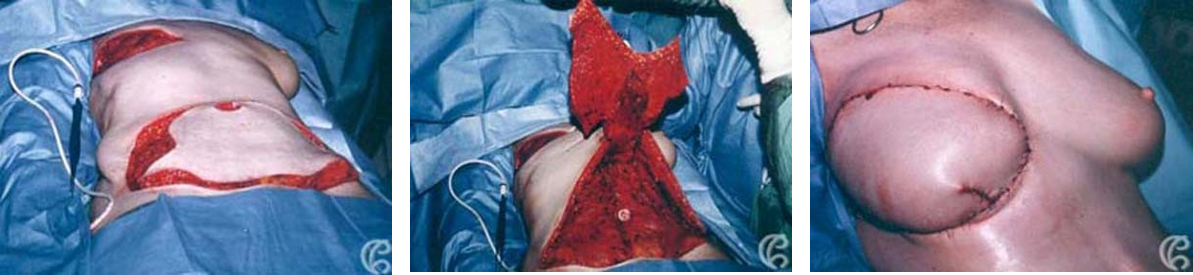
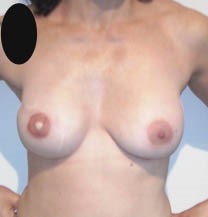
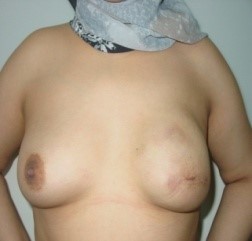
 (Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC
(Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC