Les registres du cancer sont des outils privilégiés pour étudier les caractéristiques épidémiologiques des cancers et évaluer les orientations sanitaires prises pour améliorer leur prise en charge. Le premier registre des cancers est attribué à la ville de Hambourg en Allemagne, les premiers registres français ont vu le jour entre 1975 et 1978 (1.2).
DIFI, K. BOUZID, Centre Pierre et Marie Curie (CPMC), Alger.
Date de soumission : 22 Septembre 2019.
Résumé : Introduction : L’incidence, la mortalité, la survie sont des indicateurs épidémiologiques fondamentaux pour évaluer les politiques de santé publique et estimer les besoins en prise en charge de la population. L’objectif de cet article est de présenter les dernières actualisations de ces indicateurs et s’inscrit dans l’axe stratégique N°6 du Plan Cancer Algérien 2015-2019. Méthodes : Les données sont essentiellement issues du réseau national des registres du cancer au cours de l’année 2015, fournies et mises à jour par le Centre International de Recherche sur le Cancer (CIRC). Et les données GLOBOCAN 2018 éditées par le Centre International de Recherche sur le Cancer (CIRC) le 12 septembre 2018, agence spécialisée de l’Organisation Mondiale de la Santé (OMS) sur le cancer. Résultats : En 2015, le nombre de nouveaux cas de cancers en Algérie est estimé à 42.720 cas, soit 17.088 hommes et 25.632 femmes. Le taux d’incidence standardisé est de 115,4 chez les hommes et 128,1 chez les femmes. Chez l’homme, les cancers les plus fréquents sont les cancers du côlon-rectum, les cancers du poumon, de la prostate et de la vessie. Chez la femme, les cancers les plus fréquents sont les cancers du sein, les cancers colorectaux, la thyroïde et les cancers du col utérin. Le réseau national des registres du cancer (RNRC) couvre plus de la moitié de la population algérienne (68%) avec des données indispensables à la recherche et la lutte contre le cancer. Discussion: Le cancer est actuellement l’un des principaux problèmes de santé publique en Algérie. Le taux d’incidence des cancers est en forte augmentation. Cette augmentation est due à la transition épidémiologique, marquée par l’évolution démographique, l’augmentation de l’espérance de vie, la dégradation de l’environnement et les habitudes toxiques en particulier le tabagisme. Les cancers les plus fréquents sont le cancer du sein et les cancers colorectaux chez la femme et les cancers colorectaux et du poumon chez l’homme. La survie à 5 ans des patients cancéreux est faible en Algérie par rapport aux autres pays développés. Une grande partie de ces cancers peuvent être prévue tandis que d’autres peuvent être détectés à un stade précoce. Conclusion : En Algérie, le cancer s’inscrit aujourd’hui parmi les nouveaux besoins prioritaires en santé publique. Ceci souligne la nécessité d’intensifier les efforts déjà déployés en matière de prévention, de diagnostic et de traitement du cancer.
Mots clés : Épidémiologie, incidence, survie, registre de population.
Abstract: Introduction: Incidence, mortality and survival are key indicators to assess public health policies and estimate the needs of the population for cancer management. The aim of this article is to provide the more current estimates of these indicators, in line with the sixth operational objective of the 2015-2019 Algerian Cancer Plan. Methods: The data are mainly derived from the National Network registries during the year 2015. Provided and updated by the International Agency for Research on Cancer (IARC) and the GLOBOCAN 2018 published by the International Agency for Research on Cancer (IARC) in September 12, 2018, a specialized agency of the World Health Organization (WHO) on cancer. Results: In 2015, the number of new cases of cancer in Algeria was estimated at 42.720 cases (17.088 men and 25.632 women). The standardized rate of incidence stands at 115.4 in men and 128.1 in women. The most common cancers in men are colorectal cancers, lung cancer, prostate cancer and bladder cancer. In women the most common is breast cancer, colorectal cancer, thyroid cancer and cervical cancer. The National Network of Cancer Registries (RNCD) covers more than half of the Algerian population (68%) with essential data for research and the fight against cancer. Discussion: Cancer is becoming a new priority in public health in Algeria. The incidence of cancer is increasing. This increase is due to the epidemiological transition, marked by demographic change, increasing life expectancy, environmental degradation and toxic habits especially smoking. The most common cancers are breast and colorectal cancers in women and colorectal and lung cancers in men. The five-year survival of cancer patients is low in Algeria as compared to other developed countries. Many of these cancers can be predicted while others can be detected at an early stage. Conclusion: In Algeria, cancer is now one of the new priority needs in public health. These results highlight the need for intensifying the efforts already made in cancer prevention, diagnosis, and treatment.
Keywords: Epidemiology, incidence, survival, neoplasm, registry
Haut du formulaire
Bas du formulaire
Haut du formulaire
Bas du formulaire
Introduction
Les registres du cancer sont des outils privilégiés pour étudier les caractéristiques épidémiologiques des cancers et évaluer les orientations sanitaires prises pour améliorer leur prise en charge. Le premier registre des cancers est attribué à la ville de Hambourg en Allemagne, les premiers registres français ont vu le jour entre 1975 et 1978 (1.2).
En Algérie, on est passé par plusieurs étapes : Le 1er Registre Algérien est celui de la wilaya de Sétif en 1989. À Alger, le 1re registre consacré aux cancer digestifs est mis en place en 1992 puis étendu à l’ensemble des localisations et deviendra le registre des tumeurs d’Alger en 1992. Le registre de la wilaya d’Oran est mis en place en 1994 (3.4).
Actuellement une vingtaine de wilayas sont couvertes par des registres, travaillant en réseau coordonné par le registre de Sétif depuis février 2014 (Réseau National des Registres du Cancer RNRC)
Matériel et Méthode
Mise en œuvre de l’arrêté Numéro 22 du 18 Février 2014, institutionnalisation de l’enregistrement des registres du cancer en Algérie (5). Le réseau national des registres du cancer (RNCD) couvre plus de la moitié de la population algérienne (68%). Cette large couverture a permis de fournir des données fiables. Les données de GLOBOCAN 2018 éditées par le Centre International de Recherche sur le Cancer (CIRC) ; agence spécialisée de l’Organisation Mondiale de la Santé (OMS) sur le cancer, fournit les estimations les plus récentes pour 28 types de cancers dans 184 pays pour l’année 2012 et permet également des projections dans le futur.
Résultats
On estime que le fardeau mondial du cancer a aujourd’hui atteint 18,1 millions de nouveaux cas et 9,6 millions de décès en 2018. Un homme sur cinq et une femme sur six dans le monde développeront un cancer au cours de leur vie, et un homme sur huit et une femme sur 11 vont mourir de cette maladie. A l’échelle mondiale, le nombre total de personnes vivant avec un cancer dans les cinq ans suivant le diagnostic, appelé prévalence à cinq ans, est estimé à 43,8 millions (6.7).
En Algérie, en se basant sur les données du réseau national des registres de cancer 2014, ayant ciblé une population de plus de 20 millions d’habitants, soit 68% de taux de couverture, le nombre de nouveaux cas enregistrés pour toutes les localisations chez les deux sexes est de 42.750, avec un taux brut de 106,8 pour 100.000 habitants, et un taux standardisé par rapport à la population mondiale de 115,4 pour 100.000 habitants (tableau 1).
Chez l’homme
Le nombre de nouveaux cas enregistrés pour l’année 2015, toutes localisations confondues est de 17.088 avec un taux standardisé par rapport à la population mondiale de 102,5 pour 100.000 habitants. Les cancers les plus incidents chez l’homme sont les cancers du côlon rectum, du poumon, de la prostate et de la vessie (tableau 2).
Chez la femme
Le nombre de nouveaux cas enregistrés pour l’année 2015, toutes localisations confondues est de 25.632 avec un taux standardisé par rapport à la population mondiale de 128,1 pour 100.000 habitants (tableau 1). Chez la femme, les cancers du sein dominent, suivis des cancers colorectaux, de la thyroïde, du col utérin et de l’estomac (tableau 3).
Projections 2015-2020-2025
Les projections 2015-2020-2025 pour les localisations, chez l’homme sont estimées pour 2020 à 23.072 nouveaux cas et pour 2025 à 28.962 nouveaux cas (Figure 1).
Les projections 2015-2020-2025 pour les localisations chez la femme sont estimées pour 2020 à 26.962 nouveaux cas et pour 2025 à 32.069 nouveaux cas (Figure 1).
Les projections 2015-2020-2025 pour les localisations chez les deux sexes sont estimées pour 2020 à 50.034 nouveaux cas et pour 2025 à 61.031 nouveaux cas (Figure 1).
Taux de survie
La survie nette standardisée chez les adultes (15 à 99 ans) des cancers de l’estomac, du côlon, du rectum, du foie, des poumons, du sein, du col utérin, des ovaires, de la prostate et de la leucémie était faible (4) (tableau 4).
Discussion
Le cancer est en train de devenir un fléau mondial. D’après les données épidémiologiques les plus récentes, ce fléau atteint de plus en plus les populations des pays à faible et moyen revenu (5).
En Algérie, le cancer s’inscrit aujourd’hui parmi les nouveaux besoins prioritaires en santé publique.
Cette tendance est accentuée par la croissance et le vieillissement de la population, l’urbanisation, ainsi que les changements du mode de vie qui vont induire une augmentation rapide de l’incidence. L’absence de mesure préventive, le retard au diagnostic, l’insuffisance d’établissements et de matériels dédiés font que, si des mesures ne sont pas prises rapidement, la mortalité par cancer va continuer à progresser au même rythme que l’incidence.
Le cancer du poumon est au 2ème rang chez l’homme. Son incidence reste faible comparée à celle des pays industrialisés. L’augmentation de l’incidence suit parfaitement l’augmentation de la prévalence du tabagisme en Algérie. L’âge médian de survenue est de 61 ans (3.11).
Les cancers colorectaux sont les cancers digestifs les plus fréquents aussi bien chez les hommes que chez les femmes. Les cancers colorectaux se situent au 1er rang des principales localisations chez l’homme et au 2ème rang chez la femme. L’âge médian au moment du diagnostic est de 65 ans. Le cancer colorectal occupe une position intermédiaire entre les pays industrialisés et les pays en développement. Les données sont similaires dans les pays du Maghreb (3.10.12).
L’incidence brute du cancer colorectal chez les hommes algérois a doublé entre 2008 et 2016 (12,5 en 2008 à 25,2 pour 100.000 habitants) (13) ; ce qui impose la mise en place rapide d’un programme de lutte (prévention primaire et dépistage).
Les cancers de la prostate et de la vessie sont en nette augmentation ces dernières années (3).
Chez la femme, près de 40 % des cancers féminins sont représentés par le cancer du sein. Son incidence continue son ascension et se rapproche inexorablement de l’incidence mondiale (80 nouveaux cas pour 100.000 femmes) (13). L’âge moyen des sujets atteints de cancer du sein est de 52,5 ± 12,1 ans et un âge médian de 49 ans (14.15). L’incidence du cancer du sein augmente notablement dès 35-39 ans et enregistre deux pics à 45-49 ans et 50-44 ans et diminue au-delà de 74 ans (16.17). Les cancers des voies biliaires et de la thyroïde sont en nette augmentation (3.18). Le cancer du col de l’utérus est en légère diminution ces dernières années et se trouve en quatrième position (18).
Pour espérer inverser la tendance actuelle d’une mortalité par cancer proche de l’incidence, plusieurs conditions devraient être remplies :
- Formation médicale en cancérologie des ressources humaines.
- Mise en place les structures nécessaires à l’activité pluridisciplinaire (20.21)
- Information de la population sur l’intérêt majeur de la prévention et du diagnostic précoce.
- Prise en compte les soins palliatifs.
Conclusion
Le développement du plan cancer nécessite la présence d’une volonté pour la reconnaissance du cancer comme problème prioritaire, l’existence d’un potentiel de compétences humaines et d’infrastructures, ainsi que l’existence d’une société civile dynamique. L’objectif primordial de toute mesure doit être toujours centré sur le patient qui demeure au cœur de l’engagement de tous.
Tableau 1 : Incidence globale de cancer en Algérie, 2015.
|
|
Nombre de cas |
Taux Brut |
Taux standardisé |
|
Hommes |
17,088 |
105 |
102,5 |
|
Femmes |
25,632 |
108,5 |
128,1 |
|
Total |
42,720 |
106,8 |
115,4 |
Tableau 2 : Incidence des principales localisations du cancers chez l’ homme ,Algérie ,31 Décembre 2015,
|
Localisations |
Nombre de cas |
Taux brut |
Taux standardisé |
|
|
|
100,000 |
100,000 |
|
Colo-rectum |
3,539 |
16,9 |
19,8 |
|
Poumon et bronches |
2,856 |
13,6 |
16,4 |
|
Prostate |
2,090 |
10,0 |
13,1 |
|
Vessie |
2,583 |
12,3 |
8,9 |
|
Estomac |
1,292 |
6,2 |
6,1 |
|
LNH |
924 |
4,4 |
4,9 |
|
NPC |
756 |
3,6 |
4,3 |
|
Leucémies |
305 |
1,5 |
5,8 |
|
Larynx |
441 |
2,1 |
3,2 |
Tableau 3 : Incidence des principales localisations du cancers chez la femme ,Algérie ,31 Décembre 2015.
|
Localisations |
Nombre de cas |
Taux brut |
Taux standardisé |
|
|
|
100,000 |
100,000 |
|
Sein |
11,603 |
55,3 |
62,0 |
|
Colo-rectum |
3,003 |
14,3 |
10,6 |
|
Thyroïde |
1,575 |
7,5 |
7,1 |
|
Col de l’ Utérus |
1,134 |
5,4 |
6,7 |
|
Estomac |
819 |
3,9 |
3,6 |
|
Vésicule biliaire |
714 |
3,4 |
4,3 |
|
LNH |
798 |
3,8 |
3,6 |
|
Leucémies |
546 |
2,6 |
3,2 |
Figure 1 : Courbe des projections annuelles de l’incidence du cancer en Algérie, 2015-2025.
Tableau 4 : La survie nette standardisée pour les adultes atteint de tumeurs malignes en Algérie.
|
Localisations |
Survie estimée(%) avec un IC à 95% |
|
Estomac |
10,3 (6,7-14,0) |
|
Côlon |
57,2 (45,6-68,9) |
|
Rectum |
45,5 (36,3-54,8) |
|
Foie |
17,5 (11,7-23,4) |
|
Poumon |
14,8 (11,2-18,4) |
|
Sein |
59,8 (48,6-71,1) |
|
Col utérin |
55,1 (49,8-60,4) |
|
Ovaire |
41,8 (22,2-61,4) |
|
Prostate |
58,5 (51,2-65,9) |
|
Leucémies |
13,6 (6,7-20,5) |
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Source : manuel publié par le Centre international de Recherche sur le Cancer (CIRC), auteur Jensen
- En 1999, on comptait près de 200 registres des cancers à travers le monde. Autres dates d’intérêt : 1943 : Danemark, 1950 : Canada, 1952 : Norvège, 1954 :Islande
- Hamdi-Cherif M, Sekfali N, Coleman MP. Incidence of cancer in the wilaya of Sétif, Algeria. Bull cancer. 1991; 78(2):155–167
- Cancer epidemiology in Algeria: best use of cancer registers. L. Abid J. Afr. Cancer (2009) 1:98-103 DOI 10.1007/s12558-009-0019-y.
- Hamdi Cherif M, Zaidi Z, Abdellouche D, Hamdi S, Lakhdari N, et al. Registre du cancer de Sétif (Algérie): incidence, tendance et survie, 1986–2005. J Afr Cancer. 2010; 2(4):245–258.
- Données accessibles sur http://globocan.iarc.fr/Pages/online.aspx
- Forman D, Bray F, Brewster DH, Gombé Mbalawa Ch, Kohler B, Pineros M, Steliarova, Foucher E, Swaminathan R andFerlay J Cancer in five continents volume X Lyon IARC Scientific Publications 2014; N°164:1365.
- Bray F, Znaor A, Cueva P, Korir A, Swaminathan R, Ullrich A, Wang AS et Parkin DM Planification et développement des registres du cancer basés sur la population dans les pays à revenu faible et intermédiaire Lyon Publications techniques du CIRC. 2014; N°43.
- Forman D, Bray Tangka FK, Subramanian S, Edwards P, Cole-Beebe M, Parkin DM, Bray F, Joseph R, Mery L, Saraiya M; Resource requirements for cancer registration in areas with limited resources: Analysis of cost data from four low and middle-income countries. Cancer Epidemiol. 2016; 25. Parkin DM, Kramárová E, Draper GJ, Masuyer E.
- Jensen OM, Parkin DM, Mac Lennan R, Muir CS, Skeet RG. Enregistrement des cancers principes et méthodes. IARC publications scientifiques no 95, Lyon, France.
- Zanetti R, Tazi MA, Rosso S. New data tells us more about cancer incidence in North Africa. Eur j Cancer.2010; 46(3):462–466.
- Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, et al. Globocan 2012 v1.0, Cancer incidence and mortality worldwide: IARC cancer base no
- International agency for research on cancer. 2013; Lyon, France. Registre des Tumeurs d’Alger 2016
- Chaher N, Arias-Pulido H, Terki N, Qualls C, Bouzid K, Verschraegen C, et al. Molecular and epidemiological characteristics of inflammatory breast cancer in Algerian patients. Breast Cancer Res Treat 2012;131(2):437–44.
- Corbex M, Burton R, Sancho-Garnier H. Breast cancer early detection methods for low- and middle-income countries, a review of the evidence. Breast 2012;21(4):428–34. http://dx.doi.org/10.1016/j.breast.2012.01.002 [Review].
- Guendouz H, Chetibi W, Abdelouahab A, Bendib A. Cancer du de cancer du sein de la femme de moins de 35 ans : étude rétrospective, a propos de 612 cas société française de sénologie et de pathologie mammaire. La lettre du sénologue, 52.
- Bray F. Transitions in human development and the global cancer burden. In: Wild CP, Stewart B, eds. World cancer report. 2014. Lyon: International Agency for Research on Cancer, 2014.
- Sylla BS, Wild CP. A million Africans a year dying from cancer by 2030: what can cancer research and control offer to the continent. Int J Cancer. 2012;130:245-50
- Plan national cancer 2015-2019, nouvelle vision stratégique centrée sur la maladie, October 2014. Available at http://www.sante.dz/plan_national_cancer.pd
- Chardot C, Fervers B, Bey P, Abbatucci JS, Philip T. Standards, options et recommandations pour l’organisation pluridisciplinaire en cancérologie. Bull Cancer. 1995;10:780-94.
- UICC – Guide pour l’Organisation d’un Plan National de Contrôle du Cancer à l’usage des Organisations Non Gouvernementales.


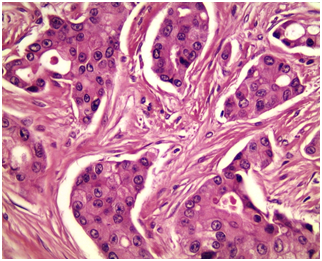
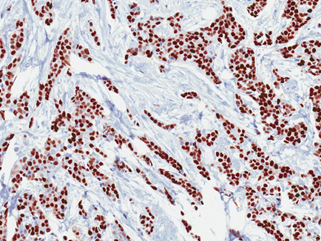
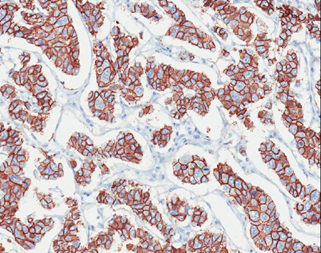
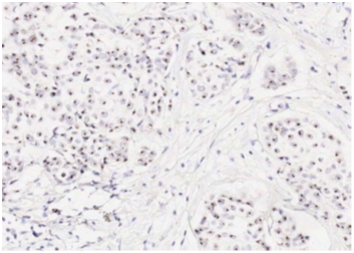
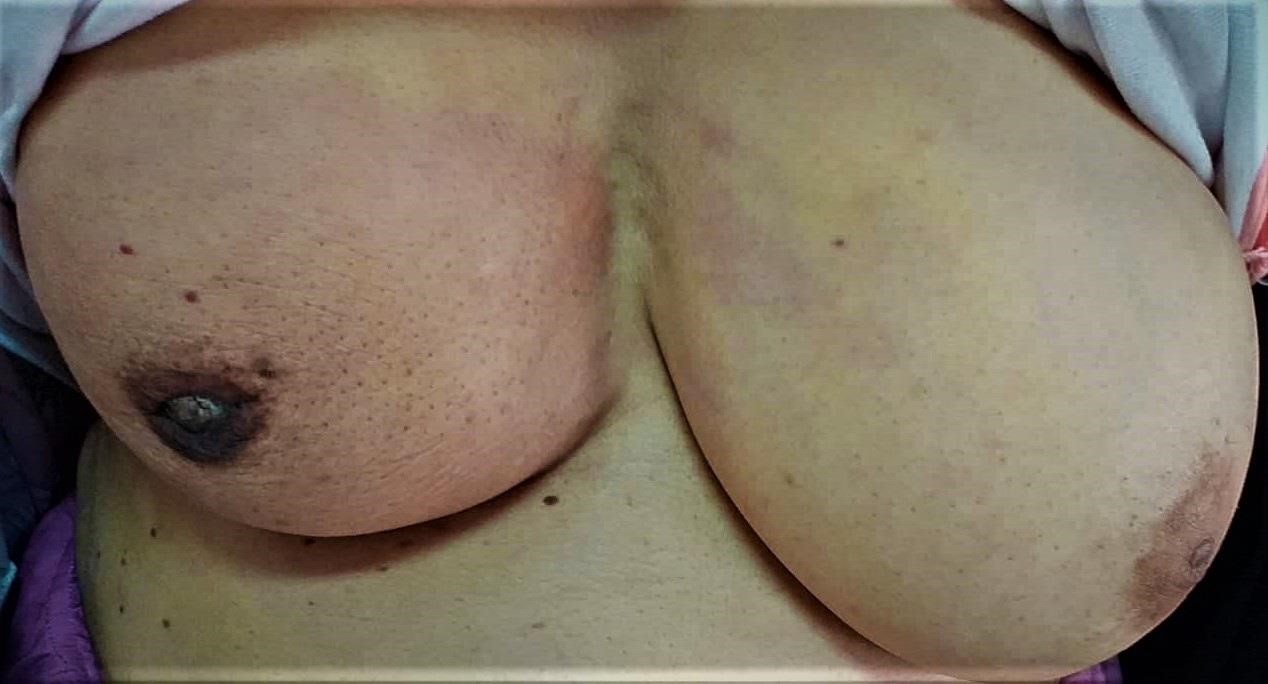
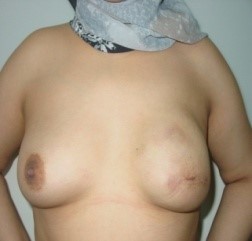


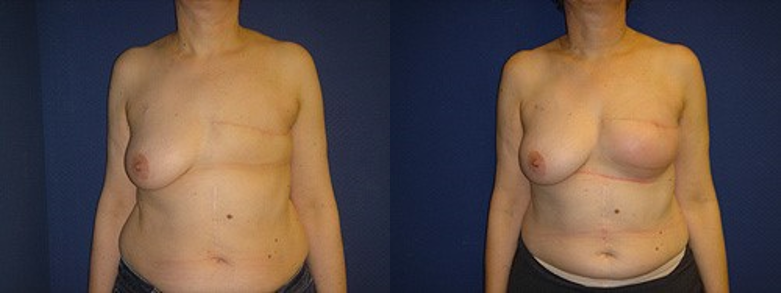
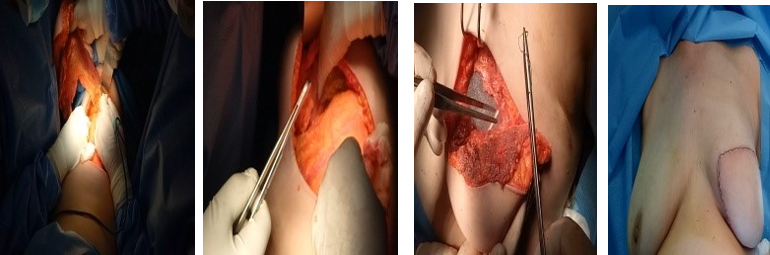
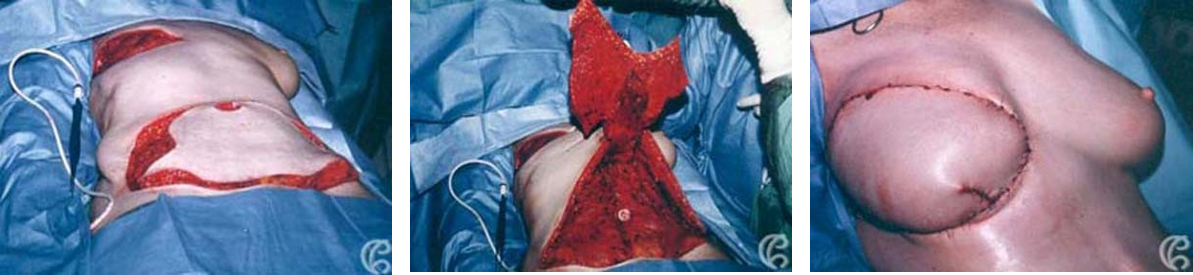
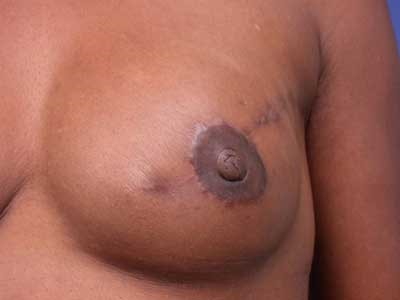
 (Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC
(Figure 5) : RM par LGD+ Prothèse Selimed 410 cc chez une patienteRM par LGD+ Prothèse Selimed 430 cc chez une patiente 36 ans après 38 mois de sa mastectomie.Lambeau extérorisé 29 ans après 15 mois de sa mastectomie.Lambeauextérorisé par la cicatrice de la mastectomie (2 cicatrices)par le sillon sous mammaire (3 cicatrices : trident); Photos du service de sénologie chirurgie B CPMC