M.K. SULAIMAN, N. AIT MOULOUD, Y. KACIMI, I. ABAYAHIA, I. TOUILEB, M. TERAHI; Service d’Ophtalmologie, CHU Nafissa HAMOUD, Hussein dey, Alger
Résumé
La maladie de Behçet (MB) est une maladie inflammatoire auto-immune multi-systémique caractérisée par des lésions aphteuses buccales, des ulcérations génitales, une iridocyclite avec hypopyon et des lésions cutanées. Alors que les manifes- tations oculaires surviennent chez près de 50 % des patients atteints de la maladie de Behçet, l’atteinte oculaire n’est la manifestation initiale que chez moins de 20 % des patients. La maladie de Behçet oculaire présente cliniquement une iridocyclite avec ou sans hypopion, une hyalite, une rétinite, une vascularite rétinienne occlusive et un œdème maculaire cystoïde. Cependant, l’uvéite antérieure est généralement la seule manifestation oculaire initiale; la forme la plus cou- rante est la panuvéite. L’évolution habituelle de la maladie est caractérisée par des périodes inflammatoires récurrentes. Les poussées inflammatoires récurrentes peuvent entraîner des dommages irréversibles et une perte visuelle importante. Un traitement précoce et efficace est nécessaire pour prévenir la morbidité oculaire. Les développements récents dans le trai- tement de la maladie de Behçet oculaire comme les agents biologiques, sont prometteurs avec un effet rapide et des taux de rémission élevés.
Mots-clés : Maladie inflammatoire auto-immune multi-systémique, irido- cyclite, vascularite rétinienne, rétinite, agents biologiques, cécité.
Abstract
Behçet’s disease (BD) is a multisystemic autoimmune inflammatory disorder characterized by oral aphthous lesions, genital ulcerations, iridocyclitis with hypopyon, and skin lesions. While ocular manifestations occur in nearly 50 % of the patients with Behçet’s disease, ocular involvement is the initial manifestation in only less than 20 % of the patients. Ocular Behçet’s disease clinically presents iridocyclitis with or without hypopyon, vitritis, retinitis, occlusive retinal vasculitis, and cystoid macular edema. However, anterior uveitis is usually the only initial ocular manifestation; the most common form is panuveitis. The usual course of the disease is characterized by recurrent inflammatory periods. Recurrent inflammatory attacks may result in irreversible damage and significant visual loss. Early and effective treatment is required to prevent ocular morbidity. Recent developments in the treatment of ocular Behçet’s disease like biological agents, are promising with a rapid effect and high remission rates.
Keywords : Multisystemic autoimmune inflammatory disorder, iridocyclitis, retinal vasculitis, retinitis, biological agents, blindness.
Introduction
Historiquement, la première description de la « maladie de la route de la soie », mieux connue sous le nom de maladie de Behçet, a probablement été faite par Hippocrate dans son troisième livre sur « les maladies endémiques ». Cepen- dant, l’essai clinique des ulcères oro-génitaux récurrents et des uvéites oculaires associées est resté obscur jusqu’à ce que le dermatologue turc Hulusi Behçet le définisse comme un syndrome observé chez trois patients autochtones d’origine moyen-orientale en 1937 (1).
La maladie de Behçet est une maladie chronique évoluant par poussées imprévisibles, spontanément mais partiellement régressives.
Son traitement est actuellement purement symptomatique et vise à juguler les poussées et à atténuer les séquelles.
La prise en charge de la maladie de Behçet doit être pluri- disciplinaire, associant internistes et ophtalmologistes (2,3). Les corticoïdes et les immunosuppresseurs ont longtemps été la base du traitement.
Etant entrés dans l’ère de la thérapie biologique, le rôle de divers médicaments biologiques spécifiques bloquant les cytokines, tels que les inhibiteurs du TNF-α (par exemple, l’adalimumab, l’infliximab), les inhibiteurs de l’interféron α-2a, les inhibiteurs de l’IL-6 et de l’IL-1 contraste avec les médicaments immunosuppresseurs conventionnels et le vieil gold-standard classique : les corticostéroïdes (systé- miques ou locaux).
Un traitement bien adapté, instauré rapidement, permet de réduire le taux de cécité de 75 à 20 %. Enfin, nous concluons en abordant la pandémie de SRAS-CoV-2 en cours, en rapportant la morbidité de Behçet durant cette pandémie, le schéma observé et les recommandations du traitement.
Clinique
Les signes oculaires de la maladie de Behçet surviennent généralement dans les 2 à 4 premières années de l’appari- tion de cette maladie, l’atteinte oculaire peut initialement commencer unilatéralement. Cependant, il s’agit générale- ment d’une atteinte bilatérale (4,5). L’âge habituel d’apparition est d’environ 30 ans et la maladie est souvent plus sévère chez les patients de sexe masculin.
L’uvéite de Behçet est récidivante, non granulomateuse et s’étend du pôle antérieur au pôle postérieur pour donner une panuvéite qui est la forme la plus courante.
Le patient consulte le plus souvent pour une baisse de l’acuité visuelle ou un simple flou visuel ; ces symptômes visuels peuvent être accompagnés de douleurs oculaires et de photophobie (6,7).
A- Uvéite antérieure
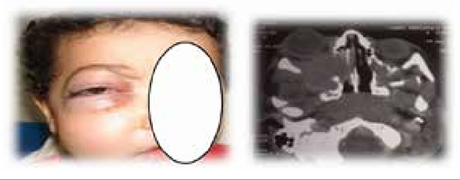
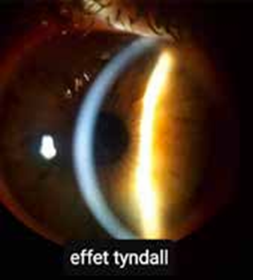
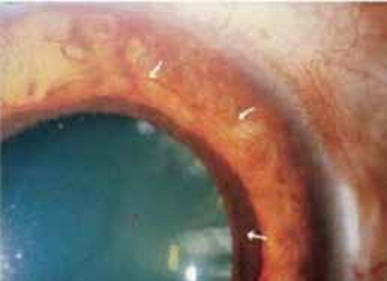
L’uvéite antérieure isolée est rare, elle se manifeste par des précipités rétro cornéens, avec un effet Tyndall important dans la chambre antérieure, associé dans un 1/3 des cas à un hypopyon composé de polynucléaires neutrophiles.
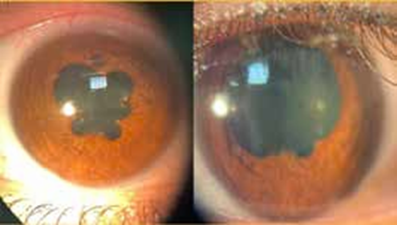
Les poussées inflammatoires récurrentes peuvent entrainer des modifications structurelles du segment antérieur notamment des synéchies postérieures, une atrophie de l’iris et des synéchies antérieures périphériques (8,9).
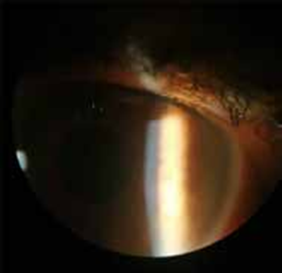
Figure 1 : Précipités rétro cornéens chez un malade atteint de la maladie de Behçet.

B- Uvéite Postérieure
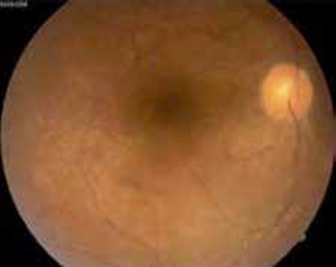
L’uvéite postérieure est la manifestation inflammatoire la plus fréquente et la plus grave. Elle est marquée principale- ment par une hyalite, d’intensité variable, pouvant être responsable d’une baisse importante de l’acuité visuelle avec un fond d’œil complètement masqué (10).
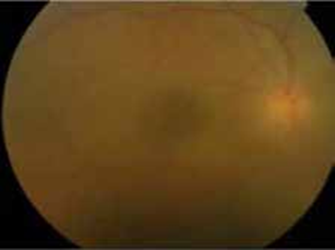
C- Vascularites rétiniennes
Les vascularites rétiniennes, principalement les périphlébites, mais également associées à l’artérite, sont une caractéristique principale et sont souvent accompagnées d’une rétinopathie vaso-occlusive avec des hémorragies rétiniennes et vitréennes, une ischémie rétinienne, une néo vascularisation et un glaucome néovasculaire secondaire (11).
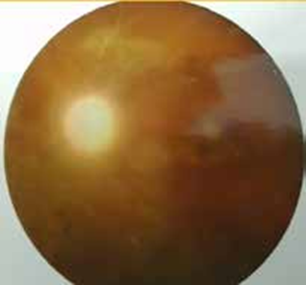
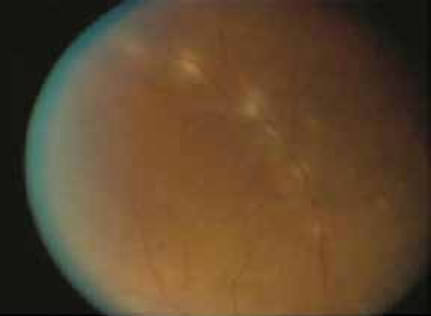
Figure 8 : Vascularite active chez un malade qui présente une maladie de Behçet.
Maladie de Behçet pédiatrique
La maladie de Behçet pédiatrique est une maladie rare et difficile à diagnostiquer. Elle touche les enfants jusqu’à l’âge de 16 ans et son schéma diffère de celui des adultes par son apparence et la prédominance des principaux signes diagnostiqués.
Comme chez les adultes, des ulcères buccaux récurrents, répandus, multiples ou uniques (12,13) représentent le signe de présentation le plus courant et souvent le premier à observer à un âge moyen de 8 à 9 ans.
Les études suggèrent une fréquence d’atteinte oculaire similaire à la fréquence observée chez les adultes voir plus faible, Cependant, la présence de signes oculaires, tels qu’une uvéite ou une rétinite antérieure et/ou postérieure, a une morbidité plus élevée et est associée à un pronostic plus sombre par rapport au pronostic observé chez les adultes.
Examens complémentaires
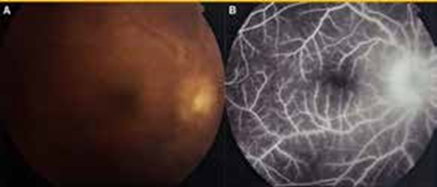
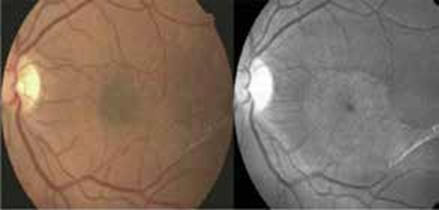
A- Photographie couleur
Bien qu’elle ne soit pas nouvelle, la photographie du fond d’œil est un outil simple, économique mais souvent négligé. Il peut documenter le degré du trouble vitré pour la surveillance de la maladie et la nature transitoire des infiltrats rétiniens, particulière à l’uvéite de Behçet.
B- L’angiographie à la Fluorescéine AF
Même s’il y a eu des progrès rapides dans les techniques d’imagerie oculaire, l’AF reste l’investigation de réfé- rence pour le diagnostic et le suivi de la vascularite occlusive ou de la vascularite active observée dans l’uvéite postérieure de Behçet, « la fuite capillaire semblable à une fougère » est caractéristique (14).
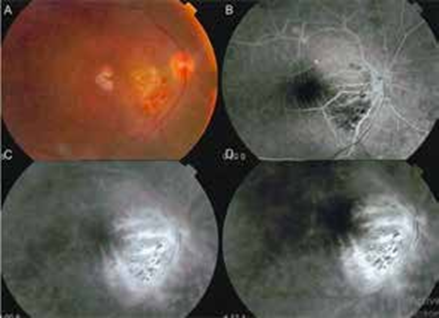
Par ailleurs l’angiographie peut objectiver, un œdème maculaire.
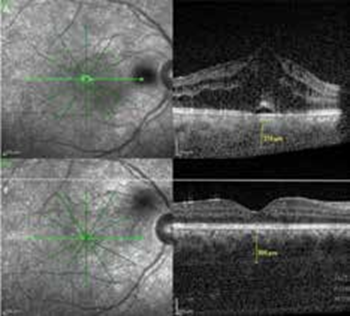
C- La Tomographie en Cohérence Optique (OCT)
La tomographie en cohérence optique (OCT) consti- tue un moyen rapide et non invasif d’investigation des complications maculaires, la plus fréquente étant l’œdème maculaire cystoïde, qui doit être étroitement surveillé par OCT.
Récemment, l’OCT a également été utilisée pour mesurer objectivement le degré d’inflammation vitréenne associée à l’uvéite de Behçet, comme outil de surveillance de l’activité. La neurorétinite de Behçet se révèle souvent par une condensation vitréenne localisée recouvrant la papille infiltrée. Ainsi, l’OCT permet une surveillance non invasive de l’infiltration discale et de la réaction inflammatoire sus-jacente (14).
D- Tomographie par cohérence optique angiographie (OCT-A)
La Tomographie par cohérence optique angiographie (OCT-A) est une nouvelle technique d’imagerie qui résout et affiche des images de haute résolution, résolues en profondeur, en face de la micro-vascu- larisation rétinienne et choroïdienne en calculant le contraste de mouvement dans les OCT B-scans acquis à plusieurs reprises au même endroit.
Il a été démontré que les principaux changements détectés par l’OCT-A étaient la non-perfusion capillaire rétinienne, les vaisseaux capillaires péri-fovéaux raréfiés, dilatés ou shuntés, la désorganisation de l’architecture normale du réseau capillaire, l’élargissement de la zone avasculaire centrale et la réduction de la capillarité (15).
De nombreuses études ont été menées pour évaluer les changements microvasculaires associés à la maladie de Behçet pendant l’activité et après la rémission, les au- teurs ont proposé l’utilisation de l’OCT-A pour surveiller l’activité de l’uvéite postérieure de Behçet.
L’OCT-A peut être supérieure à l’AF pour visualiser, caractériser et quantifier les altérations microvasculaires périfovéales dans l’uvéite de Behçet actif. Les images OCT-A permettent une visualisation claire des vaisseaux, en raison de l’absence de phénomène de fuite de colorant, observé sur AF. Cependant, l’AF reste toujours indispensable, car il n’y a pas de corrélation entre la présence d’ischémie rétinienne périphérique sur l’AF et l’une des caractéristiques pathologiques de l’OCT-A (17,18).
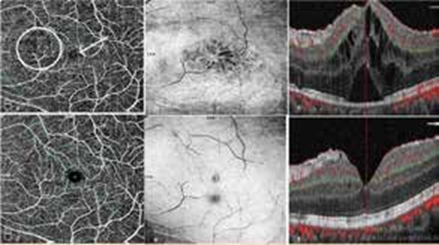
(E) En face montrant la résolution des changements cystoïdes avec la membrane épirétinienne résiduelle. (F) SD-OCT montrant la résolution des changements cystoïdes et le détachement neurosensoriel avec un œdème diffus résiduel et une membrane épirétinienne.
Traitement
La prise en charge médicale de l’uvéite de Behçet doit être adaptée en fonction du mode de présentation (antérieure, postérieure ou panuvéite), ainsi que de la gravité de la poussée, car il n’existe pas de règles standard de traitement (16). La Ligue européenne contre le rhumatisme (EULAR) a publié les premières lignes directrices pour la prise en charge de la maladie en 2008. Au cours de la dernière décennie, de nombreuses études supplémentaires ont été publiées sur différentes thérapies, ce qui a conduit à l’élaboration de lignes directrices EULAR mises à jour en 2018. Le consensus dans la prise en charge de l’uvéite s’est clairement déplacé vers une collaboration multidiscipli- naire entre des spécialistes expérimentés de l’uvéite et des rhumatologues. Une autre recommandation était la limitation de l’administration de stéroïdes au contrôle du stade à court terme et aigu, à remplacer par des traitements antirhumatismaux de fond conventionnels ou une thérapie biologique conformément aux directives de l’EULAR et de l’American Academy of Ophthalmology (AAO). Par ailleurs, l’AAO a recommandé de contourner les « traitements de fond antirhumatismaux conventionnels classiques » au profit d’agents anti-TNF-alpha dans les uvéites sé- vères menaçant la vision. Dans cette section, nous passons en revue les mises à jour sur les différents
médicaments systémiques utilisés dans la prise en charge de l’uvéite associée à la maladie de Behçet.
A- Stéroïdes
En 2018, les directives mises à jour de l’EULAR recommandaient l’administration de glucocorticoïdes chez les patients atteints de la maladie de Behçet oculaire du segment postérieur, mais uniquement en association avec d’autres thérapies telles que l’azathioprine (AZA), la cyclosporine A (CsA), l’interféron alpha ou des anticorps monoclonaux anti-TNF. Le rôle des stéroïdes systémiques a été défini pour traiter principalement un épisode aigu, contrôler la poussée et prévenir des lésions tissulaires étendues (5). En cas de hyalite sévère, de vascularite rétinienne occlusive étendue, de rétinite et de neuropathie optique, des doses élevées de stéroïdes (que ce soit un bolus de méthylprednisolone suivi de prednisone orale 1 mg/ kg/jour, ou en se limitant directement à ce dernier) sont administrées, en gardant à l’esprit les complications systémiques liées aux stéroïdes. Des stéroïdes en dégression, en plus d’une immunosuppression non cortisonique, seront ensuite initiés pour le maintien de la rémission.
Lorsque la maladie de Behçet se manifeste par une uvéite antérieure isolée, les stéroïdes topiques et les cycloplégiques sont généralement suffisants pour contrôler la maladie, mais une manifestation sous la forme d’une poussée agressive avec hypopion nécessite des stéroïdes systémiques, en particulier lorsqu’elle est associée à des facteurs de mauvais pronostic, tels que le jeune âge et le sexe masculin. Les stéroïdes régionaux, sous la forme d’injections sous-ténoniennes d’acétonide de triamcinolone (TAA), sont également efficaces pour contrôler les maladies oculaires actives et sont souvent utilisés en conjonction avec d’autres schémas thérapeutiques systémiques dans les cas graves. L’administration intravitréenne complémentaire de stéroïdes a également été rapportée pour contrôler l’inflammation oculaire et l’œdème maculaire, administrés soit sous forme d’injections intravitréennes de TAA, soit, plus récemment, sous la forme d’implants d’acétonide de fluocinolone ou de dexaméthasone, en particulier dans les cas d’œdème maculaire cystoïde réfractaire. Le succès a été signalé à la fois anatomiquement et visuellement et peut nécessiter la prise en charge de complications telles que l’hypertonie oculaire temporaire et/ou la formation de cataracte. Ces complications auraient été plus élevées avec les implants d’acétonide de fluocinolone par rapport aux implants de dexaméthasone.
B- Immunosuppresseurs
Cette classe de médicaments est utilisée pour permettre le sevrage des stéroïdes tout en contrôlant l’activité de la maladie et en réduisant ou en prévenant les rechutes. Le choix du ou des médicaments ainsi que des doses doit se faire en collaboration avec un rhumatologue expert pour le suivi médicamenteux. Actuellement, le traitement immunosuppresseur de l’uvéite de Behçet peut être grossièrement divisé en traite- ment conventionnel AZA et agents biologiques tels que les inhibiteurs du TNF-alpha et l’interféron alpha-2a.
a. Traitement conventionnel (CT)
Des essais contrôlés randomisés (ECR) ont prouvé que l’antimétabolite AZA et l’inhibiteur des lymphocytes T CsA étaient efficaces dans le traitement de l’uvéite postérieure de la maladie de Behçet ain- si que dans la prévention des rechutes. Ces résultats fondés sur des preuves ont maintenu leur validité et par conséquent, les directives EULAR mises à jour en 2018 ont recommandé l’utilisation de ces deux médicaments dans le traitement initial de l’uvéite postérieure. En revanche, le mycophénolate mofétil et le cyclophosphamide n’ont pas été inclus dans la dernière mise à jour des recommandations EULAR. Une fois le contrôle de l’inflammation par les stéroïdes d’entretien à faible dose (≤ 5 – 7,5 mg/jour) atteint pendant plusieurs mois, une réduction progressive de la dose d’immunosuppresseurs est effectuée. La dose est réduite généralement de 10 % tous les 2 à 3 mois jusqu’à l’arrêt. La durée habituelle du traitement est de 18 à 24 mois. Cependant, une durée plus longue d’un traitement à base de médicaments immunosup- presseurs est souvent nécessaire.
- L’azathioprine (AZA) est l’un des deux médica- ments de traitement conventionnel les plus couram- ment utilisés dans le contrôle de la maladie de Behçet systémique et plus particulièrement dans l’uvéite de Behçet. Il faut 2 à 3 mois pour obtenir le plein effet. Pendant cette période, le contrôle de la maladie active doit être obtenu avec des stéroïdes. La dose d’AZA habituellement utilisée est de 2,5 mg/kg/jour avec un maximum de 3 mg/kg/jour et s’est avérée efficace dans l’uvéite de Behçet, améliorant l’acuité visuelle, réduisant les rechutes et stoppant la progression vers une aggravation.
Malgré la surveillance régulière nécessaire de la for- mule sanguine et des enzymes hépatiques, l’AZA est généralement considérée comme un médicament bien toléré. Un essai de dégression progressive et de retrait peut être lancé après une période de rémission et peut s’étendre au-delà de 18 à 24 mois.
- La cyclosporine A (CsA) est le deuxième médi- cament conventionnel le plus couramment utilisé et est généralement administrée à 2 – 5 mg/kg/jour en deux doses fractionnées qui peuvent être augmentées progressivement jusqu’à ce qu’un bon contrôle soit obtenu en plus de la faible dose de stéroïdes oraux. Semblable à l’AZA, la CsA s’est avérée efficace pour améliorer l’acuité visuelle et réduire la gravité des poussées avec moins de récidives. Les principaux ef- fets secondaires de la CsA sont la néphrotoxicité et l’hypertension. En raison de sa neurotoxicité, elle est contre-indiquée en cas de neuro-Behçet. Une fois le contrôle de la maladie atteint, le médicament doit être réduit très progressivement sur une longue période comme l’AZA pour prévenir un effet rebond. L’uti- lisation concomitante d’AZA et de CsA, que ce soit en tant que traitement de première ou de deuxième intention, a montré son efficacité dans le contrôle de l’atteinte oculaire de Behçet avec une surveillance pé- riodique des effets secondaires systémiques.
- La Colchicine La colchicine est un alcaloïde tricyclique qui agit en inhibant la migration et la division des polynucléaires neutrophiles, en diminuant plus particulièrement leur chimiotactisme, modifiant leur adhésivité et en interférant avec la libération de cytokines. Elle peut être utilisée en association avec les autres traitements dans toutes les formes oculaires de la maladie de Beh- çet et permettrait de réduire les doses des immuno- suppresseurs. Elle prévient les récurrences de la mala- die, mais n’est pas suffisamment efficace pour traiter seule une poussée inflammatoire aiguë. Prescrite à la dose de 1 à 2 mg/j, elle est systématiquement utilisée dans le traitement des manifestations cutanéomu- queuses et permet de juguler l’aphtose buccogénitale. Elle est également active sur les lésions articulaires de faible gravité. Sa bonne tolérance et l’absence de surveillance biologique font de la colchicine l’un des traitements de base les plus couramment utilisés.
C- Agents biologiques
Bien que certains des médicaments conventionnels les plus couramment utilisés aient été associés à des cas d’uvéite de Behçet réfractaire ou à des effets se- condaires du traitement, leur utilisation comme trai- tements de première ligne a diminué depuis l’émer- gence des produits biologiques. En raison de leurs effets puissants et rapides, les agents biologiques sont désormais utilisés seuls ou en association dans les cas de Behçet oculaire réfractaire ou parfois même comme traitement de première ligne dans les crises graves menaçant la vision.
- Inhibiteurs de la nécrose tumorale alpha (TNF-alpha)
Dans la maladie de Behçet, la production de TNF-al- pha par les macrophages, les lymphocytes T CD4+ et CD8+ et les cellules Natural Killer, est augmentée. La réduction du TNF-alpha circulant par les agents bloquants a entraîné une amélioration spectaculaire de l’activité de la maladie, comme l’ont démontré de nombreux essais, en particulier chez les personnes atteintes panuvéite ou d’uvéite postérieure sévère (19). Les médicaments anti-TNF-alpha utilisés sont des anticorps monoclonaux recombinants dirigés contre le TNF-alpha. Le protocole de prétraitement avec des produits biologiques nécessite l’exclusion de la tuber- culose et de l’hépatite B ou C ainsi que des tumeurs malignes occultes avant de commencer le traitement en raison d’éventuelles réactivation de ces maladies par les médicaments. Plusieurs agents efficaces et interchangeables sont actuellement présents, en cas d’échec d’une option médicamenteuse. Habituelle- ment, une dose supplémentaire d’un immunosup- presseur est nécessaire avec certains des inhibiteurs du TNF-alpha pour empêcher la production d’anticorps anti-chimériques ou anti-humains, ce qui diminue l’efficacité du médicament et entraîne un échec secondaire (20).
- L’adalimumab (ADA)
est un anticorps monoclonal entièrement humain di- rigé contre le TNF-alpha. C’est l’un des rares médicaments à avoir été testé dans des ECR contre placebo, à la fois dans les uvéites non infectieuses actives et quiescentes (études VISUAL I et VISUAL II, respectivement) (21), dans lesquelles l’atteinte oculaire de Behçet représentait 7 % des cas d’uvéite inscrits. En raison de sa supériorité sur le placebo pour amélio- rer l’épaisseur centrale de la rétine et le contrôle de l’activité de la maladie (mais pas en termes d’œdème maculaire), l’Agence Européenne des Médicaments (EMA) et la Food and Drug Administration (FDA) des États-Unis ont approuvé l’ADA pour les uvéites antérieures en 2016. L’adalimumab est administré par voie sous-cutanée à la dose adulte de 40 mg toutes les 2 semaines.
De nombreuses études non contrôlées, telles que les données présentées par Fabiani et al. et Urruti- coechea-Arana et al. ont également montré des résultats significatifs concernant l’efficacité de l’ADA dans l’amélioration de l’uvéite de Behçet. Non seulement il était supérieur au placebo dans le contrôle de l’activité de la maladie, mais également un pourcentage plus élevé de patients sous ADA ont pu arrêter les stéroïdes oraux.
L’adalimumab a également été testé dans le sous-groupe pédiatrique atteint de la maladie de Behçet où l’initiation précoce du médicament chez deux enfants a permis de contrôler l’activité de la maladie avec une diminution des stéroïdes topiques et systémiques et donc à éviter les complications.
Humira est le médicament adalimumab de référence étudié dans tous les essais cités ci-dessus. Plusieurs biosimilaires-adalimumab (bio-ADA) sont encore à l’étude quant à leur efficacité dans la MB oculaire. Une étude très récente de Soheilian et al. a rapporté les résultats significativement positifs obtenus par bio-ADA dans l’amélioration de l’acuité visuelle, la diminution du voile vitré et l’amélioration de l’activité de la chambre antérieure chez 48 patients atteints de l’uvéite de Behçet réfractaire sous traitement conven- tionnel. Sota et al. rapportent de bons résultats dans le contrôle de la vascularite rétinienne et de l’activité de la maladie tout en préservant l’acuité visuelle.
- L’infliximab (IFX)
est un autre bloqueur du TNF-alpha sous la forme d’un anticorps monoclonal chimérique. Il est généralement réservé aux cas réfractaires ou utilisé en première intention en cas d’uvéite postérieure sévère avec un risque plus élevé de lésion tissulaire ou de perte de vision. L’infliximab est administré à la dose de 3 à 5 mg/kg en perfusion intraveineuse lente sur 2 à 3 h. Le régime de charge comprend la répétition de la dose à la 2e semaine, puis à la 6e semaine, puis toutes les 6 à 8 semaines pour le maintien du contrôle de la maladie.
De nombreux essais ont démontré l’effet rapide et profond de l’infliximab sur l’uvéite de Behçet. Le médicament a entraîné une rémission rapide de la maladie et une amélioration de l’acuité visuelle. Il a également réduit le nombre et la gravité des crises par rapport à d’autres immunosuppresseurs au cours des 6 premiers mois de traitement, ainsi que la thérapie à long terme. Une administration précoce au cours des 36 premiers mois contre 72 mois semblait favo- riser une valeur protectrice du résultat visuel et du contrôle de la maladie (22).
Semblable à l’ADA, l’IFX est généralement pris avec un autre médicament immunosuppresseur pour se prémunir contre les anticorps anti-chimériques et peut être associé à la réactivation de la tuberculose et de l’hépatite B ou C. De nombreux effets indésirables ont été rapportés avec l’IFX tels que des réactions allergiques, un lupus induit, une aggravation de la sclérose en plaques, une névrite optique et une embolie pulmonaire pouvant nécessiter l’arrêt du médicament.
Plusieurs études comparatives entre ADA et IFX ont été menées. En évidence, une étude multicentrique sur 177 patients a comparé l’ADA à l’IFX comme agent biologique de première intention dans les cas d’uvéite de Behçet réfractaire et a constaté que les deux groupes avaient un contrôle significativement meilleur en termes d’activité de la maladie, mais le groupe ADA avait un pourcentage plus élevé de patients avec une meilleure acuité visuelle et un taux de rétention de médicaments plus élevé avec moins de réactions liées aux médicaments.
Concernant l’IFX biosimilaire (bio-IFX), peu de rap- ports contradictoires existent quant à son efficacité dans la prise en charge de la maladie de Behçet. Alors que le bio-IFX s’est avéré décevant chez 3 patients atteints de la maladie de Behçet oculaire et neurolo- gique et a entraîné une récurrence de l’activité après le passage du médicament de référence aux biosimi- laires, une autre étude a rapporté le succès du bio- IFX dans l’obtention d’une rémission chez 4 sur 6 patients atteints de la maladie de Behçet impliquant une uvéite, une atteinte du système nerveux, vasculaire et articulaire.
- Le golimumab
est un autre anticorps anti-TNF alpha totalement humanisé qui semble avoir une efficacité prometteuse, notamment dans les cas de MB réfractaires. Des études supplémentaires sont nécessaires pour mieux évaluer le profil d’efficacité et de sécurité.
- Interféron alpha-2a
L’interféron alpha est une cytokine produite dans la nature en réponse à une infection virale ou à une tumeur avec des effets antiviraux, antiprolifératifs, antiangiogéniques et immunomodulateurs variables. En pratique médicale, l’interféron alpha-2a est généralement indiqué en deuxième intention dans les cas résistants, ou en première intention dans les uvéites postérieures très sévères ou en cas d’intolérance aux médicaments immunosuppresseurs conventionnels. Des études ont révélé qu’il améliorait l’acuité visuelle, résolvait l’œdème maculaire, réduisait considérablement le taux de rechutes et permettait parfois le retrait complet des stéroïdes.
Il n’y a pas de consensus standardisé concernant le dosage initial jusqu’à atteindre la dose d’entretien, l’accomplissement de la rémission et la quiescence pendant un minimum de 6 à 9 mois. Cependant, au début du traitement, les stéroïdes oraux doivent être réduits à une dose d’entretien de 10 mg/jour (23). Les principaux effets secondaires de l’interféron sont un syndrome pseudo-grippal, le psoriasis, l’épilepsie, la dépression, la leucopénie et les manifestations auto-immunes.
- Antagonistes de l’interleukine-6 (IL-6)
Tocilizumab (TCZ) Au cours des dernières années, plusieurs rapports ont démontré l’efficacité du TCZ, un inhibiteur de l’interleukine-6, dans le contrôle des cas d’uvéite de Behçet réfractaire au traitement conventionnel et aux anti-TNF-alpha. Le médicament a permis une rémission complète dans certains cas de Behçet oculaire, bien qu’il n’ait pas montré son efficacité dans le contrôle systémique de la maladie chez les mêmes patients et peut être envisagé chez certains patients atteints d’œdème maculaire uvéitique réfractaire (STOP – Étude sur l’uvéite). Les essais SATURN et SARIL-NIU se sont concentrés sur le sarilumab, un nouvel antagoniste de l’IL-6, dans l’uvéite non infectieuse. Cependant, le sarilumab n’a pas encore été établi dans la prise en charge de l’uvéite de Behçet.
- Antagonistes de l’interleukine-1 (IL-1)
Anakinra (ANA) et canakinumab (CAN)
ANA et CAN font actuellement l’objet d’une enquête dans le traitement de l’uvéite de Behçet. Une étude multicentrique italienne rétrospective réalisée en 2017 a déclaré que ces deux antagonistes de l’IL-1 avaient réussi à gérer l’inflammation intraoculaire dans une petite cohorte de patients atteints de la maladie de Behçet (24), un résultat confirmé dans une autre étude, qui rapporte une meilleure réponse des patients atteints de la maladie de de Behçet à l’IL -1 traitement chez les personnes atteintes d’uvéite de Behçet par rapport à la maladie de Behçet sans atteinte oculaire. La justification de l’inhibition de l’IL-1 et de son succès rapporté est basée sur le rôle possible joué par l’IL-1β exprimé par les cellules dendritiques rétiniennes, les macrophages et les neutrophiles en tant que médiateur du processus inflammatoire local.
- Antagonistes de l’interleukine-17A (IL-17A)
L’essai SHIELD a été mené pour évaluer l’efficacité du sécukinumab dans l’uvéite de Behçet. L’essai n’a pas atteint son objectif principal par rapport au placebo dans les récidives d’uvéite, cependant, il a considérablement réduit la nécessité d’un traitement immuno-suppresseur concomitant.
- Inhibiteurs de Janus kinase (JAKi)
Plusieurs études ont récemment fait état de succès avec les inhibiteurs de JAK dans le traitement des uvéites auto-immunes non infectieuses réfractaires aux traitements conventionnels et aux agents anti-TNFα, suggérant qu’ils pourraient être une alternative aux précédents (25). Certains ont également signalé le succès de l’épargne des stéroïdes. JAKi ont déjà été approuvés dans plusieurs maladies auto-immunes rhumatologiques, gastro-intestinales et dermatolo- giques. Ils agissent en inhibant la phosphorylation de la protéine transmembranaire JAK, bloquant ou régulant ainsi à la baisse la cascade d’expression des cytokines avant son initiation.
Pronostic et complications
Malgré l’utilisation de stéroïdes, d’agents immuno-modulateurs et biologiques, certains patients peuvent avoir une acuité visuelle (AV) finale médiocre. Vingt-cinq à cinquante pour cent des patients ont au mieux une AV corrigée inférieure à 1 /10 après 5 ans. Les protéines aqueuses et les cellules de la chambre antérieure, la formation de synéchies postérieures, l’hypopion, la formation de cataracte, les cellules et les exsudats du vitré, le décollement du vitré postérieur et l’œdème maculaire cystoïde, peuvent entraîner une diminution transitoire de l’AV. L’atrophie optique et le glaucome uvéitique résistant peuvent entraîner une perte visuelle permanente au stade terminal de la maladie. Les poussées de vascularites rétiniennes, de rétinite, de néovascularisation rétinienne et d’hyalite entraînent une hémorragie vitréenne et une atrophie rétinienne. Dans les cas avancés, nous pouvons observer : des artérioles rétiniennes fibrotiques et atténuées, des vaisseaux « filaires d’argent » rétrécis et obstrués, des altérations de l’épithélium pigmentaire rétinien, des cicatrices choriorétiniennes et une atrophie optique.
L’inflammation et les modalités de traitement utilisées dans la maladie de Behçet peuvent entraîner des complications. La cataracte compliquée et le glaucome secondaire sont généralement associés à une inflammation et à l’utilisation de stéroïdes. Une inflammation intraoculaire répétée peut entraîner un glaucome secondaire. Des glaucomes à angle ouvert et à angle fermé ou même un bloc pupillaire peuvent être observés. L’ischémie rétinienne peut provoquer un glaucome néovasculaire. Le glaucome néovascu- laire apparaît chez près de 6 % des patients atteints de la maladie de Behçet. L’atteinte du corps ciliaire peut entraîner une diminution de la pression intraoculaire et enfin une phtisie bulbaire peut survenir.
Les hémorragies vitréennes sont fréquemment ob- servées chez les patients atteints de Behçet avec une atteinte rétinienne sévère. Cela peut conduire à une organisation avec formation de membranes, provoquant des trous rétiniens et un décollement rétinien ultérieur. Une phtisie du globe peut enfin se produire. Si l’hémorragie intravitréenne ne se résout pas spon- tanément, elle peut être traitée par une vitrectomie par la pars plana.
La membrane épirétinienne, fibrose en forme de membrane en particulier dans la région maculaire, est causée par une inflammation du segment postérieur. L’inflammation condensée sur la macula et la bande fibreuse entre le vitré postérieur et la rétine entraîne la formation d’un trou maculaire. Chez les patients présentant une membrane épirétinienne, si la vision est sérieusement affectée, la membrane peut être retirée chirurgicalement.
Les progrès récents des méthodes d’imagerie ophtalmique ont permis une meilleure définition du pronostic visuel dans les manifestations oculaires de la maladie de Behçet. L’identification du groupe à haut risque et l’utilisation d’agents biologiques efficaces comme traitement de première intention, amélioreront le pronostic de cette maladie potentiellement cécitante.
Uvéite de Behçet et COVID-19
Les patients atteints de la maladie de Behçet peuvent être candidats à l’immunosuppression et donc plus susceptibles de contracter des infections graves que les individus sains. Un équilibre fin et critique est nécessaire chez les patients at- teints de la maladie de Behçet et de COVID-19 pour tenter de réduire la mortalité due à l’infection et d’éviter la rechute
de la maladie. Selon les recommandations actuelles des experts, il n’y a aucune raison d’arrêter les traitements topiques, la colchicine et les anti-inflammatoires non stéroïdiens. Il peut y avoir une justification pour envisager de réduire les stéroïdes systémiques à la dose la plus faible possible nécessaire. En cas de symptômes de COVID-19, les agents immunosuppresseurs et biologiques peuvent être temporairement arrêtés, mais la décision doit être adaptée en fonction des besoins des patients. Considérant leurs ef- fets bénéfiques potentiels sur l’évolution de la COVID-19, la colchicine, la pentoxifylline et la dapsone peuvent être considérées comme des options de traitement sûres lors- qu’elles sont indiquées dans la maladie de Behçet. Cependant, leur rôle nécessite une évaluation plus approfondie (26). Une analyse rétrospective menée par Bolletta et al. a montré que malgré l’immunosuppression (où certains patients ayant arrêté le traitement) ainsi que l’infection à COVID-19 chez les patients atteints de la maladie de Behçet, peu de leur cohorte a nécessité une hospitalisation, aucun n’a été admis aux soins intensifs et finalement environ un tiers a présen- té une exacerbation d’au moins un de leurs symptômes de Behçet associés.
Bien qu’il soit recommandé aux patients atteints de la ma- ladie de Behçet de se faire vacciner contre le SARS-CoV-2, des cas d’émergence ou de réactivation post-vaccination de la maladie de Behçet et de possibles poussées inflamma- toires oculaires ont été signalés (27).
Conclusion
L’atteinte oculaire est un critère majeur pour le diagnos- tic de la maladie de Behçet, les caractéristiques de l’uvéite peuvent permettre un diagnostic précoce de la maladie même dans les formes incomplètes ou purement oculaires de la maladie.
Les caractéristiques cliniques typiques comprennent une panuvéite aiguë, récurrente, non granulomateuse, une hyalite diffuse, une vascularite rétinienne occlusive et œdé- mateuse, une évolution avec des poussées imprévisibles pouvant entrainer une cécité.
Références
- Feigenbaum A. Description of Behçet’s syndrome in the Hippocratic third book of endemic diseases. Br J Ophthalmol. (1956) 40 : 355–7. doi: 10.1136/ bjo.40.6.355
- Yildiz M, Köker O, Adrovic A, Sahin S, Barut K, Kasapçopur Ö. Pediatric Behçet’s disease – clinical aspects and current concepts. Eur J Rheumatol. (2019) 7(Suppl. 1):1–10. doi: 10.5152/eurjrheum. 2019. 19121
- Abdelwareth Mohammed A, Soliman MM, Osman AA, El-Zanaty RT. Patterns of uveitis in Egypt. Ocul Immunol Inflamm. (2020) 29 : 1007–16. doi: 10.1080/09273948.2020.1714060
- Hatemi G, Seyahi E, Fresko I, Talarico R, Hamuryudan V. One year in review 2020: Behçet’s syndrome. Clin Exp Rheumatol. (2020) 38 (Suppl. 127): 3–10.
- Hatemi G, Christensen R, Bang D, Bodaghi B, Celik AF, Fortune F, et al. 2018 update of the EULAR recommendations for the management of Behçet’s syndrome. Ann Rheum Dis. (2018) 77:808–18. doi: 10.1136/an- nrheumdis-2018-213225
- Ideguchi H, Suda A, Takeno M, Ueda A, Ohno S, Ishigatsubo Y. Behçet di- sease: evolution of clinical manifestations. Medicine. (2011) 90 : 125–32. doi: 10.1097/MD.0b013e318211bf28
- Cunningham ET Jr., Tugal-Tutkun I, Khairallah M, Okada AA, Bodaghi B, Zierhut M. Behçet uveitis. Ocul Immunol Inflamm. (2017) 25 : 2–6. doi: 10.1080/09273948.2017.1279840
- Tugal-Tutkun I. Behçet’s uveitis. Middle East Afr J Ophthalmol. (2009) 16:219–24. doi: 10.4103/0974-9233.58425
- Tugal-Tutkun I, Onal S, Altan-Yaycioglu R, Huseyin Altunbas H, Urgan- cioglu M. Uveitis in Behçet disease: an analysis of 880 patients. Am J Ophthal- mol. (2004) 138 : 373–80. doi: 10.1016/j.ajo.2004.03.022
- Ozdal PC, Ortaç S, Taşkintuna I, Firat E. Posterior segment involvement in ocular Behçet’s disease. Eur J Ophthalmol. (2002) 12 : 424–31. doi: 10.1177/112067210201200514
- Çakar Özdal P. Behçet’s uveitis: current diagnostic and therapeutic ap- proach. Turkish J Ophthalmol. (2020) 50 : 169–82. doi: 10.4274/tjo.gale- nos.2019.60308
- Koné-Paut I. Behçet’s disease in children, an overview. Pediatr Rheumatol Online J. (2016) 14: 10. doi: 10.1186/s12969-016-0070-z
- Costagliola G, Cappelli S, Consolini R. Behçet’s disease in children: dia- gnostic and management challenges. Ther Clin Risk Manag. (2020) 16 : 495–507. doi: 10.2147/TCRM.S232660
- Mamdouh S, Youssef M, El-Fayoumi D, Salah M. Fundus fluorescein angiography and optical coherence tomography findings in ocular and non-ocular Behçet’s disease. Egyptian Rheumatol. (2020) 42 : 213–18. doi: 10.1016/j.ejr.2020.05.001
- Miura M, Makita S, Iwasaki T, Yasuno Y. Three-dimensional visualization of ocular vascular pathology by optical coherence angiography in vivo. Invest Oph- thalmol Vis Sci. (2011) 52: 2689–95. doi: 10.1167/iovs.10-6282
- McNally TW, Damato EM, Murray PI, Denniston AK, Barry RJ. An up- date on the use of biologic therapies in the management of uveitis in Behçet’s disease: a comprehensive review. Orphanet J Rare Dis. (2017) 12 : 130. doi: 10.1186/s13023-017-0681-6
- Khairallah M, Abroug N, Khochtali S, Mahmoud A, Jelliti B, Coscas G, et al. Optical coherence tomography angiography in patients with Behçet uvei- tis. Retina. (2017) 37:1678–91. doi: 10.1097/IAE.0000000000001418
- Accorinti M, Gilardi M, De Geronimo D, Iannetti L, Giannini D, Parra- vano M. Optical coherence tomography angiography findings in active and inactive ocular Behçet disease. Ocul Immunol Inflamm. (2020) 28 : 589–600. doi: 10.1080/09273948.2019.1612452
- Van der Houwen T, van Laar J. Behçet’s disease, and the role of TNF-α and TNF-α blockers. Int J Mol Sci. (2020) 21 : 3072. doi: 10.3390/ijms21093072
- Hazirolan D, Stubiger N, Pleyer U. Light on the horizont: biologicals in Behçet uveitis. Acta Ophthalmol. (2013) 91 : 297–306. doi: 10.1111/j.1755- 3768.2011.02348.x
- Jaffe GJ, Dick AD, Brézin AP, Nguyen QD, Thorne JE, Kestelyn P, et al. Adalimumab in patients with active noninfectious uveitis. N Engl J Med. (2016) 375: 932–43. doi: 10.1056/NEJMoa1509852
- Takeuchi M, Kezuka T, Sugita S, Keino H, Namba K, Kaburaki T, et al. Evaluation of the long-term efficacy and safety of infliximab treatment for uveitis in Behçet’s disease: a multicenter study. Ophthalmology. (2014) 121 : 1877–84. doi: 10.1016/j.ophtha.2014.04.042
- Celiker H, Kazokoglu H, Direskeneli H. Long-term efficacy of pegylated interferon alpha-2b in Behçet’s uveitis: a small case series. Ocul Immunol In- flamm. (2019) 27:15–22. doi:
- Fabiani C, Sota J, Tosi GM, Franceschini R, Frediani B, Galeazzi M, et al. The emerging role of interleukin (IL)-1 in the pathogenesis and treatment of inflammatory and degenerative eye diseases. Clin Rheumatol. (2017) 36 : 2307–18. doi: 10.1007/s10067-016-3527-z
- El-Shabrawi Y, Rath T Heiligenhaus A. Janus kinase inhibitors: next-gene- ration treatment for uveitis. Klin Monbl Augenheilkd. (2022) 239 : 695–701. doi: 10.1055/a-1741-8104
- Elmas Ö F, Demirbaş A, Bagcier F, Türsen Ü, Atasoy M, Dursun R, et al. Treat- ment considerations for Behçet disease in the era of COVID-19: a narrative review. Dermatol Ther. (2021) 34:e14507. doi: 10.1111/dth.14507
- Bolletta E, Iannetta D, Mastrofilippo V, De Simone L, Gozzi F, Croci S, et al. Uveitis and other ocular complications following COVID-19 vacci- nation. J Clin Med. (2021) 10: 5960. doi: 10.3390/jcm10245960