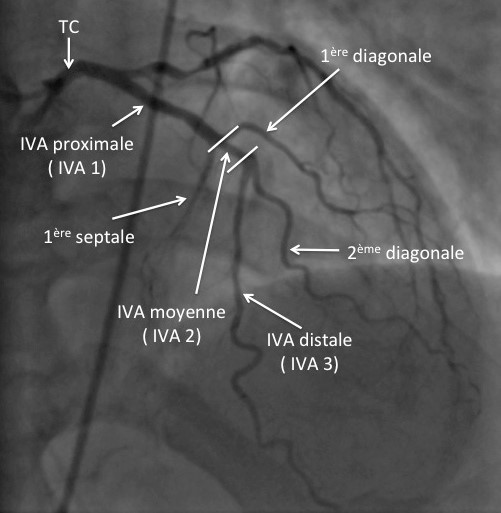
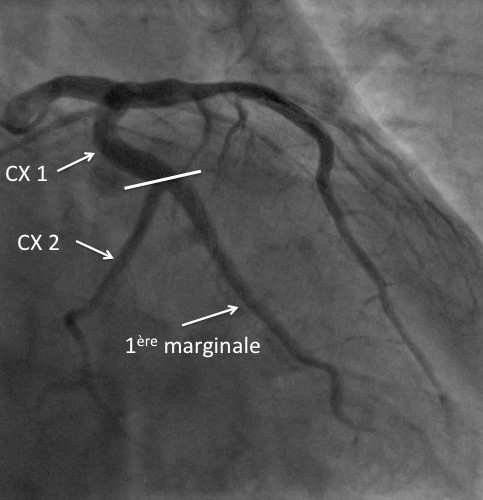
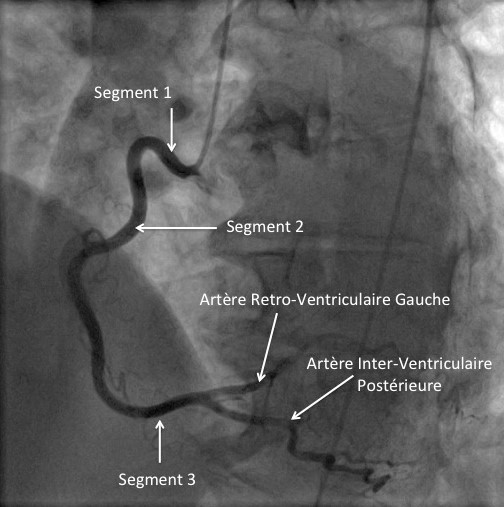
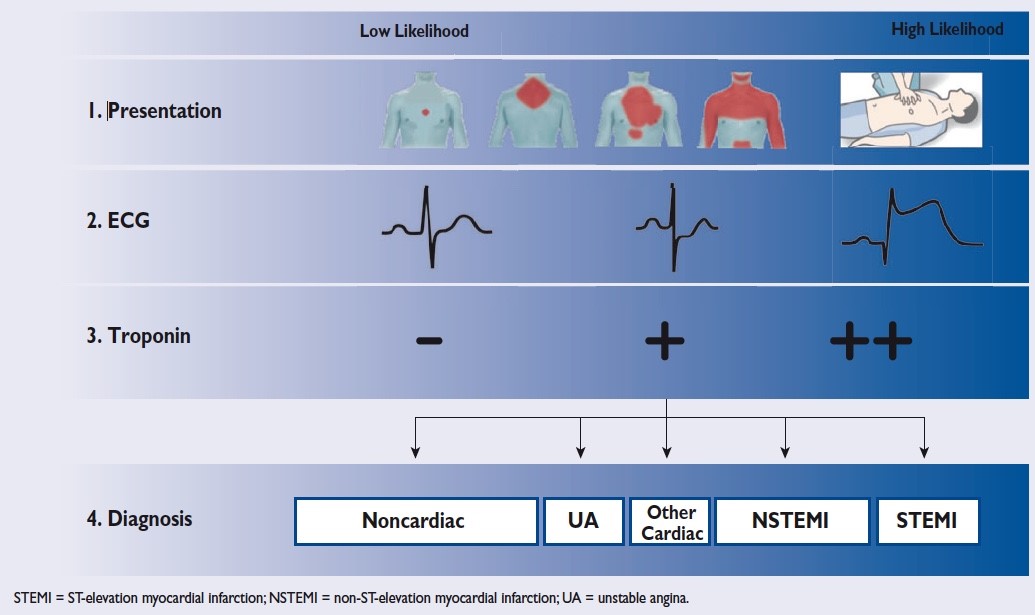
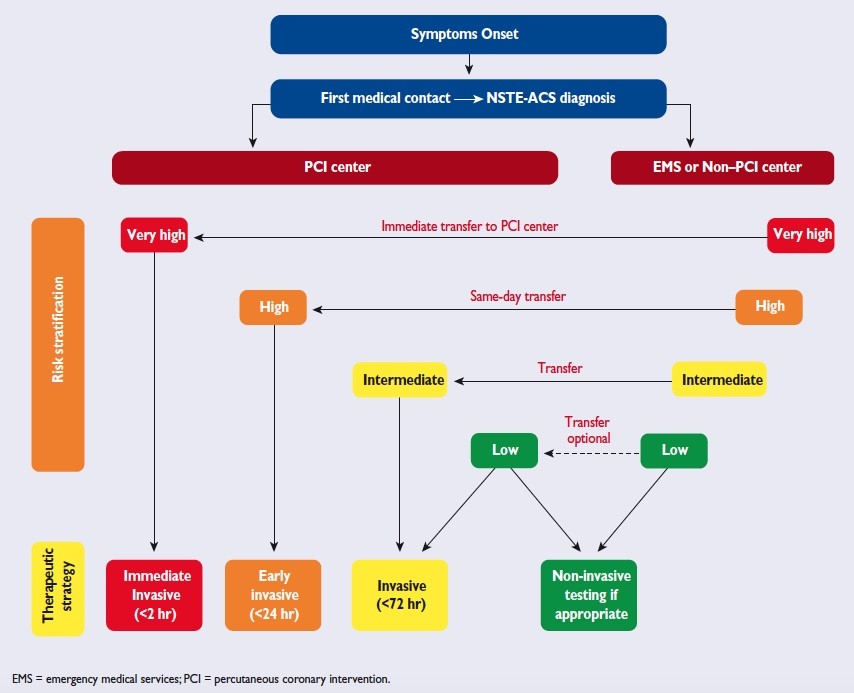
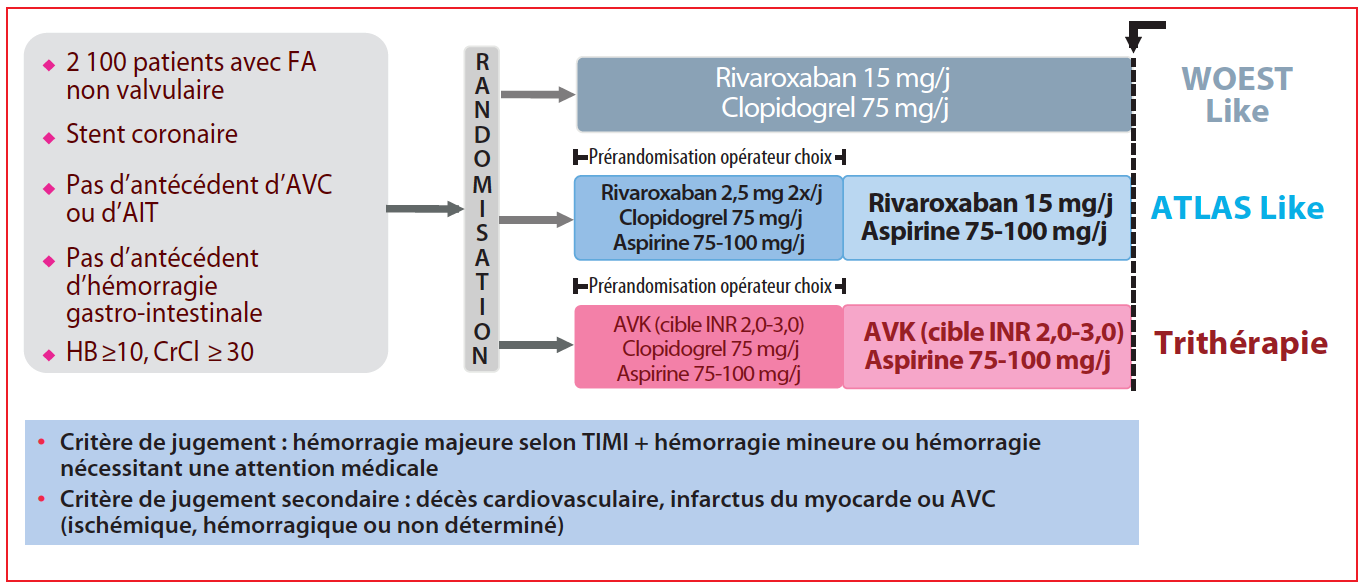
Malgré les avancées diagnostiques et thérapeutiques, les syndromes coronaires aigus restent l’une de causes les plus fréquentes de décès dans le monde. La connaissance des mécanismes physiopathologiques de l’accident athérothrombotique implique des facteurs anatomopathologiques
Y.Bououdina, M. Chettibi, Service de Cardiologie, CHU Issaad Hassani, Beni Messous, Alger.
Date de soumission : 08 octobre 2019
Résumé : Malgré les avancées diagnostiques et thérapeutiques, les syndromes coronaires aigus restent l’une de causes les plus fréquentes de décès dans le monde. La connaissance des mécanismes physiopathologiques de l’accident athérothrombotique implique des facteurs anatomopathologiques et biochimiques liés à la plaque d’athérome ainsi que des facteurs biomécaniques agissant comme triggers. La connaissance et la compréhension des mécanismes impliqués est nécessaire afin de permettre une détection plus précoce des plaques à risque de thrombose, et une meilleure prise en charge en conséquence.
Mots clés : Athérothrombose, rupture de plaque, syndromes coronaires aigus, plaque vulnérable, stress pariétal endothélial.
Abstract: Despite advances in diagnosis and treatment, acute coronary syndromes remain one of the most common causes of death worldwide. Knowledge of the physiopathological mechanisms of atherothrombosis involve anatomopathological and biochemical factors related to the coronary artery plaque, and biomechanical factors such as endothelial shear stress. Reducing adverse clinical events remains the ultimate goal for diagnostic tests and medical therapies, the comprehension of these mechanisms is necessary to improve the management of high-risk patients.
Key words: Atherothrombosis, ruptured plaque, acute coronary syndromes, vulnerable plaque, endothelial shear stress.
Introduction
L’athérosclérose est une pathologie inflammatoire chronique, diffuse et évolutive. Elle présente trois territoires de prédilection : coronaire, cérébral et périphérique. Sa gravité est principalement liée au risque permanent d’accident aigu thrombotique notamment les syndromes coronaires aigus.
Malgré les avancées diagnostiques et thérapeutiques, les syndromes coronaires aigus demeurent un véritable enjeu de santé publique. En 2016, plus de 15,2 millions de décès étaient dus à des complications athérothrombotiques, dont plus de 9 millions étaient liés à l’atteinte coronaire (3).
Les facteurs de risques de l’athérosclérose sont bien connus. A côté des facteurs non modifiables, liés au patient tel que l’hérédité familiale, les facteurs de risques tels que l’obésité, les dyslipidémies, le tabac, le diabète ou encore l’hypertension artérielle ; représentent le premier angle d’attaque de cette maladie évolutive dont les complications sont aussi imprévisibles que redoutables.
La physiopathologie de l’accident athérothrombotique est complexe, elle implique des mécanismes liés à la plaque et des mécanismes liés aux conditions hémodynamiques. La connaissance des différentes étapes physiopathologiques de l’athérothrombose a permis le développement des grands axes thérapeutiques. Mais, bien que, bien étudiée, certains aspects restent encore à obscures, tels que les mécanismes impliqués dans l’érosion de plaque.
Rappel sur l’athérosclérose
-L’athérosclérose est une pathologie chronique, résultant d’un déséquilibre entre les entrées et les sorties de lipides.
-Elle est responsable de l’accumulation de lipoprotéines de basse densité (LDL-cholestérol) dans l’intima artérielle
-Les quatre mécanismes impliqués dans la formation de la plaque d’athérome sont :
- La pénétration des lipoprotéines dans l’intima artérielle
- Le recrutement des monocytes et leur transformation en macrophages puis en cellules spumeuses
- La réaction inflammatoire chronique avec la formation de la chape fibreuse
-Les lipides de la plaque sont d’abord intracellulaires puis deviennent extracellulaires. L’ensemble formera ce qu’on appelle le cœur lipidique. La plaque d’athérome est constituée d’une chape fibreuse se situant entre la lumière artérielle et le centre lipidique.
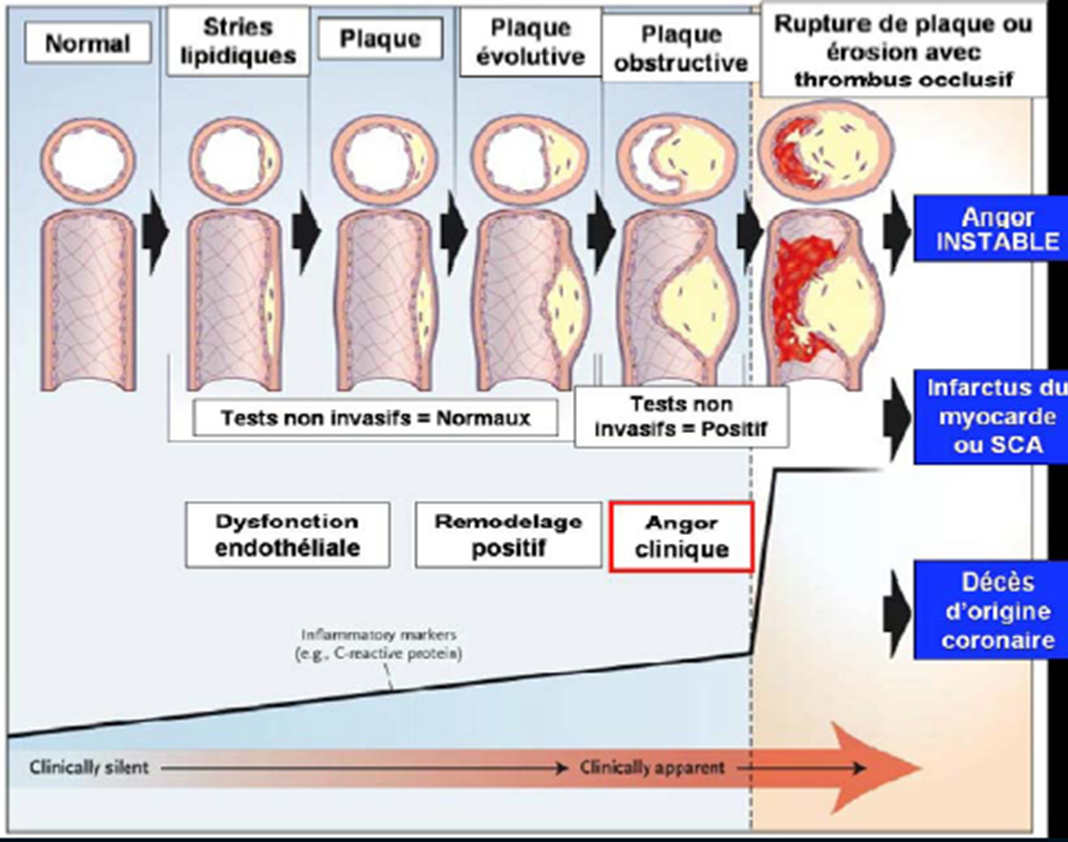
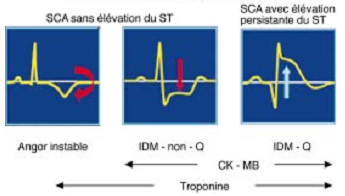
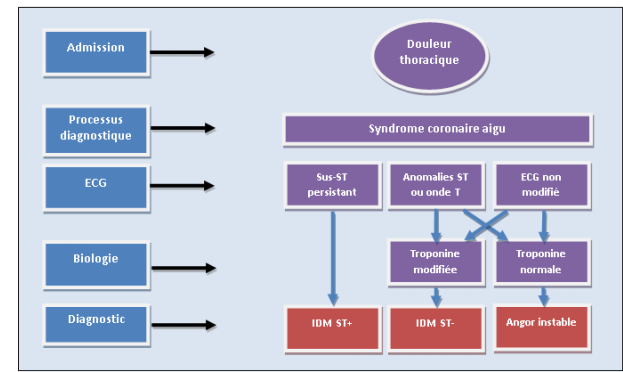
L’évolution de la plaque d’athérome commence très tôt sous forme d’une strie lipidique. Elle va croitre progressivement jusqu’à devenir hémodynamiquement obstructive, pouvant devenir cliniquement symptomatique et être responsable d’un syndrome coronaire chronique (autrefois appelé angor stable). Cette évolution peut être émaillée d’accidents aigus responsables d’une obstruction totale ou sub totale de l’artère plus connus sous le nom de syndromes coronaires aigus.
Image 1 : schéma représentant les étapes évolutive de la plaque d’athérome (d’après Jérôme Leoni, Physiopathologie de l’athérosclérose, mécanismes et prévention)
L’atherothrombose :
-L’athérothrombose est définie comme une déstabilisation de plaque d’athérome, aboutissant à la formation de thrombus à la surface de la plaque. Deux mécanismes principaux sont responsables de cette déstabilisation de plaque : la rupture de plaque et l’érosion de plaque.
-La rupture de plaque est définie par une solution de continuité, ou un « gap » dans chape fibreuse qui sépare le noyau lipidique de la lumière vasculaire.
– Le terme d’érosion de plaque a été introduit dans les années 90, il désigne une solution de continuité retrouvée au niveau de l’endothélium, mettant à nu l’intima de l’artère. L’examen anatomopathologique de l’artère thrombosée ne retrouve pas d’atteinte de l’intégrité de la chape fibreuse.
– Parallèlement à la rupture et à l’érosion, l’hémorragie de plaque peut être à l’origine du syndrome coronaire aigu. Elle peut survenir à partir d’une rupture de plaque ou à partir d’une néovascularisation.
-La rupture de plaque reste de loin le mécanisme le plus fréquent responsable des syndromes coronaires aigu ( 79% des infarctus du myocarde, 65 % des morts subites d’origine coronaire)(3). Elle est plus fréquente chez l’homme. L’érosion de plaque quant à elle se voit surtout chez les femmes de moins de 50 ans.
Rupture de la plaque :
La survenue de ces déstabilisations de plaque résulte de la synergie de deux types de facteurs :
-Des facteurs intrinsèques liés à la composition de la plaque, son activité métabolique et inflammatoire.
-Des facteurs extrinsèques liés essentiellement aux forces biomécaniques s’exerçant sur la plaque. La connaissance de ces facteurs permettra de différencier la plaque dite « vulnérable », à haut risque de rupture, de la plaque dite « stable ».
Facteurs intrinsèques
Il est admis que la plaque vulnérable a un cœur lipidique riche avec une chape fibreuse épaisse et se localise le plus souvent au niveau des segments proximaux des principales artères épicardiques.
-Lorsque la taille du noyau lipido-necrotique occupe plus de 40 % du volume total de la plaque, le risque de rupture est élevé. Ce cœur lipidique consistance molle, va alors transmettre aux berges de la plaque, les forces exercées par le stress hémodynamique, au sommet de la plaque.
-La capsule fibreuse conditionne la résistance de la plaque. La vulnérabilité de la plaque va dépendre de la cellularité et de la qualité de la matrice extracellulaire de la chape qui la recouvre. Avec le temps, la production, par les cellules inflammatoires locales de différents médiateurs pro-apoptotiques tels que IL-1 TNFa et INFg, va diminuer la proportion de CML, en particulier au niveau des zones d’épaulement.
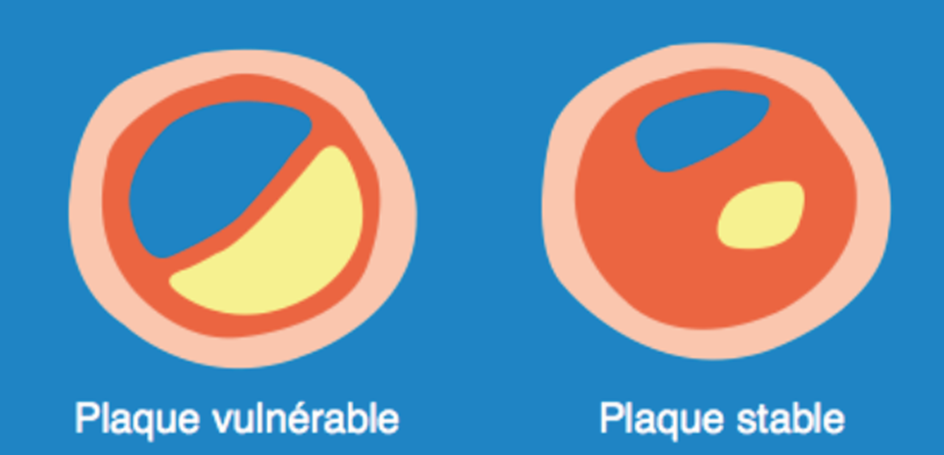
Image 2 : Schéma représentatif d’une plaque vulnérable par rapport à la plaque stable (d’après , N.Berrada L’athérothrombose : la maladie et les avancées thérapeutiques des vingt dernières années)
Facteurs extrinsèques :
Outre une fragilisation par des facteurs intrinsèques, la plaque subit également des contraintes externes augmentant la vulnérabilité de la plaque. Ces contraintes sont principalement représentées par le stress pariétal et les forces de friction engendrées par le flux sanguin turbulent au contact de la plaque.
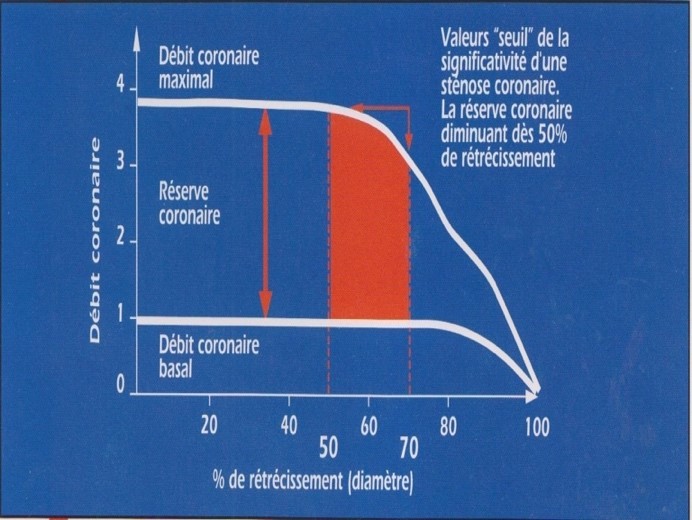
Dans l’étude PREDICTION (Prediction of Progression of Coronary Artery Disease and Clinical Outcome Using Vascular Profiling of Shear Stress and Wall) (1) un faible stress pariétal local était un facteur indépendant prédicteur de la progression de plaque d’athérome. Selon la morphologie de la plaque, le stress pariétal endothélial, est plus faible en amont et en aval de la sténose, favorisant la formation et la progression de la plaque
En contraste un stress pariétal élevé, s’appliquait au point le plus serré de la sténose, et augmentait la vulnérabilité et la thrombogénicité au niveau de la plaque, par conséquent représentait un facteur favorisant d’accident athérothrombotique. Une lésion hémodynamiquement obstructive (évaluée par FFR), engendrant un flux sanguin plus turbulent, et un stress pariétal plus important, serait alors plus susceptible de se rompre(1)
Comment reconnaitre la plaque à risque de rupture ?
Bien que ces caractéristiques soient bien connues, l’étude microscopique des plaques responsables de l’accident athérothrombotique a permis de décrire les caractéristiques de la plaque « vulnérable » et de distinguer les deux types de plaques
La plaque à risque de rupture : le prototype de la plaque à risque de rupture contient un large cœur nécrotique très riche en lipide avec une chape fibreuse fine (≤65µm) et inflammatoire. Ce sont généralement des plaques de grande taille, avec un remodelage positif marqué (phénomène de Glagov), limitant l’obstruction vasculaire (plaque moyennement obstructive à l’angiographie). D’autres caractéristiques sont décrites telles que une néovascularisation, des calcifications irrégulières et une inflammation adventitielle. (3)
La plaque à risque d’érosion : il s’agit d’un groupe de plaque de caractéristiques plus hétérogènes et ne sont pas encore bien étudiées. Il s’agirait de plaque moins étendues, avec un moindre remodelage, peu calcifiées, et de faible activité inflammatoire(5). Des études récentes par OCT ont décrit des érosions de plaque chez des patients ayant bénéficié de thromboaspiration avec intégrité de la chape fibreuse. Ces études sont en cours, mais il ne semble pas aisé de distinguer les plaques stables des plaques à risque d’érosion.(3)
-Dans PROSPECT, (Providing Regional Observations to Study Predictors of Events in the Coronary Tree), une large étude prospective, ayant inclus 697 patients admis pour syndrome coronaire aigu, ayant bénéficié d’une coronarographie avec imagerie intra coronaire multimodale des 03 artères coronaires, et traitement de la lésion coupable. Sur un suivi médian de 3.4 années, la survenue d’un évènement cardiovasculaire majeur, était jugé comme lié à la lésion coupable ou à une lésion non coupable(1).
Bien que la récurrence d’évènement ischémique fût liée de façon égale à la lésion coupable ou non coupable, la lésion non coupable était le plus souvent angiographiquement modérément sténosante, avec une surface de la lumière vasculaire ≤0.4cm2, ainsi qu’un noyau nécrotique volumineux et chape fibreuse fine.
Rôle de l’inflammation
Les différents facteurs de risque cardiovasculaire impliqués dans la maladie athérothrombotique engendrent la stimulation des processus inflammatoires. En exemple, l’angiotensine II participant à la pathogénèse d’hypertension artérielle, déclenche la production du NF-kb, important facteur de l’inflammation. De la même manière les cellules contenues dans la graisse abdominale, impliquée dans le diabète et l’insulinorésistence, produisent des facteurs pro-inflammatoires. Ces sites extravasculaires d’inflammation produisent des cytokines stimulant les cellules inflammatoires de l’intima artérielle. Des biomarqueurs tels que la CRP (C réactive protein) est un facteur prédicteur du risque cardiovasculaire.
Sur le plan histopathologique, l’analyse des lésions ayant provoqué un infarctus du myocarde fatal a révélé une stimulation de l’inflammation, notamment une accumulation de macrophages, et de cellules T activées, ainsi qu’une épaisseur réduite de la coiffe fibreuse aux sites de rupture de plaque et de thrombose. Les métallo-protéinases matricielles et les cystéines protéinases, produites par les macrophages activés, se localisent aux sites de rupture. Plusieurs de ces enzymes digèrent le collagène fibrillaire, réduisant l’épaisseur de la chape fibreuse et par conséquent la stabilité mécanique de la plaque. (6)
Facteurs déclenchants d’accident aigus
Plusieurs études ont identifiés des facteurs de risque transitoires favorisant la survenue de syndromes coronaires aigus. On retrouve, l’activité physique et sexuelle, le stress, l’infection, ou la prise de Cocaïne(5). Il semble que ces facteurs déclenchants engendrent une activation du système sympathique, ce qui augmente la pression artérielle, la fréquence cardiaque, le stress pariétal et l’activation plaquettaire. Le risque absolu de survenue d’un évènement cardiovasculaire dépend du risque du patient, et de la présence d’une coronaropathie préexistante(7).
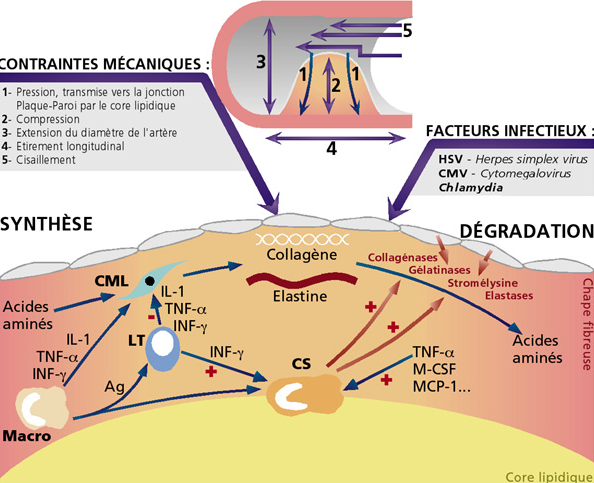
Image 3 : schéma représentant les différents facteurs intrinsèques et extrinsèques impliqués dans fragilisation de la plaque d’après Jérôme Leoni, Physiopathologie de l’athérosclérose, mécanismes et prévention)
Le processus thrombotique
La rupture ou l’érosion de la plaque met en effet le sang circulant au contact des éléments thrombogènes du cœur lipidique, provoquant ainsi l’activation des plaquettes, de la coagulation, et la formation du thrombus
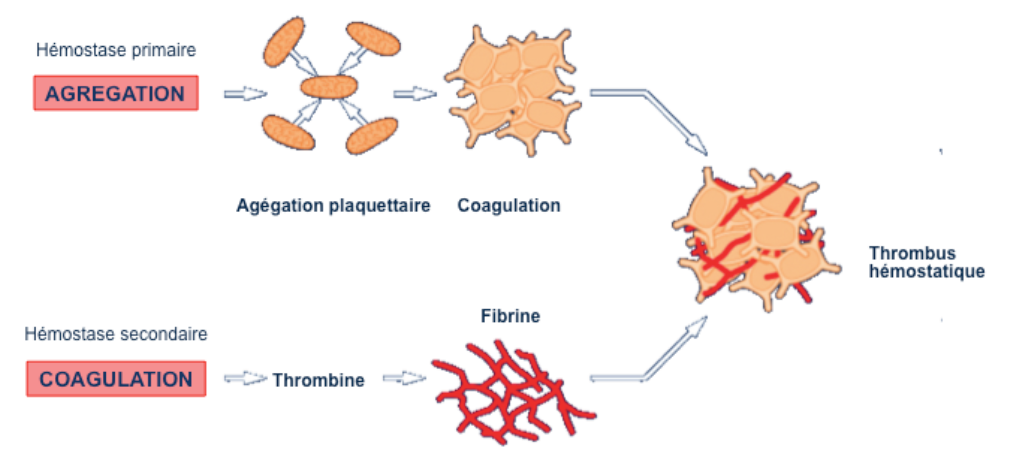
Image 4 : Principales étapes de la formation du thrombus(d’après , N.Berrada L’athérothrombose : la maladie et les avancées thérapeutiques des vingt dernières années)
La lésion de la plaque va mettre à nu le collagène et les microfibrilles du sous-endothélium qui représentent les points d’appel à l’adhésion plaquettaire. Cette étape nécessite l’intervention du facteur de Willebrand qui permettra la formation des ponts les reliant aux sites des glycoprotéines Ib plaquettaires(4).
L’activation plaquettaire va induire un changement de conformation des glycoprotéines GP IIb/IIIa . Ces GPIIb/IIIa activées interagissent spécifiquement, en présence de calcium, avec plusieurs protéines circulantes, et notamment avec le fibrinogène, ce qui permet la formation de ponts entre les plaquettes activées, c’est l’agrégation plaquettaire proprement dite.
La seconde conséquence fonctionnelle importante de l’activation des plaquettes est la libération du contenu de leurs granules. L’ADP et la sérotonine d’origine granulaire activent alors de nouvelles plaquettes adjacentes et participent à l’interaction paroi vasculaire/plaquettes. La synthèse du thromboxane A2, par les plaquettes activées à partir de l’acide arachidonique fournit un autre puissant agent vasoconstricteur favorisant l’agrégation plaquettaire (4)
Parallèlement à l’agrégation plaquettaire, l’activation de la cascade enzymatique de la coagulation, aboutira à la transformation du fibrinogène en fibrine, venant consolider le thrombus en formation.
La taille de l’agrégat plaquettaire dépend en grande partie de l’importance du stress pariétal induit par le flux sanguin qui sera d’autant plus important si de la sténose coronaire est obstructive. Lorsque l’agrégat atteint une taille suffisante pour modifier les conditions locales d’écoulement du sang, la coagulation devient alors efficace: le réseau fibrillaire de fibrine stabilise l’agrégat plaquettaire.
Image 5 : schéma représentant la cascade d’activation de l’agrégation plaquettaire (d’après Jérôme Leoni, Physiopathologie de l’athérosclérose, mécanismes et prévention)
Evolution :
Selon son importance et sa rapidité d’installation le thrombus peut avoir différentes modalités évolutives :
-La formation d’un thrombus au site d’une érosion ou d’une rupture de plaque expose au risque d’embolisation dans le territoire d’aval
-Le thrombus peut augmenter rapidement de volume et devenir complétement obstructif thrombus. Ces occlusions, si elles ne sont pas recanalisées peuvent passer à la chronicité, et être à l’origine du développement de circulations collatérales de suppléance
-Une incorporation progressive du thrombus à la plaque athéromateuse (thrombolyse physiologique). Cette dernière modalité évolutive, aboutit à la reperméabilisation partielle du vaisseau, au prix d’une augmentation du volume de la plaque .Cette augmentation de volume de plaque a pour conséquence l’aggravation de la sténose artérielle locale et sa fragilisation avec un risque de rupture.
L’athérosclérose est une maladie à évolution lente, sur plusieurs dizaines d’années, et offre ainsi l’opportunité d’un dépistage précoce et d’une prise en charge personnalisée du patient. Différentes modalités d’imagerie ont prouvé leur efficacité en pratique clinique pour la détection et la mesure de l’étendue de cette pathologie : l’IPS, le rapport intima –media à l’echodoppler artériel des carotides ainsi que le score calcique
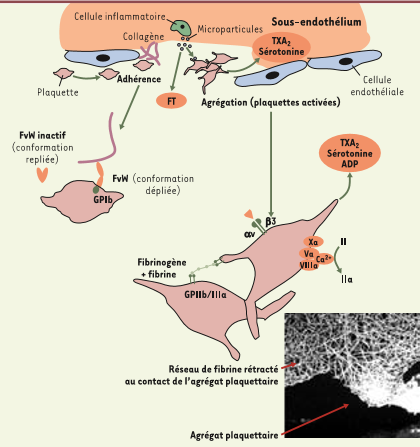
Image 5 : Schéma représentant les différentes modalités évolutive après rupture de plaque (d’après le polycopié du collège des enseignants de médecine vasculaire)
Messages clés
-L’atherothrombose est une pathologie inflammatoire, dont l’évolution est émaillée par accidents athérothrombotiques imprévisibles pouvant engager le pronostic vital
-Son évolution est lente, progressive et à bas bruit, elle laisse la possibilité au praticien de ralentir sa progression.
-Sa prise en charge repose essentiellement sur la prévention, par une lutte acharnée contre les facteurs de risques cardiovasculaires.
– La vulnérabilité de la plaque d’athérome est substrat physiopathologique de l’atherothrombose.
-Le mécanisme le plus fréquent est la rupture de plaque, en particulier dans la population masculine
-La plaque dite vulnérable, est une plaque contenant un cœur lipido-necrotique volumineux et une chape fibreuse fines, avec une activité inflammatoire importante
-Les forces biomécaniques s’exerçant sur la plaque d’athérome, dues au flux sanguin turbulent, augmentent le stress pariétal, la vulnérabilité de la plaque et favorisent l’activation plaquettaire.
-Une plaque hémodynamiquement obstructive, augmente la vulnérabilité de la plaque, par une augmentation de la turbulence du flux sanguin.
-Les données angiographiques et de l’imagerie multimodale intra coronaire a permis de mieux identifier les caractéristiques de la plaque vulnérable.
Conclusion :
La vulnérabilité de la plaque d’athérome est substrat physiopathologique de l’atherothrombose, elle résulte de la synergie de facteurs hémodynamiques tels que le stress pariétal endothélial, l’ischémie, de l’activation cellulaire et du remodelage vasculaire. La connaissance des caractéristiques physiologiques de cette plaque vulnérable associées aux données angiographiques et multimodales coronaires peuvent aider identifier les patients à risque. Toutefois la survenue d’un syndrome coronaire aigu est toujours imprévisible, et le meilleur traitement reste la prévention.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Référence :
1- Ford, T. J., Berry, C., De Bruyne, B., Yong, A. S. C., Barlis, P., Fearon, W. F., & Ng, M. K. C. (2017). Physiological Predictors of Acute Coronary Syndromes. JACC: Cardiovascular Interventions, 10(24), 2539–2547. doi:10.1016/j.jcin.2017.08.059
2-Jacob Fog Bentzon, Fumiyuki Otsuka, Renu Virmani, Erling Falk, – Mechanisms of Plaque Formation and Rupture Circulation Research. 2014;114:1852–1866 https://doi.org/10.1161/CIRCRESAHA.114.302721
3- Erling Falk, Masataka Nakano, Jacob Fog Bentzon, Aloke V. Finn, and Renu Virmani, Update on acute coronary syndromes: the pathologists’ view, European Heart Journal (2013) 34, 719–728.
4- Jean-Philippe Collet, Rémi Choussat and Gilles Montalescot, L’agrégation plaquettaire et ses inhibiteurs dans les syndromes coronariens aigus M/S : médecine sciences, Volume 20, Number 3, mars 2014
5- White SJ, Newby AC, Johnson TW. Endothelial erosion of plaques as a substrate for coronary thrombosis. Thromb Haemost. 2016 Mar;115(3):509-19. doi: 10.1160/TH15-09-0765. Epub 2016 Jan 21.
6- G. K. Hansson,1 P. Libby,2 and I. Tabas3 PMID: 26260307 Inflammation and plaque vulnerability ,J Intern Med. 2015 Nov; 278(5): 483–493. doi: 10.1111/joim.12406
7-Kurose S, Iwasaka J, Tsutsumi H, Yamanaka Y, Shinno H, Fukushima Y, Higurashi K, Imai M, Masuda I, Takeda S, Kawai C, Kimura Y. Effect of exercise-based cardiac rehabilitation on non-culprit mild coronary plaques in the culprit coronary artery of patients with acute coronary syndrome. Heart Vessels. 2016 Jun;31(6):846-54. doi: 10.1007/s00380-015-0681-1. Epub 2015 Apr 21