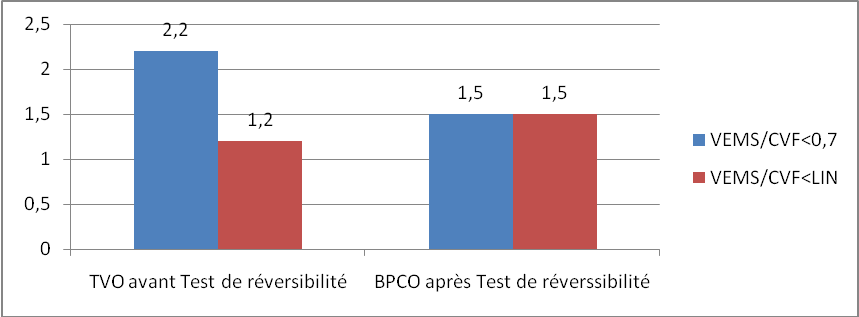
Les exacerbations sévères, l’échec du traitement, la difficulté du diagnostic sont les motifs fréquents d’hospitalisation de la BPCO. La prise en charge de la BPCO en milieu hospitalier est rationnelle, elle dépend de la situation clinique et de son historique.
L. Baough, N. Zidouni, M. Gharnaout, Service de Pneumo-Phtisiologie Matiben CHU Issaad Hassani, Béni-Messous, Alger
Date de soumission : 20 février 2021
Résumé : Les exacerbations sévères, l’échec du traitement, la difficulté du diagnostic sont les motifs fréquents d’hospitalisation de la BPCO. La prise en charge de la BPCO en milieu hospitalier est rationnelle, elle dépend de la situation clinique et de son historique. La présence de critères de gravité guide la priorité des modalités de prise en charge du patient BPCO. Les patients présentant une exacerbation de BPCO avec insuffisance respiratoire aiguë doivent bénéficier précocement de la ventilation non invasive (VNI). Celle-ci permet de diminuer la morbi-mortalité et d’améliorer les symptômes. La sévérité de la maladie ne constitue pas une contre-indication à une réhabilitation respiratoire (RR) mais nécessite d’adapter l’évaluation et le contenu du programme. La discussion multidisciplinaire en milieu hospitalier est nécessaire dans l’évaluation de la pathologie associée à la BPCO.
Mots clés : BPCO très sévère, exacerbations, critères de gravités, insuffisance respiratoire aiguë, prise en charge multidisciplinaire.
Abstract: Severe exacerbations, treatment failure, difficulty in diagnosis are the frequent reasons for hospitalization of COPD. The management of COPD in a hospital is rational, it depends on the clinical situation and its history. The presence of severity criteria guides the priority of the management methods for the COPD patient. Patients with exacerbated COPD with acute respiratory failure should benefit from non-invasive ventilation (NIV) early on. This reduces morbidity and mortality and improves symptoms. The severity of the disease is not a contraindication to respiratory rehabilitation (RR) but requires adapting the evaluation and the content of the program. Multidisciplinary discussion in the hospital setting is necessary in the assessment of the pathology associated with COPD.
Keywords: very severe COPD, exacerbations, criteria of severity, acute respiratory failure, multidisciplinary management.
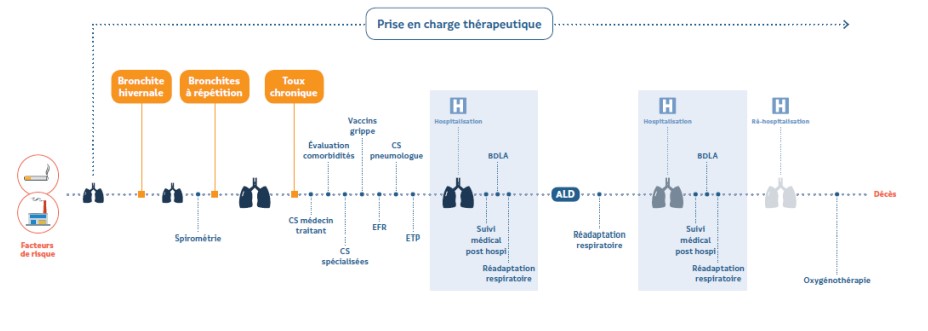
La stratégie de prise en charge de la BPCO en milieu hospitalier est globale et multidisciplinaire, caractérisée par des investigations et une thérapeutique qui est guidée par le tableau clinique du patient et le degré de sévérité de la BPCO.
Quels sont les critères d’hospitalisation de la BPCO ?
Parmi les causes d’hospitalisation sous citées, les exacerbations sévères constituent le motif le plus fréquent.
- Exacerbations fréquentes ou épisode récent d’évolution défavorable
- Exacerbation chez un sujet âge avec ou sans comorbidités
- Incertitude diagnostique, absence de réponse au traitement initial
- Signes cliniques ou gazométriques de gravité immédiate
- Nécessité et indication d’une oxygénothérapie au stade IV de la BPCO
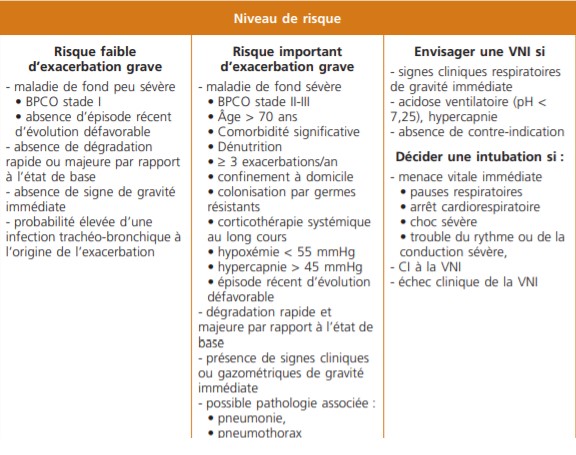
L’ATS/ERS et la SPLF (1,2) ont élaboré des échelles de gravité de la BPCO afin de guider la prise en charge thérapeutique (tableau 1).
Tableau 1. Échelle de gravité de l’exacerbation de la BPCO
Les exacerbations motifs d’hospitalisation
Une augmentation du volume, une modification de coloration des expectorations associées à une fièvre chez un sujet âgé atteint de BPCO sévère est le tableau le plus courant de motif d’hospitalisation
Ce tableau peut s’associer à d’autres critères de gravité (Tableau 2). La recherche de ces critères de gravité est une priorité dans l’attitude du pneumologue avant de décider la conduite thérapeutique.
Tableau 2. Signes de gravité immédiate d’une exacerbation d’une BPCO (3)
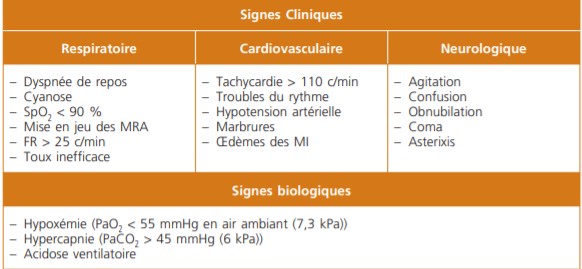
Rechercher le facteur déclenchant de l’exacerbation guide l’attitude thérapeutique
Il existe différents facteurs déclenchant des exacerbations aiguës de BPCO (EABPCO), principalement les infections, virales et bactériennes, mais sont également incriminés la pollution, l’arrêt des traitements de fond ou un terrain génétique spécifique. Toutes ces étiologies peuvent aussi se combiner pour déclencher une EABPCO (4). Néanmoins dans 1/3 des cas, la cause des exacerbations reste inexpliquée.
Les virus (tels que les rhinovirus et le virus influenzae) sont responsables des EA BPCO dans près de la moitié des cas (5).
Les bactéries pyogènes telles que H. influenzae, Streptococcus pneumoniae, Moraxella catarrhalis et P aeruginosa peuvent coloniser les voies aériennes inférieures des patients atteints de BPCO à l’état stable. Retrouver ces bactéries lors d’une EABPCO rend donc plus difficile leur imputabilité dans la genèse de l’exacerbation (6). La purulence, ou la majoration de la purulence de l’expectoration lors d’une EA BPCO semble être le meilleur marqueur d’une origine bactérienne de cette exacerbation.
La présence d’une ou de comorbidités associée(s) à la BPCO guide le pneumologue dans la demande de la poursuite des examens paracliniques.
Les comorbidités associées à la BPCO (Tableau 3), sont fréquentes et souvent multiples et doivent être recherchées systématiquement, particulièrement les maladies cardiovasculaires (7), (insuffisance coronarienne, infarctus du myocarde), sont souvent retrouvées dans la BPCO.
Tableau 3. Les comorbidités à rechercher lors de l’hospitalisation d’un malade BPCO
|
Cancer du poumon ;
|
|
Pathologies cardiovasculaires (la consultation d’un cardiologue est recommandée dans l’année qui suit le diagnostic) ;
|
|
Syndrome d’apnée du sommeil ;
|
|
Dénutrition, fonte musculaire ;
|
|
Ostéoporose ;
|
|
Dépression et/ou anxiété ;
|
|
Co addictions (alcool, cannabis) ;
|
|
Diabète ;
|
|
Anémie ;
|
|
Reflux gastro-œsophagien.
|
Quels sont les examens paracliniques à réaliser devant une exacerbation sévère (8)?
Selon l’état du patient, des examens complémentaires communs à toute exacerbation seront demandés :
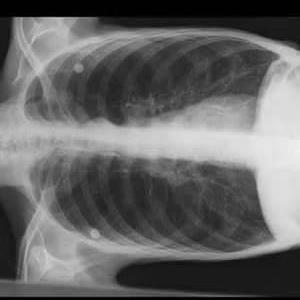
- Radiographie du thorax
- NFS avec un équilibre leucocytaire
- Gazométrie
- ECG
- Ionogramme
- Glycémie, urée et créatinémie
Selon le contexte clinique et biologique ces explorations pourront être complétées par le dosage d’une peptide natriurétique (BNP ou Pro BNP), troponines, DDimères, angioscanner thoracique et/ou un écho-Doppler veineux des membres inférieurs si complication cardiaque.
D’autres examens complémentaires seront pratiqués en dehors de toute exacerbation et selon l’orientation clinique, dans le cadre de la recherche d’une complication, d’un diagnostic difficile, d’une association avec une autre pathologie respiratoire (pneumopathie interstitielle, SAOS, cancer bronchique). Les examens suivant seront réalisés :
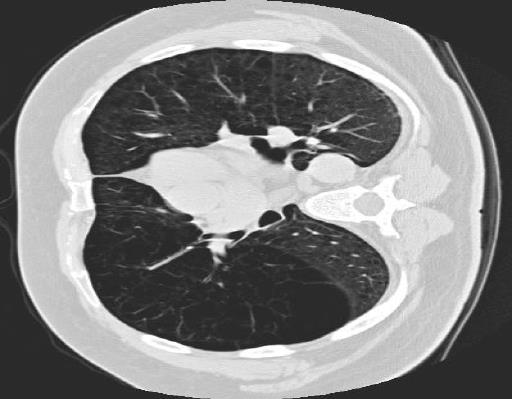
- Une TDM thoracique
- Une endoscopie bronchique selon les symptômes et le contexte clinique ou radiologique.
- Une pléthysmographie à la recherche d’une distension, de lésions emphysémateuses, d’un syndrome restrictif et si nécessaire dans le cadre de l’évaluation précédant la mise en place d’une réhabilitation respiratoire (RR)
- Diffusion de la DLCO
- Un enregistrement polysomnographique si suspicion d’un syndrome d’apnée du sommeil associé
- Test de marche de 6 minutes si dyspnée stade 3 ou 4 de l’échelle MMRC,
- Dosage de l’α 1 antitrypsine si forme d’emphysème évocatrice d’un déficit
- Épreuve d’exercice maximal cardiorespiratoire notamment avant indication d’une RR
Le traitement médicamenteux en milieu hospitalier
L’utilisation des bronchodilatateurs dans la BPCO sévère hospitalisée
Les bêta mimétiques à brève durée d’action sont recommandés par voie nébulisée (9). En l’ absence de réponse rapide, un anticholinergique est associé. Les méthylxanthines n’ont pas d’indication.
La survenue d’une tachycardie ou d’une hypokaliémie est exceptionnelle avec les aérosols de bêta-2-mimétiques. Les anticholinergiques sont à utiliser avec prudence en cas de glaucome ou d’obstacle prostatique.
Aucune recommandation précise n’existe. Ainsi, on pourrait proposer :
- Bêta-2-mimétiques : 2 fois 5 mg de salbutamol en nébulisation sous air, à 20 min d’intervalle ;
- Au décours, une nébulisation associant salbutamol et ipratropium (0,50 mg), en cas d’amélioration insuffisante ;
- Salbutamol toutes les 30 min si les symptômes persistent.
Après amélioration, les nébulisations de béta-2-mimétiques seront espacés toutes les 4 h.
La place des corticoïdes dans les exacerbations sévères de la BPCO
Les corticoïdes systémiques tels que la prednisolone, la prednisone et la cortisone, sont couramment utilisés dans le traitement des patients.
Les recommandations actuelles (10) préconisent de traiter ces patients avec des corticoïdes systémiques pendant 7 à 14 jours.
La posologie orale est de 30-40 mg de prednisolone par jour pendant 7-14 jours, à défaut 40 mg de méthylprednisolone seront administrés en IV.
Quel antibiotique choisir ?
Le critère de choix de l’antibiothérapie est probabiliste, elle doit être active sur les principaux germes suspectés et doit tenir compte des résistances locales. Le choix des molécules proposées dépend de la gravité de l’exacerbation ou de la BPCO sous-jacente.
Leur emploi est d’autant plus justifié que l’exacerbation est sévère et la suspicion d’infection bactérienne est forte, l’antibiothérapie doit être proposée en cas de franche purulence de l’expectoration. La procalcitonine pourrait s’avérer utile pour aider le clinicien à décider d’une antibiothérapie.
Les antibiotiques utilisés (béta-lactamines, macrolides, pristinamycine, télithromycine, C3G et fluoroquinolones) sont d’efficacité équivalente.
En présence de critères de gravité, l’antibiothérapie de première intention sera amoxicilline-acide clavulanique (3 g/jour) ou une C3G injectable (céfotaxime 3 g/j, ceftriaxone 2 g/j), une fluoroquinolone antipneumococcique. En l’absence de critères de gravité un traitement par amoxicilline, télithromycine, pristinamycine ou macrolide est recommandé (11). Cette antibiothérapie ne s’adresse qu’à la surinfection bronchique et doit être limitée à 5 jours, maximum de 10 jours en cas d’exacerbation sévère. En cas de pneumonie, on se référera aux recommandations spécifiques.
Les médications non pharmacologiques
La nécessité d’une oxygénothérapie impose le recours à l’hospitalisation
C’est la pierre angulaire du traitement hospitalier des EAC. L’objectif est d’obtenir une SaO2 > à 90% et une PaO2> à 8kPa (60mmHg). Le risque de l’oxygénothérapie est représenté par l’apparition ou une aggravation insidieuse d’une hypercapnie.
Pour cela un contrôle du débit d’oxygénothérapie (conscience, FR, SpO2, gaz du sang), doit être réalisé 30 minutes après le début de l’oxygénothérapie pour s’assurer d’une oxygénation optimale et de l’absence d’une hypercapnie ou d’une acidose respiratoire.
L’oxygénothérapie évite les complications liées à une hypoxémie sévère, optimise la délivrance en oxygène des tissus périphériques et diminue la dyspnée.
L’indication de la ventilation non invasive (VNI) est préconisée dans la décompensation respiratoire de la BPCO
Chez la BPCO en décompensation respiratoire, la VNI est indiquée en dehors d’un épisode associé à une décompensation hypercapnique.
L’’intérêt de la VNI est bien établi, sur de multiples critères en cas d’exacerbation avec insuffisance respiratoire aiguë. Elle doit être instaurée précocement, avant que ne surviennent une acidose sévère ou une défaillance multiviscérale.
La VNI exige une surveillance clinique et paraclinique, particulièrement au début de sa mise en œuvre : fréquence respiratoire, tension artérielle, fréquence cardiaque, oxymétrie de pouls, gazométrie, ECG.
La gravité initiale du tableau clinique pourra cependant imposer d’emblée l’intubation endo-trachéale immédiate : arrêt cardiaque ou bradycardie extrême, apnée ou bradypnée < 8/min, coma, une mauvaise tolérance par un patient agité non coopérant ainsi que les contre-indications classiques de la VNI (vomissements, hémorragie digestive haute, traumatisme crânio-facial grave, obstruction de voies aériennes supérieures, pneumothorax non drainé, état de choc, arythmie sévère).
La ventilation non invasive (VNI) en pression positive, en cas d’exacerbations aiguës, améliore les gaz du sang et le pH, réduit la mortalité hospitalière, diminue la fréquence du recours à la ventilation mécanique invasive et à l’intubation trachéale, diminue le temps de séjour à l’hôpital et la morbi-mortalité (12).
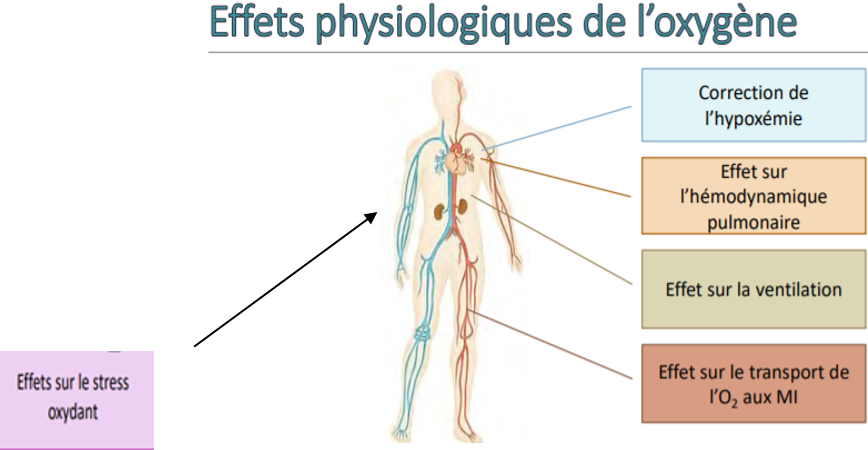
Le patient à sa sortie nécessite-t-il une oxygénothérapie de longue durée ?
Une évaluation initiale de la BPCO très sévère va permettre d’identifier la nécessité de l’indication de L’oxygénothérapie de longue durée (OLD)
Cette évaluation faite en dehors de l’exacerbation permet de définir si le patient est répondeur :
- Diminution d’au moins 1 point sur l’échelle visuelle analogique de dyspnée
- Augmentation du périmètre de marche au TM6 de 10%
- Augmentation du temps d’endurance
L’indication de l’OLD :
Patients en hypoxémie sévère, avec une PaO2 < 55 mm Hg ou une PaO2 entre 56 et 59 mm Hg, associée à des signes cliniques d’hypoxie tissulaire, signes cliniques de cœur pulmonaire chronique (CPC) et/ou diagnostic avéré d’hypertension artérielle pulmonaire (HTAP), (pression artérielle pulmonaire moyenne > 25 mm Hg mesurée lors d’un cathétérisme droit),
- Désaturations artérielles en O2 nocturnes sans relation avec un syndrome d’apnée du sommeil (SaO2 < 90% plus de 30% du temps d’enregistrement),
- Polyglobulie (Ht > 55%) ;
- Bénéfique si la durée est > 15 heures/jour ;
Fig 2. : L’oxygénothérapie de longue durée diminue le taux de mortalité.
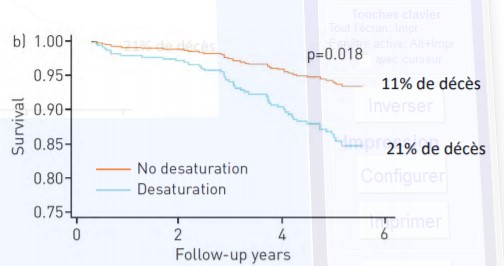
Autres traitements
La kinésithérapie respiratoire incluant la stimulation de la toux et l’expiration forcée a un intérêt pour désencombrer l’arbre bronchique. Cependant, sa fréquence et sa durée ne sont pas standardisées. La percussion thoracique et le drainage postural parfois controversés semblent être bénéfiques chez les patients produisant plus de 25 ml/j d’expectorations ou ceux présentant des atélectasies.
Correction des troubles électrolytiques et de la dénutrition. La prévention des maladies thromboemboliques est justifiée notamment chez les patients immobilisés, déshydratés.
La prise en charge de la maladie doit être globale et multidisciplinaire
Quel que soit le stade de la BPCO l’avis de spécialistes en coordination avec le pneumologue est sollicité dans les situations suivantes :
- Dans l’évaluation approfondie des comorbidités le spécialiste peut être sollicité (cardiologue, endocrinologue, psychiatre, ou autre spécialiste).
- Dans l’évaluation des expositions professionnelle (pneumologue en lien avec le médecin du travail)
- Dans l’indication de la RR et/ou maintien d’une activité physique adaptée (pneumologue, cardiologue, kinésithérapeute, psychologue, diététicien).
- Dans la persistance, rechute du tabagisme (le pneumologue, psychologue, diététicien.)
- Dans la prise en charge d’une BPCO très sévère (stade IV) associée à une insuffisance respiratoire sous OLD et ou VNI, une coordination est nécessaire entre le médecin généraliste le pneumologue et le prestataire.
Au terme de l’hospitalisation du patient, pourra-t-il bénéficier d’une réhabilitation ?
La réhabilitation respiratoire (RR) est un programme de prise en charge multidisciplinaire de la BPCO qui contient un réentraînement à l’effort dont l’efficacité a été démontrée dans l’amélioration de la qualité de vie, de la dyspnée, de la tolérance à l’effort, et plus récemment de la survie.
Parmi les outils essentiels à utiliser en plus de l’avis des autres spécialistes pour décider de l’indication d’une RR : L’index BODE (Tableau 4), système gradué multidimensionnel évaluant les expressions respiratoires et systémiques, respecterait davantage la physiopathologie et la clinique de la BPCO. Ce score est utilisé aussi pour évaluer l’efficacité d’une réhabilitation respiratoire.
Tableau 4. Score de BODE
| |
0
|
1
|
2
|
3
|
| |
IMC(kg/m2)
|
<21
|
>21
|
|
|
|
0
|
VEMS (% de la valeur théorique)
|
>65
|
50-64
|
36-49
|
<35
|
|
D
|
MMRC (0-4)
|
0-1
|
2
|
3
|
4
|
|
E
|
Distance parcourue lors du test de marche de 6-minutes (m)
|
>350
|
250-349
|
150-249
|
<149
|
La sévérité de la maladie ne constitue pas une contre-indication à une RR mais nécessite d’adapter l’évaluation et le contenu du programme
Un bilan fonctionnel respiratoire et cardiologique sera fait en dehors de toute exacerbation chez le patient à la recherche de contre-indication à l’entrainement à l’exercice.
Quelles sont les contre-indications de la RR ?
Il est recommandé de rechercher systématiquement les contre-indications de l’entraînement à l’exercice avant de débuter une RR :
- Contre-indications cardiovasculaires à l’exercice.
- Instabilité de l’état respiratoire (acidose respiratoire non compensée)
- Affection interférant avec le processus de RR (maladie neuromusculaire évolutive, maladie psychiatrique)
Il est recommandé de rechercher des contre-indications relatives :
- Affection intercurrente évolutive (pathologies locomotrices par exemple)
- Manque persistant de motivation et d’observance du patient.
- Avant le programme de RR chez un patient atteint de BPCO, il est recommandé d’évaluer les déficiences, l’incapacité fonctionnelle et le désavantage psychosocial du patient.
Conclusion
La BPCO peut évoluer dans les cas extrêmes vers une détresse respiratoire aiguë et une mort par asphyxie. Mais la BPCO expose également à plus de risque d’infection bronchique, à des exacerbations dont certaines nécessiteront une hospitalisation.
Ces exacerbations sont fréquentes et responsables d’une charge considérable pour la collectivité.
Aucune thérapeutique ne peut ralentir le déclin du VEMS en dehors de l’arrêt du tabagisme.
- Les bronchodilatateurs améliorent l’incapacité,
- Les corticoïdes inhalés n’enrayent pas la chute du VEMS,
- Les corticoïdes systémiques doivent être évités au long cours.
- La réhabilitation respiratoire permet de réduire les symptômes et d’améliorer la qualité de vie en augmentant la tolérance à l’effort.
- Les exacerbations de la maladie sont fréquentes et responsables d’une charge considérable pour la collectivité.
Liens d’intérêts : Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. GOLD, 2020.
- B Delclaux Exacerbations de BPCO : signes de gravité et facteurs pronostiques, RMR, Vol 34, N° 4 : 353–358, 2017
- Guideline-chronic obstructive pulmonary disease. 2006. Pothirat C et al. Int J Chron Obstruct Pulm Dis 2015 ; 10 : 1291–1298
- Wedzicha J.A., Seemungal T.A. COPD exacerbations: defining their cause and prevention. Lancet. 2007;370:786–796.
- Greenberg SB, Allen M, Wilson Respiratory viral infections in adults with and without chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2000.
- Molyneaux P.L., Mallia P., Cox M.J. Outgrowth of the bacterial airway microbiome after rhinovirus exacerbation of chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2013;188:1224–1231.
- McAllister D.A., Maclay J.D., Mills N.L. Diagnosis of myocardial infarction Following hospitalization for exacerbation of COPD Eur Respir J 2012 ; 39 : 1097-1103
- Jébrak. Quelles sont les investigations nécessaires lors d’une exacerbation de BPCO chez un patient hospitalisé ? RMR vol : 34, N°4 : 375-381,l 2017
- McCrory DC, Brown CD. Anti-cholinergic bronchodilators versus beta2-sympathomimetic agents for acute exacerbations of chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2002 ; 4 : CD003900
- Niewoehner DE, Erbland ML, Deupree RH, Collins D, Gross NJ, Light RW, Effect of systemic glucocorticoids on exacerbations of chronic obstructive pulmonary disease. N Engl J Med1999;340:1941—7
- Stolz D, et al. Antibiotic treatment of exacerbations of COPD: a randomized, controlled trial comparing procalcitonin-guidance with standard therapy. Chest 2007 ;
- Jose Luis Lopez-Campos, Lights and shadows of non-invasive mechanical ventilation for chronic obstructive pulmonary disease (COPD) exacerbations. Annals of thoracic Medicine. 2015 Apr-Jun; 10(2): 87–93
Télécharger le PDF de cet article