O. DRALI (¹), N. LAMDJADANI (2), H. BERRAH (¹), Z. ARRADA(¹) (1) Service de Pédiatrie B ; (2) Service d’Épidémiologie et de Statistiques, CHU Nafissa Hammoud, Hussein Dey, Alger.
Résumé : Selon l’OMS, le lait maternel est l’aliment naturel et idéal pour le nourrisson durant les premiers mois de sa vie. Dans les pays en développement, on observe une tendance au déclin de l’allaitement maternel. Nous nous proposons, à travers ce travail d’évaluer les connaissances et les pratiques sur l’allaitement maternel et de déterminer les facteurs qui influencent les mères à la mise en route de l’allaitement.
Mots-clés : Allaitement maternel, Algérie, connaissances, pratiques.
Abstract : According to WHO, breast milk is the natural and ideal food for infants during the first months of life. In developing countries, there is a trend towards declining breastfeeding. We propose through this work, to evaluate breastfeeding knowledge and practices and determine the factors that influence mothers to start breastfeeding.
Key-words : Breastfeeding, Algeria, knowledge, practices.
Introduction
Les bénéfices de l’allaitement maternel sont nombreux, et ce dans tous les milieux socio-économiques. Ils concernent la santé des enfants et de leur mère, la relation mère-bébé, mais aussi l’équilibre socioéconomique des familles, des États, et la protection de l’environnement.
Ce geste que des millions d’années d’évolution humaine n’ont pas modifié, fait partie intégrante de notre patrimoine biologique et humain.
Matériel et méthodes
Il s’agit d’une étude prospective, analytique et transversale réalisée entre mars 2014 et mars 2016. 508 femmes ayant des enfants âgés entre 0 et 24 mois ont été interrogées lors des différentes séances de vaccination.
Les renseignements étaient retranscrits sur une fiche technique préétablie et l’exploitation statistique était réalisée sur logiciel SPSS 22.
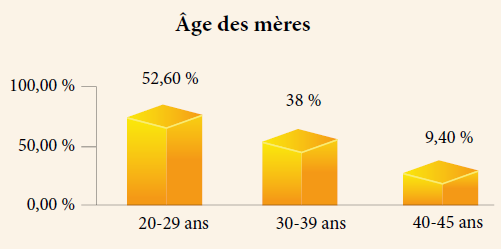
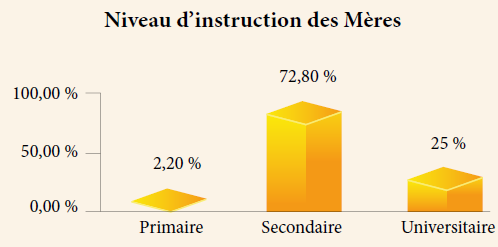
Les difficultés retrouvées au cours d’un allaitement maternel (AM) antérieur étaient dominées par une insuffisance lactée (60 %).
Environ 50,3 % n’avaient aucune idée sur la valeur du colostrum. Seules 12,2 % des parturientes ont bénéficié des informations prénatales sur l’AM. 67,3 % des mères avaient donné d’autres liquides non lactés.
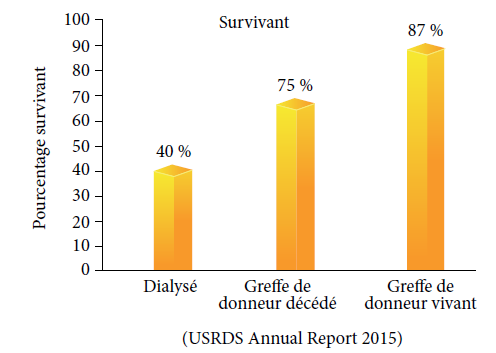
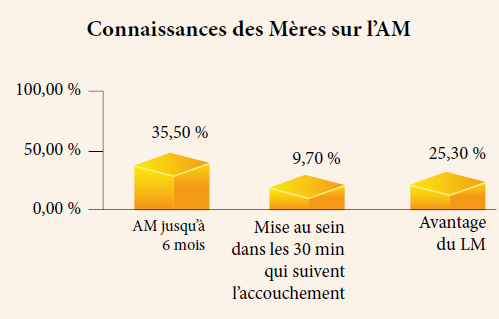
Seulement un tiers des mères savaient que l’allaitement maternel devait être exclusif jusqu’à 6 mois et 25 % avaient connaissance des avantages du lait maternel.
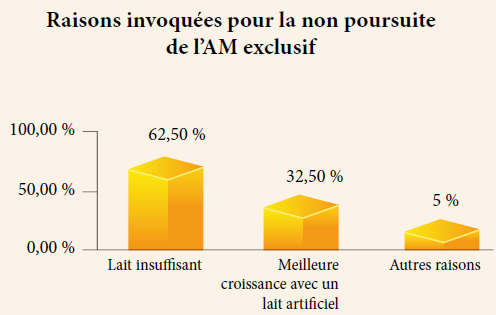
Les raisons invoquées par les mères pour la non poursuite de l’AM étaient dans 62,5% des cas une insuffisance lactée suivie dans 32,5% des cas par une meilleure croissance avec le lait artificiel.
Il n’y a pas de corrélation statistiquement significative entre la durée de l’allaitement maternel exclusif et l’âge de la mère ainsi que son niveau d’étude (P>0,05). Elle diminue par contre de façon statistiquement significative avec la parité ainsi qu’avec la profession de la mère (P<0,05).
Discussion
Depuis la fin du XIXe siècle, des substituts de lait humain ont été commercialisés, l’alimentation au lait industriel est devenue la norme. Notre étude relève comme d’autres études un faible taux d’allaitement maternel exclusif jusqu’à six mois soit 8 %, alors que c’est ce mode d’allaitement qui est prôné par l’OMS et l’UNICEF (1).
Notre taux est faible contrairement à celui retrouvé au Maroc par Barkat et al. soit 31 % en 2004. Aux États- Unis selon l’étude de Sheally et al. (2), plus de la moitié des mères allaitent leurs enfants uniquement avec du lait maternel jusqu’à 4 mois.
Selon l’OMS et l’UNICEF le lait maternel est l’aliment naturel et idéal pour le nourrisson durant les premiers mois de sa vie. Tout enfant doit recevoir exclusivement le lait de sa mère dès la naissance et le plus longtemps possible pendant au moins les deux premières années de la vie (1).
Le lait maternel a des avantages énormes : c’est un aliment complet, équilibré, économique, spécifique et stérile, sa température est idéale car il est donné directement du sein de la mère à la bouche de l’enfant. L’allaitement au sein maintient une relation psychoaffective favorable au bon développement de l’enfant et permet un meilleur épanouissement de la mère et de l’enfant. L’allaitement constitue la meilleure façon de nourrir un nouveau-né en bonne santé (2).
Certains travaux ont montré que l’introduction précoce des aliments de complément est associée à une augmentation du risque des maladies diarrhéiques (3).
Selon l’OMS et l’UNICEF, seulement 55 % des nourrissons dans le monde bénéficient pendant les 4 premiers mois de leur vie d’un allaitement maternel exclusif, ce qui est très insuffisant.
Dans les pays en développement, on observe une tendance au déclin de l’allaitement maternel, surtout dans les grandes villes. Dans les sociétés rurales traditionnelles d’Afrique, d’Asie, et d’Amérique du sud les femmes sont valorisées par leur maternité où l’allaitement au sein prend une part importante.
Cependant, certaines pratiques socioculturelles ou religieuses peuvent empêcher un allaitement maternel exclusif telle que la croyance du « colostrum mauvais » car considéré à tort comme sale (1).
Plusieurs raisons ont été évoquées pour expliquer ce déclin dans nos pays parmi lesquelles la perte des valeurs traditionnelles, la migration des familles dans les villes, le retard de la première tétée, les pressions commerciales (publicités) abusives des fabricants de laits artificiels (3).
Pour permettre aux mères de débuter et de maintenir l’allaitement exclusif au sein pendant 6 mois, l’OMS et l’UNICEF recommandent :
- De commencer l’allaitement dans la première heure qui suit la naissance ;
- De s’en tenir à l’allaitement exclusif au sein c’est-à-dire que le nourrisson ne doit absorber que du lait maternel et aucune autre nourriture ou boisson, pas même de l’eau ;
- D’allaiter à la demande c’est-à-dire aussi souvent que l’enfant le réclame, de jour comme de nuit;
- De ne pas utiliser de biberons, de tétines ou de sucette
Nous avons noté dans notre étude qu’il n’y a pas de corrélation statistiquement significative entre la durée de l’allaitement maternel exclusif et l’âge de la mère et son niveau d’étude (p>0,05). Kobela a retrouvé par contre que l’âge, la parité, le niveau d’éducation, le travail externe de la mère et le milieu urbain sont les facteurs influençant négativement l’allaitement maternel. Mais Nlend et al. (3) ont décrit que la durée de l’allaitement maternel exclusif croit avec le nombre d’enfants.
L’étude des coûts-bénéfices sanitaire et psychologiques de l’allaitement est particulièrement difficile en raison de nombreux facteurs socio-économiques, psychosociaux, et environnementales. Selon la littérature scientifique, allaiter le bébé au sein présente de nombreux avantages. L’allaitement maternel diminue le risque d’al-
lergies primaires chez l’enfant, sauf peut-être pour les enfants prédisposés aux allergies (4). Le risque d’asthme, de dermatite atopique, de rhinite allergique et d’allergie aux protéines de lait de vache augmenterait en l’absence d’allaitement, tout comme le risque infectieux (5).
Grâce au colostrum (et parce que l’allaitement ne fait pas appel à de l’eau non-potable pour préparer un lait artificiel), l’allaitement au sein diminue le risque d’infections des voies aériennes supérieures (6) et le risque d’otites moyennes aiguës (6). Dans les pays dits développés, un allaitement de plus de 4 mois diminue le risque d’infections respiratoires sévères nécessitant une hospitalisation (7).
Dans les pays en voie de développement, les bénéfices de l’allaitement sont encore plus marqués, diminuant fortement la mortalité par pneumonie ou infection respiratoire basse et la mortalité générale de l’enfant (et du nourrisson de moins de six mois par cause de diarrhée) (5). En effet, l’accès à une source d’eau potable de bonne qualité, préalable indispensable à l’utilisation de substituts de lait humain, est souvent peu aisé, avec un risque de contamination infectieuse important. L’allaitement maternel est d’autant plus recommandé dans ce contexte, avec la possibilité de sauver près de 1,3 million d’enfants chaque année si l’allaitement était massivement utilisé (8). Les selles seraient moins acides, ce qui limiterait l’érythème fessier. Le lait maternel se digérerait plus facilement (entre 20 minutes et 2 heures). La mécanique de succion au sein (« tétée physiologique ») permettrait un meilleur développement de la mâchoire, et diminuerait le risque de malocclusion dentaire ou leur gravité, indépendamment de la qualité du lait ; à condition toutefois de ne pas poursuivre au-delà de l’âge d’évolution physiologique de la déglutition, soit vers 1 an et demi à deux ans (9).
S’il dure plus de 4 mois, l’allaitement diminue aussi les risques de pathologie digestive (les études faites dans les pays développés, un moindre risque de diarrhée et d’hospitalisations pour ce motif).
Il semble aussi diminuer le risque d’obésité (10,11), mais cela reste discuté (12).
Il semble également réduire la fréquence des diabètes de type 1 et 2 chez les enfants ayant reçu un allaitement au sein de plus de 4 mois. La réduction du risque pour le type 2 chez l’adulte serait de 39 % et de 19 à 27 % pour celui de type 1 en fonction des études. (6) Il semble légèrement diminuer le risque de lymphome (13), de cancers, d’hypercholestérolémie (14) chez les enfants plus âgés et chez les adultes ayant été allaités, mais non le risque de leucémie (13).
L’allaitement au sein semble diminuer le risque de troubles du déficit de l’attention et d’hyperactivité chez l’enfant (15,16).
De façon générale, chez le nouveau-né de petit poids de naissance (moins de 2.500 g), l’allaitement maternel diminue la mortalité et la morbidité, et améliore la croissance et le développement cérébral (17).
Une étude britannique de 1992 a montré que des pré-maturés alimentés avec du lait maternel par voie nasale, et sans contact direct avec leur mère durant quelques semaines, présentaient à l’âge de 8 ans un quotient intellectuel de 8 points plus élevé que la moyenne d’un groupe d’enfants nourris de la même manière, mais avec du lait artificiel.
Les enfants allaités présentent en moyenne un meilleur développement psychomoteur, et cette relation semble aussi liée proportionnellement à la durée d’allaitement maternel (18,19).
De nombreuses études épidémiologiques ont montré que les enfants allaités ont un quotient intellectuel plus élevé d’en moyenne 1,5 à 2 points (20-23).
Une étude américaine a également observé une relation dose-effet entre la durée d’allaitement maternel et le QI (24). Cette relation pourrait persister jusqu’à l’âge adulte (25). Néanmoins, l’effet direct de l’allaitement maternel sur les capacités cognitives de l’enfant est très discuté dans la communauté scientifique. En effet, la catégorie socio-économique ou le QI de la mère pourraient confondre cette relation (26,27). Le DHA (acide gras oméga-3) présent dans le lait maternel, et absent du lait de vache, pourrait néanmoins expliquer un effet du lait maternel sur le développement cérébral et rétinien.
Conclusion
Beaucoup d’insuffisances au niveau des connaissances et du comportement à l’échelle de l’institution hospitalière restent à combler en matière de promotion de l’allaitement maternel, en particulier dans le domaine de la communication entre les femmes et les professionnels de santé en mettant l’accent sur l’information et l’éducation des mères pendant les séances de vaccination, de consultations pédiatriques et prénatales ainsi sur la nécessité de l’allaitement maternel exclusif pendant les six premiers mois de la vie.
Comme élément important de la santé publique, l’allaitement maternel doit donc être protégé, soutenu et encouragé. Cette protection doit s’exprimer dans le cadre de réglementations et de programmes, aux niveaux international, national et local.
Liens d’intérêts :
Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références :
- OMS/ UNICEF 2007.
- Nlend A, Wamba G, Same Eboko C. Alimentation du nourrisson de 0 à 36 mois en milieu urbain camerounais. Méd Afr Noire 2007 ; 44 (1) :47-51
- Sheally KR, Scanlon KS, Labiner-Wolfe J, Fein SB, Grummer-Strawn LM. Characteristics of breastfeeding practices among US mothers. Pediatrics 2008; 122: S50-S55
- Duchen K, YU G, Jorkston B. Atopic sensitization during the first year of life in relation to long chain polyunsatured fatty acid levels in human milk, Pediatr Res 1998; 44 (4): 478-84
- Rédaction Prescrire Moins d’infections avec le lait maternel qu’avec le lait artificiel. Rev Prescrire 2008;28(297):510-515.
- Stanley I. Breastfeeding and Maternal and Infant Health Outcomes in Developed Countries Agency for Healthcare Research and Quality April 2007. The results from our meta-analyses of cohort studies of good and moderate methodological quality showed that breastfeeding was associated with a significant reduction in the risk of AOM.
- Bachrach VRG, Scharz E, Bachrach LR. Breastfeeding and the risk of hospitalization for respiratory disease in infancy. A meta-analysis. Arch Pediatr Adolesc Med 2003; 157: 237-243
- Jones G, Steketee RW, Black RE, Bhutta ZA, Morris SS; Bellagio Child Survival Study Group. How many child deaths can we prevent this year? ». Lancet 2003; 362:65-71
- Raymond JL. Approche fonctionnelle de l’allaitement et malocclusions. Revue Orthopédie Dento faciale 2000; 34:379-402.
- Kries R, Koletzko B, Sauerwald T. Étude Relation inverse entre la durée de l’allaitement et la prévalence de l’obésité, Breast feeding and obesity: cross sectional study. BMJ. 1999 Jul 17;319(7203):147-50)
- Heather MC. Fat , Young, and Poor: Why Breastfeeding Is a Critical Weapon in the Fight Against Childhood Obesity ; Breastfeeding medicine, Vol.7, no 5, 2012 – Mary Ann Liebert,
- Martin RM, Patel R, Kramer MS et al. Effects of promoting longer-term and exclusive breastfeeding on adiposity and insulin-like growth factor-I at age 11.5 years, a randomized trial. JAMA, 2013;309:1005-1013
- Xiao O, Clemens J, Wei Zheng. Infant Breastfeeding and the Risk of Childhood Lymphoma and Leukaemia. Oxford Journals Medicine International Journal of Epidemiology 1995;24(1):27-32.)
- OMS. Review: Evidence of the long term effects of breastfeeding » WHO Systematic review.2007
- Aviva M, Kachevans K, Mimouni F, Shuper A, Ey Raveh. Breastfeeding May Protect from Developing Attention-Deficit/Hyperactivity Disorder. Breastfeeding Medicine 2013.P 13-20.
- Romain L. Enfants : le lait maternel en prévention de l’hyperactivité ? . Breast-feeding Medicine 2013.P10-15.
- Edmond K, Bahl R, Optimal feeding of low-birth-weight infants: technical review. Geneva: WHO, 2006
- Jonathan Y, Agostini M. Breastfeeding Duration and Cognitive Development at 2 and 3 Years of Age in the EDEN Mother–Child Cohort , The Journal of Pediatrics, vol. 163, 1er janvier 2013
- Vasiliki L, Koutra K. Breastfeeding duration and cognitive, language and motor development at 18 months of age: Rhea mother–child cohort in Crete, Greece. Journal of Epidemiology and Community Health, vol. 69, 1er mars 2015, p. 232-239
- Anderson J, Johnstone B. Breast-feeding and cognitive development: a meta- analysis. The American Journal of Clinical Nutrition, vol. 70, 1er octobre 1999, p. 525-535
- Brion A, Debbie A. What are the causal effects of breastfeeding on IQ, obesity and blood pressure? Evidence from comparing high-income with middle-income cohorts. International Journal of Epidemiology, vol. 40, 1er juin 2011, p. 670-680
- Geoff D, David B. Effect of breast feeding on intelligence in children: prospective study, sibling pairs analysis, and meta-analysis, BMJ, October 2006.
- Roumeliotaki T. Breastfeeding and child cognitive development: New evidence from a large randomized trial. Archives of General Psychiatry, vol. 65, 1er mai 2008, p. 578-584
- Vassilaki M. Infant feeding and childhood cognition at ages 3 and 7 years: Effects of breastfeeding duration and exclusivity. JAMA Pediatrics, vol. 167, 1er septembre 2013, p. 836-844
- Cesar G Vict, Bernardo Lessa Horta, Christian Loret de Mola et Luciana Que- vedo. Association between breastfeeding and intelligence, educational attainment, and income at 30 years of age: a prospective birth cohort study from Brazil. The Lancet Global Health, vol. 3, 1er janvier 2015
- Jacobson. L. Breastfeeding effects on intelligence quotient in 4- and 11-year-old children. Pediatrics, vol. 103, 1er mai 1999
- Rosanvallon P. La nouvelle question sociale. Repenser l’État-providence, Le Seuil, 1995, p. 213.