S. TALEB, A.T. BAZZI, C. OUANEZAR, A. LANSARI, S. KERROUMI, S. HAOUACHE,
H. MEROUCHE, M.J. YOUSFI Service d’Urologie, Etablissement Hospitalier et Universitaire 1er Novembre 1954, Oran Faculté de médecine d’Oran.
Résumé : Le prolapsus urogénital est défini par toute saillie permanente ou à l’effort dans la lumière vaginale de tout ou partie des parois vaginales. Il s’agit d’une entité anatomo-clinique correspondant à la défaillance des systèmes de soutènement et de suspension des organes pelviens des femmes, qui font issue à travers l’orifice vulvo-vaginal. Les troubles de la statique pelvienne toucheraient 5 à 10 % de la population féminine et ils représentent tous les désordres fonctionnels et/ou anatomiques, urinaires, gynécologiques ou digestifs. La cystocèle est définie par la bascule de la paroi antérieure du vagin au-delà des reliquats hyménaux. Elle peut être associée à des troubles urinaires ou d’autres désordres pelviens. La corrélation entre la symptomatologie fonctionnelle de la patiente et les constatations anatomiques est importante. Celle-ci se fait par l’appréciation de la gêne ressentie. La cystocèle se manifeste par une multitude de signes cliniques d’ordre obstructifs et irritatifs. L’incontinence urinaire est le signe dominant. Ceci est dû à l’association fréquente de la cystocèle et d’une faiblesse du support urétral. L’analyse de notre série vient confirmer le résultat de la théorie, avec une prédominance des cystocèles de haut grade, et que les signes urinaires en fréquence sont la dysurie, l’incontinence urinaire d’effort puis l’urgenturie. Plusieurs études ont montré la prédominance des signes obstructifs, ainsi que l’impériosité dans les formes de haut grade. Elle a montré également que l’incontinence urinaire était plus fréquente dans les formes de cystocèle de grade 1 et 2.
Mots-clés : Cystocèle, prolapsus urogénital, signes urinaires obstructifs, signes urinaires irritatifs.
Abstract : The urogenital prolapse is defined by any permanent projection or effort in the vaginal lumen of all or part of the vaginal walls, it is an anatomo-clinical entity corresponding to the failure of the systems of support, and suspension of the organs pelvic women, which exit through the vaginal vulvar opening. The disorders of the pelvic statics affect 5 to 10% of the female population and they represent all the functional and/or anatomical disorders, urinary, gynaecological or digestive. The cystocele is defined by the tilt of the anterior wall of the vagina beyond the hymeneal remnants. It can be associated with urinary disorders or other pelvic disorders. The correlation between functional symptomatology of the patient and anatomical findings is important; this is done by the appreciation of the discomfort felt. The cystocele is manifested by a multitude of obstructive and irritative clinical signs. Urinary incontinence is the dominant sign. This is due to the frequent association of cystocele and weakness of the urethral support. The analysis of our series confirms the result of the theory, with a predominance of high-grade cystocele, and that the urinary frequency signs are dysuria, urinary stress incontinence, and urgency. Several studies have shown the predominance of obstructive signs, as well as urgency in high- grade forms. She also showed that urinary incontinence was more common in grade 1 and 2 cystocele forms.
Key-words : Cystocele, urogenital prolapse, obstructive urinary tract, urinary irritative signs.
Introduction
Le prolapsus génital est défini par toute saillie permanente ou à l’effort dans la lumière vaginale, de tout ou une partie des parois vaginales. Il s’agit d’une entité anatomo-clinique correspondant à la défaillance des systèmes de soutènement et de suspension des organes pelviens de la femme, qui font issue à travers l’orifice vulvo-vaginal.
La cystocèle vaginale ou hernie de la vessie est la saillie plus au moins importante de la vessie dans le vagin.
Il s’agit en fait d’un prolapsus génital dans le vagin dont la cause est l’altération des moyens de fixité de la partie antérieure du pelvis.
Rares sont les cystocèles isolées, elles s’intègrent dans le cadre des troubles de la statique pelvienne. L’exploration urodynamique permet une évaluation objective du fonctionnement vésico sphinctérien et une analyse physiopathologique des symptômes pour laquelle il existe une terminologie précise.
Épidémiologie
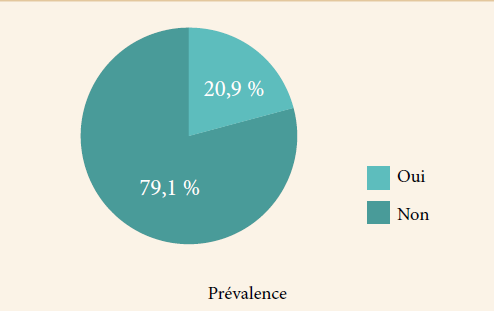
Les troubles de la statique pelvienne toucheraient 5 à 10 % de la population féminine. Il s’agit d’une pathologie fréquente puisque 10 à 20 % des femmes qui ont accouché par voie basse auraient au moins un élément de prolapsus.
Quelques travaux ont suggéré que la prévalence du prolapsus urogénital dans une population générale varie de 2 à 2,6 % si on considère que le prolapsus atteint l’introït. Ce chiffre est plus important si on prend en compte tous les stades de prolapsus et il peut dépasser 30 %.
En suède, pour 31 % des femmes âgées de 20 à 59 ans, un prolapsus est découvert lors d’un examen clinique de routine.
Une femme a un risque de 11 % d’être opérée d’un trouble de la statique pelvienne.
Les cystocèles isolées sont rares, l’atteinte du plancher pelvien est le plus souvent multi- élémentaire. Peu d’études se sont intéressé à la symptomatologie propre de la cystocèle. Cependant, des études tendent à évaluer les signes fonctionnels urinaires avant et après la chirurgie, ainsi que l’étude urodynamique des différents troubles
Classification des prolapsus
De nombreux systèmes de classification des prolapsus génitaux ont été élaborés. Les classifications les plus souvent utilisées sont celles de Baden et Walker et de l’Internationale Continence Society (ICS).
Elles utilisent une représentation du vagin de profil avec pour point de référence l’orifice hyménal.
A. La classification Half Way System de Baden et Walker
- Simple dans sa compréhension et rapide dans son exécution,
- Descriptive non quantitative,
- Ne prend pas en compte les conditions d’examen,
- Le point de repère est l’hymen.
- Grade 0 : position normale de l’étage étudié
- Grade 1 : descente à mi-chemin entre la normale et l’hymen
- Grade 2 : descente jusqu’à l’hymen
- Grade 3 : extériorisation au-delà de l’hymen
- Grade 4 : extériorisation ou éversion
B. La classification de l’ICS ou Pelvic Organ Quantification System
Cette classification :
- Est objective et reproductible, précise et rigoureuse,
- Permet une description quantitative en précisant les conditions d’examen clinique,
- Trop longue à réaliser et difficile à enseigner,
- Recommande une description des segments vaginaux prolabés sans présumer de leur contenu.
L’orifice vulvaire est le point zéro, ce qui est en dehors est positif. Le point accessoire est l’épine ischiatique (fond du vagin normalement en place).
Cinétique pelvienne
L’utérus, organe de la gestation a besoin d’une grande liberté pour jouer son rôle, avec en contrepartie des risques de perturbation statique pouvant entraîner la perturbation d’autres fonctions :
- La miction sous l’effet d’un prolapsus vésical associé,
- La défécation par une rectocèle secondaire,
- Des douleurs pelviennes par la ptose du tractus urogénital.
Lors de la contraction puis de la poussée :
- La vessie subit une translation vers le bas et surtout vers l’arrière,
- Le tube génital subit également une translation vers l’arrière : l’utérus et la partie supérieure du vagin vers le coccyx, alors que le cap vaginal s’efface,
- Le rectum vient s’écraser sur le ligament ano-coccygien. Dans ce mouvement, la vessie et l’utérus évoluent ensemble dans l’excavation pelvienne.
Le col utérin vient verrouiller l’excavation recto-utérine anciennement « cul-de-sac de Douglas ») et écrase le rectum sur le ligament ano-coccygien. Ce sont les muscles élévateurs de l’anus qui sont le moteur de l’occlusion pelvienne car leur rôle est de fermer l’excavation pelvienne.
S’ils sont lésés, ils laissent se prolaber les organes pelviens dans cette fente. La cystocèle résulte de l’altération du fascia vésico-pelvien, avec un défet du support anatomique du col vésical et de l’urètre proximal expliquant ainsi la fréquence de l’incontinence urinaire, la fermeture de l’angle vésico-urétral crée une « pseudo-valvule» ostiale vésicale, qui assure une « fausse » continence. Ceci explique le caractère « providentiel » de certains prolapsus vis-à-vis de l’incontinence urinaire.
Clinique
La cystocèle est définie par la bascule de la paroi antérieure du vagin au-delà des reliquats hyménaux. Elle peut être associée à des troubles urinaires et à d’autres désordres de la paroi pelvienne. Peuvent donc être associées à la cystocèle, une cervicocystoptose et une uré- térocèle témoignant de la faiblesse du support urétral. La cystocèle peut s’associer à une incontinence urinaire d’effort qui peut être masquée dans les grandes cystocèles.
Dans ce cas, seront présentés plutôt des signes obstructifs (dysurie, sensation de vidange incomplète, jet intermittent). Dans d’autres cas, la cystocèle se présente par des signes irritatifs liés à la distension urétro-trigonale. Fréquemment les patientes consultent pour une tuméfaction vaginale ou aggravation de celle-ci. La recherche de signes urinaires exige une attention particulière.
L’interrogatoire et l’examen clinique constituent la pierre angulaire de l’étude des cystocèles. Il est donc fondamental de préciser les troubles, leurs conditions de survenue, d’essayer d’identifier la gêne réelle ressentie par la patiente, de préciser la nature de sa demande, et surtout de rechercher les signes sous estimés par la patiente. Ceci a été fait par plusieurs études en se basant sur des questionnaires appréciant ces signes fonctionnels M.H.U. (Mesure du Handicap Urinaire) et l’impact sur la vie courante I.I.Q (Incontinence Impact Questionnaire ).
L’incontinence urinaire est le premier signe à chercher, car souvent sous estimée et patente, d’importance variable et de multiples caractères d’apparition et dont l’appréciation de l’importance, de l’évolutivité du retentissement et de la tolérance par des questionnaires validés est essentielle, tel que le questionnaire de l’impact sur le prolapsus traduit de Pelvic Floor Distress Inventory et Pelvic Floor Impact Questionnaire.
- La dysurie rarement avouée par les patientes, mais son importance tient de l’obstruction et ses conséquences sur le profil mictionnel, peuvent ainsi masquer une incontinence d’effort. Ceci est dû à l’obstruction de l’urètre par l’effet pelote ou bien par une mauvaise contraction vésicale.
- La pollakiurie ou urgenturie résulte d’une instabilité vésicale ou bien est d’ordre psychogène.
La symptomatologie urinaire et non urinaire est variée dans tous les prolapsus urogénitaux. Une revue de littérature [2], traitant 97 articles sur le prolapsus urogénital a objectivé la présence des signes suivants :
| Protrusion vaginale | 97% |
| Dysurie | 33% |
| Incontinence U.E | 33% |
| Pollakiurie | 14 % |
| Constipation | 25% |
| Douleur pelvienne | 17% |
L’étude de Gemma Blain et coll. [03], sur 1.022 prolapsus a montré que la fréquence des signes urinaires était :
| Incontinence urinaire d’effort | 78,1% |
| Incontinence par urgenturie | 72,8% |
| Pollakiurie | 38,2% |
| Nycturie | 47,7% |
| Signe obstructif | 28,6% |
Les cystocèles isolées sont rares, l’atteinte du plancher pelvien est le plus souvent multi-élémentaire. Peu d’études se sont intéressées à la symptomatologie propre du cystocèle. Cependant, des études tendent à évaluer les signes fonctionnels urinaires avant et après la chirurgie, ainsi que l’étude urodynamique des différents troubles.
Ainsi, dans une étude de Rouache Y et coll [4], sur 50 patientes, dont 58 % présentaient une cystocèle de grade 3 ; et 21% des patientes présentaient une cystocèle de grade 4, la symptomatologie pré opératoire était :
| Dysurie | 32% | |
| Signes d’hyperactivité vésicale | 22% | |
| Incontinence urinaire symptomatique | 36% | |
| Incontinence urinaire masquée | 20% | |
| Pesanteur pelvienne | i | 100% |
montofixation laparoscopique dans le traitement du prolapsus urogénital et dans les 44 cas retenus les résultats sont les suivants :
| Dysurie | 45,83% |
| Nycturie | 29,16 % |
| Incontinence urinaire à l’effort | 37,5% |
Nous avons utilisé la classification de Baden et Walker comme moyen de classification. Le prolapsus de l’étage antérieur est le plus fréquent dans notre série avec le classement des grades suivants :
| Grade 1 | 4,16% |
| Grade 2 | 8,34 % |
| Grade 3 | 37,5 % |
| Grade 4 | 50 % |
Les résultats primaires de notre étude montrent la faisabilité de cette technique laparoscopique, les résultats à court terme étant les suivants :
| Incontinence urinaire d’effort | 9 % |
| Dysurie | 0 % |
| Nycturie | 4 % |
Nous constatons la prédominance des cystocèles de haut grade avec prédominance des signes obstructifs. Les résultats post opératoires montrent l’efficacité de la promontofixation à travers l’amélioration des différents signes cliniques urinaires à court terme mais qui restent un facteur de réussite de cette technique mini invasive, pour lequel le Service d’Urologie à l’EHU reste un des précurseurs nationaux.Une autre étude de Bégler-F.J [5], sur 37 patientes qui présentent trois cystocèles de grade 1, cinq cystocèles de grade 2, dix cystocèles de grade 3 et dix-neuf cystocèles de grade 4, les signes cliniques étaient :
| Tuméfaction vaginale 94 % |
| Incontinence urinaire dont deux masquées 40,5 % |
| Impériosité 29,7 % |
| Miction en deux temps 16,2 % |
Rosenzweing et coll [6], ont étudié 30 femmes divisées en trois groupes selon la sévérité de la cystocèle. Ils ont pu démontrer que les patientes se plaignaient des mêmes symptômes, à l’exception de sensation de boule dans le vagin qui était plus fréquente chez le groupe de cystocèles de haut grade.
Aucune femme dans le groupe de haut grade ne se plaignait de signe d’obstruction urinaire basse ; à l’inverse des formes mineures où l’on retrouve 40% du groupe avec des cystocèles de grade 2 présentent des difficultés à la miction.
Gardy et coll [7], ont étudié 62 femmes dont 29 de grade 1 et 2 pour lesquelles 23 femmes présentaient une incontinence urinaire d’effort confirmée à l’urodynamique. De plus, parmi le groupe de patientes qui présentent une large cystocèle, 33 femmes présentaient un résidu post mictionnel significatif.
Romanzi et coll [9], ont étudié 60 femmes divisées en deux groupes selon la sévérité de la cystocèle : 35 de grade 1 et 2 ; et 25 femmes de grade 3 et 4. Cette étude a montré la prédominance des signes obstructifs, ainsi que l’impériosité dans les formes de haut grade. Elle a montré également que l’incontinence urinaire était plus fréquente chez les femmes de cystocèle de grade 1 et 2.
Cosimo et coll [8], sur une étude de 83 patientes divisées en quatre groupes selon la classification de Baden et Walker, a montré que l’incontinence urinaire d’effort était le signe le plus fréquent dans chaque groupe en l’absence d’incontinence urinaire par urgenturie. Les signes d’obstruction urinaire basse étaient plus présents chez les patientes de large cystocèle que les autres.
Discussion
La fréquence des signes urinaires diffère d’une étude à l’autre. Cela résulte de l’utilisation de différents questionnaires et de l’hétérogénéité des groupes étudiés. Ainsi, on peut retenir sur les différentes séries que l’incontinence urinaire d’effort est le symptôme dominant.
Celle-ci peut être masquée ou apparaît en premier lieu. La dysurie et les signes obstructifs sont plus fréquents dans les formes majeures que les formes mineures confirmées par l’étude récente de Jason et coll. et de Gemma Blain et coll [03].
Ce dernier, sur une étude de 1.022 prolapsus, dont 120 cystocèles isolées, a confirmé qu’il existe une corrélation entre la sensation de boule dans le vagin et les signes d’obstruction vésicale à l’inverse de l’incontinence urinaire d’effort. De plus, aucune relation n’a été retrouvée avec l’incontinence par urgenturie.
A l’inverse, l’étude de Ghetti et coll [10], portant sur 905 femmes qui présentent différents grades de prolapsus, ne montre pas de relation entre l’apparition des signes urinaires obstructifs et irritatifs et le degré de gravité du prolapsus selon la classification POPQ.
Cette diversité de signes cliniques, et en présence d’incontinence masquée, nous incite à bien comprendre et à explorer la physiopathologie de ces troubles urinaires, mais ceci n’explique pas la survenue de l’incontinence lors de la réduction du prolapsus hors cystocèle ; expliquant ainsi le rôle du soutien du vagin, de l’urètre dans la continence.
Conclusion
Toutes les études, malgré le nombre restreint des malades, nous confirment la corrélation entre les signes cliniques et la gravité de la cystocèle.
L’utilisation du débitmètre nous permet une étude objective et quantitative de la miction. Pour la majorité des auteurs, l’effet obstructif de la cystocèle est rattaché à la normalisation des paramètres après réduction de celle-ci (Qmax et RPM).
L’hyperactivité vésicale est mise en évidence plus fréquemment dans les cystocèles de haut grade, selon les séries de Romanzi et Jason P. contrairement à l’étude de Rosenzweig.
L’incontinence par urgenturie n’a été retrouvée que dans 15 % des cas dans la série de Romanzi et elle est indépendante de la sévérité du prolapsus.
Références
- Marijke C., Ph. Slieker-Ten Hove, M-A,P-T, Anneliesl. Symptomatic pelvic organ prolapsed and possible risk factors in a general population American journal of obstetrics and gynecology – February 2009.
- Serge P. Marin Kovic And Stuart L. Stanton Incontinence and voiding difficulties associated with prolapsed The journal of urology Vol. 171 – 1021-1028 march2004
- Gemma Blain and Hans Peter Dietz. Symptoms of female pelvic pro- lapsed correlation with organ descent in women with single compartment prolapsed – Australian and New Zealand journal of obstetrics and gyneco- logy – 2008, Vol. 48 – p. 317 321
- Yannick Rouach, Philipe Sebe, Jerome David Barouk, Philipe Thibault, Francois Haab Résultat à moyen terme du traitement des cystocèles de grade 3 et 4 par plaque de xénogreffe porcine pelvicol TM Progrès d’uro- logie 2007 17, 4, 850-854
- J. Begler Fonnier, A Nguyen, C. Courtieu Traitement des cystocèles par plaque biologique – étude rétrospective de 37 cas Pelvi perinéologie (2006) Vol. 1:335-341
- Bruce A. Rosenzwing, Alex R. Soffici, Shari Thomas, N. Bathia The jour- nal of reproductive medicine – Vol. 37, number 2 – fev1992
- Gardy M. Kozminski, Delancey, Elkins T, Mc Guire E J Stress inconti- nence and cystocèles Journal of urology, 145(6) :1211-3
- Oliva Cosimo, Paparella, Pierluigi. A clinical and urodynamic study of pa- tients with varying degrees of cystocèle Maturitas 27 (1997) 125 – 132
- Lauri J. Loranzi, David C, Chaikin and Jerry G. Blaivas The effect of genital prolapse invoiding. 9. The journal of urology – Vol. 161 581 – 586 February 1999
- Chiara Ghetti Md, W. Thomas Gregory Md, Srenee Edwards Md, Lesley N, Otto and Amanda L. Clark Md. Pelvic organ descent and symptoms of pelvic floor disorders American journal of obstetrics and gynecology
- Takumi Yamada. Need for sling surgery in patients with large cystocèles and masked stress urinary incontinence International journal of urology (2001) 8, 599-603
- Richardson Da, Bentae. The effect of utero vaginal prolapsed on urethral vesical pressure dynamics AM Journal obstetrics gynecology 1983 146 901-905
- Jason P, Gilleran, Gary E. Le Mack and Philippe Ezimmern. Reduction of moderate to large cystocèle during urodynamic evaluation using a vagi- nal gauze pack :8 years experience B J U international 2005 97, 292-295
- Chaikin D C, Asnat G and Jerry G. Blaivas. Predicting the need for anti incontinence surgery in continent women undergoing repair of severe urogenital prolapsed. Journal of urology 2000, 603 (531-4)