A. HAZOUT (1), C. NEDIR (2), M. DERGUINI (3)La Verrière, France Clinique Feriel, Bab Ezzouar, Alger Service de Gynécologie, CHU Bachir Mentouri, Kouba, Alger
Historique
Depuis l’avènement des inducteurs de l’ovulation, et, en particulier des Ménotropines (HMG) (Oelsner et Lunenfeld B.1978) les cliniciens chérissent l’idée de marqueurs infaillibles non seulement de ce qu’il est convenu d’appeler la « réserve folliculaire » ovarienne » (RO) mais aussi de la qualité des ovocytes et des spermatozoïdes.
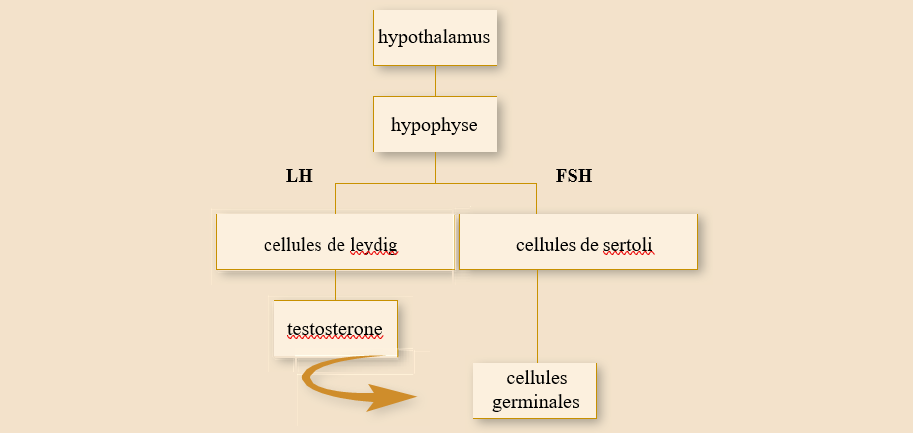
Depuis des décennies, les endocrinologues, convertis à la médecine de la reproduction, ont progressivement attribué à la FSH (hormone folliculo-stimulante) et à la LH (hormone lutéinisante) des vertus multiples et variées dont certaines sont confirmées à travers une théorie bicellulaire communément admise.
Schématiquement, la FSH, stimule les cellules de la granulosa des follicules antraux, et la LH les cellules de la thèque qui, par le biais des androgènes secrétés et aromatisés en œstrogènes, nous fournissent un des marqueurs indirects : l’œstradiol. Ce marqueur, fort utile est FSH dépendant et, selon la longueur du cycle, peut varier au point de troubler l’interprétation du clinicien, en particulier chez les femmes âgées de plus de 35 ans, et/ou les jeunes dont la RO est altérée et chez lesquelles les cycles se raccourcissent.
Le cas particulier des ovaires plurifolliculaires avec LH basale plasmatique élevée, androgènes parfois élevés, œstrogènes élevés, FSH souvent normale, prolactine parfois élevée et une résistance à l’insuline élevée à 70% chez les femmes obèses ou non, sera traité distinctement.
Une élévation de la FSH basale au delà de 10 UI (Scott et al 1989) apparaissait comme rédhibitoire et de très mauvais pronostic. Cependant la FSH seule n’est pas interprétable compte tenu de son interdépendance avec l’œstradiol. Puis, des études plus précises tenant compte des différents paramètres ont fixé un cut-off de 9,43 pour la FSH (Creus et al. 2000).
Ce cut-off ne permet néanmoins pas d’écarter une chance de grossesse ou une possibilité de stimulation quand les valeurs de la FSH sont supérieures. La FSH augmente aussi régulièrement avec l’âge.
Puis un grand espoir est né de l’Inhibine B ; un taux inférieur à 45 g/ml était lié à une mauvaise réponse, à une augmentation des annulations de cycles de stimulations, à une diminution des ovocytes et des taux de grossesses mais il existait un taux de faux positif élevé qui ne permet pas d’en faire un bon marqueur.
En effet cette protéine de la famille du TGF béta est FSH et E2 dépendante et rend son interprétation encore plus délicate. L’élévation de l’œstradiol (E2) provoque parallèlement une chute de la FSH, par rétrocontrôle négatif, comme le fait d’ailleurs l’INHB dont la production est également sous l’influence de la FSH. De plus le dosage de l’Inhibine B est délicat.
Plus récemment l’Hormone Anti Müllérienne (AMH) ou (MIS : Mullerian inhibitor substance) est apparue comme le meilleur marqueur de la RO, avec l’avantage de ne quasiment pas varier au cours du cycle dans la mesure ou elle n’est ni FSH, ni œstradiol ni Inhibine B dépendante. Le dosage de l’AMH quel que soit le moment du cycle, s’est donc installé depuis le début des années 2000 comme le meilleur reflet de la RO (Seifer D. et al 2002 ; Hazout A. et al. 2004).
L’hormone anti-müllerienne ou AMH a été découverte dans les années 1950 par le chercheur Alfred Jost. Présente dès les toutes premières semaines de la gestation, elle joue un rôle clé dans la formation des organes sexuels de l’enfant à naître. En effet, entre la 8ème et la 10ème semaine de grossesse, la Müllerian Inhibiting Substance (MIS), est secrétée par les cellules de Sertoli dans les gonades (futurs testicules) des embryons masculins. L’objectif : inhiber le développement des canaux de
Müller qui constituent l’ébauche de l’utérus, des trompes et d’une partie du vagin. En parallèle, les gonades sécrètent de la testostérone qui favorise la différenciation vers un appareil génital masculin (développement des canaux de Wolff).
A contrario, chez les embryons femelles, les canaux de Müller se développent en voies génitales féminines, en l’absence d’AMH.
Chez la femme, le taux d’AMH dans le sang tend à décroître avec l’âge en parallèle du nombre de follicules, contrairement aux autres hormones hypophysaires (FSH et Inhibine B). A ce titre, l’hormone anti-müllerienne est considérée comme le meilleur reflet de la réserve ovarienne (Yao et al. 2015).
De plus, l’AMH est un bon indicateur du taux de succès de certains protocoles d’assistance médicale à la procréation (AMP) et d’éventuels risques d’hyperstimulation ovarienne. En effet, il existe une corrélation entre le taux d’AMH > 2,5 ng et le nombre d’ovocytes ponctionnés après une stimulation ovarienne. Enfin, même si son évaluation n’est pas recommandée à des fins diagnostiques (pas de valeur seuil établie), le taux d’hormone anti-müllerienne peut être, quand il est élevé, un indicateur d’un syndrome des ovaires polykystiques (SOPK). Cette élévation s’explique notamment par le nombre augmenté de petits follicules en croissance chez les patientes atteintes de ce syndrome.
Chez la femme, il doit être observé au regard de l’âge de la patiente et du compte des follicules antraux (AFC) par voie échographique (comptage de follicules entre 4 et 9mm en début de cycle).
Ainsi, si certains travaux ont montré qu’il y avait une valeur d’AMH seuil en-dessous de laquelle les grossesses deviennent rares (< 0,5 ng/ml) pour certaines femmes (âgées de 35/ 42 ans) (LI Y et al 2018) ; d’autres ont mis en avant qu’un taux bas d’AMH n’est pas un facteur excluant les couples jeunes (moins de 35 ans), candidats à la FIV (Gomes et al. 2016 ; Cateau Jonard S. et al. 2011). Autre particularité à noter : le taux d’AMH n’est pas un indicateur de la qualité de l’ovocyte.
Chez l’homme, le taux d’AMH est un bon indicateur de la spermatogénèse. Selon certains travaux de recherche, le taux d’AMH dans le liquide séminal est considérablement moins élevé chez les hommes présentant une azoospermie que chez les patients ne rencontrant pas de problème de fertilité.
Par ailleurs, ce même taux est en corrélation avec le nombre de spermatozoïdes et le volume des testicules.
L’évaluation du taux d’AMH est donc non seulement importante dans le cadre d’un bilan de fertilité, mais aussi extrêmement utile pour préciser un protocole de soin chez les patients azoospermiques, dès lors que l’azoospermie est non obstructive (Fenichel et al. 1999).
Un travail récent de Alfano et al. (Nature : Scientific Reports 2018) démontre que l’AMH plasmatique < 4,62 ng/ml et le ratio AMH/total Testostérone (tT) plasmatique < 1,02 ng/ml seraient prédictifs d’un recueil positif (23 vs 24) de spermatozoïdes chez les hommes souffrant d’une azoospermie non obstructive idiopathique avec une précision de 93 et 95 % en spécificité et sensibilité (p=0.008).
C’est un travail sur une série courte (47 patients), à confirmer sur de grandes séries, mais hautement significatif.
Enfin, le taux d’AMH est utile dans la recherche de certaines pathologies pédiatriques masculines (testicules ectopiques, puberté précoce, etc.).
Introduction :
Force est de constater que quand un gynécologue reçoit un couple infertile, il s’attarde d’emblée sur les causes féminines éventuelles alors que l’homme est impliqué dans 59 % des cas.
C’est dire l’importance, y compris d’un point de vue de santé publique, de l’interrogatoire et de l’examen de l’homme avant tout.
Cependant beaucoup de nos confrères et consœurs rechignent à examiner un homme, par pudeur ou par manque de pratique. Ils s’en remettent au spermogramme habituel sans s’attarder, en particulier sur les facteurs environnementaux ou vasculaires qui pourraient altérer la spermatogénèse même secondairement à une paternité plus ou moins récente.
Ils préfèrent aussi confier leurs patients à un urologue ou à un andrologue qui a l’avantage de bien connaître l’anatomie des organes génitaux externes mais qui est moins rompu aux problèmes de reproduction.
L’examen de la femme est rendu plus aisé depuis l’avènement de l’échographie pelvienne qui ne remplace pas l’examen clinique mais qui le complète avec une bonne précision quant à l’état de l’utérus et des annexes.
Le but de cet article est de passer en revue, de façon très pratique, les fondamentaux d’un examen du couple infertile aujourd’hui.
Nous commencerons fort logiquement par l’homme avant d’aborder l’exploration de la femme en ne perdant jamais de vue que, dans la grande majorité des cas les deux membres du couple sont impliqués.
Un préalable important : si la majorité des complications périnatales est d’origine infectieuse, la majorité des complications en périconceptologie est le plus souvent d’origine infectieuse ! (La Vignera et al. 2014)
L’exploration de l’homme :
L’interrogatoire est essentiel :
Durée de l’infertilité, traitements déjà effectués pour le couple, avortements spontanés et nombre et résultats d’éventuelles AMP, consommation de tabac ou de stupéfiants.
Analyser les antécédents infectieux (maladies infantiles, vaccinations, rapports douteux, maladies virales ou de système, qualité des rapports sexuels, douleurs à l’éjaculation, dysurie ou pollakiurie)
L’examen clinique :
Palpation des testicules : un testicule mesure environ 4 à 5 cm longueur et 2 à 3 centimètres d’épaisseur. Son poids se situe aux alentours de 20 grammes (variable suivant les individus). Son volume excède 10 ml.
Sa consistance est ferme ; des varices scrotales se situent le plus souvent à gauche (90 %) puisque la veine spematique débouche à angle droit dans la veine rénale gauche alors que le reflux est moins fréquent à droite puisque la veine spermatique droite débouche à angle aigu sur la veine cave inférieure) ; la palpation des épididymes doit être attentive : (plats ou tendus) et des déférents (présents ou absents). S’il existe des antécédents infectieux connus, faire un toucher rectal pour examen de la prostate.
Au terme de cet examen vous devez avoir la clef du problème masculin, complété au moindre doute par une échographie testiculaire avec doppler veineux spermatique voire une échographie prostatique à la recherche de microcalcifications témoins de prostatite chronique. Vous aurez hélas ainsi à découvrir parfois des cancers du testicule infra cliniques.
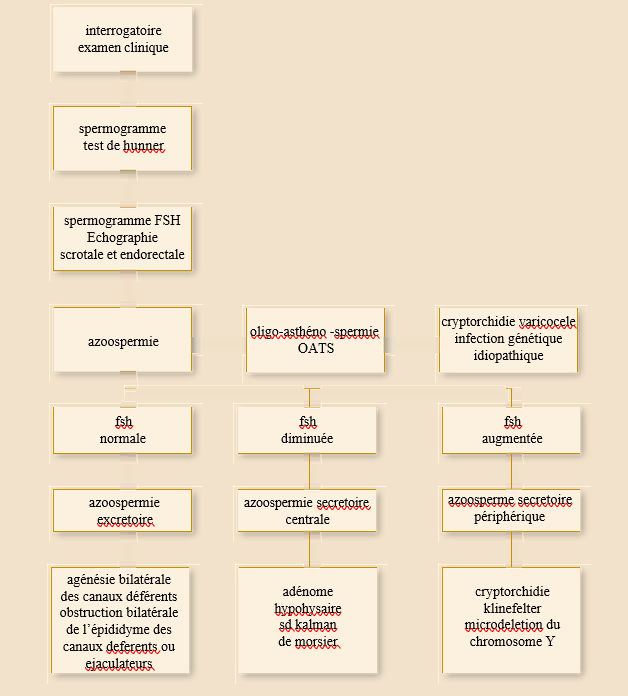
Les examens complémentaires :
- le spermocytogramme + spermoculture avec recherche de chlamydiae, mycoplasme et waddlia chondrophila (Baud D et al 2018)
- Un « swelling test » (test hypo-osmotique : HOST) peut être utile dans les cas d’asthéno-tératospermie plus ou moins sévère : en effet seule la la morphologie serait corrélée à la fragmentation de l’ADN nucléaire (DF) et surtout, le HOST est corrélé aux paramètres du sperme (concentration, mobilité, morphologie). La morphologie du sperme est prédictive du taux de DF et du HOST
- Selon la morphologie du sperme (taux d’anomalies < 4 % (normes OMS de 2010) les résultats du HOST et les antécédents du couple, une analyse de la fragmentation et/ou de la décondensation de l’ADN spermatique peuvent ne pas s’imposer ou apporter des arguments pronostiques et thérapeutiques supplémentaires.
En fonction de l’examen clinique :
- L’échographie testiculaire avec une étude doppler veineuse spermatique et manœuvre de Valsalva à la recherche d’un reflux notable, témoin d’une varicocèle,
- L’échographie prostatique si forte suspicion de prostatite chronique,
- En dehors des azoospermies sécrétoires avec hypogonadisme les dosages hormonaux et le caryotype systématique ne se justifient pas mais si le caryotype doit être pratiqué il devra s’accompagner d’une étude des microdélétions de la zone AZF de l’Y.
- L’évaluation du stress oxydatif demeure un challenge. Il est quantifiable dans le plasma séminal mais aussi dans le sérum sanguin à travers l’évaluation de l’ADN libre (cfDNA : cell free DNA) (Hazout A. Brevet Européen 2012).
- Le statut de méthylation du sperme :
La méthylation de l’ADN (DNAm) est une modification chimique post réplicative, réversible et transmissible; elle intervient en position C5 de la Cytosine Pyrimidine dans un contexte CpG. C’est un mécanisme épigénétique impliqué dans une large variété de processus biologiques incluant l’empreinte génomique parentale, l’expression de gènes spécifiques à certains tissus et la stabilité du génome.
Durant la vie d’un homme, il y a trois principales périodes de reprogrammation épigénomique. Chacune de ces périodes connaît des phases de DNA déméthylation et méthylation.
- en phase préimplantatoire
- dans les cellules germinales primordiales
- elle commence au début de la spermatogénèse Acquise par les spermatogonies de type A, des changements surviennent au delà puis restent stables (Trasler 2009).
La DNAm est influencée par les facteurs environnementaux mais la plupart des études ont été faites sur des cellules somatiques. ALU et Line 1 ont été proposés comme marqueurs indirects du % de méthylation globale (DGML).
La DGML est fortement indépendante du taux de DF et de l’abondance relative des protamines.
On ne connaît pas encore les déterminants de la méthylation du sperme normal ; seule l’abstinence est corrélée avec la méthylation (- 43,1). Le tabac est corrélé au LINE1 méthylation.
Ce qui nous intéresse est que concentration, morphologie et mobilité sont négativement corrélés au statut de méthylation du sperme, positivement corrélé à la DF (débattu mais en cours de validation). La méthylation du sperme est stable dans le temps et peut donc représenter un bon marqueur de l’influence environnementale +++.
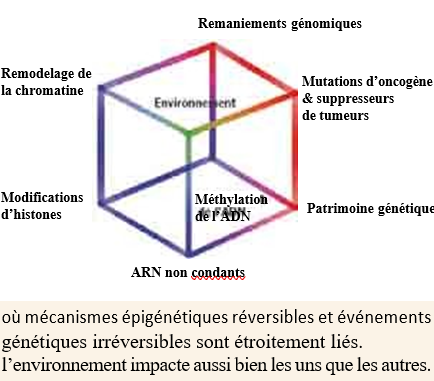
À la croisée des générations, ovocytes et spermatozoïdes assurent donc la continuité de l’espèce en livrant à la génération suivante un capital génétique gravé dans le marbre de la molécule d’ADN et un patrimoine épigénétique réversible, sous forme de modifications biochimiques. La méthylation de l’ADN en particulier a des propriétés intrinsèques de stabilité et d’héritabilité permettant sa transmission des gamètes parentaux à l’embryon, voire de persistance tout au long de la vie de l’individu, comme une mémoire parentale non génétique.
Au total, nous voyons que dans certaines situations d’échecs à répétition, il faut s’interroger au delà d’un spermogramme même apparemment normal. Dans la vraie vie, point n’est besoin de demander systématiquement tout l’arsenal diagnostique sus décrit ; ceci nous ramène à l’importance d’un bon examen clinique, seul capable d’orienter vers telle ou telle exploration complémentaire. Exceptionnellement des mutations du MTHFR (Méthylène Tétra Hydro Folate Reductase) expose à des hypométhylation de l’ADN du sperme et à des échecs d’implantation surtout s’il y a homozygotie (Aarabi M et al 2018).
L’exploration de la femme
En préambule, nous avons mis l’accent sur le souci des cliniciens de mieux appréhender la physiologie de l’ovulation, et en AMP, la stimulation de l’ovulation. Cependant, pour des raisons essentiellement éthiques, il est difficile de nos jours de déterminer l’essentiel : la compétence ovocytaire.
Le seul critère objectif de la compétence d’un ovocyte mature est la capacité à être fécondé et à assurer, après fécondation tous les processus du développement embryonnaire.
Autant dire que nos connaissances à ce jour sont limitées même si nous avons appris beaucoup de la recherche chez les espèces animales mono-ovulantes.
Pour être didactique nous devons rappeler que la croissance et la maturation d’un ovocyte humain dure environ 80 jours à partir du follicule primordial, qu’elle évolue par vagues successives et qu’une dominance des premiers assure un cycle ovulatoire menstruel.
Nous connaissons les mécanismes de stimulation simultanée de la FSH et, dans une moindre mesure de la LH ; mais nous ignorons encore les mécanismes intimes de l’organisation de la dominance d’un ovocyte.
Nous savons qu’il y a des récepteurs de la FSH sur les cellules de la granulosa murale et de la corona radiata mais qu’il n’y a pas de récepteurs au niveau de l’ovocyte. Nous savons qu’il y a des récepteurs de la LH au niveau de la thèque du follicule qui entraîne la sécrétion des androgènes convertis en œstrogènes, par aromatisation, au niveau des cellules de la granulosa. Ainsi, l’œstradiol est indirectement le reflet de la croissance folliculaire.
Nous savons aussi qu’il y a des échanges nutritionnels entre les cellules de la granulosa et l’ovocyte ; les unes assurant la croissance de l’autre qui secrète également des facteurs de croissance (GDF9, BMP15 et autres Connexines..), qui assurent la survie des cellules de la corona radiata.
Au passage vous constaterez que c’est un exemple rare de dialogue entre une cellule somatique (diploïde) et une cellule germinale. (Chez l’homme la cellule germinale est l’émanation d’une cellule somatique : la cellule de Sertoli)
Compte tenu de toutes ces données vous êtes conscients que, quand vous stimulez des ovaires au début d’un cycle vous n’intervenez que pour parfaire la croissance
du follicule prédestiné dominant, et hâter la maturation de quelques retardataires.
Mais il ne s’agit que d’une stimulation folliculaire (appréciée sur des critères hormonaux et échographiques), qui ne préjuge en rien de la qualité ovocytaire (aneuploïdie, maturation, compétence). Par exemple chez les femmes âgées de 40 ans, et parfois moins, l’ADN mitochondrial perd un quart de son génome soit, environ, 7.900 paires de bases (Bentov et al. 2011). Par ailleurs il y a beaucoup plus d’ovocytes aneuploïdes. Ceci explique en partie des échecs plus nombreux.
De nos jours, héritant des critères classiques, il est d’usage de demander en début de cycle les dosages hormonaux plasmatiques suivants : FSH, E2, LH, Progestérone (pour éliminer un corps jaune pseudo gestatif) l’Inhibine B pour certains et l’AMH pour la majorité. Ces dosages suivent une échographie pelvienne pour AFC.
En réalité, on peut se contenter de l’AFC et du taux plasmatique d’AMH, avec ces deux critères vous aurez un reflet fidèle du nombre de follicules ovariens recrutables et de leur qualité fonctionnelle. De plus, l’un et l’autre critère peuvent vous orienter vers un diagnostic de syndrome d’ovaires polyfolliculaires et vous permettre d’adapter votre thérapeutique inductrice de l’ovulation.
Le problème des PCOS :
Depuis la conférence parrainée par le NIH en 1990 sur le PCOS, le syndrome englobe un spectre plus large de signes et de symptômes de dysfonction ovarienne que ceux décrits par les critères de diagnostic originaux par Stein-Leventhal en 1935.
A Rotterdam en 2003, le PCOS est défini comme un syndrome de dysfonction ovarienne avec hyperandrogénie et une morphologie « polykystique » des ovaires (> 12 follicules de 2 à 9 mm dans chaque ovaire et ou un volume ovarien > 10 ml. Mais le PCOS reste un syndrome et, deux critères, hyperandrogénie et morphologie PCO (PCOM), ne sont pas suffisants pour un diagnostic clinique.
Autres manifestations cliniques : irrégularités menstruelles, oligo-anovulation, signes d’excès d’androgènes et l’obésité. La résistance à l’insuline et les taux sériques élevés de LH sont également des caractéristiques communes au PCOS, avec un risque accru de diabète de type 2 et d’accidents cardiovasculaires.
En 2010, dernière conférence de consensus, deux critères sur trois sont requis mais chacun des trois items OA (oligo anovulation), HA (hyperandrogénie), et PCOM (morphologie ovarienne de type PCOS) doit être mis à jour.
Le désarroi des cliniciens vient de notre méconnaissance de l’étiopathogénie des PCOS. Tout a été avancé ou presque. Stein Leventhal soulignait un ratio FSH/LH inversé. Puis ce fut la dérégulation des pulses de GnRH, l’hypersécrétion de LH, la dérégulation des cellules thécales, les androgènes, puis la dysfonction pancréatique et l’obésité !!!!
Il faut savoir que la résistance à l’insuline, variable, n’affecte que 50 à 70 % des femmes obèses ou non !! Les cas familiaux : 35 % des mères et 40 % des sœurs ; un trait héréditaire dominant de faible pénétrance et d’expression variable. Des études d’association du génome large (GWAS) ont révélé 11 locis à risque, indépendants, pour le PCOS
Chez les non obèses deux gènes de la région LHCGR (hypo-méthylés), STON1-GTF2A1L et LHCGR, sont surexprimés. Les non obèses possèdent des altérations significatives dans l’expression du récepteur de la LH, ce qui entraîne la sécrétion excessive d’androgènes par l’ovaire.
Chez les obèses, l’INSR (Récepteur à l’insuline : hyper-méthylé) est sous-exprimé. Les femmes obèses, ont une sous-expression du récepteur à l’insuline dans les tissus métaboliques et une surexpression dans l’ovaire. Ce qui entraîne une résistance à l’insuline périphérique et une production excessive d’androgènes ovariens.
Toutes les études auxquelles nous faisons référence fournissent une base génétique et moléculaire de l’hétérogénéité clinique signalée dans les PCOS. (Jones M.R.et al. Plos One 2015).
Le PCOM (PCOS like) est également rencontré chez les femmes normo-ovulatoires !
Des études récentes ont montré des anomalies endocriniennes subtiles chez les femmes avec PCOM isolé qui ressemblent à ceux trouvés chez les femmes atteintes de PCOS. En raison de la forte corrélation entre l’AMH et nombre de follicules, un niveau élevé d’AMH sérique a été proposé comme un marqueur de substitution du PCOM.
L’AMH devrait donc être intégré dans les classifications diagnostiques du PCOS. (Dewailly at al.2017) Le cut-off des PCOS est plus élevé chez les femmes jeunes que chez les plus âgées. Dans la population âgée, la performance diagnostique de l’AMH est supérieure à celle du FNPO (AUC = 0,948 (0,927-0,970) vs 0,874 (0,836-0,912), respectivement, p = 0,00035) (Lie Fong et al. 2017) Le cut-off de l’AMH et le nombre de follicules antraux distinguant les femmes réglées non PCOM des PCOS,
étaient plus élevés chez les femmes jeunes que chez les femmes plus âgées. Le PCOM à un âge avancé peut être associé à une forme sub-clinique de PCOS, (qui peut également être présent chez les jeunes femmes régulièrement réglées).
Au total :
- La définition de l’HA biologique n’est toujours pas résolue.
- Les critères utilisés pour définir l’OA sont insuffisants.
- La définition de PCOM proposée en 2003 est désormais obsolète avec l’utilisation de la dernière génération de machines à ultrasons.
- Le test de sérum anti-Müllerian hormone (AMH) semble de plus en plus être un excellent substitut de la numération folliculaire et est susceptible d’apparaître comme le marqueur PCOM officiel (Dewailly D 2017).
| Variable | AUC (CI) | Cut-off value | Sensitivity (%) | Specificity (%) |
| Yong women | ||||
| FNPO | 0.903 (0.891-0.940) | 11.25 | 87.6 | 85.0 |
| 11.75 | 85.2 | 92.9 | ||
| 12.25 | 84.2 | 95.6 | ||
| 12.75 | 83.0 | 98.2 | ||
| Serum AMH (ug/l) | 0.903 (0.876-0.930) | 4.5 | 88.6 | 76.1 |
| 5.0 | 85.4 | 79.4 | ||
| 5.5 | 82 | 84.1 | ||
| 6.0 | 79.3 | 87.6 | ||
| Old women | ||||
| FNPO | 0.874 (0,863-0.912) | 9.75 | 80.0 | 84.9 |
| 10.75 | 79.5 | 93.5 | ||
| 11.75 | 74.1 | 96.8 | ||
| 12,70 | 71.7 | 97.8 | ||
| Serum AMH (ug/l) | 0.948(0.927-0.970) | 4.0 | 84.9 | 87.1 |
| 4.5 | 83.9 | 91.1 | ||
| 5.0 | 82.4 | 93.5 | ||
| 5.5 | 76.6 | 95.7 | ||
| AUC, area under the curve. | ||||
En résumé, retenons que AMH plasmatique et AFC suffisent à appréhender correctement une réserve folliculaire ovarienne.
De plus l’échographie peut éliminer un hydrosalpynx et des anomalies endocavitaires utérines : polypes, hyperplasie de l’endomètre à plus de 14 mm, un myome sous muqueux (les myomes interstitiels ou sous séreux ne gênent en rien l’obtention d’une grossesse). L’âge reste le seul facteur limitant tant pour la femme que pour l’homme.
En conclusion :
Nous avons choisi, riche de notre expérience et nos acquisitions nouvelles dans un débat quotidien, de vous présenter, simplement, une problématique encore peu dépouillée, hélas, de nombreuses idées reçues. C’est comme pour nos problèmes sociétaux : difficile de se débarrasser des préjugés et des avantages acquis de longue date !!! Nous faisons trop d’examens complémentaires inutiles plutôt que pas assez. Chaque examen doit avoir une justification émanant d’un examen clinique rigoureux. Par exemple quand il y a des spermatozoïdes dans un éjaculat le caryotype et divers dosages hormonaux ou biochimiques ne se justifient pas. En revanche, avant d’entreprendre une ICSI, notre responsabilité étant engagée, il faut s’attarder sur les anomalies de l’ADN du noyau et sur le statut de méthylation du spermatozoïde injecté. Pourquoi ? … : parce que le risque de transmission de cancers et de maladies épigénétiques est plus élevé et que notre rôle d’informer est important au plan médico légal.
| Hypométhylation de l’ADN | Conséquences |
| Hypométhylation globale | Réactivation de séquences génomiques endoparasitaires et des séquences répétés, Instabilité génomique et chromosomique |
| Hypométhylation du corps du gène | Activation de sites incorrects d’initiation de la transcription |
| Perte de mé thylation de promoteurs | Activation de gènes oncogènes et pro-métastatiques |
| Hyperméthylation de l’ADN | Conséquences |
| Méthylation des promoteurs (ilôts CpG) | Répression des gènes suppresseurs de tumeurs Répression des régulateurs de gènes suppresseurs de tumeurs Inactivation des gènes suppresseurs de métastases |
| perte de l’empeinte parentale | Dérégulation des gènes soumis à empreinte |
Un jour, les jeunes générations de gynécologues devront justifier leurs indications et les moyens mis en œuvre. Reste un gros travail à faire pour en savoir plus sur
l’ovocyte dont les mécanismes de transcriptions sont plus complexes et les facultés de réparations des altérations de l’ADN d’autant plus grandes que les femmes sont jeunes. Cette aptitude de l’ovocyte à réparer est une chance quand un homme âgé est le conjoint d’une femme jeune mais hélas les projets parentaux impliquent en général des couples à peu près du même âge ; les décennies à venir offriront des opportunités nouvelles aux patients, il reste beaucoup à apprendre sur la contribution précise des mécanismes épigénétiques. Quant à la transition entre recherche fondamentale et clinique, elle demeure un défi formidable. In fine c’est ce qui nourrit notre passion.
Références :
- Oelsner G, Serr DM, Mashiach S, Blankstein J, Snyder M, Lunenfeld B. Fertil Steril. 1978 Nov;30(5):538-44.The study of induction of ovulation with menotropins: analysis of results of 1897 treatment cycles.
- Scott RT, Toner JP, Muasher SJ, Oehninger S, Robinson S, Rosenwaks Z. Fertil Steril. 1989 Apr;51(4):651-4 Follicle-stimulating hormone levels on cycle day 3 are predictive of in vitro fertilization outcome.
- Creus M, Peñarrubia J, Fábregues F, Vidal E, Carmona F, Casamitjana R, Vanrell JA, Balasch J. Hum Reprod. 2000 Nov;15(11):2341-6 Day 3 serum inhibin B and FSH and age as predictors of assisted reproduction treatment outcome.
- Seifer DB, Maclaughlin DT, Christian BP, Feng B, Shelden RM. Early follicular serum mullerian-inhibiting substance levels are associated with ovarian response during assisted reproductive technology cycles. Fertil. Steril. 2002 Mar; 77(3):468-71.
- André Hazout, Philippe Bouchard, David B. Seifer, P. Aussage, Anne Marie Junca, Paul Cohen-Bacrie, Serum antimüllerian hormone/müllerian-inhibiting substance appears to be a more discriminatory marker of assisted reproductive technology out- come than follicle-stimulating hormone, inhibin B, or estradiol, Fertility & Sterility, Volume 82, Issue 5, Pages 1323–1329, novembre 2004
- Josso N., Gouédard L. Biologie de l’hormone anti-müllérienne et de son récepteur, Médecine thérapeutique Endocrinologie. Vol. 2, N° 2, mars-avril 2000 : 154-60
- J. Visser, Rôle de l’AMH (hormone anti-Müllerienne) dans le recrutement follicu- laire initial et cyclique, Journal de Gynécologie Obstétrique et Biologie de la Repro- duction, Vol 35, N° 5-C2, septembre 2006 pp. 30-34
- Yao L et al. Int J Clin Exp Med. (2015) The role of serum AMH and FF AMH in predicting pregnancy outcome in the fresh cycle of IVF/ICSI: a meta-analysis.
- Gomez RThe influence of AMH on IVF success.et al. Arch Gynecol Obstet. (2016)
- Li Y, Tan JQ, Mai ZY, Yang DZValue of anti-Müllerian hormone in predicting pre- gnant outcomes of polycystic ovary syndrome patients undergone assisted reproductive technology]. Zhonghua Fu Chan Ke Za Zhi. 2018 Jan 25;53(1):23-30.
- Fenichel P, Rey R, Poggioli S, Donzeau M, Chevallier D, Pointis G. Anti-Mullerian hormone as a seminal marker for spermatogenesis in non-obstructive azoospermia. Hum Reprod 1999 Aug; 14(8): 2020-4.
- Catteau-Jonard S, D Dewailly Anti-mullerian hormone and polycystic ovary syn- drome. Gynecol Obstet Fertil 2011 (39)
- Massimo Alfano et al. Nature : scientific reports 2018) Anti-Mullerian Hormone- to-13. Testosterone Ratio is Predictiveof Positive Sperm Retrieval in Menwith Idiopathic Non-ObstructiveAzoospermia
- La Vignera S, Condorelli RA, Vicari E, Salmeri M, Morgia G, Favilla V, Cimino S, Calogero AE.Microbiological investigation in male infertility: a practical overview.J Med Microbiol. 2014 Jan;63(Pt 1):1-14.
- Baud D. et al HR 2018 vol.33 N°I pp-3-10 Waddlia chondrophila, a Chlamydia related bacterium, has a négative impact on human spermatozoa
- Trasler JM. Epigenetics in spermatogenesis.Mol Cell Endocrinol. 2009 Jul 10;306(1-2):33-6.
- Aarabi M, Christensen KE, Chan D, Leclerc D, Landry M, Ly L, Rozen R, Trasler J. Testicular MTHFR deficiency may explain sperm DNA hypomethylation associated with high dose folic acid supplementation. Hum Mol Genet. 2018 Apr 1;27(7):1123-1135
- Bentov Y, Yavorska T, Esfandiari N, Jurisicova A, Casper RF. The contribution of mitochondrial function to reproductive aging. J Assist Reprod Genet. 2011 Sep;28(9):773-83
- Fertil Steril. 2004 Jan;81(1):19-25. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome.
- Jones MR, Brower MA, Xu N, Cui J, Mengesha E, Chen YD, Taylor KD, Azziz R, Goodarzi MO. Systems Genetics Reveals the Functional Context of PCOS Loci and Identifies Genetic and Molecular Mechanisms of Disease Heterogeneity. PLoS Genet. 2015 Aug 25;11(8)
- Dewailly D. Age-stratified thresholds of anti-Müllerian hormone improve predic- tion of polycystic ovary syndrome over a population-based threshold. Clin Endocri- nol (Oxf). 2017 Dec;87(6):649-650.
- Lie Fong S, Laven JSE, Duhamel A, Dewailly D. Polycystic ovarian morphology and the diagnosis of polycystic ovary syndrome: redefining threshold levels for fol- licle count and serum anti-Müllerian hormone using cluster analysis. Hum Reprod. 2017 Aug 1;32(8):1723-1731