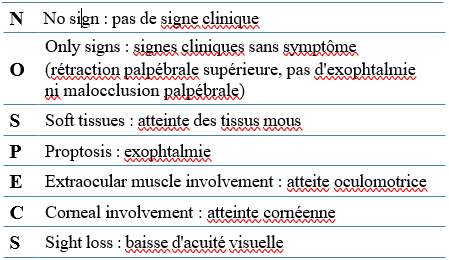
H. YAHIA, M. BELOUI, Service de Biologie Cellulaire (Histo-Embryologie et Génétique Cliniques, Unité Cytopathologie), CHU Nefissa Hamoud, Alger.
Résumé : Le système de Bethesda en cytopathologie thyroïdienne représente une étape majeure vers la standardisation, la reproductibilité, l’amélioration de la prise en charge clinique et a une grande valeur prédictive. Nous avons revu rétrospectivement les ponctions à l’aiguille fine (PAF) thyroïdiennes entre janvier 2016 et décembre 2017. Les résultats ont été catégorisés selon la classification de Bethesda en stade I/non diagnostic II/cytologie bénigne III/atypie ou lésion de signification indéterminée IV/néoplasme folliculaire V/cytologie suspecte VI/cytologie maligne. Un échantillon de 294 cas a pu avoir une corrélation histologique définitive. La distribution des cas dans les catégories Bethesda concorde avec les différentes études, le nombre de cas de malignité étant plus élevé pour les néoplasmes folliculaires. La nouvelle classification des tumeurs thyroïdiennes OMS 2017 introduit une nouvelle entité pour les carcinomes papillaires, variante vésiculaire encapsulée, renommés NIFTP «tumeurs non invasives d’architecture vésiculaire avec des noyaux de type papillaire», ce qui a diminué sensiblement le risque de malignité pour les catégories LFSI, NF et CS. Nous avons calculé le taux de sensibilité qui est de 94 %, la spécificité de 92 %, une valeur prédictive positive de 91 % et une valeur prédictive négative de 95 %. Le système Bethesda permet donc une standardisation des comptes-rendus, améliore les perceptions de la terminologie diagnostique entre les cytopathologistes et les cliniciens, et conduit à des approches de gestion plus cohérentes.
Mots-clés : Nodule thyroïde, cytoponction à l’aiguille fine, Système Bethesda, corrélations cyto-histologiques.
Abstract : Bethesda’s thyroid cytopathology system represents a major step towards standardization, reproducibility, improved clinical management, and has a high predictive value for fine needle thyroid needle aspiration. We retrospectively reviewed thyroid fine needle aspiration between January 2016 and December 2017. The results were categorized according to Bethesda classification in stage I/non-diagnosis II/benign cytology III/atypia or lesion of undetermined significance IV/follicu- lar neoplasia V/suspected cytology VI/malignant cytology. A sample of 294 cases could have a definitive histological correlation. The distribution of cases in the Bethesda categories is consistent with the different studies, with the number of cases of malignancy being higher for follicular neoplasms. The new thyroid tumour classification OMS 2017 introduces a new entity NIFTP «Non-invasive Follicular Thyroid Neoplasm with Papillary-Like Nuclear Features «, significantly decreased the risk of malignancy for the LFSI, NF and CS categories. We calculated the sensitivity rate of 94%, the specificity of 92%, a positive predictive value of 91% and a negative predictive value of 95%. The Bethesda system thus allows reports standardization, improves the perceptions of the diagnostic terminology between cytopathologists and clinicians, and leads to more coherent management approaches.
Key-words : Thyroid nodule, fine needle aspiration, Bethesda System, cyto-histological correlations.
Introduction
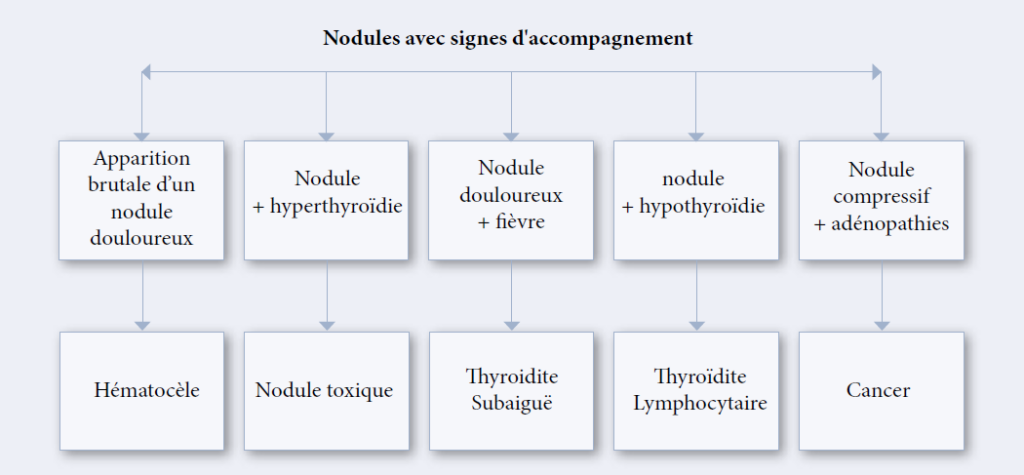
En Algérie, la pathologie thyroïdienne est un véritable problème de santé publique. La forte prévalence dans la population de nodules thyroïdiens (plus de 50 %) avec nette prépondérance féminine (8/1 homme) est due de plus en plus à la découverte échographique de nodules non palpables.
La ponction à l’aiguille fine est un geste simple, peu onéreux et répétitif permettant de classifier les nodules thyroïdiens en précisant ceux qui doivent être opérés.
La cytologie thyroïdienne (aux mains d’opérateurs qualifiés) conduit à des diagnostics fiables de bénignité et de malignité avec une spécificité et une sensibilité de l’ordre de 90 %.
Le diagnostic cytologique se fera en utilisant la classification Bethesda (2010-2017 du NCI-USA) résultant d’un travail multidisciplinaire avec adoption d’une terminologie cytologique et de recommandations managériales communes. [1,3]
Dans la classification Bethesda, le diagnostic cytologique n’est jamais forcé conduisant à refaire le prélèvement quand il est insuffisant ou de proposer à la chirurgie les patients avec cytologie borderline.
L’examen cytologique occupe une place centrale et essentielle dans la prise en charge des nodules thyroïdiens réduisant le nombre de patients à opérer et réduisant ainsi le nombre de complications post opératoires.
A l’avenir l’apport de l’immuno-cytochimie et de la biologie moléculaire sur produits de cytoponction thyroïdienne devrait améliorer la sensibilité et la spécificité des diagnostics cytologiques. [19,20]
Matériels et méthodes
Notre étude regroupe toutes les cytologies effectuées dans notre service de Janvier 2016 à Décembre 2017. Pendant cette période 4.829 cytoponctions thyroïdiennes ont été examinées et analysées par le système Bethesda ; un échantillon de 294 cas a pu avoir une corrélation histologique. Le choix des nodules pour la cytoponction a été influencé par l’examen échographique et le système TIRADS [6,7]
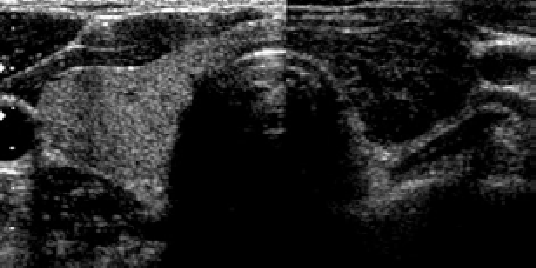
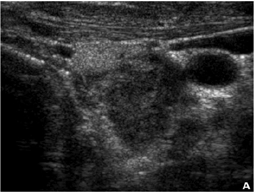
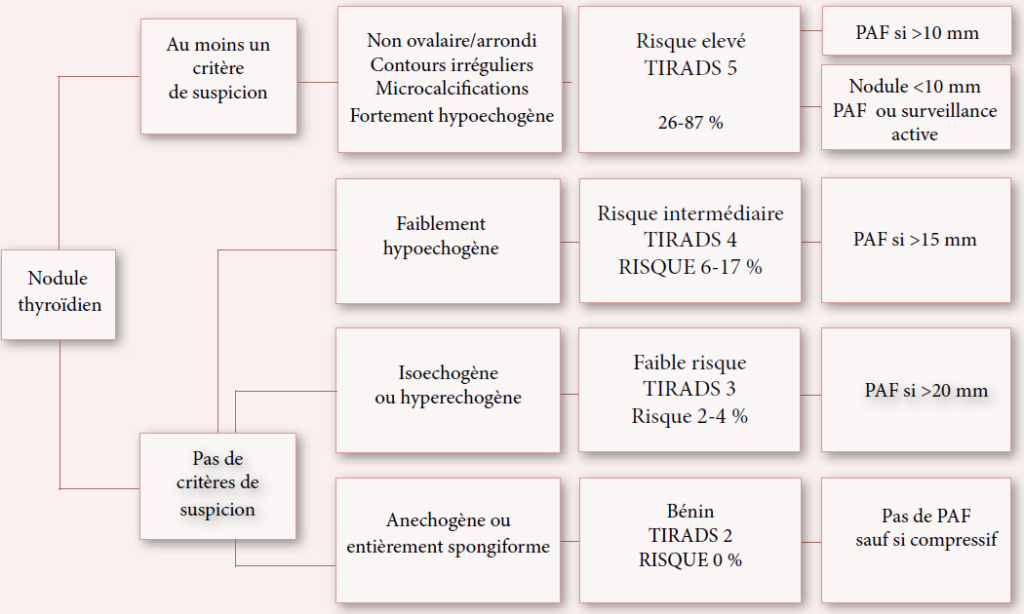
La ponction à l’aiguille fine des nodules est actuellement indiquée selon les recommandations de l’ATA [4,5]. Ces indications sont étroitement liées aux caractéristiques échographiques suspectes (nodule solide hypoéchogène, contours irréguliers, microcalcifications, vascularisation centrale, présence d’adénopathies suspectes) [4,5,9].
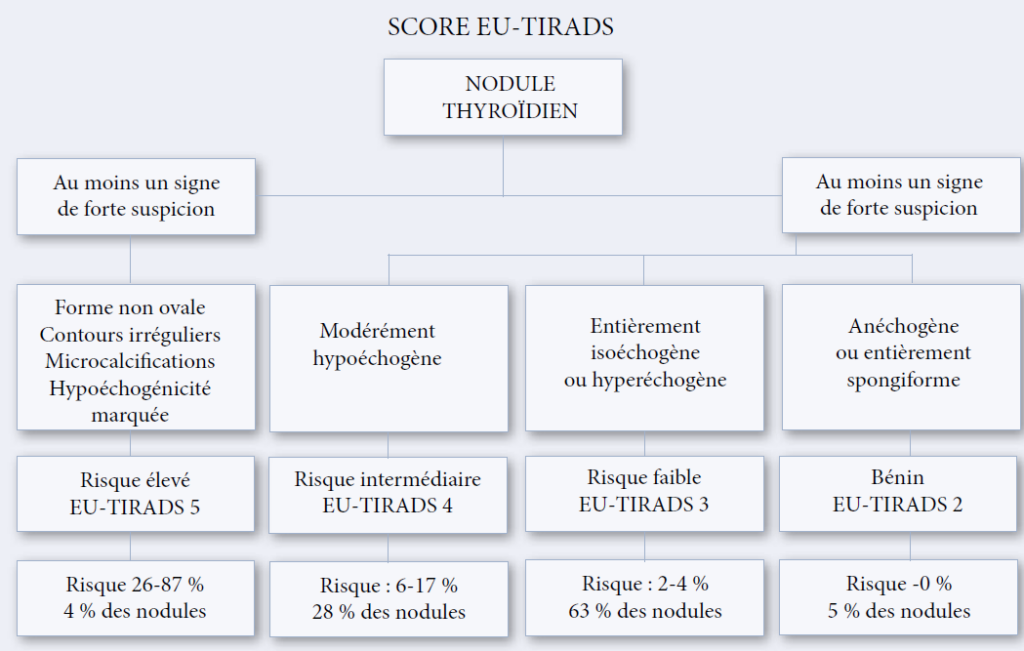
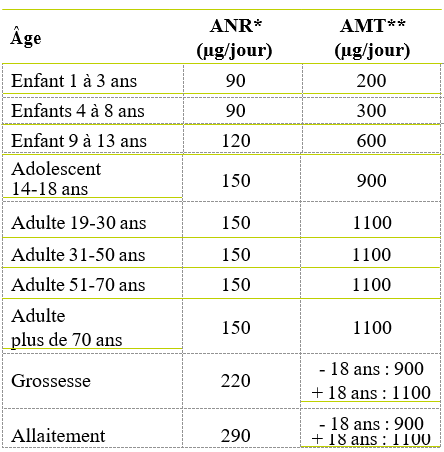
Le système TIRADS en échographie thyroïdienne s’est nettement propagé sur le plan international et a permis de développer un vocabulaire standardisé d’analyse et de compte-rendu destiné à homogénéiser les descriptions. Il propose aussi une stratification quantitative du risque de malignité. Le tableau 1 résume la classification TIRADS avec les indications de cytoponction [6,7].
Cytoponction thyroïdienne
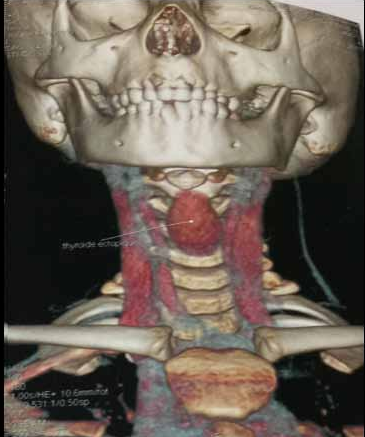
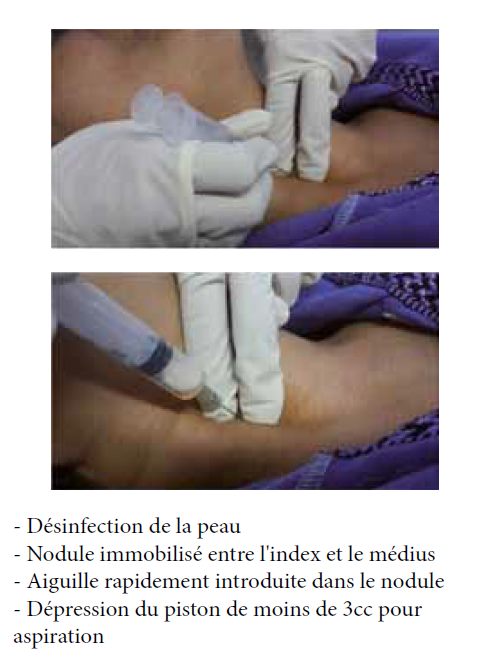
Le geste de cytoponction se fait sur un patient alité aidé ou non d’un échographe ; après avoir repéré le nodule, l’aiguille est introduite (figure 1) ; le matériel est déposé sur des lames de verres et étalé ; Les frottis sont séchés à l’air libre et colorés par la coloration May-Grünwald Giemsa. Pour la coloration Papanicolaou, les frottis sont fixés par un spray à base d’alcool.
La lecture se fait au microscope ordinaire : elle s’intéresse à l’architecture des amas, l’aspect cellulaire et nucléaire. La conclusion sera rédigée selon les critères du système Bethesda avec ses recommandations. [1,2,3]
Classifications NCI/Bethesda
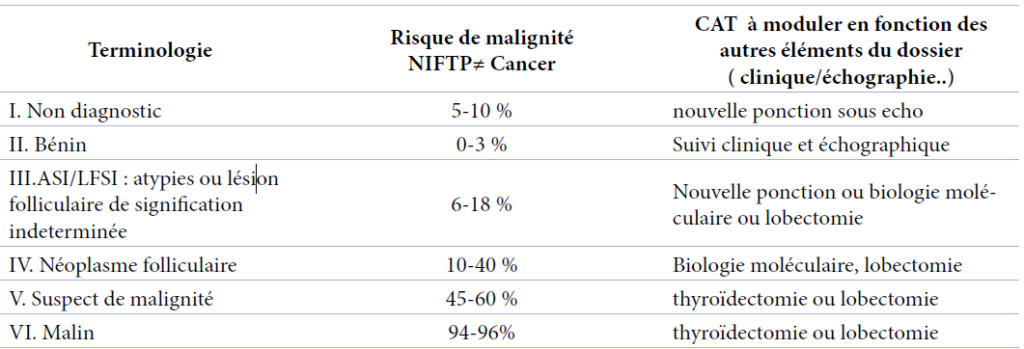
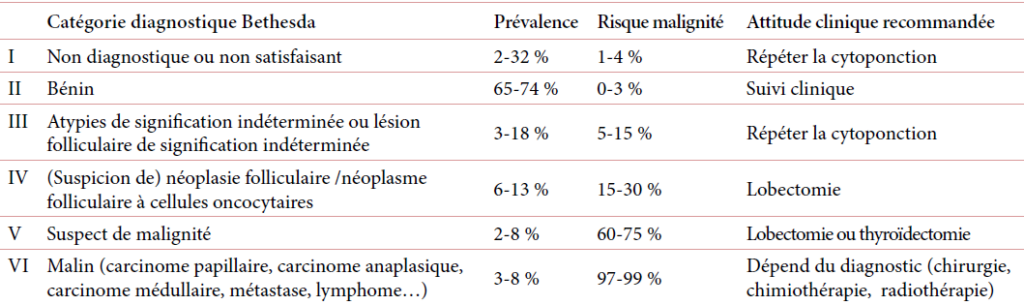
La terminologie Bethesda, publiée en 2010 [1,3] puis revisitée en 2017 [2], est corrélée à une évaluation du risque de cancer par catégorie lésionnelle et à une attitude thérapeutique adaptée. Elle donne un diagnostic sur lequel va reposer l’ensemble des décisions de surveillance ou de traitement dont le patient devra bénéficier. Elle permet ainsi une prise en charge standardisée des patients. Les six catégories diagnostiques sont classées comme suit :

Ce système décrit également le risque de malignité dans chaque catégorie et leur gestion clinique recommandée (tableau 2).
Classification Bethesda 2017
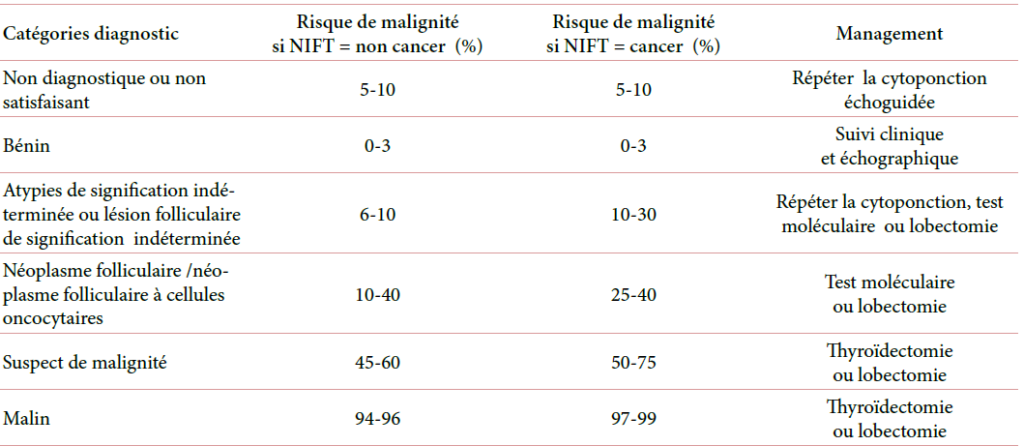
L’évolution de la terminologie de Bethesda pour les cytoponctions thyroïdiennes est étroitement liée à la nouvelle classification histologique OMS 2017 dans laquelle apparait une nouvelle entité le NIFTP : les carcinomes papillaires d’architecture vésiculaire encapsulés et non invasifs ne sont plus nommés «carcinomes» mais «tumeurs non invasives d’architecture vésiculaire avec des noyaux de type papillaire». Ainsi, pour chaque catégorie, le risque de malignité va plus ou moins diminuer [2] (Tableau3).
Critères cyto-morphologiques de diagnostic
Satisfaisant pour l’évaluation et Non diagnostic
Le frottis est jugé satisfaisant s’il contient au moins six groupes de cellules folliculaires composés d’au moins 10 cellules bien conservées. Les frottis mal étalés, mal fixés, mal colorés sont jugés insatisfaisants
Bénin
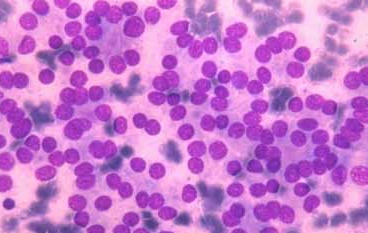
Les cas classés bénins comportent tout les critères cyto- morphologiques de bénignité (nodule colloïde, nodule hyperplasique, nodule toxique, thyroïdite lymphocytaire chronique) (figure 2).
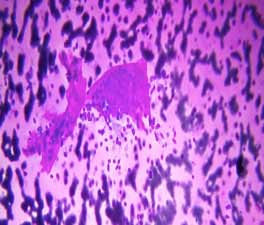
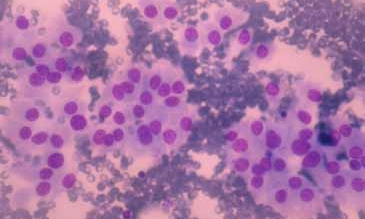
Atypie de signification indéterminée / lésion folliculaire de signification indéterminée (LFSI) Selon le système Bethesda, les lésions qui sont regroupées dans cette catégorie comportent des caractéristiques cytologiques qui ne peuvent pas être considérées comme étant bénignes mais aussi qui n’ont pas tous les critères pour être classées dans la catégorie suspecte (figure 3).
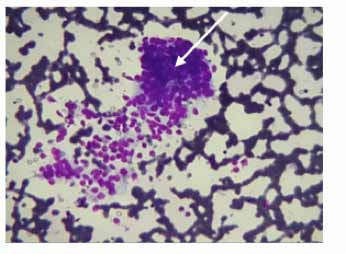
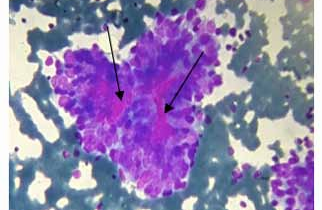
Néoplasme folliculaire / suspect pour un néoplasme folliculaire / Néoplasme folliculaire à cellules oncocytaires Les frottis de NF comportent une cellularité moyenne à riche, une substance de colloïde pauvre ou absente, une architecture microfolliculaire ou trabéculaire prédominante (figure 4).
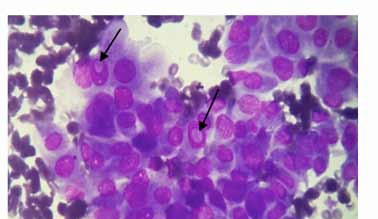
Le néoplasme à cellules de Hürthle (ou cellules oncocytaires) est une lésion dont les frottis comportent une cellularité presque exclusive en cellules oncocytaires (figure 5).
Il faut rappeler que la cellule oncocytaire est une cellule métaplasique et est retrouvée dans la plupart des lésions bénignes comme par exemple les thyroïdites lymphocytaires, les nodules basedowifiés et les nodules avec remaniements kystiques.
Suspect de malignité
Cette catégorie regroupe les cas présentant quelques critères cyto-morphologiques suggérant un carcinome papillaire, carcinome médullaire, lymphome, ou carcinome métastatique.
Catégorie maligne
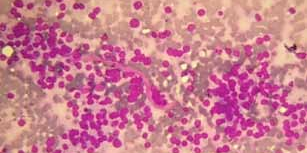
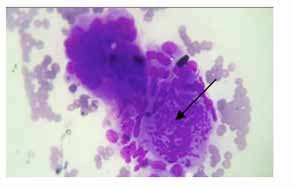
Les lésions comportant tous les critères cyto-morphologiques de malignité ont été classées dans cette catégorie. Les tumeurs malignes regroupent les carcinomes papillaires (figures 6 et 7), les carcinomes médullaires (figure 8), les carcinomes anaplasiques (figure 9), les lymphomes et métastases.
Résultats
Parmi les 4.829 cas de cytoponctions au cours de la période de janvier 2016 à décembre 2017, 449 cas (9%) se sont avérés non diagnostiques, 3.588 (74%) bénins, 242 LFSI (5%), 80 NF/92 NFO (3,5 %), 141 CS (3%) et 237 CM (5%) (tableau 4).
| n | % | |
| NDC | 449 | 9 % |
| CB | 3588 | 74 % |
| LFSI | 242 | 5 % |
| NF/NFO | 80 /92 | 3,5 % |
| CS | 141 | 3 % |
| CM | 237 | 5 % |
| TOTAL | 4829 | 100 % |
Le sex-ratio est de 8 femmes pour 1 homme et l’âge moyen est de 48 ans.
Pour la catégorie maligne nous avons recensés 237 cas avec 197 (83 %) carcinomes papillaires, 22 (9,2 %) carcinomes médullaires, 9 (3,8 %) carcinomes anaplasiques,6 (2,5 %) métastases intra-thyroïdiennes et 3 (1,2 %) lymphomes de la thyroïde (tableau 5).
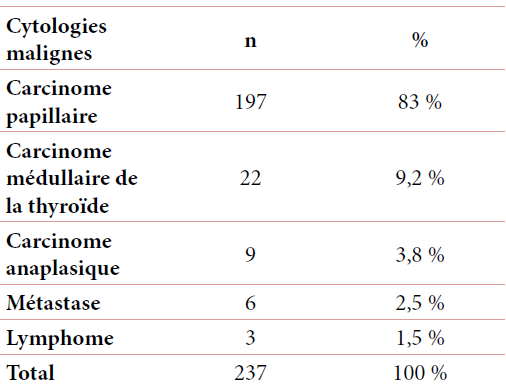
Tableau 5 : Distribution des cytologies malignes.
Un diagnostic histopathologique définitif a pu être disponible pour un échantillon de 294 cas.
La répartition de 294 cas de PAF avec les 6 catégories de Bethesda ainsi que leur corrélation histologique est représentée au tableau 6.
| HISTOPATHOLOGIE | TYPE HISTOLOGIQUE | |||||||||||||||
| CYTOLOGIE BETHESDA | BENIN | MALIN | CP | CMT | MICROCP | NIFTP | TPMI | n | ||||||||
| CB | 115 76,6 % | 6 | 4% | 29 | 19,3 % | 150 | ||||||||||
| LFSI | 7 50% | avec NIFTP 57% | 6 | 42,8% | sans NIFT 35,7% | 4 | 28,5% | 1 | 7% | 1 | 7% | 1 | 7% | 14 | ||
| NF | 5 38,4% | 8 | 61,5% | 7 | 53,8% | 1 | 7,69% | 13 | ||||||||
| NFO | 13 76,4% | 3 | 17,6% | 1 | 5,8% | 17 | ||||||||||
| CS | 7 17,5% | avec NIFTP 20% | 33 | 82,5% | sans NIFT 80 % | 27 | 2,5% | 2 | 5% | 3 | 7,5% | 1 | 2,5% | 40 | ||
| CM | 2 3% | 63 | 97% | 60 | 92,3% | 3 | 4,6% | 65 | ||||||||
| TOTAL | 294 | |||||||||||||||
Tableau 6 : Corrélations cyto-histologiques
Parmi les cas qui ont été classés bénins, 150 patients ont une corrélation histopathologique : 115 cas (76,6 %), ont eu la confirmation de la bénignité, et 6 cas ont une histologie maligne dont (4 %) concernaient le nodule ponctionné ; le taux de microcarcinome retrouvé sur cytologie bénigne est de 19,3 % (29 patients).
Pour les cas de LFSI, 14 corrélations cyto-histopathologie démontrent 7 cas de bénignité (50 %), 4 cas ont été diagnostiqués comme carcinome papillaire (28,5 %), un cas de microcarcinome papillaire, 1 cas de LFSI, a un diagnostic définitif de NIFTP ; et un cas a été diagnostiqué tumeur à potentiel de malignité incertaine (TPMI). Nous avons examinés 30 cas NF dont 13 NF et 17 NFO ; pour les NF nous retrouvons 5 histologies bénignes (38,4 %), 8 histologies malignes (53,8 %), dont et 7 CP et 1 micro-carcinome papillaire (7,69 %). Concernant les NFO les corrélations cyto-histologiques objectivent 13 histologies bénignes (76,4 %), dont 9 adénomes oncocytaires, 3 histologies malignes (17,6 %) dont 2 CP (11,7 %), et 1 microcarcinome papillaire (5,8 %).
Parmi les cytologies suspectes 40 cas ont eu une confirmation en histologie : 27 cas de carcinomes papillaires et 2 cas de carcinome médullaire ; 1 cas de cytologie suspecte de carcinome papillaire a un diagnostic définitif de NIFTP ; 3 cas de microcarcinome papillaire.
Au total le taux de malignité pour la catégorie suspecte est de 82,5 % si NIFTP n’est pas pris en considération et de 80 % avec NIFTP.
Pour 7 cytologies suspectes nous retrouvons une histologie bénigne soit 17,5 % des cas si NIFTP est exclu et 20 % si NIFTP est inclus comme bénin.
Nous avons corrélé 65 cas de cytologie maligne. 63 cas (97 %) ont une histologie maligne et 2 cas (3 %) ont une histologie bénigne. Parmi les 63 cas nous avons 60 carcinomes papillaires et 2 carcinomes médullaires La sensibilité est de 94 % ; la spécificité est de 92 % ; valeur prédictive positive VPP = 91 % et la VPN=95 %
Discussion
Nous observons dans cette étude une nette prédominance féminine avec un sex-ratio femme/homme de 8 ce qui est décrit dans la littérature [8,10,11]. La moyenne d’âge rejoint également celle des autres études ; elle se situe dans la 40ème décennie [8,10,11].
Au sein de notre service, en dehors de la réception de frottis provenant de différents centres hospitaliers, le cytopathologiste effectue lui-même la technique de PAF, ce qui assure des frottis de meilleure qualité.
La distribution de nos cas selon le système Bethesda rejoint la prévalence étudiée par les auteurs [1,14,16] sauf pour la catégories néoplasme folliculaire qui est en dessous des cas attendus (3 %) au lieu de 6 à 13% .
Dans notre série, 108 CB sur 115 (76,6 %) ont été confirmées par l’histologie.
Ce taux correspond aux vrais négatifs. Dans les séries de la littérature, il varie de 75 à 97 % alors que le taux des faux négatifs varie de 3 à 26 % [11,12,15]. Nous avons 4% de faux négatifs. Ceux-ci ont une importance particulière et sont une préoccupation majeure pour les cliniciens. Bien que le taux de faux négatifs varie de 2 % à 11 %, il est de moins de 2 % dans la plupart des cliniques ayant une expérience adéquate en cytologie [17].
Répéter la PAF après vérification échographique (et score TIRADS) est une stratégie idéale pour diminuer les taux de faux négatifs et pour rassurer les cliniciens.
Dans notre série, 63 cytologies malignes sur 65 soit 97 % des cas, se révélaient être malignes à l’histologie. Dans la littérature ce taux varie de 94 à 100 % [10,11,12,14].
Nos deux faux positifs étaient des diagnostics cytologiques basés sur les critères morphologiques du carcinome papillaire et dont l’histologie révélait une hyperplasie vésiculaire bénigne pour un cas, et un adénome folliculaire pour le deuxième cas.
Sur 40 cytologies suspectes, 33 étaient malignes en histopathologie soit 82,5 % des cas, ce qui prouve la grande fiabilité du diagnostic cytologique ; le carcinome papillaire est le diagnostic le plus fréquent avec 72,5 % des cas. Toutes les cytologies suspectes de carcinome mé dullaire ont été confirmées en histopathologie.
Nous observons dans notre série 50 % de bénignité pour les LFSI et 42,8 % de malignité. Ce dernier taux est supérieur au taux retrouvés dans la littérature qui est de 10 à 30% [1,18].
Nous retrouvons un cas de tumeur à potentiel de malignité incertain (TPMI) ; ce patient a subi une PAF de contrôle qui était toujours en faveur de LFSI. L’hétérogénéité de cette catégorie exclut tous les scénarios pour lesquels l’interprétation de LFSI est appropriée [25].
Pour les LFSI dont l’histologie était bénigne, 4 cas ont subi une intervention sans répéter la cytoponction, ce qui est plus de la moitié des cas ; le deuxième contrôle avec un suivi clinique est nécessaire pour éviter la chirurgie ; le mot « lésion indéterminée » peut prêter à confusion sur la nature de la pathologie, de ce fait certains spécialistes préfèrent opérer le patient afin d’avoir un diagnostic définitif ce qui n’est pas le but recherché par le système Bethesda qui recommande une deuxième cytoponction pour les cas de cette catégories [13].
Le Bethesda 2017 rajoute l’option des tests moléculaires afin de pouvoir limiter au maximum le geste de chirurgie [2,19,20]. Le diagnostic de néoplasme folliculaire se base sur la présence d’une architecture vésiculaire avec des noyaux augmentés de volume ; le diagnostic histologique de carcinome folliculaire repose sur la mise en évidence d’une authentique invasion capsulaire ou vasculaire ce qui est impossible à détecter en cytopathologie [4,5,11,12].
La prévalence selon la littérature est de 15 à 30 % alors que notre étude retrouve un taux de malignité élevé 61,5 % incluant 53,8 % de CP.
Pour les 8 cas malins l’histologie était en faveur du carcinome papillaire variante folliculaire. Cette variante est faite presque exclusivement de vésicules dont les thyréocytes comportent des signes nucléaires de carcinome papillaire ; ces signes sont retrouvés très rarement en cytologie ce qui explique le classement de ces cas dans la catégorie NF [16,24].
Avec l’introduction du NIFTP, le risque de malignité diminue de 42 à 37 % (de 10 %) alors que la bénignité augmente 7 %. Ce nom a été proposé afin d’éviter le surtraitement de ces lésions de très bon pronostic, sans oublier l’impact psychologique du mot « cancer » sur la vie du patient et celle de son entourage. Les atypies dans les NIFTP sont moins prononcées par rapport aux carcinomes papillaires classiques et pour cette raison elles ne sont que très rarement classées en CM [21,22,23].
La grande majorité des NFO sont des adénomes oncocytaires et hyperplasie oncocytaire bénigne (76,4 %) nous retrouvons 2 carcinomes papillaires oncocytaires. La présence de cellules oncocytaires sur les frottis représente souvent des cellules de réparation dans les thyroïdites lymphocytaires les nodules en remaniements kystiques, les hyperthyroïdies. Une cellularité riche nécessite l’observation minutieuse de l’aspect architectural et des signes nucléaires à la recherche de carcinome [1,2,25].
Notre étude retrouve 35 cas microcarcinomes papillaires avec 29 cas (19,3 %) sur 115 cytologies bénignes; leur incidence est en augmentation en raison de l’amélioration des techniques diagnostiques (échographie cervicale et cytoponction). Certaines publications avancent une responsabilité des radiations ionisantes [26].
Leur découverte fortuite sur l’histologie définitive reste fréquente et impose souvent une reprise chirurgicale pour totalisation et curage. La littérature s’accorde à conclure que le risque de décès lié au microcarcinome est très faible : de l’ordre de 0,3% [23].
Pour le calcul des vrais positifs et des faux positifs, les auteurs regroupent dans la littérature les cytologies « suspectes » et « malignes ». Dans notre étude, nous avons fait de même : le taux de sensibilité qui est de 94 %, la spécificité de 92 %, une valeur prédictive positive de 91 % et une valeur prédictive négative de 95 %. Avec ces résultats, nous pouvons estimer que notre technique, est très fiable pour la détection des cancers de la thyroïde.
Conclusion
La combinaison de l’examen clinique, échographique et cytologique reste le pilier de la sélection des patients pour la chirurgie thyroïdienne.
Le système Bethesda apporte un résultat net et précis. La sensibilité, la spécificité de la PAF pour le diagnostic de la malignité ont éclipsé l’utilité d’autres méthodes de diagnostic et cette procédure, combinée avec la classification Bethesda, a assumé un rôle dominant dans la détermination de la gestion des patients avec nodule thyroïdien. Cette étude démontre que la PAF donne des résultats positifs en corrélation en histopathologie avec une sensibilité et spécificité élevées, ainsi que la VPP et la VPN.
La biologie moléculaire introduite dans le Bethesda 2017 améliore nettement cette sensibilité.
Le travail en équipe multidisciplinaire avec un vocabulaire uniforme et standardisé est la règle d’or pour atteindre notre objectif principal qui est la meilleure prise en charge du patient.
Références :
- Cibas ES, Ali SZ. The Bethesda system for reporting thyroid cytopathology. Thyroid 2010
- Cibas ES, Ali SZ. The Bethesda system for reporting thyroid cytopathology. Thyroid 2017
- Cochand-Priollet B, et al. Cytopathologie thyroïdienne : le système de Bethesda 2010.Annales de pathologie (2012)32,177-183.
- American Thyroid Association (ATA) Guidelines Taskforce on Thyroid Nodules and Differentiated Thyroid Cancer 2015, Cooper DS,
- Doherty GM, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2009; 19:1167-1214.
- Russ G et al, Le système TIRADS en échographie thyroïdienne. Journal de radiologie (2011)92,701-713.
- Tramalloni J, Wémeau JL. Consensus français sur la prise en charge du nodule thyroïdien : ce que le radiologue doit connaître. EMC – Radiologie et imagerie médicale – cardiovasculaire – thoracique – cervicale 2012;0(0):1-18 Article 32-705-A-10
- Amrikachi M, Ramzy I, Rubenfeld S, Wheeler TM: Accuracy of fine- needle aspiration of thyroid. Arch Pathol Lab Med 2001;125:484–488
- Cho E, et al., High suspicion US pattern on the ATA guidelines, not cytologic diagnosis, may be a predicting marker of lymph node metastasis in patients with classical papillary thyroid carcinoma, The American Journal of Surgery (2017), https://doi.org/10.1016/j.amj- surg.2017.12.006
- Muratli A, Erdogan N, Sevim S, Unal I, Akyuz S. Diagnostic efficacy and importance of fine-needle aspiration cytology of thyroid nodules. J Cytol 2014;31:73-8.
- Ko HM, Jhu IK, Yang SH, Lee JH, Nam JH, Juhng SW, et al. « Clinicopathologic analysis of fine needle aspiration cytology of thethyroid. A review of 1,613 cases and correlation with histopathologic diagnoses ». Acta Cytol 2003;47:727-32.
- Park HS: Cytohistopathologic comparative study of aspiration biopsy cytology from various sites. Korean J Cytopathol 1991;2:8–19
- Kelman AS, Rathan A, Leibowitz J, Burstein DE, Haber RS: Thyroid cytology and the risk of malignancy in thyroid nodules: Importance of nuclear atypia in indeterminate specimens. Thyroid 2001;11:271 277
- Sclabas GM, Staerkel GA, Shapiro SE, et al. Fine needle aspiration of the thyroid and correlation with histopathology in contemporary series of 240 patients. Am J Surg 2003;186:702—10.
- Cheung YS, Poon CM, Mak SM, et al. Fine needle aspiration cytology of thyroid nodules- How well are we doing? Hong Kong Med J 2007;13:12—5.
- Bongiovanni M, Spitale A, Faquin WC, Mazzucchelli L, Baloch ZW. The Bethesda System for Reporting Thyroid Cytopathology: a meta-analysis. Acta Cytol. 2012;56:333-339.
- Cibas ES, Alexander EK, Benson CB, et al. Indications for thyroid FNA and pre-FNA requirements : A synopsis of the National cancer institute thyroid fine-needle aspiration state of the Science conference. Diagn Cytopathol 2008;36:390-9.
- Pothier DD, Narula AA. Should we apply suctionduring fine needle cytology of thyroid lesions ? A systematic review and meta-analysis. Ann R Coll Surg Engl2006;88:643-5.
- Nikiforov YE, Yip L, Nikiforova MN. New strategies in diagnosing cancer in thyroid nodules : impact of molecular markers. Clin Cancer Res. 2013;19:2283-2288.
- Nikiforov YE. Molecular diagnostics of thyroid tumors. Arch Pathol Lab Med. 2011;135:569-577.
- Z W. Baloch Noninvasive Follicular Thyroid Neoplasm With Papillary-Like Nuclear Features (NIFTP): A Changing Paradigm in Thyroid Surgical Pathology and Implications for Thyroid Cytopathology MD,Cancer cytopathology p 616-620
- Faquin WC, Wong LQ, Afrogheh AH, et al. Impact of reclassifying noninvasive follicular variant of papillary thyroid carcinoma on the risk of malignancy in The Bethesda System for Reporting Thyroid Cytopathology. Cancer Cytopathol. 2016;124:181-187.
- Howitt BE, Chang S, Eszlinger M, et al. Fine-needle aspiration diagnoses of noninvasive follicular variant of papillary thyroid carcinoma. Am J Clin Pathol. 2015;144:850-857.
- Noof A. Alabdulqader Application of the Bethesda System for Reporting Thyroid Cytopathology in the Eastern Province of Saudi Arabia: A Follow-Up Study Acta Cytologica 2015;59:233–238
- Cibas ES: Fine-needle aspiration in the workup of thyroid nodules. Otolaryngol Clin North Am 2010; 43: 257–271.
- Grodski, S., et al., Increasing incidence of thyroid cancer is due to increased pathologic detection. Surgery, 2008. 144(6): p. 1038-43; discussion 1043.