Pr C. HAOUICHAT1, Dr B. NECHE1, Dr M. BOUMAAzA1, Dr M. SAADI1, Pr N. KECHOUT2, Pr N. ATTAL2, Pr H. DJOUDI1 ,Service de Rhumatologie, CHU Douera, Alger. Service d’Immunologie, Institut Pasteur d’Algérie, Alger
Résumé :
Introduction : le Rituximab (RTX) est la première biothérapie disponible en Algérie depuis 2008 avant les anti-TNF Alpha, ce qui justifie son utilisation en première intention dans le traitement de la polyarthrite rhumatoïde (PR) active réfractaire au méthotrexate ou un autre DMARDs, et naïve de toute biothérapie.
Objectif : évaluer l’efficacité et la tolérance du RTX chez des malades présentant une PR active (DAS >3.2), naïve aux biothérapies, réfractaire au Méthotrexate ou aux autres traitements de fond (DMARDs) et ayant un recul d’au moins une année.
Patients et méthode : étude prospective mono centrique menée entre Mai 2008 et Mai 2017, dans le service de rhumatologie de l’hôpital de Douera.
Tous les patients adultes des deux sexes, suivis pour PR traitée par RTX, réfractaire aux traitements conventionnels et naïve de biothérapies, ont été inclus avec un recul d’au moins un an après la première cure. Le diagnostic de la PR a été retenu selon les critères de l’ACR 1987 (American College of Rheumatology) ou ACR/EULAR (European League Against Rheumatism) en cas de PR récente. Une évaluation clinique, biologique et radiologique était pratiquée à 3,6 et 12 mois après la première perfusion, comportant le DAS28, le HAQ, VS, CRP, FNS, le dosage des Im munoglobulines et la numération des lymphocytes B (CD19) ainsi que le calcul du Sharp modifié à 12 mois.
Résultats : L’efficacité du traitement a été évaluée chez les patients ayant un recul d’au moins une année après la première cure, soit 74 malades, une malade a été exclue de l’étude pour poussée de PR à la première perfusion. La majorité de la population d’étude se composait de femmes, soit 93% (69 femmes). L’âge moyen était de 49 ans ± 13.79 (extrêmes de 24-70ans). La durée moyenne d’évolution de la maladie était de 17 ans ± 10.53 (extrêmes de 2- 49 ans). La PR était érosive dans 97% des cas, 75% avaient un facteur rhumatoïde positif. L’anti CCP positif était chez 60% des malades.
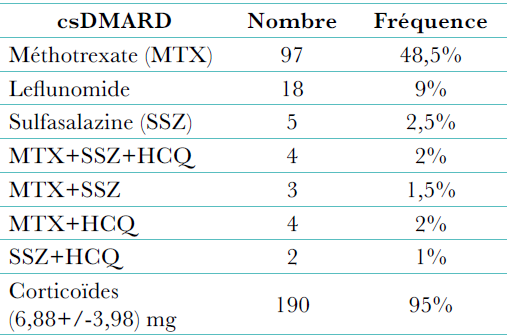
Le méthotrexate en monothérapie ou associé à un ou deux DMARDs était observé chez 66% des patients, 18% étaient sous un autre DMARDS (salazopyrine, leflunomide, hydroxychloroquine) et 15% sous aucun traitement de fond. Un traitement par corticoïdes a été retrouvé chez 71% des patients avec une dose moyenne de 10mg/j.
Le recul moyen après la première perfusion de RTX était de 45,7 mois ± 20,90 À l’inclusion, le DAS moyen était de 5.3±1.5 (3.24 – 7.08), le HAQ moyen était de 1.44 (0.25 – 2.4) et le Sharp modifié moyen de 198 ± 120.5 (0 – 448).
À 12 semaines, la réponse EULAR était de 79 %, 65 patients sur 74 étaient répondeurs avec 32% de bons répondeurs et à 24 semaines, la réponse au traitement était maintenue chez 58 patients sur 70 malades, soit 83%, avec 40% de bons répondeurs. 4 patients n’ont pas répondu d’emblée et ont été switchés vers une autre biothérapie. Après 48 semaines, le taux de rémission (bonne réponse EULAR) était de 24% (17/70), le délai moyen de rechute était de 8.8 mois. 47 patients (67%) ont été retraités avec un délai moyen de retraitement de 9 mois. L’amélioration cliniquement pertinente (≥ 0,3) du HAQ était observée chez 63% des patients à la 24ème semaine. La progression radiologique était lente du fait que la majorité des patients présentaient une polyarthrite ancienne et évoluée. La tolérance au traitement était bonne chez 67 patients, soit 89% : 1 cas de poussée de PR à la première perfusion qui a été exclu de l’étude, 3 cas d’infections urinaires à Escherichia-coli, 2 cas d’infection cutanée (zona et furonculose), un cas d’infection respiratoire haute et 1 cas d’hypertension artérielle.
Conclusion : cette étude observationnelle démontre l’efficacité et la tolérance du RTX utilisé en première intention chez près de 80% de patients à 12 semaines de traitement et souligne l’intérêt de disposer d’un registre de suivi du RTX et de toutes les autres biothérapies utilisées en Algérie.
Mots-clés : Rituximab, polyarthrite rhumatoïde, efficacité, tolérance, biothérapie.
Abstract :
Introduction : Rituximab (RTX) is the first biotherapy available in Algeria since 2008 before anti-TNF Alpha, which justifies its first-line use in the treatment of active methotrexate-refractory rheumatoid arthritis (RA) or other DMARDs and Naive of any biotherapy.
Objective: To evaluate the efficacy and safety of RTX in patients with active RA (DAS > 3.2), naive to biotherapies, refractory to Methotrexate or to other treatments (DMARDcs) and having a follow-up of at least one year .
Patients and method : A prospective, mono-centric study conducted between May 2008 and May 2017, in the department of rheumatology of the Douera hospital.
All adult patients of both sexes, followed for PR and treated with RTX, refractory to conventional and naïve biotherapeutic treatments were included with a follow-up of at least one year after the first course. The diagnosis of RA was selected according to the criteria of the American College of Rheumatology (ACR 1987) or ACR / EULAR (European League Against Rheumatism) In the case of recent RA. Clinical, biological and radiological evaluation was performed at 3.6 and 12 months after the first infusion, including DAS28, HAQ, ESR, CRP, NFS, immunoglobulin assay and B-cell count (CD19) Calculation of the modified Sharp at 12 months.
Results : Treatment efficacy was evaluated in 74 patients with a follow-up of at least one year after the first course. One patient was excluded from PR study due to a PR surge at the first infusion.
The majority of the study population consisted of women, or 93% (69 women). The mean age was 49 ± 13.79 (range of 24-70 years). The mean duration of the disease was 17 years ± 10.53 (range 2-49 years).97% of RA were erosive and 75% had a positive rheumatoid factor. AntiCCP positive was found in 60% of patients. 66% of the patients were on methotrexate as monotherapy or in com- bination with one or two DMARDs, 18% were under another DMARDS (salazopyrine, leflunomide, hydroxychlo- rochine) and 15% under no treatment. Treatment with corticosteroids was found in 71% with an average dose of 10mg / day. The mean follow-up after the first infusion of RTX was 45.7 months ± 20.90. At baseline, mean DAS28 was 5.3 ± 1.5 (3.24-7.08), the mean HAQ was 1.44 (0.25- 2.4) and the Sharp modified mean of 198 ± 120.5 (0-448). A12 weeks, the EULAR response was 79%, 65 of 74 patients were responders with 32% good responders, and at 24 weeks the response to treatment was maintained in 83% (58/70 patients) with 40% responders. Four patients did not respond at the 12th week and were Switched to another biotherapy.
After 48 weeks, the remission rate was 24% (17/70 patients), the mean relapse time was 8.8 months. Forty-seven (67%) patients were retreated with an average 9-month, relevant improvement of HAQ (≥ 0.3)was observed in 63% of patients at week 24.
Radiological progression was slow because the majority of patients had advanced and old arthritis.
We found a good tolerance in 67 patients (89%). 1 case of RA surgery at the first infusion, that was excluded from the study, 3 cases of urinary infection with Escherichia coli, 2 cases of skin infection (shingles and furunculosis) , One case of high respiratory infection and 1 case of high blood pressure.
Conclusion : This observational study demonstrates the efficacy and safety of RTX used as first-line treatment in nearly 80% of patients at 12 weeks of treatment, and highlights the value of having a follow-up registry for RTX and all other biotherapies used in Algeria.
Key-words : rituximab, rheumatoid arthritis, efficacy, tolerance, biotherapy.
Introduction :
La polyarthrite rhumatoïde (PR) est le plus fréquent des rhumatismes inflammatoires chroniques[1], responsable à long terme d’une augmentation de la morbidité et de la mortalité et d’un handicap fonctionnel majeur [2,3]. La meilleure connaissance des mécanismes physiopathologiques en cause a permis le développement de nouvelles molécules biologiques ciblées sur certains médiateurs de l’immunité : les cytokines pro inflammatoires, les lymphocytes B et les lymphocytes T… [4].
Depuis plus d’une dizaine d’années, les traitements biologiques ont révolutionné la prise en charge des patients atteints de PR. Toutefois, ces médicaments ont montré une certaine limite puisque 30 % des patients environ ne répondent pas au traitement ou échappent après une réponse initiale[5,6]. En plus des effets secondaires potentiellement graves rapportés, notamment dans un pays d’endémie tuberculeuse où l’incidence de la tuberculose est intermédiaire.
Le Rituximab (RTX) est la première biothérapie disponible en Algérie depuis 2008, cet anticorps est dit chimérique car il est partiellement humanisé et contient des séquences d’origine murine, dirigé contre le CD20, retrouvé à la surface des lymphocytes B matures. Ce médicament a obtenu l’AMM en France en 1997 dans le traitement des lymphomes B et depuis, son utilisation s’est étendue à de nombreuses autres pathologies non malignes et notamment dans celui de la PR active en 2006. La Haute Autorité de Santé (HAS) recommande en pratique clinique d’utiliser le RTX dans la PR après échec et/ou intolérance et/ou contre-indication à deux anti- TNF, alors que la Société Française de Rhumatologie (SFR) et l’European League Against Rheaumatism (EULAR) recommandent son utilisation en première intention dans des conditions particulières (antécédent personnel de lymphome, tuberculose latente avec impossibilité de chimio prophylaxie, risque élevé de tuberculose, antécédent personnel de sclérose en plaque, antécédent personnel de cancer de moins de 5 ans …) [7-9].
Pour ce qui est de son efficacité, elle a été démontrée dans le traitement de la PR au cours de trois principales études cliniques randomisées contre placebo [10-12]. La première étude [10] a été réalisée chez 161 patients insuffisamment répondeurs au méthotrexate et a permis de montrer que l’association du RTX au méthotrexate était supérieure à la poursuite du méthotrexate seul et que l’association paraissait donner des résultats supérieurs au RTX administré seul. Un résultat supplémentaire très intéressant de cette étude est la constatation que l’administration de ce médicament en perfusion intraveineuse de 1 g, au jour 1 et au jour 15, permettait d’obtenir une réponse thérapeutique durable supérieure à 6 mois et pouvait même se prolonger au-delà d’une année. Parallèlement, le RTX entraînait une disparition des lymphocytes B sanguins dans la majorité des cas pendant plus de 6 mois. L’étude DANCER [11] a démontré également que le RTX administré chez des patients insuffisamment répondeurs au méthotrexate, à raison de deux perfusions de RTX à j1 et j15, de 1 g ou 500 mg par perfusion, permet d’obtenir deux fois plus de répondeurs que la poursuite du méthotrexate seul. Enfin, l’étude REFLEX [12] a montré aussi que le RTX administré à 1 g à j1 et j15, en association avec le méthotrexate, permettait également une réponse thérapeutique supérieure à la poursuite du méthotrexate seul, dans une population de patients insuffisamment répondeurs à au-moins un anti-TNF. La diminution de la progression radiologique de la PR sous RTX a été également observée au cours de cette étude.
Notre étude avait pour objectif d’évaluer l’efficacité et la tolérance du RTX utilisé en première intention dans le traitement de la PR active (DAS >3.2), réfractaire aux traitements conventionnels et naïve de biothérapie, après un suivi d’au moins une année.
Patients et méthodes :
– Patients :
Etude prospective mono centrique, menée entre Mai 2008 et Mai 2017, dans le service de rhumatologie de l’hôpital de Douera.
Tous les patients adultes des deux sexes, suivis pour PR réfractaire aux traitements conventionnels et naïve de biothérapies, traitée par RTX, ont été inclus avec un recul d’au moins un an après la première cure. Le diagnostic de la PR a été retenu selon les critères de l’ACR 1987 (American College of Rheumatology) ou ACR/EULAR (European League Against Rheumatism) en cas de PR récente [13]. Non inclus, les patients ayant une contre-indication au RTX (insuffisance cardiaque sévère (NYHA classe IV) ou de maladie cardiovasculaire sévère non contrôlée, infections sévères, chroniques et/ou récidivantes (bactériennes, virales)). Etaient exclus de l’étude, les patients ayant présenté un effet secondaire grave. Un consentement éclairé a été signé par les patients inclus.
– Méthode :
• Bilan pré-thérapeutique :
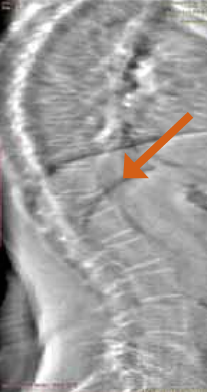
Nous avons réalisé chez tous les patients un bilan, comportant l’hémogramme, l’électrophorèse des protéines sériques, le bilan hépatique, le bilan inflammatoire (VS et CRP), l’électrocardiogramme, l’examen cytobactériologique des urines, les sérologies (hépatiques B et C, VIH), la numération des lymphocytes B (CD19) et le dosage pondéral des immunoglobulines (IgG, IgA, IgM) ainsi que la radiographie du thorax, des mains de face et de l’avant pied (face et déroulé).
Une vaccination systématique contre le pneumocoque était administrée au moins quatre semaines avant la première perfusion de RTX.
• Protocole thérapeutique :
Deux stratégies thérapeutiques ont été utilisées :
- Le premier protocole : les patients ont été traités par du RTX en perfusion intraveineuse à raison de 1 gramme (g), à j1 et à j 15, précédée d’une prémédication constituée par la perfusion en intraveineux de 100 mg de méthylprédnisolone associée au paracétamol 1 g et à un antihistaminique. Le retraitement était à la demande : les patients ont été retraités à la rechute après réponse initiale et avec les mêmes modalités que la première cure (N = 75 patients).
- Le deuxième protocole : les patients ont été traités en première cure par du RTX en perfusion intraveineuse à raison de 1 g, à j1 et à j 15, précédée d’une prémédication. Le retraitement est basé sur une approche ciblée au cours de laquelle les patients ont été évalués à 24 semaines après chaque cure, ceux avec un DAS28 ≥2.6 ont été retraités systématiquement avec réduction de dose à 500 mg × 2 pour chaque cycle de retraitement (N = 5 patients).
• Évaluation :
N’ont été analysés que les patients traités par le premier protocole, soit les 75 patients.
L’activité de la maladie a été évaluée par le score composite (DAS28), qui comporte RM (raideur matinale), NAD (nombre d’articulations douloureuses), NAG (nombre d’articulations gonflées), VS (vitesse de sédimentation) ou, CRP (C reactive protein).
Le score DAS28 a été évalué avant le début du traitement, à 3 mois, à 6 mois et à 12 mois [14,15].
– Évaluation de l’efficacité du Rituximab
À 3 mois, à 6 mois et à 12 mois ; par l’évolution du DAS28. La réponse thérapeutique est mesurée par le delta DAS28 (DAS28) qui correspond à la différence entre le DAS28 initial avant instauration du RTX et le DAS28 à l’instant t (3 mois, 6 mois et 12 mois). Les résultats sont exprimés en bonne réponse : diminution du DAS supérieure à 1,2, réponse modérée : baisse comprise entre 0.6 et 1,2 et réponse nulle : diminution du DAS inférieure à 0,6.
Le retentissement fonctionnel de la PR a été estimé par le score HAQ (Health Assessment Questionnaire), avant le début du traitement à 6 mois et à 12 mois, défini comme amélioration cliniquement pertinente (≥ 0,3) du HAQ initial à l’inclusion.
La progression structurelle a été évaluée par l’indice de Sharp modifié avant le début du traitement et à 12 mois.
– Évaluation de la tolérance du Rituximab
Les effets indésirables survenus chez les patients traités par le RTX ont été recueillis au cours des 12 premiers mois de traitement (allergie, hypertension, infections, neutropénie, …). Etaient considérés comme graves, les effets indésirables mettant en jeu le pronostic vital et ayant conduit à une hospitalisation et un arrêt définitif du RTX.
Résultats :
- Caractéristiques de la population d’étude à l’inclusion : Quatre-vingt-dix (90) patients présentant une PR ont été traités par RTX, entre Mai 2008 et Mai 2017. L’efficacité du traitement a été évaluée chez les patients ayant un recul d’au moins une année après la première cure et ayant reçu le premier protocole avec le retraitement à la demande, soit 74 malades, une malade a été exclue de l’étude vu l’effet secondaire grave (poussée de PR). Les caractéristiques des patients à l’inclusion sont résumées dans le tableau 1.
| Caractéristiques des patients | N=75 |
| Age, moyen, (ans) | 49.25 ans ± 13.79 |
| Sexe, femmes, n(%) | 69 (93%) |
| Durée d’évolution, moyen, (an) | 17 ans ± 10.53 |
| DAS 28, moyen | 5.3 ± 1.5 (3.24 – 7.08) |
| HAQ moyen | 1.44 (0.25 – 2.4) |
| Sharp modifié moyen (extrêmes) | 198 ± 120.5 ( 0 – 448) |
| Facteurs rhumatoïdes, n(%) | 55 (75%) |
| ACPA positif, n(%) | 44 (60%) |
| Corticothérapie, n(%) | 52 (71%) |
La majorité de la population d’étude se composait de femmes, soit 93% (69 femmes). L’âge moyen était de 49 ans ± 13.79 (extrêmes de 24-70ans). La durée moyenne d’évolution de la maladie était de 17ans ± 10.53 (extrêmes de 2-49 ans).
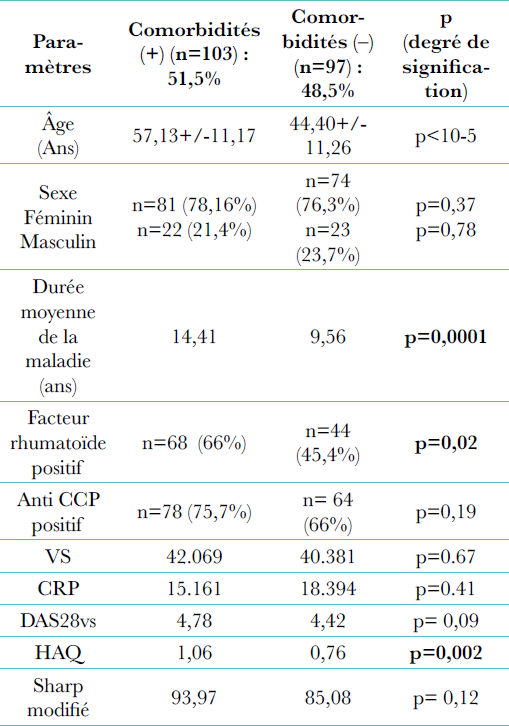
Pour les comorbidités associées à la PR, l’hypertension artérielle a été retrouvée chez 24 % des patients, 12 % étaient diabétiques, 3 % présentaient une cardiopathie (NYHA classe ≤ III), le Gougerot Sjögren a été retrouvé associé à la PR dans 4 % des cas et l’asthme chez 4 % des patients .
• Caractéristiques de la polyarthrite rhumatoïde à l’inclusion :
Tous les patients avaient une PR active, le DAS28 moyen était de 5.3 ±1.5 (3.24 – 7.08), 44 patients (59.5%) avaient une activité sévère (DAS28 ›5.1) et 30 patients (40.5%) avaient une activité modérée (3.2 ‹ DAS28 ≤ 5.1).
La PR était érosive dans 97% des cas, avec un Sharp modifié moyen de 198 ± 120.5 (0 – 448) et 75% des patients avaient un facteur rhumatoïde positif. L’anti CCP positif était retrouvé chez 60% des malades. Le méthotrexate en monothérapie ou associé à un ou deux DMARDs observé chez 66% des patients et 18% étaient sous un autre DMARDs (salazopyrine, leflunomide, hydroxy-chlorochine), 15% n’étaient sous aucun traitement de fond (bilan hépatique perturbé). Un traitement par corticoïdes a été observé chez 71% avec une dose moyenne de 10 mg/j.
Le retentissement fonctionnel évalué avec l’indice HAQ était en moyenne de 1.44 (0.25 – 2.4).
Le recul moyen après la première perfusion de RTX était de 45.7 mois ± 20.90
• Évaluation de l’efficacité :
Les figures 1 et 2 résument cette évaluation.
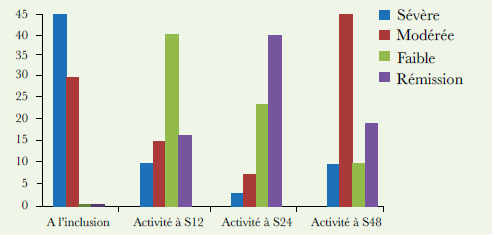
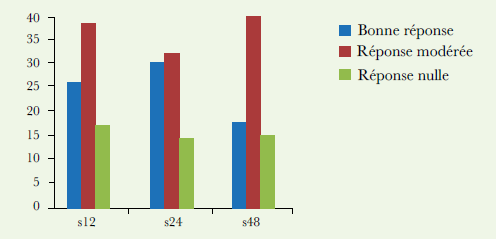
À 12 semaines, la réponse EULAR était de 79 %, 65 patients sur 74 étaient répondeurs avec 32% de bonne réponse. Quatre patients n’ont pas répondu d’emblée et ont été switchés vers une autre biothérapie.
À 24 semaines, la réponse au traitement était maintenue chez 58 patients sur 70 malades, soit 83%, avec 40% de bons répondeurs.
Après 48 semaines, le taux de rémission (bonne réponse EULAR) était de 24% (17 patients sur les 70), le délai moyen de rechute était de 8.8 mois.
Quarante-sept patients (67%) ont été retraités avec un délai moyen de retraitement de 9 mois.
L’amélioration cliniquement pertinente (≥ 0,3) du HAQ était observée chez 63% des patients à la 24ème semaine.
La progression radiologique était lente du fait que la majorité des patients présentait une polyarthrite ancienne et évoluée.
Sur la cohorte de malades suivis, l’étude de la cinétique du taux des lymphocytes B circulants sur toute la période d’étude n’a pu être réalisée que sur 20 patients, soit 27%.
Le taux de lymphocytes B avant traitement se situait entre 3 et 15 %. Des prélèvements à 3 mois ont été effectués montrant la disparition des lymphocytes B circulants. Après 6 mois, le taux était de 0 à 1,35%. Les prélèvements réalisés à 12 mois ont montré une ascension du taux des lymphocytes B entre 2-9% sauf dans 2 cas où le taux est resté à 0% (figure 3).
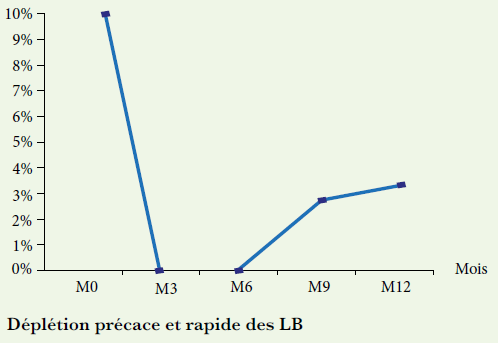
Figure 3 : Ginétique des CD19 ou cours du traitement sous Rituximab
Les taux des IgG, des Ig A et des IgM étaient dans les limites normales excepté chez 4 patients où il y a eu diminution du taux des IgM (figure4).
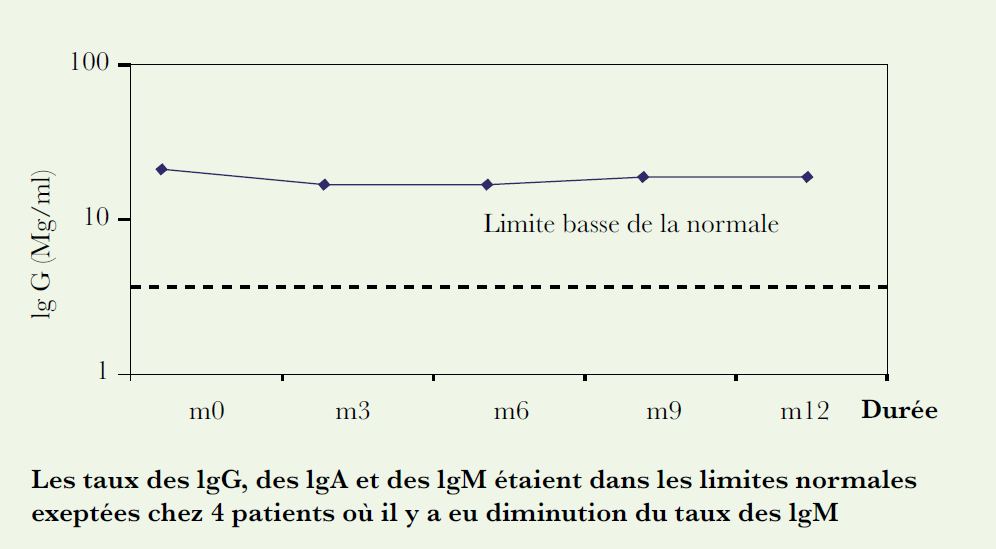
• Évaluation de la tolérance :
La tolérance au traitement était bonne chez 66 patients, soit 89%.
Une malade a été exclue de l’étude pour une poussée de PR à la première perfusion.
Nous avons observé deux cas de réactions allergiques transitoires, 6 cas d’infections bactériennes et virales : 3 cas d’infections urinaires à Escherichia-coli, 2 cas d’infection cutanée (zona et furonculose), un cas d’infection respiratoire haute. Une hypertension artérielle a été observée chez une patiente.
Discussion :
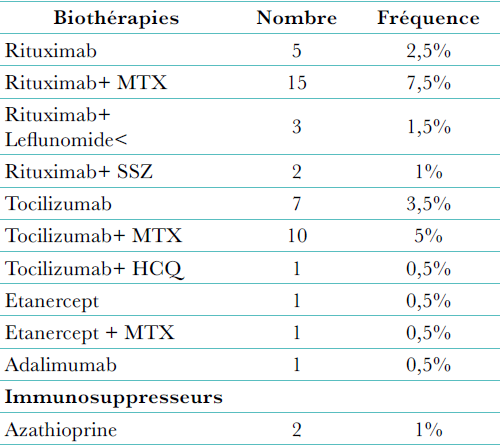
Nous avons rapporté, dans ce travail, les résultats du traitement par le RTX associé ou non au méthotrexate, en première ligne, dans une cohorte de patients atteints de PR réfractaire aux traitements conventionnels, sans recours préalable aux anti-TNF alpha.
L’efficacité du RTX dans la PR a été démontrée dans 3 grandes études cliniques randomisées contre placebo [17-19].
En effet, en 2001 Edwards et Cambridge [10] ont décrit les 5 premiers patients atteints de polyarthrite rhumatoïde réfractaire au traitement conventionnel, traités par le RTX. Le traitement comportait 4 perfusions hebdomadaires de RTX (initialement 300 mg, puis 600 mg) associées à deux perfusions de cyclophosphamide (750 mg) et une corticothérapie per os (30 à 60 mg/j). Tous les patients ont eu une excellente réponse clinique. Cette efficacité est maintenue au moins 6 mois et deux patients ont été retraités après 34 et 49 semaines avec de nouveau une excellente réponse. Ces résultats ont été confirmés par d’autres études ouvertes [11, 12,16].
Dans notre étude, on a observé à 12 semaines une efficacité clinique et biologique qui se traduit par une amélioration significative du DAS28, avec un taux de répondeur EULAR de 79 % et un taux de patients en rémission (bonne réponse) de 32 %. Cette amélioration est maintenue à 24 semaines avec même une augmentation du taux de réponse EULAR à 83% et le taux de patients en rémission à 40%, puis une dégression de la réponse au traitement a été observée à un an, avec diminution du taux de rémission à 24%.
D’autres études algériennes ont évalué la réponse clinique au RTX chez des patients atteints de PR sévère, réfractaire au MTX et viennent conforter nos résultats. En effet, plusieurs études ont été réalisées dans des services de rhumatologie (EHS Ben-Aknoun (BEK), CHU Bab-El-Oued (BEO)) et dans le service de médecine interne de Kouba (KB), elles ont concerné respectivement 52, 17 et 13 patients. L’âge moyen dans ces cohortes était entre 42, 49 et 51 ans, la durée moyenne d’évolution de la PR variait de 12 à 17 ans [17-19].
Le taux de réponse EULAR à 12 semaines était de 52% dans l’étude de BEK, de 82% dans celle de BEO, de 76% dans celle de KB.
Résultats similaires ont été retrouvés dans une étude marocaine, rétrospective portant sur 55 patients atteints de PR avec une durée moyenne d’évolution de 8,16 ± 3,80 ans, l’’âge moyen de la population était de 51,51± 9,42 (27-73) ans, la réponse EULAR à 12 semaines était de 81% et une augmentation du taux de réponse atteignant 94% à 24 semaines [20].
La comparaison de notre étude avec celles rapportées dans la littérature internationale est difficile en raison des différences méthodologiques, notamment dans les protocoles thérapeutiques, les caractéristiques démographiques des patients, les critères d’évaluation, le recours au traitement anti-TNF au préalable. Cependant, certaines études méritent d’être citées : l’étude de Somerville et al [21] qui s’est intéressée à l’efficacité à 12 semaines du RTX, avait retrouvé une réponse de 85 %, et un DAS28 moyen qui s’est amélioré de 7,2 à 5,6 de façon significative, résultats semblables à notre étude. Pour ce qui est de la réponse à 24 semaines observée dans la série (83 %), elle témoigne de l’efficacité croissante du RTX jusqu’au sixième mois, c’est une réponse supérieure à celle retrouvée dans la série de Soliman et al [22] qui est de 60 %, et comparable à celle de la série Quartuccio et al [23] et de la série de Abourazzak et al [20] qui était respectivement de 84 % et 94%.
Délai de retraitement :
L’efficacité est progressive et ne se juge qu’entre le 4ème et le 6ème mois. Pour envisager de retraiter un patient, il faut que celui-ci ait répondu à la première cure de RTX et que la tolérance soit satisfaisante. Il n’est pas recommandé de retraiter les patients moins de 6 mois après la cure précédente, compte tenu de la déplétion lymphocytaire B prolongée induite par chaque cure.
En effet, l’intervalle de temps approximatif préconisé par les auteurs varie de 4 à 18 mois [24, 25] alors que d’autres préconisent un retraitement systématique basé sur la valeur du DAS 28 [26,27].
Dans notre étude, le délai de retraitement variait entre 9 et 12 mois, approche thérapeutique guidée par la déplétion rapide et précoce des lymphocytes B dès la première perfusion de RTX, suivie d’une réascension des taux à partir du 6ème mois jusqu’à atteindre les valeurs initiales entre 9 et 12 mois.
La cinétique du taux des lymphocytes B avant et durant les 12 mois après introduction du RTX observée dans notre étude, concorde avec les données de suivi de l’étude de Leandro et al [28] qui ont observé que le taux des anti-corps, en particulier les facteurs rhumatoïdes et les anti- CCP, baisse significativement (notamment les IgA et les IgG). Parallèlement, les taux d’immunoglobulines (IgA, IgG, IgM) baissent légèrement mais cette diminution n’est pas significative sauf chez quelques patients (de l’ordre de 10%). Les LB réapparaissent progressivement après avoir été indétectables dans le sang périphérique en moyenne pendant 8,4 mois. Cette reconstitution précède la réapparition des auto-anticorps avec, dans près de 80% des cas, une rechute clinique survenant 0 à 17 mois après la réapparition des LB [29].
Tolérance :
La tolérance au traitement par le RTX a été largement démontrée par les grandes études menées sur plus de 900.000 patients atteints de lymphomes [30,31].
Dans la PR, les études cliniques ont montré que le principal évènement indésirable constaté a été la réaction allergique aux perfusions, notée dans au moins 30% des cas. La majorité de ces effets apparaissaient pendant la première perfusion.
Dans notre étude, seulement deux cas de réactions allergiques mineures ont été observés à la première perfusion et rapidement résolutives après diminution du débit.
Globalement, la tolérance dans notre étude était bonne chez 66 patients, soit 89%, résultat comparable à celui retrouvé dans la série de Lupo et al [32] qui est de 80 %, et celui de la série de Mowlah et al [33] qui est de 88 %. Quant aux effets secondaires majeurs nécessitant l’arrêt du RTX, nous n’avons observé qu’un cas de poussée de PR à la première perfusion.
Les effets indésirables les plus fréquents dans notre étude étaient des infections, de l’ordre de 8%, il s’agissait d’infections urinaires, cutanées et un cas de pneumopathie bactérienne, résultats similaires ont été rapportés dans la série de BEO [18].
Toussirot et al [34], ont rapporté dans leur étude, la tolérance du RTX chez des patients avec antécédents d’infection bactérienne sévère ou récurrente, sur un suivi moyen de 20 mois, six patients avaient présenté de nouvelles infections. La relation entre l’infection et le traitement est difficile car dans la PR il y a un trouble du système immunitaire et un risque élevé d’infection. Aucun cas de tuberculose n’a été rapporté dans la série, d’ailleurs le risque de tuberculose sous RTX n’a pas été décrit dans la littérature [35].
En fin, plusieurs méta-analyses ont montré que le RTX est parmi les biothérapies les mieux tolérées en comparaison avec les autres biothérapies [36].
Pour le risque de cancer, on n’a pas noté la survenue de cancer chez nos patients avec un recul moyen après la première perfusion de 45.7 mois ± 20.90 (extrêmes de 3–96 mois). Dans la littérature, le RTX n’augmente pas le risque de cancer au cours de la PR [32-34].
Conclusion :
Il s’agit d’une étude observationnelle qui démontre l’efficacité et la tolérance du RTX utilisé en première intention, chez près de 80% de patients à 12 semaines de traitement, avec un taux de réponse qui continue à augmenter jusqu’à 24 semaines. Il représente donc une bonne alternative thérapeutique après échec aux traitements conventionnels (DMARDS) chez les malades présentant une PR dans un contexte particulier, à savoir l’incidence de la tuberculose et le coût diminué d’un traitement par RTX par rapport aux autres biothérapies. Cette étude souligne aussi l’intérêt de disposer de recommandations nationales de la prise en charge de la PR, ainsi que d’un registre de suivi des biothérapies. Déclaration d’intérêts :
Les auteurs déclarent n’avoir aucun conflit d’intérêt en rapport avec cet article.
Références :
- Sangha O. Epidemiology of rheumatic diseases. Rheumatology (Oxford) 2000;39 Suppl. 2:3–12.
- Corbett M, Dalton S, Young A, Silman A, Shipley M. Factors pre- dicting death, survival and 2. Functional outcome in a prospective study of early rheumatoid disease over fifteen years. Br j 2. Rheuma- tol 1993;32:717–23.
- Pincus T, Callahan LF, Sale WG, Brooks AL, Payne LE, Vaughn WK. Severe functional declines, work disability, and increasedmor- talityinseventy-fiverheumatoidarthritispatientsstudiedover nine years.
- Arthritis Rheum 1984;27:864–72.
- Olsen Nj, Stein CM. New drugs for rheumatoid arthritis. N Engl j Med 2004; 350:2167—2179
- O’Dell jR, Haire CE, Erikson N, Drymalski W, Palmer W, Eckhoff Pj et al. Treatment of rheumatoid Arthritis with methotrexate alone, sulfasalazine and hydroxychloroquine, or a combination of all
- Three medications. N Engl j Med 1996; 334(20):1287–91.6.
- Verstappen S. j W G jacobs1, M j van der Veen et al. Intensive treatment with methotrexate in Early rheumatoid arthritis: aiming for remission. Computer Assisted Management in Early Rheumatoid Arthritis (CAMERA, an open-label strategy trial) Ann Rheum Dis 2007;66:1443-9
- Smolen jS, Landewe R, Breedveld FC, et al. EULAR recommen- dations for the management of Rheumatoid arthritis with synthetic and biological disease-modifying anti rheumatic drugs. Annals of The rheumatic diseases. jun 2010;69(6):964-975.
- Smolen jS, Landewe R, Breedveld FC, et al. EULAR recommen- dations for the management of Rheumatoid arthritis with synthetic and biological disease-modifying anti rheumatic drugs: 2013 update. Annals of the rheumatic diseases. Mar 2014;73(3):492-509.
- Cécile Gaujoux-Viala, Laure Gossec, Alain Cantagrel, Maxime Dougados, BrunoFautrel, Xavier Mariette et al . Recommandations de la société française de rhumatologie pour la prise en charge de La polyarthrite rhumatoïde .Rev de rhum 81(2014)303-312
- Edwards jC, Cambridge G. Sustained improvement in rheuma- toid arthritis following a protocol designed
- To deplete B lymphocytes. Rheumatology (Oxford) 2001; 40:205—211
- Cohen SB, Emery P, Greenwald MW et al. for the REFLEX trial group. Rituximab for rheumatoid
- Arthritis refractory to anti-tumor necrosis factor therapy. Arthritis Rheum 2006;54:2793–806.
- Emery P, Fleischmann R, Filipowicz-Sosnowska A et al. for the DANCER study group. The efficacy and safety of rituximab in patients with active rheumatoid arthritis despite methotrexate treat- ment. Results of a phase IIb randomized, double-blind, placebo controlled, dose-ranging trial.
- Arthritis Rheum 2006;54:1390–400.
- Arnett FC, Edworthy SM, Block DA, McShane Dj, Fries jF, Coo- per NS et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum 1988;31:315-324.
- Prevoo MI. Modified disease activity scores that include twenty eight-joint counts, developpement and validation in a prospective lon- gitudinal study of patients with rheumatoid arthritis. Arthritis rheuma 1995;38(1):44-48
- Van Riel PL. provisional guidelines for measuring disease activity in clinical trials on rheumatoid arthritis. Br j Rheumatol 1992;31(12):793-94
- Kneitz C, Wilhelm M, Tony H-P. Improvement of refractory rheumatoid arthritis after depletion of B cells. Scand J Rheumatol 2004; 33:82—86.
- Lefkir S, Ladjouze A. et al Le rituximab dans la polyarthrite rhu- matoïde. 23ème congrès de la société française de rhumatologie 2010 (poster).
- Dahou C, Benaziez R, Abtroun S. et al. Efficacité et tolérance du rituximab au cours de la polyarthrite rhumatoïde naïve d’anti-TNF alpha. 22ème congrès de la société française de rhumatologie 2009 (Poster).
- TebaibiaA,BoudjellaMA, MahiMet al .Efficacité de l’association rituximab méthotrexate dans le traitement de la polyarthrite rhuma- toïde réfractaire aux traitements conventionnels. Revue Algérienne de Médecine Interne 2013 ; 00 : 21-7
- F.E. Abourazzak, R. Boussaadani Soubai, H. Chellat, I. El Mezouar et T. Harzy. The use of rituximab in rheumatoid arthritis : about 55 patients. Rev Med Brux 2015 ; 36 : 133-8
- Somerville M, Gaffney K, Scott DGI, jois RN, Masding A : Ri- tuximab therapy in patients with Resistant rheumatoid arthritis : real- life experience. Rheumatology 2007 ; 46 : 980-2
- Soliman MM, Hyrich KL, Lunt M, Watson KD, Symmons DP, Ashcroft DM : Effectiveness of rituximab in patients with rheumatoid arthritis : observational study from the British Society for Rheumato- logy Biologics Register. j Rheumatol ER 2012 ; 39 : 240-6
- Quartuccio L, Fabris M, Salvin S et al. : Rheumatoid factor posi- tivity rather than anti-CCP positivity, a lower disability and a lower number of anti-TNF agents failed are associated with response to rituximab in rheumatoid arthritis. Rheumatology (Oxford) 2009 ; 48 : 1557-9
- Smolen j, Keystone E, Emery P. et al. Consensus statement on the use of rituximab in patients with rheumatoid arthritis. Ann Rheum Dis 2007;66:143-150
- Emery P, Furst DE, Ferraccioli G et al. Long-term efficacy and safety of a repeat treatment course of rituximab in rheumatoid arth- ritis patients with an inadequate response to disease-modifying anti- rheumatic drugs. Ann Rheum Dis 2006;65(Suppl II):OP0017.
- Rogier M. T, koen Vos et al. Disease activity–guided rituximab therapy in rheumatoid arthritis. The effects of re-treatment in initial non-responders versus initial responders. Arthritis & rheumatism vol. 58, no. 12, december 2008, pp 3657–3664
- Emery P, Mease Pj, Rubbert-Roth A, et al. Retreatment with rituximab based on a treatment-to-target approach provides better disease control than treatment as needed in patients with rheuma- toid arthritis: a retrospective pooled analysis. Rheumatology. Dec 2011;50(12):2223-2232.
- Leandro Mj, Edwards jC, Cambridge G. Clinical outcome in 22 patients with rheumatoid arthritis Treated with B lymphocyte deple- tion. Ann Rheum Dis 2002; 61:863—866. 9.
- Cambridge G, Leandro Mj, Edwards jC, et al. Serological changes following B lymphocyte Depletion therapy for rheumatoid arthritis. Arthritis Rheum 2003; 48:2146—2154.
- Kimby E: Tolerability and safety of rituximab (MabThera). Can- cer TreatRev. 2005 jul 27; [Epubahead of print]. Available online at www.sciencedirect.com
- Achemlal L, Mikdame M, Nouijai A, Bezza A, El Maghraoui A. Dramatical improvement of chemo resistant bone lymphoma with rituximab. Clin Rheumatol. 2005; 25 :1-2 [Epubahead of print] 14
- Lupo G, Gottenberg j, Combe B et al. : Suivi prospectif du trai-
- tement par rituximab chez 410 patients ayant une maladie auto-im- mune réfractaire : premières données des registres AIR-PR et AIR. Revue du Rhumatisme 2007 ; 74 : 1020-1
- Mowlah S, Rughoobur-Bheekhee A, Hessamfar M et al. : Profil de tolérance au long cours du rituximab dans les maladies immuno- inflammatoires. Rev Med Interne 2013 ; 34 : 58-9
- Toussirot E, Pertuiset H, Sordet C et al. Tolérance du rituximab dans la polyarthrite rhumatoïde chez des patients avec antécédent d’infections bactériennes sévères ou récurrentes : étude observation- nelle de 30 cas suivis en pratique courante. Revue du Rhumatisme 2010 ; 77 : 169-73
- Gottenberg jE, Ravaud R et al. Risk factors for severe infections in patients with rheumatoid Arthritis treated with Rituximab in the Auto Immunity and Rituximab Registry. Arthritis Rheum. 2010;62(9):2625-32. 4
- Singh jA, Wells GA, Christensen R, et al. Adverse effects of bio- logics: a network meta-analysis and Cochrane overview. Cochrane Database Syst Rev. 2011 ; 16 :CD008794