Au service d’hématologie et de thérapie cellulaire de l’EHU-Oran, 330 patients souffrant de Lymphome de HODGKIN (LH) de stades étendus IIB bulky, III et IV, âgés de 16 à 75 ans ont été pris en charge du 01-01-2004 au 31-12-2019.
A. Arabi, L. Charef, S. Bouchama, N. Hakiki, K. Amani, S. Osmani, N. Yafour
Service d’Hématologie et de Thérapie Cellulaire EHU-Oran.
Date de soumission: 01 Décembre 2021.
Résumé : Au service d’hématologie et de thérapie cellulaire de l’EHU-Oran, 330 patients souffrant de Lymphome de HODGKIN (LH) de stades étendus IIB bulky, III et IV, âgés de 16 à 75 ans ont été pris en charge du 01-01-2004 au 31-12-2019. Dans ce travail nous analysons le profil de ces patients ainsi que les résultats des protocoles thérapeutiques utilisés 6 ABVD (groupe A), 8 ABVD (groupe B) ou BEACOPP (groupe C) en première ligne. L’âge moyen de ces patients était de 32 ans (extrêmes 16 à 75 ans), le sexe ratio H/F 0,91 et les stades IV au nombre de 208 (63%). Au terme de la première ligne de traitement nous avons enregistré 60% de RC, 20% de RP ainsi que 15% d’échecs, 2,5% de progression-réfractaire et 2,5% de décès précoces. À la date de point nous avons enregistré 73% de réponses objectives (RO) RC, RCu et RP ainsi que 20% de formes réfractaires. Ces résultats sont commentés à la lumière des conditions locales de prise en charge.
Mots clés : Lymphome, Hodgkin lymphome, Chimiothérapie, BEACOPP, Traitement adapté au stade
Abstract: In the hematology and cell therapy department of the EHU-Oran, 330 patients suffering from Hodgkin lymphoma (LH) of extended stages IIB bulky, III and IV, aged 16 to 75 years were treated from Jan. 1st 2004 to Dec. 31st 2019. In this work, we analyze the profile of these patients as well as the results of the therapeutic protocols used 6 ABVD (A group), 8 ABVD (B group) or BEACOPP (C group) in first line treatment. The mean age of these patients was 32 years (range 16 to 75 years), the sex ratio M/F 0.91, and stages IV were 208 (63%). At the end of the first line of treatment we recorded 60% CR, 20% RP as well as 15% failures, 2.5% refractory or progression and 2.5% early death.
At the point date we recorded 73% of objective responses (RO) RC, RCu and RP as well as 20% of refractory forms. These results are discussed in the light of local care conditions.
Keywords: Lymphoma, Hodgkin lymphoma, Chemotherapy, BEACOPP, Stage-adapted treatment
Introduction
Le lymphome de Hodgkin (LH) est une hémopathie maligne du tissu lymphoïde. L’étiologie reste inconnue, cependant, il a été établi que l’infection par le virus EBV est responsable de l’apparition ultérieure de 25 à 40% des lymphomes3 de Hodgkin ; on pense également que l’âge, la race, l’ethnie, le sexe et le niveau socio-économique jouent un rôle1
C’est l’un des lymphomes les plus fréquents avec une incidence de 2 à 3 cas/100.000 habitants/an dans les pays développés1. En Algérie, son incidence est passée de 0,7 à 1,8 cas/100.000 habitants/an2, ce qui signifie que chaque année, environ 900 nouveaux patients atteints de lymphome de hodgkin sont pris en charge, ce chiffre étant appelé à augmenter dans le temps.
Au niveau de la prise en charge thérapeutique, le bilan d’extension initial ainsi que l’évaluation ultérieure reposent actuellement sur le PETSCAN qui occupe une place capitale dans la prise en charge du LH6,7,8. Il est recommandé dans la recherche d’une réponse précoce (PETSCAN 2 ou PETSCAN intermédiaire), et en fin de traitement (PETSCAN 3).
La première ligne de traitement dépend du stade de la maladie, des facteurs pronostiques et de l’existence ou non de comorbidités9 : ABVD + Radiothérapie (dans les stades localisés IA, IB, IIA, IIB non bulky du médiastin), ABVD ou BEACOPPesc (dans les stades IIB bulky, III et IV).
Sous ces conditions, le lymphome de Hodgkin est généralement considéré comme guérissable dans la plupart des cas, en particulier dans les stades localisés, ceci grâce à des protocoles de chimiothérapie, aujourd’hui bien standardisés, associés ou non à une radiothérapie.
Cependant, les stades étendus IIB bulky, III et IV, posent encore des problèmes de prise en charge thérapeutique liés à l’existence de formes réfractaires ainsi qu’à la toxicité tardive des chimiothérapies administrées.
Nous rapportons dans ce travail notre expérience basée sur la prise en charge de 330 patients de stades étendus IB bulky, III et IV, recrutés dans notre service entre le 01-01-2004 et le 31-12-2019.
Patients et méthodes
Au service d’hématologie et de thérapie cellulaire de l’EHU-Oran, 330 patients présentant un lymphome de Hodgkin de stades étendus IIB bulky, III et IV, âgés de 16 à 75 ans ont été pris en charge du 01-01-2004 au 31-12-2019, soit une moyenne de 22 patients de stade étendu par année.
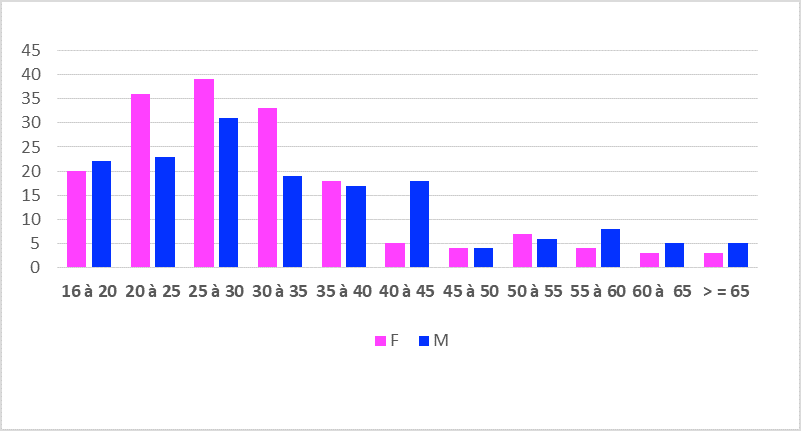
L’âge médian des patients était de 29 ans (16-75 ans), dont 68% dans la tranche 16-35 ans. Le sex-ratio H/F de 0,91 ; une très légère prédominance féminine, retrouvée pratiquement dans toutes les tranches d’âge (Figure 1).
Avec un délai moyen de 5,6 mois, le diagnostic a été histologique dans 100% des cas, et le type scléro-nodulaire majoritairement retrouvé (77% des cas). L’immunohistochimie a été faite dans 59% des cas.
Le PETSCAN a été fait chez 15% de nos patients. Dans l’immense majorité des cas, il s’agissait d’un PETSCAN intermédiaire.
Au plan thérapeutique, et pour notre analyse, les patients ont été regroupés en fonction des 3 différents protocoles reçus en première ligne. Ainsi, 34 patients du groupe 1 ont reçu 6 cures ABVD avec ou sans radiothérapie, 180 patients du groupe 2 ont reçu 8 cures ABVD et 116 patients du groupe 3 ont reçu 2 cures BEACOPPesc plus 4 cures ABVD.
Les calculs courants ont été faits sur Excel®, les calculs des survie selon la méthode de Kaplan-Meier.
Figure 1 : Recrutement par année et par sexe.
Résultats
Il existe une nette prédominance de stades IV (63%). Le caractère « bulky » médiastinal est retrouvé dans 43% des cas ; il est plus fréquent chez le sexe féminin (Figure 2 et Tableau 1). Soixante-huit pour cent des stades IIB bulky du médiastin ont pu bénéficier de la radiothérapie.
Après la première ligne de traitement nous avons enregistré 80% de réponses objectives (RO) dont 60% de RC et 20% de RP ainsi que 15% d’échecs ; 2,5% de progression-réfractaire et 2,5% de décès précoces (Tableau 2). Sur les 264 patients ayant obtenu une RO, 42 (62%) rechuteront par la suite.
Au total, en dehors de l’ABVD et du BEACOPP, nous avons appliqué jusqu’à 5 lignes de traitement selon les cas en utilisant les protocoles suivants DHAC, BGEV, ICE, ESHAO, IVOX, M-BACOD, DEXA-BEAM.
À la date de point (03-11-2021) nous avons enregistré 73% de RO (RC, RCu, RP) dont 64% de RC, ainsi que 6% de PDV, 2% d’échecs (rechute, progression, échec) et 19% de décès (Tableau 3).
Si l’on se réfère à la définition des formes réfractaires (incapacité à atteindre une rémission après un traitement de première ligne et patients en rechute précoce) on a donc 20% de formes réfractaires.
La survie globale tous groupes confondus est de 66% à 139 mois. Elle est de 84% à 104 mois pour le groupe C (BEACOPP), 68% à 139 mois pour le groupe A (6 ABVD) et 59% à 139 mois pour le groupe B (8 ABVD). Il n’y a pas de différence significative entre les groupes : Log Rank 0,414 et 0,756 entre le groupe A et les groupes B et C respectivement.
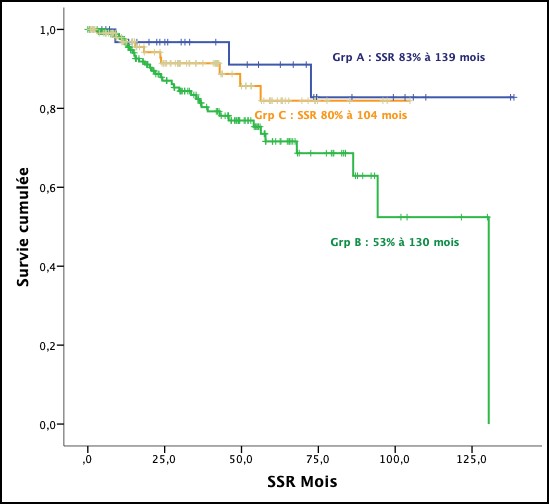
La survie sans rechute tout groupes confondus est quant à elle, de 44% à 139 mois. Elle est de 83% à 139 mois pour le groupe A, 80% à 104 mois pour le groupe C, et 53% à 94 mois pour le groupe B. La différence est significative entre le groupe A et B : Log Rank 0,032. Elle est moindre entre le groupe C et B : Log Rank 0,071. Il n’y a pas de différence significative entre les groupes A et C : Log Rank 0,521.
Figure 2 : Recrutement par stade
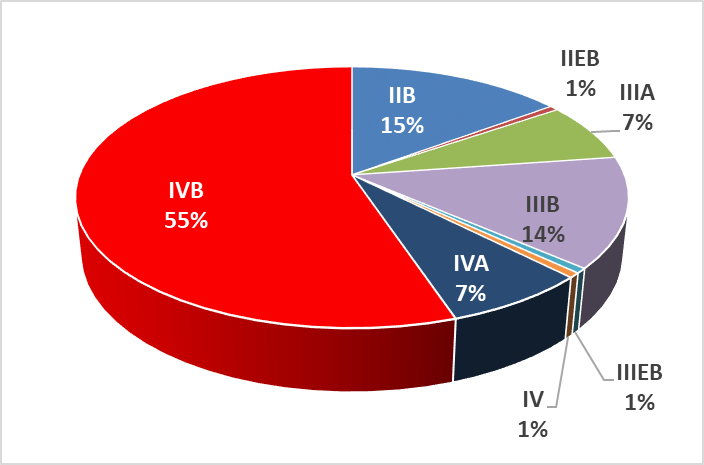
Tableau 1 : Répartition des formes bulky en fonction du sexe.
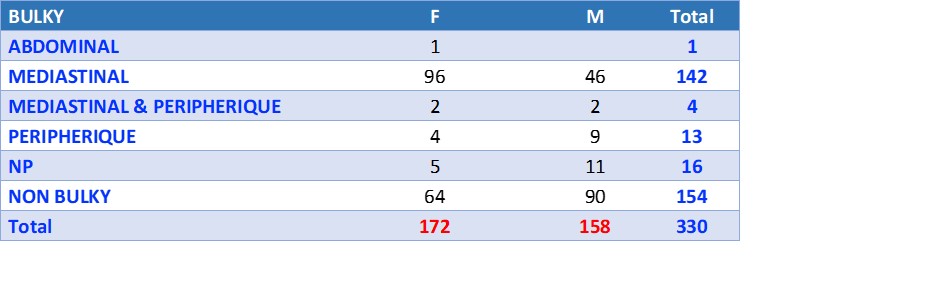
Tableau 2 : Résultats en première ligne thérapeutique.
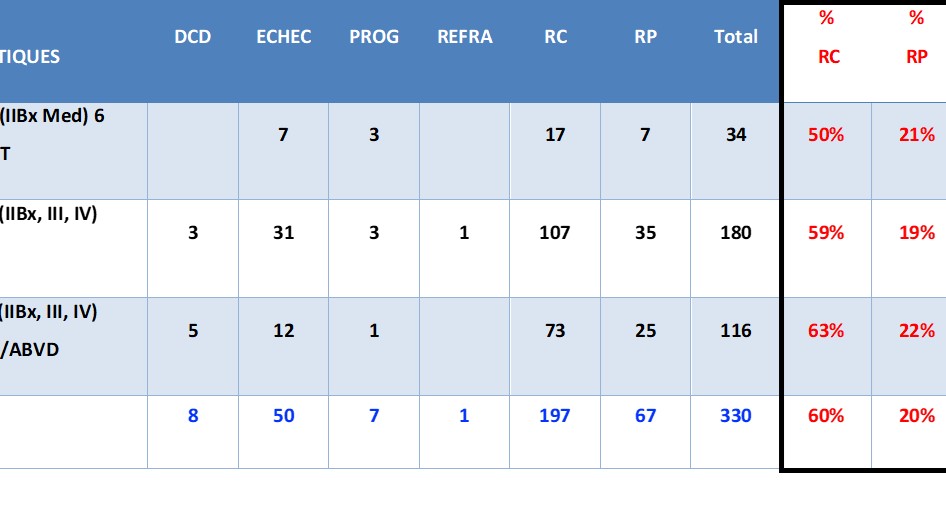
Tableau 3 : Résultats thérapeutiques à la date de point
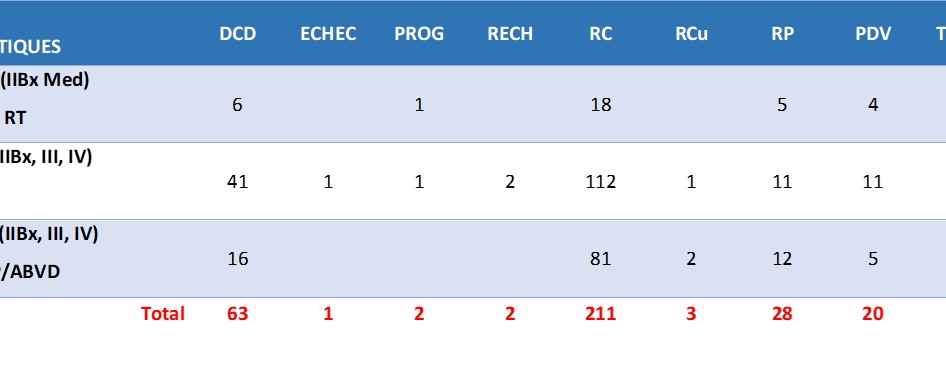
Figure 3 : Survie globale tous groupes confondus
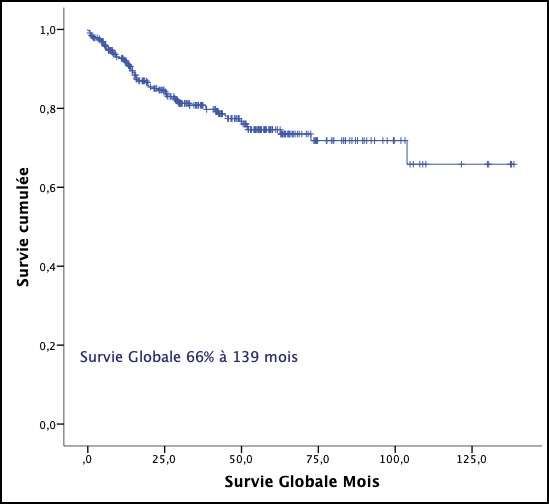
Figure 4 : Survie globale selon les groupes
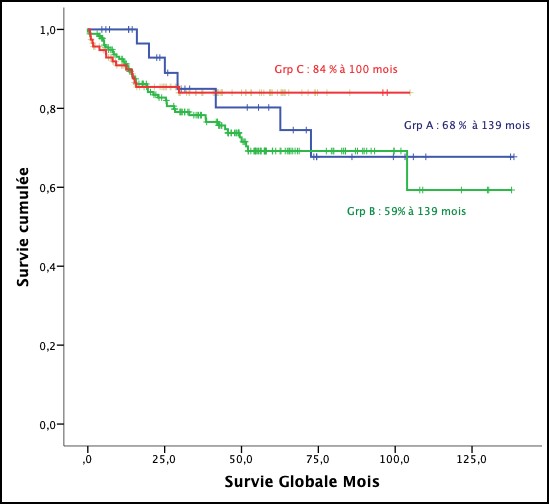
Figure 5 : Survie sans rechute tous groupes confondus
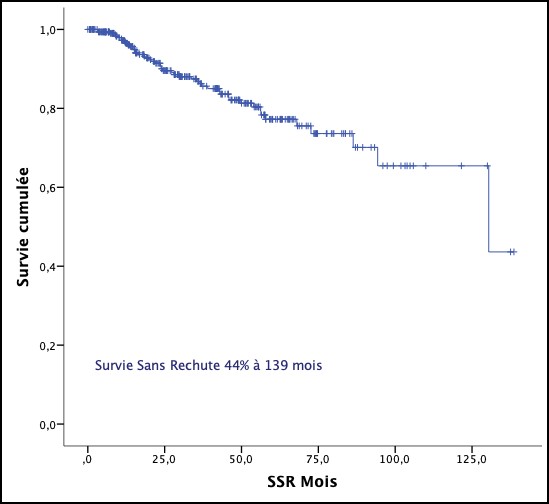
Figure 6 : Survie sans rechute selon les groupes
Discussion
Avec un recrutement moyen de 41 patients par année dont 22 sont des stades étendus, notre population étudiée se caractérise par un âge relativement jeune, avec un pic à 25-30 ans et un âge médian de 29 ans, qui semble légèrement inférieur à la médiane dans les populations européennes (qui est de 33 ans4). Ceci est certainement en rapport avec la structure de la pyramide des âges de la population algérienne17.
Par ailleurs, il existe une légère prédominance féminine (sex-ratio H/F de 0,91) retrouvée pratiquement dans toutes les tranches d’âge, ceci diffère également des populations européennes dans lesquelles la prédominance masculine est constante.
La fréquence des stades étendus IIB bulky, III et IV est plus grande du fait d’un délai diagnostic long estimé à 5-6 mois, ce qui implique pour nous une prise en charge plus complexe à gérer du fait du nombre élevé de formes réfractaires (estimé à 20% dans notre série), associé à l’irrégularité quant à la disponibilité des drogues et des traitements de soutien, à l’éloignement des patients, en effet un patient résidant à plus de 100 km de notre centre ne peut se permettre des déplacements durant 3 jours consécutifs en domicile – hôpital de jour pour y recevoir un protocole BEACOPPesc.
Ceci nous amène à opter pour un protocole en fonction, au minimum, du lieu de résidence du patient et de la disponibilité des drogues.
Or actuellement on obtient dans les pays développés 96,4% de survie globale à 5 ans dans les stades localisés13.
Dans les stades étendus, l’obtention d’un consensus a été plus compliquée, l’école Allemande restant une fidèle du BEACOPPesc, alors que le reste des pays Européens et les États-Unis préféraient l’ABVD ; une comparaison de ces 2 protocoles a montré une survie sans évènement à 7 ans de 85% pour le BEACOPPesc et de 73% pour l’ABVD (p=0,004)14,15.
Mais la toxicité du traitement est nettement plus importante dans le Groupe ayant reçu le BEACOPPesc.
Gallamini et coll.16 ont démontré la valeur pronostique du PETSCAN intermédiaire et grâce à cette donnée, le traitement des stades étendus est standardisé : 2 cycles BEACOPPesc et évaluation : si PETSCAN négatif, désescalade par 4 ABVD, si PETSCAN positif, selon les cas, adjonction de 2 cycles BEACOPPesc, ou passage à un protocole de rattrapage.
Quant aux formes réfractaires, aux États-Unis, Ann S. La Casce rapporte entre 15 et 30% de LH réfractaires10. Une chimiothérapie comprenant Brentuximab, Nivolumab ou Pembrolizumab suivie d’une autogreffe de cellules souches permet d’obtenir 75% de rémission complète
Dans le même ordre d’idée, Alison J. Moskowitz publie 90% de rémission complète avec une survie sans progression à 2 ans de 84% chez 60 patients présentant un LH réfractaire11 traités par Brentuximab Vedotin.
Or dans notre contexte, aucune de ces drogues n’est disponible, et ceci nous oblige à choisir des protocoles plus classiques (DHAC, BGEV, GEMOX, ICE, ESHAP, IVOX, M-BACOD, DEXA-BEAM). Avec ces protocoles, une deuxième ligne a été nécessaire dans 115 cas avec obtention d’une rémission complète dans 33 cas (29%) ; une troisième ligne a été faite dans 82 cas avec obtention d’une rémission complète dans 20 cas (24%), puis une quatrième ligne dans 62 cas avec obtention d’une rémission compète dans 6 cas (10%), et une cinquième ligne dans 56 cas avec obtention d’une rémission complète dans 2 cas (4%), soit un total de 53% de RC sur les 115 réfractaires.
Date de soumission
01 Décembre 2021.
Références
- Harris NL, Jaffe ES, Diebold J, et al. The WHO classification of hematological malignancies, report of the clinical advisory committee meeting. Mod Pathol 2000; 13: 193
- T Abad – Presse Médicale -9 juillet 2017
- Urayama KY, Jarrett RF, Hjalgrim H, et al. Genome-wide association study of cHL and EBV status defined subgroups. J Natl Cancer Inst 2012; 104: 240–53.
- Yung L, Linch D. Hodgkin’s lymphoma. Lancet 2003; 361: 943–51
- Greaves P, Clear A, Coutinho R, et al. Expression of FOXP3, CD68, and CD20 at diagnosis in the microenvironment of classical Hodgkin lymphoma is predictive of outcome. J Clin Oncol 2013; 31: 256–62.
- Eichenauer DA, Aleman BMP, André M, et al. Hodgkin lymphoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2018; 29 (suppl 4): iv19–29. 1
- Barrington SF, Mikhaeel NG, Kostakoglu L, et al. Role of imaging in the staging and response assessment of lymphoma: consensus of the International Conference on Malignant Lymphomas Imaging Working Group. J Clin Oncol 2014; 32: 3048–58. 1
- Cheson BD, Fisher RI, Barrington SF, et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin lymphoma: the Lugano classification. J Clin Oncol 2014; 32: 3059–68. 1
- Klimm B, Goergen H, Fuchs M, et al. Impact of risk factors on outcomes in early-stage Hodgkin’s lymphoma: an analysis of international staging definitions. Ann Oncol 2013; 24: 3070–76.
- Ann S. LaCasce. Treating Hodgkin Lymphoma in the new millenium : Relapsed and refractory disease. Hematological Oncology 2019 ; 375(S1) ; 87-91
- Alison J.Moskowitz.Optimizing The Role of Brentuximab Vedotin in Classical Hodgkin Lymphoma Therapy.Hematology 2018 ; 207-2012
- Jacobs EM, Peters FC, Luce JK, Zippin C, Wood DA. Mechlorethamine hcl and cyclophosphamide in the treatment of hodgkin’s disease and the lymphomas. JAMA : the journal of the American Medical Association. 1968; 203(6):392–398. [PubMed: 4865234] 3
- Howlader, N.N, A.Krapcho, M.Miller, D.Bishop, K.Kosary, CL.Yu, M.Ruhl, J.Tatalovich, Z.Mariotto, A.Lewis, DR.Chen, HS.Feuer, EJ., Cronin, KA., editors. SEER Cancer Statistics Review, 1975-2014. National Cancer Institute; Bethesda, MD: based on November 2016 SEER data submission, posted to the SEER web site, April 2017.; undefined 5
- Merli F, Luminari S, Gobbi PG, et al. Long-Term Results of the HD2000 Trial Comparing ABVD Versus BEACOPP Versus COPP-EBV-CAD in Untreated Patients With Advanced Hodgkin Lymphoma: A Study by Fondazione Italiana Linfomi. Journal of Clinical Oncology. 2016; 34(11): 1175–1181. [PubMed: 26712220] 5
- Carde P, Karrasch M, Fortpied C, et al. Eight Cycles of ABVD Versus Four Cycles of BEACOPPescalated Plus Four Cycles of BEACOPPbaseline in Stage III to IV, International Prognostic Score >/= 3, High-Risk Hodgkin Lymphoma: First Results of the Phase III EORTC 20012 Intergroup Trial. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2016; 34(17):2028–2036. [PubMed: 27114593] 5
- Gallamini A, Hutchings M, Rigacci L, et al. Early interim 2-[18F]fluoro-2-deoxy-D-glucose positron emission tomography is prognostically superior to international prognostic score in advanced-stage Hodgkin’s lymphoma: a report from a joint Italian-Danish study. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2007; 25(24): 3746–3752. [PubMed: 17646666] 5
- Algérie « fiche pays » – Population data.net ; 2020